國內獸用診斷試劑情況匯總及注冊方法
向昭穎 楊佳穎

診斷試劑是指采用免疫學、微生物學、分子生物學等原理或方法制備的、在體外用于對人類或動物疾病的診斷、檢測及流行病學調查等的診斷試劑。常用的檢測方法有酶聯免疫/酶免法(ELISA),免疫熒光法,PCR等等。
1注冊方法
為進一步加強獸醫診斷制品(以下簡稱診斷制品)注冊評審工作,滿足動物疫病診斷、監測、檢疫和評估等工作需要,2015年12月農業部發布中華人民共和國農業部公告第2335號,對獸醫診斷制品注冊要求規定如下。
1)嚴格執行診斷制品注冊分類的規定。凡與我國已批準上市銷售、檢測方法和檢測標的物相同的同類診斷制品比較,在敏感性、特異性、穩定性和便捷性等方面無根本改進的診斷制品不作為新獸藥審批。
2)體外診斷制品應在注冊資料中提供臨床檢測數據和總結報告,不再要求進行臨床試驗審批。
3)對無國家標準的試驗用動物,研制者應當制定動物質量標準和檢測方法,可不提供實驗動物合格證和實驗動物使用許可證等證件的復印件。
4)診斷制品的中試應在GMP車間或符合生物安全要求的實驗室進行。
5)加強診斷制品生產及檢驗用菌(毒、蟲)種和細胞等主要原材料的管理。申請人提出獸藥注冊申請時,應提交菌(毒、蟲)種基礎種子批的制備和鑒定記錄、菌(毒、蟲)種的標準、鑒定報告,以及基礎細胞種子批的制備和鑒定記錄、細胞種子的標準、鑒定報告等資料。
6)加強診斷制品所用對照品(包括標準抗原、標準血清等質控標準物質)以及成品的敏感性、特異性和重復性檢驗用樣品盤的制備、檢驗、標定管理。必要時,標定工作由研究單位委托中國獸醫藥品監察所進行。
7)加強診斷制品的比對試驗研究。應在不少于3家實驗室進行診斷制品的比對試驗。承擔比對試驗的實驗室應為農業部考核合格的省級以上獸醫主管部門設置的獸醫實驗室。有國家獸醫參考實驗室或農業部指定的專業實驗室的,應至少選擇1家國家參考實驗室或農業部指定的專業實驗室實施比對試驗。
8)涉及《國家中長期動物疫病防治規劃(2012-2020年)》明確的16種優先防治動物疫病的診斷制品,如研究單位參加了國際參考實驗室組織的國際間比對,或采用國際、國家參考實驗室提供的標準樣品或試劑作為平行對照檢測研究的,應提交相應比對結果或試驗報告。
9)申報單位在提出注冊申請前,應將全部研究報告、原始記錄等資料歸檔備查。
2國內獸用診斷試劑批準文號情況
截止2019年1月23日,獲取國內新獸藥證書產品46個(表1),呈逐年遞增趨勢。
在有效期內的進口獸藥注冊證書9個(表2),以豬用疾病診斷試劑為主。
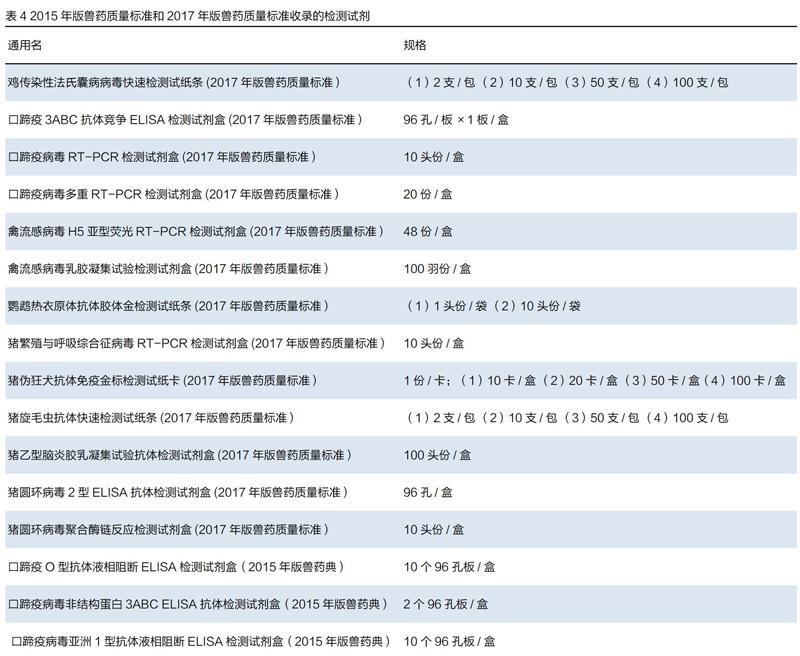
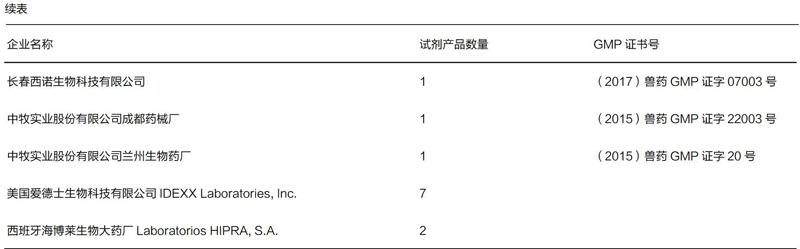
目前國內獲得批準文號在有效期內的診斷試劑產品有35個,由14家生產企業生產(表3),其中10家企業獲得GMP獸藥證書。另有14個診斷試劑產品被收錄在2017年版獸藥質量標準(表4),2個診斷試劑產品被收錄在2015年獸藥質量標準。在2019年1月4日,中國動物疫病預防控制中心公布了第一批非洲豬瘟現場快速檢測試劑名錄11個(表5)。
2.1國內新獸藥情況
獲取國內新獸藥證書的46個產品中,一類新獸藥產品2個,二類新獸藥22個,三類新獸藥22個。
2.2進口獸藥注冊情況
2.3批準文號情況
其中針對狂犬病的檢測試劑有3個,針對禽類疾病的檢測試劑有7個,針對牛、羊疾病的檢測試劑8個,針對豬類疾病的檢測試劑14個,另有口蹄疫病毒非結構蛋白3ABC ELISA抗體檢測試劑盒。
診斷試劑行業是生物制藥行業的重要組成部分,未來檢驗產品的種類將快速擴大;總體來看,診斷試劑技術的發展趨勢總體分為兩方面,一方面是將向高度集成、自動化發展,一方面是將向簡單、快速發展。

