大豆肽鈣螯合物的制備、穩定性及表征
王俊強,孔祥珍,華欲飛
(江南大學 食品學院,江蘇 無錫 214122)
鈣是維持人類生命健康重要的礦物質之一,其約占成年人體重的2%,缺鈣會增加人體骨折和患骨質疏松癥的風險,隨著全球人口老齡化現象的加劇,研究新型鈣補充劑,以增加人體對鈣的吸收利用率越來越受到人們的關注[1]。另外,鈣還具有參與細胞內代謝、凝血、神經傳導、骨骼生長等重要功能[2]。
大豆蛋白作為一種優質的植物蛋白[3],具有降血脂、降膽固醇和預防骨質疏松、更年期綜合征等生理功能[4-5]。大豆蛋白的水解產物可以良好地保留大豆蛋白中的氨基酸,同時,大豆蛋白被水解成小分子的多肽后,更容易被人體吸收利用[6]。另外,有研究認為大豆肽可以參與調節細胞免疫、神經遞質,同時具有促進腦功能的作用[7]。Bao等[8]的研究表明,大豆蛋白水解產物具有鈣螯合能力,可以作為鈣補充劑的生產原料。呂瑩等[9]通過Caco-2實驗證實,大豆肽鈣螯合物對促進腸道細胞對鈣的吸收和轉運過程起到了重要的作用。
本文研究了大豆肽具有螯合能力的相對分子質量分布,結合氨基酸分析說明了具有鈣螯合能力的大豆肽的特征,研究了大豆肽鈣螯合物在磷酸鹽緩沖液中的鈣保留率和不同pH條件下的穩定性。同時通過Zeta電位分析和XRD研究大豆肽鈣螯合物的作用類型。最后,通過DSC和TGA對比大豆肽及大豆肽鈣螯合物的熱穩定性。以期為大豆肽鈣螯合物的進一步研究提供基礎數據。
1 材料與方法
1.1 實驗材料
低溫脫脂豆粕,山東禹王集團;堿性蛋白酶,諾維信(中國)生物技術有限公司。氫氧化鈉、鹽酸、無水氯化鈣、無水乙醇、硝酸、磷酸氫二鈉、磷酸二氫鈉,分析純;乙腈,HPLC。
K9840自動凱氏定氮儀,Himac CR21 GⅡ型冷凍離心機,恒溫干燥箱,AA-240原子吸收分光光度計(火焰型),D-2000 Elite 高效液相色譜儀,835-50 型氨基酸自動分析儀,Nano Brook Omni 型多角度粒度與高靈敏度Zeta電位分析儀,尼魯噴霧干燥機,制備級高效液相色譜儀,X射線衍射儀,DSC3型差示掃描量熱儀,TGA2型熱重分析儀。
1.2 實驗方法
1.2.1 大豆肽的制備
將低溫脫脂豆粕粉碎后,按料液比1∶5加85%乙醇醇洗60 min,42℃干燥后,按料液比1∶9加入去離子水,于pH 4.5條件下酸沉1 h,8 500 r/min離心30 min,沉淀加入9倍體積的去離子水充分分散,于pH 9.0、60℃條件下加入2%的堿性蛋白酶水解4 h,調pH至中性滅酶,8 500 r/min離心30 min,上清噴霧干燥,即得大豆肽。
1.2.2 大豆肽鈣螯合物的制備
配制100 mL 4%的大豆肽溶液,調節pH至7.8,加入4 mL 2 mmol/L的CaCl2溶液,于40℃恒溫水浴振蕩器中反應1 h,4 000 r/min離心10 min,上清中加入8倍體積無水乙醇,靜置30 min,離心,加入85%乙醇洗兩次,每次醇洗時間為30 min,離心后沉淀于42℃烘干,即得大豆肽鈣螯合物。
1.2.3 大豆肽鈣螯合物在磷酸鹽溶液中的穩定性
向pH 8.0的磷酸鹽(10~200 mmol/L)緩沖液(PBS)中添加大豆肽鈣螯合物,使溶液中鈣含量為1 mg/mL,于37℃下振蕩水浴30 min,離心后,測定上清中鈣含量,計算鈣保留率,同時,向溶液中添加相同含量的CaCl2作對照。鈣保留率按下式計算。
鈣保留率=離心后上清中鈣含量/溶液中鈣含量×100%
1.2.4 氨基酸組成的測定
采用OPA FMOC柱前衍生,通過氨基酸自動分析儀進行測定。稱取約0.1 g大豆肽或大豆肽鈣螯合物于水解管內,加入8 mL 6 mol/L的HCl溶液,混勻后放于110℃的烘箱內消解22 h。取出冷卻,將消解液轉移到25 mL容量瓶中,用4.8 mL 10 mol/L氫氧化鈉溶液中和,并用水定容至刻度。采用雙層濾紙過濾,取1 mL濾液離心(10 000 r/min,10 min),取上清液進行測定。
1.2.5 大豆肽鈣螯合物的脫鈣
稱取25 mg大豆肽鈣螯合物,加入5 mL 0.2 mol/L的pH 8.0 PBS中,于旋渦振蕩器上振蕩5 min,10 000 r/min離心10 min,上清液為脫鈣后的大豆肽鈣螯合物。該方法可脫除大豆肽鈣螯合物中99%以上的鈣,且大豆肽無損失。
1.2.6 大豆肽鈣螯合物在不同pH條件下的穩定性
將一定量的大豆肽鈣螯合物溶解于去離子水中,使溶液中鈣含量為1 mg/mL,分別調pH至2.0~8.0,于37℃下振蕩水浴2 h,離心(10 000 r/min,10 min),測定上清的相對分子質量。
1.2.7Zeta電位分析
參考劉成梅等[10]的方法并加以改進。將大豆肽或大豆肽鈣螯合物配制成0.1%的溶液,調節pH至7.8,進行Zeta電位的測定。
1.2.8 XRD分析
分別將大豆肽、氯化鈣、大豆肽鈣螯合物制成粉末,進行XRD分析,掃描角度5°~90°。
1.2.9 DSC分析
分別稱取3 mg左右的大豆肽及大豆肽鈣螯合物于坩堝內,置于差示掃描量熱儀中,進行熱穩定性分析,同時進行空白對照。溫度范圍25~200℃,升溫速度10℃/min,N2流速50 mL/min。
1.2.10 TGA分析
分別稱取大豆肽及大豆肽鈣螯合物3 mg于坩堝中,將坩堝置于熱重分析儀中,測定溫度25~900℃,升溫速度10℃/min,N2流速30 mL/min,記錄樣品質量,計算并繪制質量損失率曲線。
1.2.11 數據處理
所有實驗數據均通過IBM SPSS Statistics 25和Origin 2018進行數據處理與作圖。
2 結果與討論
2.1 堿性蛋白酶水解大豆肽的水解度和鈣結合量
低溫脫脂豆粕經醇洗酸沉后用堿性蛋白酶進行水解,水解4 h過程中的水解度隨時間的變化見圖1。
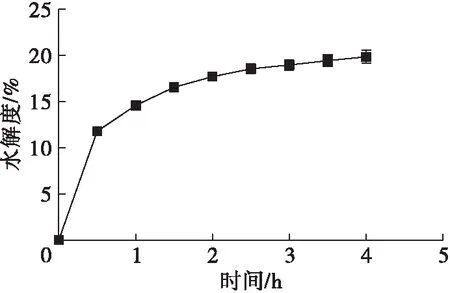
圖1 豆粕水解度隨時間變化趨勢
由圖1可知,豆粕在pH 9.0條件下水解,其在最初0.5 h迅速水解,之后水解速度逐漸降低,經過4 h,水解度可達19.84%。對經此工藝水解獲得的大豆肽進行鈣螯合力的測定,得到其鈣結合量為53.03 mg/g。
2.2 大豆肽鈣螯合物在磷酸鹽溶液中的穩定性
人體攝入的磷元素主要以無機鹽形式在腸道被吸收,濃度約為20 mmol/L[11]。為了模擬大豆肽鈣螯合物在人體內的穩定性,并為后續分析大豆肽鈣螯合物的性質提供依據,研究了大豆肽鈣螯合物在不同濃度的PBS溶液中的鈣保留率。結果見圖2。
從圖2可以看出,與無機鈣相比,大豆肽鈣螯合物在低濃度的PBS中具有更高的鈣保留率,在10 mmol/L的PBS中,鈣保留率可達74.5%,當PBS為20 mmol/L時,大豆肽鈣螯合物的鈣保留率仍有62.17%,表明大豆肽鈣螯合物在低濃度的PBS中具有更好的穩定性。當PBS的濃度為40~120 mmol/L時,大豆肽鈣螯合物的鈣保留率穩定在50%左右,當繼續增加PBS濃度時,鈣保留率迅速下降,當PBS濃度為200 mmol/L時,鈣保留率低于1%。這表明大豆肽與鈣離子在結合過程中,可能存在低親和性位點和高親和性位點兩類結合位點,這一結果與張曉維[12]的報道相一致。

圖2 大豆肽鈣螯合物與CaCl2在不同濃度磷酸鹽緩沖液中的鈣保留率
2.3 氨基酸組成
為了研究大豆肽中氨基酸組成對大豆肽與鈣離子反應的影響,測定了大豆肽及大豆肽鈣螯合物的氨基酸組成,結果見表1。

表1 大豆肽和大豆肽鈣螯合物的氨基酸組成及含量 %
由表1可知,大豆肽與鈣反應后,谷氨酸含量由21.70%增加到35.69%,天冬氨酸含量從12.63%增加到14.14%,這兩種氨基酸的含量大幅增加,可能是由于谷氨酸和天冬氨酸均屬于酸性氨基酸,其側鏈基團均含有—COOH,能夠提供鈣離子結合位點,因此在螯合反應過程中有重要作用。這一結果與王小林[13]、崔宇[14]等的研究相一致。
2.4 相對分子質量分布
分別測定了大豆肽、大豆肽鈣螯合物及大豆肽鈣螯合物經0.2 mol/L的PBS脫鈣后的螯合肽的相對分子質量,結果見表2。

表2 大豆肽、大豆肽鈣螯合物和螯合肽的相對分子質量分布 %
由表2可知,77.85%的大豆肽相對分子質量小于1 kDa,超過50%的大豆肽相對分子質量小于0.5 kDa。與大豆肽相比,81.81%的螯合肽相對分子質量小于1 kDa,有顯著提高。而相對分子質量在1~3 kDa的螯合肽占比減少,處于3~5 kDa的螯合肽則有所增加,表明與鈣離子螯合能力較強的大豆肽相對分子質量主要集中在小于1 kDa。與螯合肽相比,大豆肽鈣螯合物的相對分子質量則明顯向高相對分子質量范圍遷移,如相對分子質量處于5~10 kDa的占比提高了11.07個百分點,處于3~5 kDa的占比提高了6.28個百分點,處于1~3 kDa的占比提高了13.75個百分點,而小于1 kDa的相對分子質量占比有明顯的下降,表明大豆肽鈣螯合物具有更高的相對分子質量。
2.5 大豆肽鈣螯合物在不同pH條件下的穩定性
螯合肽與大豆肽鈣螯合物的相對分子質量分布存在明顯的差異,通過表征不同pH條件下的相對分子質量分布可以說明大豆肽鈣螯合物在不同pH條件下的穩定性,結果見圖3。

圖3 不同pH條件處理后大豆肽鈣螯合物的相對分子質量分布圖
從圖3可以看出,大豆肽鈣螯合物在各pH條件下的相對分子質量分布沒有明顯差異,且與所制備的大豆肽鈣螯合物的相對分子質量分布情況較為一致,表明大豆肽鈣螯合物在各pH條件下均有良好的穩定性,不同pH條件下均沒有發生較大程度的解離。
2.6 Zeta電位
目前的研究認為鈣離子與多肽的結合位點主要是游離氨基和游離羧基,在反應過程中可能導致表面電荷性質的改變,因此通過Zeta電位分析可以反映鈣離子與大豆肽作用的情況。Zeta電位結果顯示,大豆肽平均電位為-37.73 mV,在與鈣離子結合后,電負值顯著下降至-12.32 mV,表明大豆肽與鈣離子結合的過程中大豆肽表面所帶電荷明顯減少,說明大豆肽與鈣離子形成了新的化合物。
2.7 XRD分析
分別對大豆肽、氯化鈣及大豆肽鈣螯合物進行XRD分析,結果如圖4所示。

圖4 CaCl2、大豆肽及大豆肽鈣螯合物的XRD圖譜
從圖4可以看出,CaCl2在XRD圖譜中有明顯的特征衍射峰,而大豆肽僅在20°時有1個較寬的衍射峰。在大豆肽與CaCl2反應后,CaCl2的特征衍射峰消失,同時,大豆肽鈣螯合物在20°的衍射峰強度有所下降,峰寬收窄,且衍射峰向右偏移至22.5°,同時在42.5°處出現1個微弱的衍射峰,表明大豆肽與鈣離子發生了化學反應,形成了新的化合物。
2.8 DSC分析(見圖5)

圖5 大豆肽及大豆肽鈣螯合物的DSC分析
從圖5可以看出,大豆肽在136.60℃處有1個吸熱峰,該吸熱峰為大豆肽的化學鍵斷裂導致的,鍵能為223.51 J/g,在鈣離子與大豆肽發生螯合反應后,該吸熱峰向右偏移至159.58℃,鍵能為149.81 J/g,吸熱峰值的升高表明大豆肽鈣螯合物具有更好的熱穩定性,而鍵能的降低是由于大豆肽的化學鍵受到了鈣的影響。
2.9 TGA分析(見圖6)

圖6 大豆肽及大豆肽鈣螯合物的TGA曲線
從圖6可以看出,大豆肽及大豆肽鈣螯合物都出現了3個失重區,溫度范圍分別位于50~120℃、120~350℃、350~900℃。王飛鏑[15]研究認為在50~120℃范圍內的失重對應的主要為可凍結水(自由水和束縛水),這部分水位于肽鏈外側,最容易失去。而處于120~350℃范圍內的失重主要是氫鍵以及肽鏈上不同位置的化學鍵的斷裂[16],在這一失重區,大豆肽失重率約為40%,而大豆肽鈣螯合物的失重率約為30%,大豆肽的失重率高于大豆肽鈣螯合物的失重率,同時,在這一區間,大豆肽鈣螯合物的失重溫度高于大豆肽的失重溫度。表明大豆肽鈣螯合物相較于大豆肽具有更好的熱穩定性,這一結果也與DSC的結果相一致。當溫度超過350℃時,大豆肽及大豆肽鈣螯合物的失重則主要表現為灰化的過程。
3 結 論
大豆肽在水解4 h條件下,水解度可達19.84%,大豆肽與鈣離子進行螯合反應,鈣結合量為53.03 mg/g,且制備的大豆肽鈣螯合物在低濃度磷酸鹽存在時仍具有良好的穩定性,在磷酸鹽緩沖液濃度為10 mmol/L時,鈣保留率為74.5%,20 mmol/L磷酸鹽緩沖液中鈣保留率為62.17%。具有較高螯合能力的大豆肽的相對分子質量主要集中在小于1 kDa的范圍內。谷氨酸和天冬氨酸是參與大豆肽鈣螯合反應重要的氨基酸。大豆肽鈣螯合物在各pH條件下均沒有發生明顯的解離現象,表明其在不同pH條件下均具有較好的穩定性。Zeta電位分析表明,大豆肽與鈣離子發生反應后,其表面的電負性有顯著的下降。大豆肽鈣螯合物在XRD圖譜中的衍射峰有所收窄,且氯化鈣的特征峰消失,表明大豆肽與鈣離子形成了新的化合物。對大豆肽及大豆肽鈣螯合物的DSC分析和TGA分析表明,大豆肽與鈣離子發生螯合反應后,生成的大豆肽鈣螯合物具有比大豆肽更好的熱穩定性。

