納濾和反滲透組合回收鹽湖提鋰尾液中鋰的研究
董守龍,楊尚明,張世春,申朝貴,馬曉平
(青海鋰業有限公司,青海格爾木816000)
鋰作為一種重要的能源金屬,被廣泛應用于新能源、醫藥、航天航空、制冷劑等領域,以鋰為原料制備的高新技術產品的開發和應用已深入人們的日常生活[1-2]。隨著世界鋰鹽產品的需求量逐年增加,對LiOH和Li2CO3等鋰鹽原材料的需求也在不斷地攀升[3]。
中國是一個鋰資源大國,鋰資源主要分布于青海和西藏的鹽湖中[4],鹽湖鹵水中鎂鋰比普遍較高是中國鹽湖提鋰過程所面臨的困難之一[5]。從鹽湖鹵水中提鋰的方法主要有離子篩吸附法、溶劑萃取法、浸取煅燒法、離子選擇膜分離法等,其中浸取煅燒法和離子選擇膜分離法應用較為成熟[6-8]。
鹽湖提鋰后的尾液中仍含有大量的鋰,直接外排至鹽田會造成鋰資源的浪費,并且會對鹽湖系統造成破壞,而降低提鋰尾液中的鎂鋰比是回收提鋰尾液中鋰的關鍵。筆者采用納濾和反滲透組合的方式,成功地回收了電滲析提鋰后尾液中的鋰,探討了最佳操作條件,并制備了電池級Li2CO3。
1 實驗部分
1.1 原料與儀器
原料:提鋰尾液(主要離子含量見表1);NaOH(分析純);Na2CO3(分析純)。
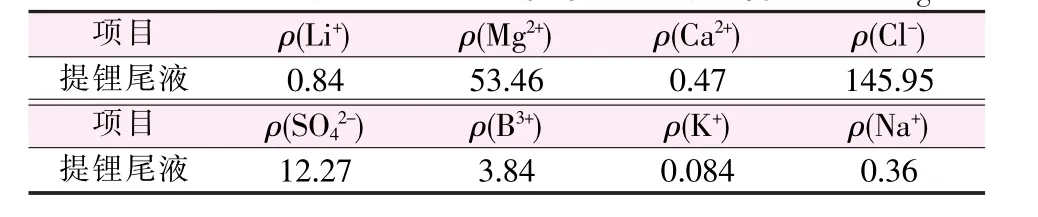
表1 提鋰尾液中主要離子含量 g/L
儀器:AB204-S電子天平;SevenCompact pH計;S2-AAS3000原子吸收光譜儀;納濾實驗設備,納濾膜及反滲透膜;DHG-9053A干燥箱。
1.2 實驗方法
以某公司提供的7種型號的卷式納濾膜為納濾元件對提鋰尾液進行納濾實驗,分別檢測富鋰液相(納濾透過液)和濃液(納濾截留的Mg2+含量較高的液相)中的主要離子含量。探討了過濾壓力、實驗溫度和提鋰尾液的稀釋倍數對提鋰尾液中鎂鋰納濾分離效果的影響,選擇納濾效果最佳的納濾膜。以納濾效果最佳的納濾膜為納濾元件,在較優操作條件下采用二級納濾對提鋰尾液進行鎂鋰分離,再通過反滲透對富鋰液相進行濃縮,濃縮后的富鋰液相用于生產碳酸鋰,富含其他離子的濃液則外排至尾液池,經過蒸發濃縮排入鹽田再回收利用。
2 結果與討論
2.1 納濾膜選擇及操作參數探討
2.1.1 納濾膜選擇
取20 L稀釋6倍的提鋰尾液,控制實驗溫度為25℃、過濾壓力為3 MPa,采取單級納濾,考察7種型號的納濾膜對提鋰尾液鎂鋰分離的性能,實驗結果見圖1、圖2。圖1為7種型號納濾膜對Li+回收率和Mg2+截留率。從圖1看出,1號納濾膜對Mg2+截留率和Li+回收率最高,這對于降低提鋰尾液中的鎂鋰比和回收鋰資源非常關鍵。圖2為7種型號納濾膜的平均通量和通量變化曲線。從圖2看出,1號納濾膜平均通量較低,并且隨著實驗的進行其通量變化較小;6號納濾膜平均通量和通量變化都較大,而Mg2+截留率和Li+回收率都較低。以降低鎂鋰比和回收鋰資源為出發點,選擇1號納濾膜作為實驗對象。
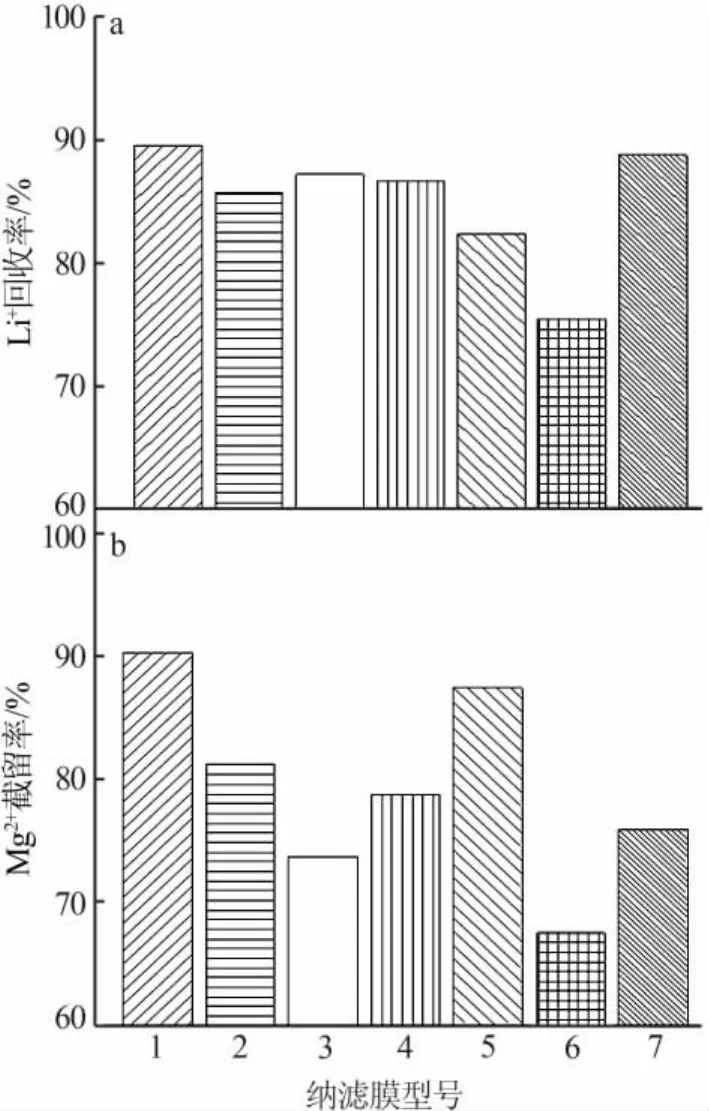
圖1 不同型號納濾膜對Li+回收率(a)和Mg2+截留率(b)
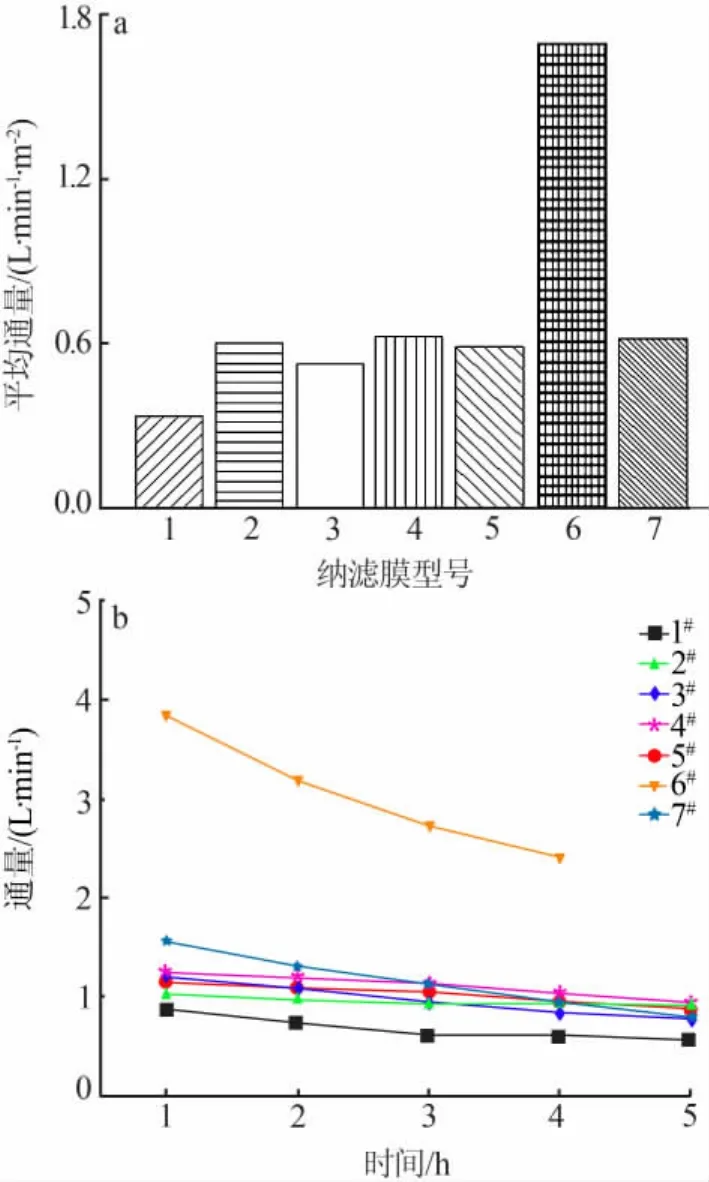
圖2 不同型號納濾膜的平均通量(a)和通量變化曲線(b)
2.1.2 操作參數探討
為探討納濾過程的最佳操作條件,以1號膜為實驗對象,在膜要求的范圍內分別取不同過濾壓力、實驗溫度和提鋰尾液稀釋倍數進行單級納濾實驗,考察各因素對納濾效果的影響。
1)過濾壓力的影響。取20 L稀釋6倍的提鋰尾液,控制實驗溫度為25℃,在不同過濾壓力下進行納濾實驗,考察過濾壓力對Mg2+截留率、Li+回收率、平均通量的影響,結果見圖3。從圖3看出,隨著過濾壓力增大,Mg2+截留率降低、Li+回收率和平均通量都有所提高。這是因為,一價Li+可以相對容易地穿過膜,隨著其通量增大Li+回收率增大,而其通量增大后膜表面的Mg2+濃度稍微增大,壓力增大時Mg2+透過率稍微增大,導致 Mg2+截留率降低[9]。
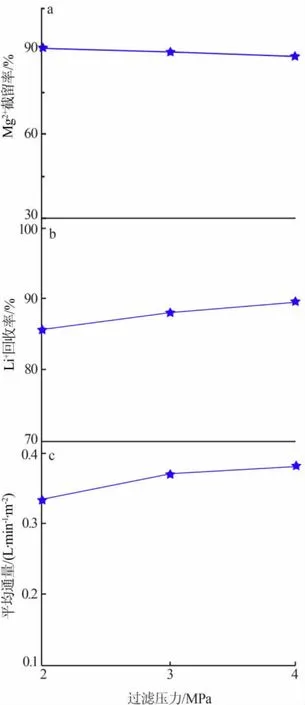
圖3 過濾壓力對納濾效果的影響
2)實驗溫度的影響。取20 L稀釋6倍的提鋰尾液,控制過濾壓力為4 MPa,在不同實驗溫度下進行納濾實驗,考察實驗溫度對Mg2+截留率、Li+回收率、平均通量的影響,結果見圖4。從圖4a、b看出,Mg2+截留率和Li+回收率隨著溫度的升高基本不變。由圖4c看出,平均通量隨著溫度的升高而增大。這是因為,在較高溫度下水分子活性增強,通量稍有增加。根據冷卻水用量和膜性能的要求,控制實驗溫度為35℃。
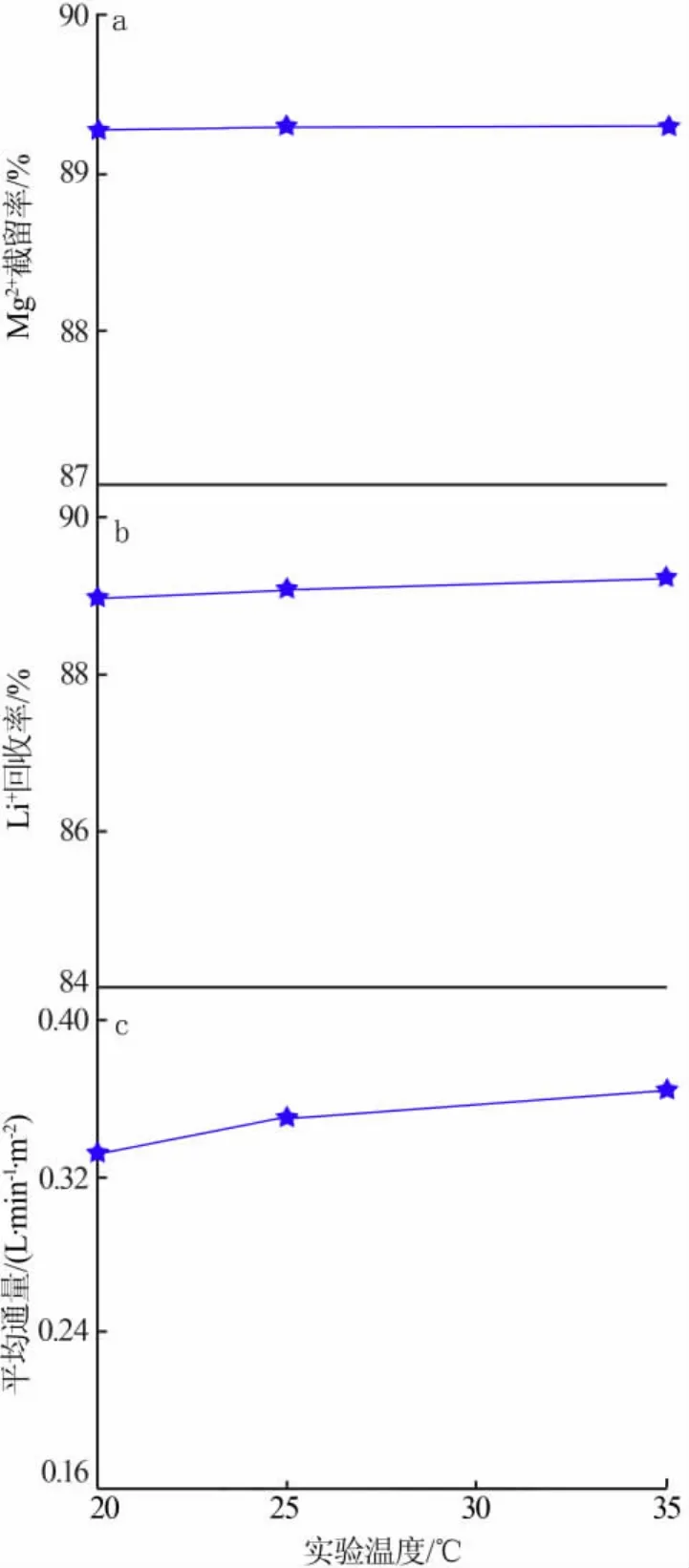
圖4 實驗溫度對納濾效果的影響
3)稀釋倍數的影響。取3 L提鋰尾液,分別稀釋6、7、8倍,控制實驗溫度為35℃、過濾壓力為4 MPa進行納濾實驗,考察提鋰尾液稀釋倍數對Mg2+截留率、Li+回收率、平均通量的影響,結果見圖5。從圖5a、c看出,Mg2+截留率和平均通量隨著提鋰尾液稀釋倍數的增加而增大。從圖5b看出,Li+回收率隨著提鋰尾液稀釋倍數的增加而降低。這是因為,提鋰尾液稀釋倍數增大,液相中離子濃度降低,導致納濾膜濃水側的滲透壓降低,有效分離壓力增大,因此平均通量增大。提鋰尾液稀釋倍數越大,納濾膜兩側Li+滲透壓越低,Li+透過率有所降低,因此Li+回收率降低。
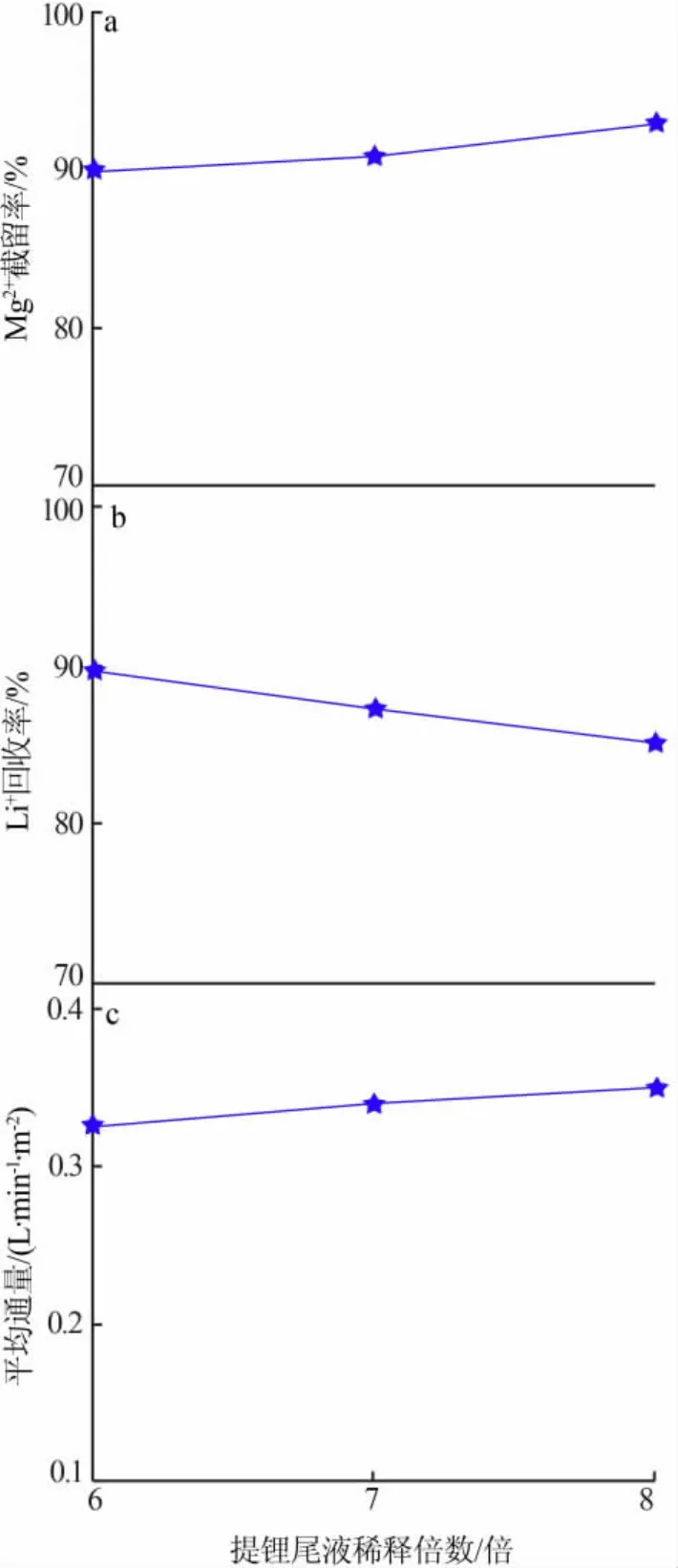
圖5 提鋰尾液稀釋倍數對納濾效果的影響
綜合以上實驗結果看出,過濾壓力、實驗溫度及提鋰尾液稀釋倍數都對納濾效果有影響。實驗選擇過濾壓力為4 MPa、提鋰尾液稀釋倍數為6倍、實驗溫度為35℃。
2.2 二級納濾及反滲透濃縮
稀釋6倍的提鋰尾液首先進行第一次納濾,分離出一部分Mg2+,得到富鋰液相;將Mg2+含量較高的濃液外排至鹽田蒸發濃縮后回收利用。富鋰液相繼續進行二級納濾,進一步分離其中的Mg2+,得到富鋰液相。富鋰液相進行反滲透(RO)濃縮;濃液用于稀釋提鋰尾液。二級納濾和反滲透組合回收提鋰尾液中的鋰工藝流程圖見圖6。
1)二級納濾結果。將一級納濾所得富鋰液相進行二級納濾,對一、二級納濾分離所得富鋰液相中的主要離子含量進行檢測分析,結果見表2。從表2看出,二級納濾所得富鋰液相中的鎂鋰質量比降低至13.5,說明納濾膜對分離提鋰尾液中的Mg2+具有很好的截留效果。
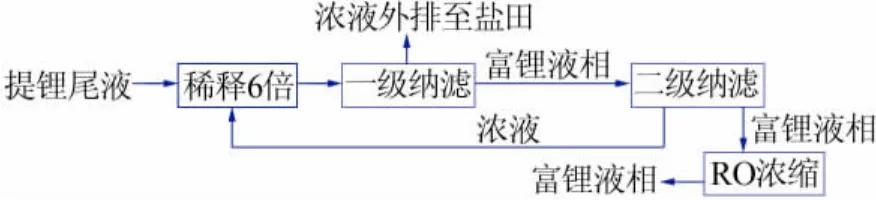
圖6 二級納濾和反滲透組合回收提鋰尾液中的鋰工藝流程圖
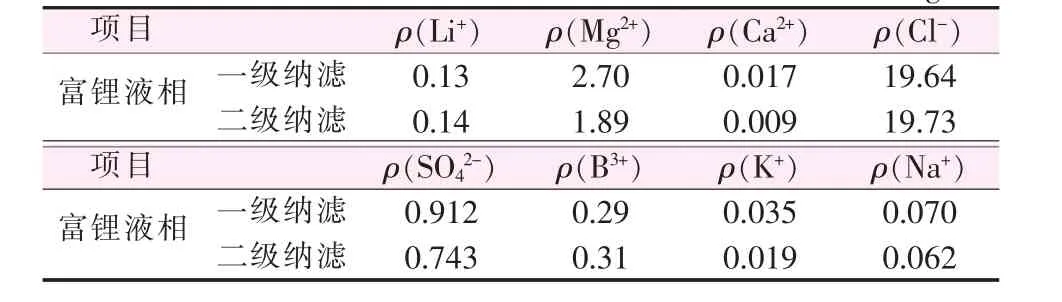
表2 一級和二級納濾透過液中的主要離子含量 g/L
2)反滲透濃縮結果。二級納濾所得富鋰液相經過反滲透濃縮3倍,測量濃縮所得富鋰液相中的主要離子含量,結果見表3。由表3看出,反滲透完成后的液相中鎂鋰比為13.8,Li+質量濃度為0.39 g/L。

表3 反滲透濃縮液中的主要離子含量 g/L
綜合以上實驗結果看出,二級納濾和反滲透組合工藝可以將提鋰尾液中的鎂鋰質量比降低至13.8,所得富鋰液相中Li+質量濃度為0.39 g/L。該富鋰液相可以作為制備Li2CO3的原料鹵水。
2.3 Li2CO3的制備
將反滲透濃縮制備的富鋰液相在室外自然條件下蒸發濃縮,待Li+質量濃度上升至5 g/L左右時過濾分離出其中的固相結晶鹽,檢測液相中的主要離子含量,結果見表4。
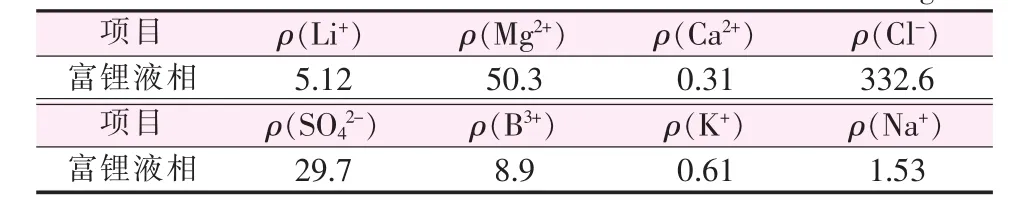
表4 反滲透濃縮液自然蒸發濃縮后的主要離子含量 g/L
將分析純NaOH配制成質量分數為30%的燒堿溶液,與上述自然蒸發濃縮后的富鋰液相按照n(Mg2+)∶n(OH-)=1∶2.25 反應生成 Mg(OH)2沉淀,除去富鋰液相中的Mg2+。控制反應溫度為55℃、攪拌轉速為65 r/min。反應結束后固液分離得富鋰液相。
將分析純Na2CO3配制成質量分數為20%的純堿溶液,與上述除鎂后的富鋰液相按照n(Ca2+)∶n(CO32-)=1∶1.25 在相同條件下反應生成 CaCO3沉淀,除去富鋰液相中的Ca2+。反應結束后固液分離,所得富鋰液相中的主要離子含量見表5。從表5看出,除鈣鎂后的富鋰液相中的Mg2+、Ca2+含量很低。但是,采用該方法除去富鋰液相中鎂,消耗的燒堿量較大,經濟成本較高。可以采用電滲析的方法對富鋰液相中的Mg2+進行分離,然后將富鋰液相作為生產Li2CO3的原料。
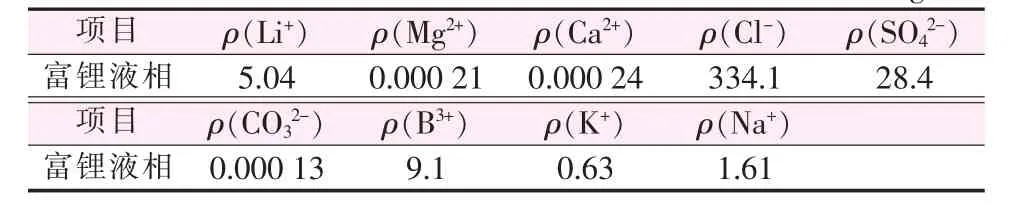
表5 除鈣鎂后富鋰液相中的主要離子含量 g/L
取3 L除鈣鎂后的富鋰液相,與質量分數為20%的純堿溶液按照n(Li+)∶n(CO32-)=2∶1.25 在 85 ℃條件下反應制備Li2CO3,控制攪拌轉速為65 r/min、反應時間為45 min,反應至20 min時向反應釜內加入300mL質量分數為15%的EDTA-2Na溶液。反應結束后固液分離得到初級Li2CO3,將初級Li2CO3與85℃的RO水按照固液質量比為1∶6漿洗2次,然后干燥,得到電池級Li2CO3。檢測電池級Li2CO3中的主要離子含量,并與YS/T 582—2013《電池級碳酸鋰》作對比,結果見表6。由表6看出,以提鋰尾液經納濾和反滲透組合工藝制備的富鋰鹵水為原料,制備的碳酸鋰產品指標達到電池級碳酸鋰行業標準的要求。
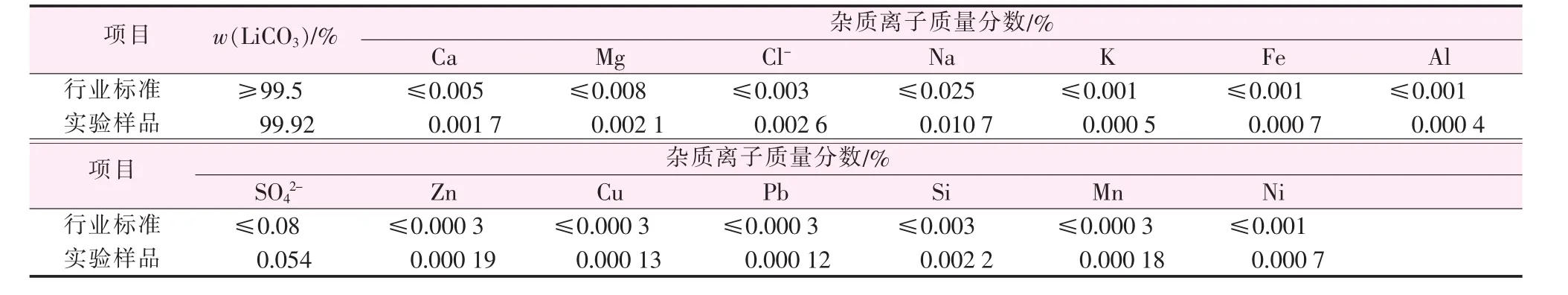
表6 制備的電池級碳酸鋰樣品分析結果及與行業標準對比
3 結論
采用納濾和反滲透組合工藝成功地回收了提鋰尾液中的鋰。考察了過濾壓力、實驗溫度和提鋰尾液稀釋倍數對提鋰尾液中鎂鋰分離的效果,得到較優操作條件:過濾壓力為4 MPa、提鋰尾液稀釋倍數為6倍、實驗溫度為35℃。采用二級納濾對提鋰尾液進行鎂鋰分離,再通過反滲透對富鋰液相進行濃縮,得到鎂鋰質量比為13.8、鋰離子質量濃度為0.39 g/L的富鋰液相。富鋰液相經過濃縮除雜,然后與純堿反應,可制備電池級碳酸鋰。其中作為電池級碳酸鋰生產原料的富鋰液相的除鎂過程,可以采用電滲析的方法,比傳統的Mg(OH)2沉淀法成本更低。

