芽孢桿菌Bacillus sp.dwc-2對模擬地下水中U(Ⅵ)的還原行為研究
王 靜,劉 軍,2,趙長菘,涂 鴻,賀含毅,楊吉軍,廖家莉,楊遠友,*,劉 寧
(1.四川大學 原子核科學技術研究所,輻射物理及技術教育部重點實驗室,四川 成都 610064;2.成都理工大學 核技術與自動化工程學院,四川 成都 610059)
鈾是最重要的核能資源之一,具有放射性和化學毒性[1]。鈾的主要化學價態為6價,在溶液中的溶解度大,易遷移至生物圈。U(Ⅵ)遷移時會與環境介質中的微生物等發生相互作用,如沉淀、氧化還原等反應[2-5],當U(Ⅵ)被還原為U(Ⅳ)時,鈾的溶解度和遷移率降低,從而減弱鈾的遷移。因此關注環境中鈾的生物還原行為具有重要意義。
鈾的生物還原行為近年來受到廣泛重視。梁君等[6]研究發現,絲狀真菌黑曲霉還原U(Ⅵ)為U(Ⅳ),且U(Ⅳ)產物是單核U(Ⅳ)原子緊密包圍的輕元素殼組成的形態。Stirling等[7]發現硫酸鹽還原菌代謝過程中產生的H2S會參與并促進鈾的生物還原;Zhou等[8]的研究表明,Fe(Ⅲ)金屬還原菌產生的電子參與了鈾的生物還原;Newsome等[9]報道了在乳酸鈉和乙酸存在時,U(Ⅵ)從鐵還原菌得到電子從而被還原。此外,Ding等[10]發現了芽胞桿菌Bacillussubtilis胞外表面復合物之間斥力抑制鈾的還原過程;Zhang等[11]也認為U(Ⅵ)的生物還原受形成的復合體類型的影響。
芽胞桿菌Bacillussp.dwc-2是從中國西南地區某處典型土壤中分離出的一種優勢菌。本研究小組[12]曾初步探討了厭氧條件下Bacillussp.dwc-2還原去離子水中U(Ⅵ)的行為。本文擬在此基礎上進一步在厭氧條件下研究Bacillussp.dwc-2對模擬地下水中U(Ⅵ)的還原行為,重點考察時間、地下水中主要無機陰離子、腐殖酸(HA)以及富里酸(FA)對芽孢桿菌還原鈾的影響,并通過EDS、SAED、TEM、XPS對還原機制進行初步探討,以便在接近真實環境條件下了解微生物對U(Ⅵ)的還原行為與機理。
1 實驗
1.1 主要試劑與儀器
UV-2450型紫外可見分光光度計,日本島津;ZDX-35BI型座式壓力蒸汽滅菌鍋,上海申安醫療器械廠;TG16G離心機,湖南凱達科學儀器有限公司;pHs-3C精密pH計,上海精密科學儀器有限公司雷磁儀器廠;ZQLY-180GF振蕩培養箱,上海知楚儀器有限公司;LSHZ-300型恒溫冷凍水浴振蕩器,太倉市豪誠實驗儀器制造有限公司;DELLIX型真空手套箱,成都德力斯實業有限公司。
1.2 Bacillus sp.dwc-2對U(Ⅵ)的還原
培養分離Bacillussp.dwc-2后,以4 000 r/min離心5 min,然后用0.05 mol/L NaCl溶液洗滌3次,最后將洗凈的Bacillussp.dwc-2放入真空手套箱中備用。
將配置好的250 mL UO2(NO3)2·6H2O溶液(U(Ⅵ)溶液)加入500 mL燒杯中,并用0.1 mol/L NaOH或HNO3調節溶液pH值為7.0,再用N2(99.999%)除氧30 min,將處理后的溶液移入500 mL厭氧培養瓶中,放置在真空手套箱內,使氧含量低于1 mg/L,隨即加入一定質量的Bacillussp.dwc-2,在恒溫振蕩器上以150 r/min的轉速振蕩一定時間,之后以10 000 r/min離心分離,測量上清液中U(Ⅵ)的濃度,下層沉淀物經過冷凍干燥后進行表征。
1.3 材料表征
將冷凍干燥后的下層沉淀物在厭氧手套箱中制作為材料表征用樣品。樣品在充滿氮氣的環境中送至檢測中心。采用Escalab 250Xi X射線光電子能譜(XPS)儀進行U價態分析;采用透射電子顯微鏡(TEM)和區域電子衍射(SEAD)分析樣品的內部結構。
1.4 數據處理
分析還原反應前后溶液中U(Ⅵ)的含量,按式(1)計算還原率R:
R=(c0-ct-ca)/c0×100%
(1)
其中:c0和ct分別為還原反應前和還原反應進行到t時刻溶液中U(Ⅵ)的濃度,mg/L;ca為Bacillussp.dwc-2吸附的總U(Ⅵ)的濃度,mg/L。通過XPS peak 4.1分峰計算U(Ⅳ)、U(Ⅵ)的面積比,從而計算吸附的U(Ⅵ)和還原的U(Ⅳ)占芽孢桿菌總吸附鈾的比值,得到ca和還原的U(Ⅳ)濃度。
2 結果與討論
2.1 Bacillus sp.dwc-2還原U(Ⅵ)的影響因素
1) 時間
1)做好頂層設計,助推實驗室管理制度體系化。設立由單位領導及各相關部門負責人組成的實驗室安全管理委員會,按專業類別下設實驗室安全專家咨詢組,例如:化學、生物、輻射、環境保護、特種設備、職業健康等安全專家咨詢組;為委員會評價和審核各項管理制度、安全手冊、規范及細則等提供專業性意見或建議,促進實驗室管理制度體系化發展。
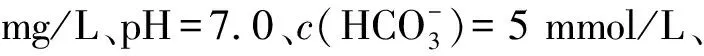
2) 無機陰離子
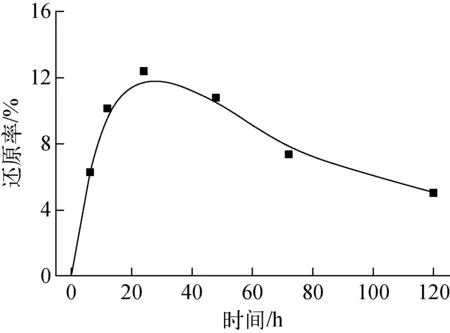
圖1 時間對Bacillus sp.dwc-2還原U(Ⅵ)的影響Fig.1 Effect of time on U(Ⅵ) reduction by Bacillus sp.dwc-2
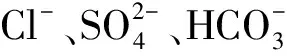
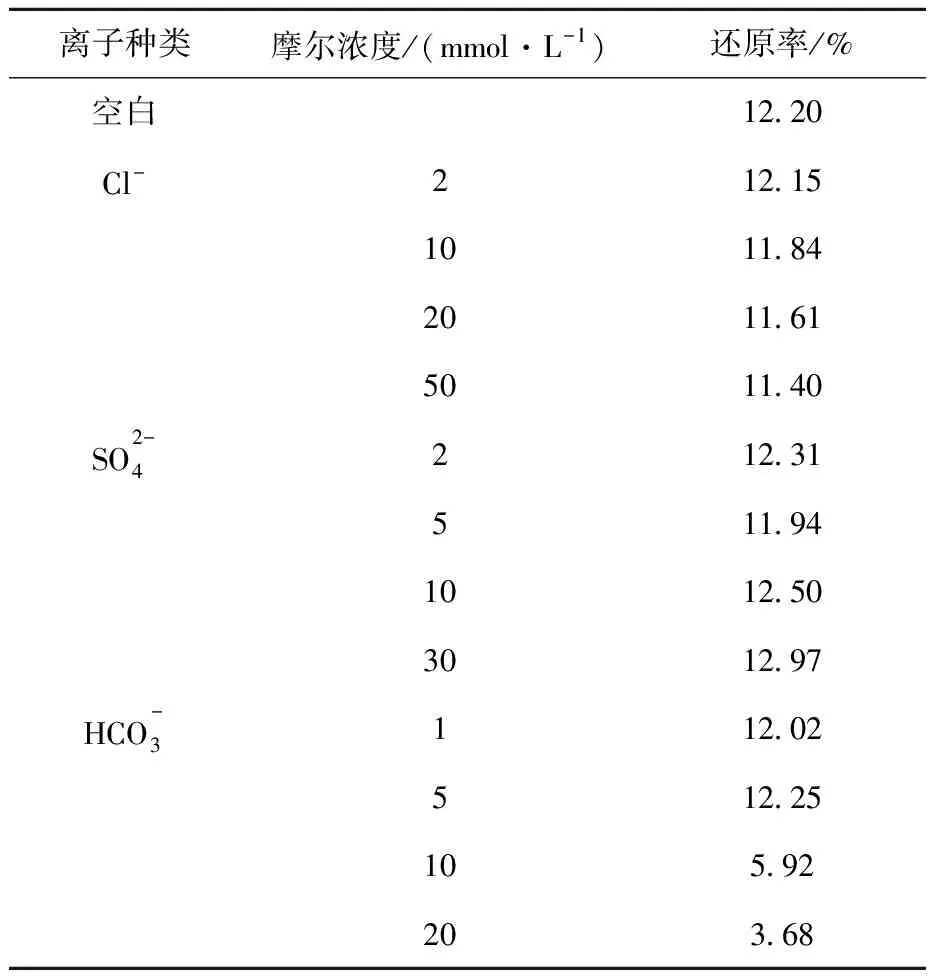
表1 無機陰離子對Bacillus sp.dwc-2還原U(Ⅵ)的影響Table 1 Effect of anion on U(Ⅵ) reduction by Bacillus sp.dwc-2
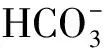
3) 腐殖酸
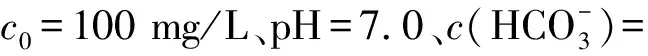
4) 富里酸
在與腐殖酸因素研究的相同條件下,富里酸(FA)濃度(0~200 mg/L)對Bacillussp.dwc-2還原U(Ⅵ)的影響示于圖3。由圖3可見,在0~25 mg/L濃度范圍內,Bacillussp.dwc-2對U(Ⅵ)的還原率隨FA濃度的升高而增加,最大還原率為16.2%。此后繼續增大FA濃度,Bacillussp.dwc-2對U(Ⅵ)的還原率有所降低,200 mg/L時還原率只有5.3%。相對于HA,FA對Bacillussp.dwc-2還原U(Ⅵ)的促進作用大,可能是因為HA攜帶的羧基較FA多,羧基與U(Ⅵ)離子形成新的配合物,配合作用成為主要反應,從而減弱了Bacillussp.dwc-2對U(Ⅵ)的還原。
2.2 還原U(Ⅵ)后的Bacillus sp.dwc-2樣品的表征
1) XPS分析
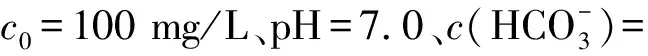
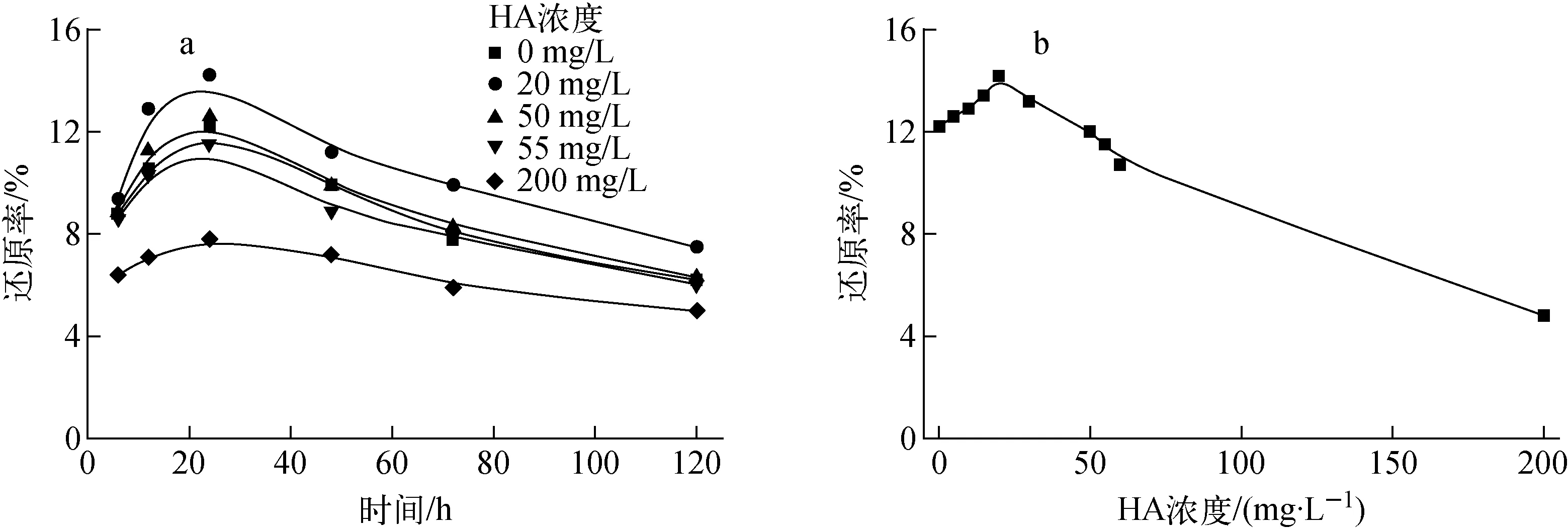
圖2 HA濃度對Bacillus sp.dwc-2還原U(Ⅵ)的影響Fig.2 Effect of HA concentration on U(Ⅵ) reduction by Bacillus sp.dwc-2
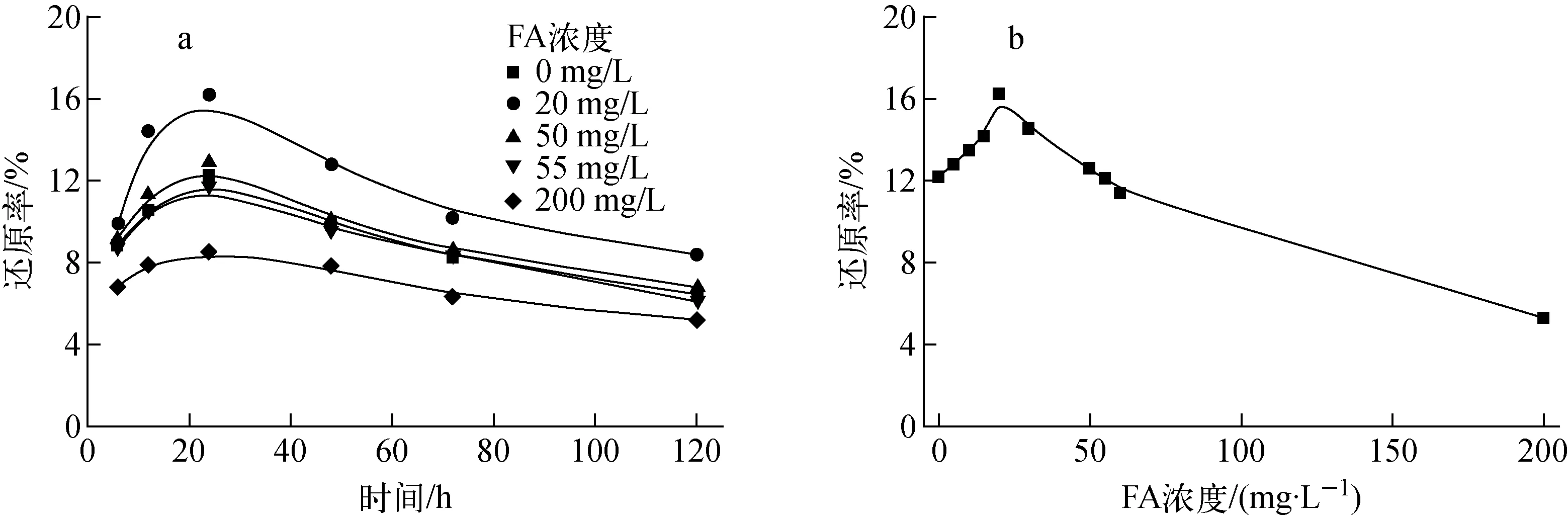
圖3 FA濃度對Bacillus sp.dwc-2還原U(Ⅵ)的影響Fig.3 Effect of FA concentration on U(Ⅵ) reduction by Bacillus sp.dwc-2
圖4a、b為U 4f的XPS譜。所有數據均參照文獻[10,12,21-22]進行解析處理,分析結果準確。XPS譜中的U 4f7/2U(Ⅵ)和U 4f5/2U(Ⅵ)峰值中心點位于(391.9±0.2) eV和(381.5±0.2) eV,U 4f7/2U(Ⅳ)和U 4f5/2U(Ⅳ)峰值中心點位于(390.8±0.2) eV和(380.1±0.2) eV。已有研究[23]表明,位于381.5 eV處的特征峰是≡SOUO2+,可知羥基(≡SO-)與U(Ⅵ)形成了配合物,表明U(Ⅵ)離子的吸附主要是由于芽孢桿菌表面上羥基的配合作用。上述結果顯示芽孢桿菌還原U(Ⅵ)過程中吸附和還原同時存在。

圖4 U(Ⅵ)還原后U 4f(a,b)、C 1s(c,d)、O 1s(e,f)的XPS譜Fig.4 XPS pattern of U 4f (a, b), C 1s (c, d), O 1s (e, f) after U(Ⅵ) reduction
由圖4a、b可知,不加HA和FA時,最大還原率為12.2%。HA和FA濃度為25 mg/L時,U(Ⅳ)與Bacillussp.dwc-2吸附的總U(Ⅵ)的峰面積比最大,此時還原率最大。最大還原率分別為14.2%和16.2%。HA和FA濃度繼續增大,該比值下降,還原率有所下降。


2) TEM-EDS、SAED分析
3 結論
1)Bacillussp.dwc-2對U(Ⅵ)在24 h時達到最大還原率12.2%,HA濃度和FA濃度為25 mg/L時,Bacillussp.dwc-2對U(Ⅵ)的最大還原率分別為14.2%和16.2%。
3) 低濃度的HA和FA在U(Ⅵ)的生物還原中是電子載體,促進U(Ⅵ)的生物還原;隨HA和FA濃度的增加,HA、FA在U(Ⅵ)離子表面形成致密的腐殖層,抑制了鈾酰離子與菌體間電子的轉移,減弱了U(Ⅵ)的還原。相對于FA,HA對U(Ⅵ)的還原影響較弱。
4) TEM-SAED和XPS證實了還原過程中U(Ⅳ)的存在。
上述結果有助于進一步了解真實地下水環境中微生物還原U(Ⅵ)的行為。

