計算機輔助解析甲氨蝶呤/聚乙烯亞胺納米粒組裝機制與內在結構
雷遠正 孫丹云 湯悅
[摘要] 目的 納米粒的組裝機制與內部結構的表征是納米粒研究領域中的難點,本文擬通過計算機模擬技術分析甲氨蝶呤/聚乙烯亞胺納米組裝體的組裝機制與內在結構。 方法 通過分子對接、混合能計算與耗散動力學模擬等計算機模擬技術計算甲氨蝶呤/聚乙烯亞胺納米組裝體混合體系中的分子間作用力、混合能和介觀模擬結構。結果 甲氨蝶呤與聚乙烯亞胺之間的分子間作用力為-12.98 kcal/mol,主要由靜電作用、氫鍵作用和疏水作用組成;經過200 ns的耗散動力學模擬,甲氨蝶呤與聚乙烯亞胺形成了核殼結構的納米聚集體。 結論 甲氨蝶呤/聚乙烯亞胺納米組裝體是以甲氨蝶呤分子為內核,聚乙烯亞胺分子為外殼的核殼結構納米粒,而其組裝的驅動力則主要由甲氨蝶呤的兩個羧基與聚乙烯亞胺的氨基之間的強靜電作用力提供。
[關鍵詞] 納米粒;分子對接;介觀模擬;甲氨蝶呤
[中圖分類號] R944? ? ? ? ? [文獻標識碼] A? ? ? ? ? [文章編號] 1673-7210(2020)03(a)-0008-04
[Abstract] Objective The assembly mechanism and characterization of the internal structure of nano-drug are difficult problems in the field of nano-drug research. In this paper, the assembly mechanism and internal structure of Methotrexate/Polyethyleneimine nano-assembly were analyzed by computer simulation technology. Methods Computer simulation techniques such as molecular docking, mixing energy calculation and dissipation dynamics simulation were used to calculate intermolecular forces, mixing energy and mesoscopic simulation structures in the mixture system of Methotrexate/Polyethylenimine nanocomposites. Results The intermolecular force between methotrexate and polyethyleneimine was -12.98 kcal/mol, mainly composed of electrostatic action, hydrogen bond action and hydrophobic action. After 200 ns of dissipation dynamics simulation, methotrexate and polyethyleneimine formed a core-shell structure of nano-aggregate. Conclusion Methotrexate/Polyethyleneimine nanoassembly is core-shell nanoparticles with methotrexate as core and polyethyleneimine as shell. The driving force of the assembly is mainly provided by the strong electrostatic interaction between the two carboxyl groups of methotrexate and the amino group of polyethyleneimine.
[Key words] Nanomedicine; Molecular docking; Mesoscopic simulation; Methotrexate
甲氨蝶呤(methotrexate,MTX)是臨床上常用的一種細胞周期特異性細胞毒性藥物,可用于包括急性白血病等多種惡性腫瘤的治療[1-3]。傳統的MTX口服片,由于MTX與消化道上皮細胞的長時間接觸,極易引起上皮細胞的增殖抑制,介導胃炎、消化道出血等嚴重的胃腸副作用[4]。本課題組前期通過聚乙烯亞胺(polyethyleneimine,PEI)與MTX的自組裝成功構建了超高載藥性能的MTX口服納米制劑,但其組裝機制仍有待進一步探索[5]。
分子間相互作用力是兩個分子特異性非共價鍵識別的關鍵[6-7]。在分子識別過程中,空間立構、靜電作用及疏水作用發揮著重要作用[8]。隨著計算化學、計算機科學與藥學等交叉學科的快速發展,計算機輔助技術已被廣泛的應用于新藥研發的藥物篩選、藥物設計與藥理作用機制的分析中[9-12]。本課題組通過計算機模擬已成功實現了對納米組裝機制、載藥機制、響應機制與藥物釋放機制的模擬[13-15]。受此啟發,本研究通過Autodock 4.2軟件對PEI與MTX之間的分子間作用力進行分析[16],并通過耗散粒子動力學(dissipative particle dynamics,DPD)[17-20]模擬分析PEI與MTX組裝過程,從而解析MTX/PEI納米粒的組裝機制。
1 資料與方法
1.1 3D空間構象的準備與優化
在Drugbank數據庫中下載MTX的分子結構式,在Matreilas Studio 2016軟件中打開,加氫后,采用Forcite模塊中的Geometry Optimization任務對MTX的3D結構進行能量最小化處理,獲得合理的MTX的3D空間構象。考慮到計算機的計算能力,在Materials Studio 2016中利用分子結構的編輯功能構建n = 20的PEI的分子結構式,并進一步采用Forcite模塊中的Geometry Optimization任務對MTX的3D結構進行能量最小化處理。
1.2 Autodock分子對接
在AutoDockTools 4.2中以受體導入PEI的分子結構,進行加氫和加電荷后以PDBQT格式存儲。隨后以配體導入MTX的分子結構,添加電荷后以PDBQT格式存儲。在準備好配體與受體分子構象后,使用AutoGrid進行能量格點計算,Gird Box大小設置為126×126×126個網格點,每個小網格點的距離為0.0375 nm。采用拉馬克遺傳算法(lamarckian,GA)進行構象搜索,初始種群數設置為100,能量評定最大次數為2 500 000,其他參數采用默認值進行分子對接計算。
1.3 分子間混合能的計算
將優化后的水分子、PEI和MTX分子導入到Materials Studio 2016的工作界面,采用Blends模塊中的Mixing任務,在Compass 2.0力場下進行混合能的模擬計算,模擬質量選擇Fine,其他參數默認。
1.4 DPD介觀模擬
1.4.1 PEI、MTX與水的粗粒化處理? 將PEI、MTX與水分子分別設置為3個DPD粒子,分別命名為P、M和W,粒子半徑設置為6.46 ?魡,分子量設置為54。其中PEI的粒子對應著20個重復的PEI單元,MTX的粒子MTX對應著1個MTX分子,而水分子的粒子Water對應著3個水分子。
1.4.2 珠子間相互作用參數的計算? 取密度ρ = 3,則珠子間相互作用參數aij與Flory-Huggins相互作用參數(χ)之間存在以下線性關系:
基于Blends中計算的Flory-Huggins參數,最終計算出P、M與W珠子間的相互作用參數,并進一步構建DPD力場,用于后續的DPD模型的構建與模擬。
1.4.3 DPD模型的構建與優化? 首先,基于PEI、MTX與水分子的珠子,構建PEI、MTX與Water的介觀分子,隨后按照1∶1∶8的比例構建PEI、MTX與Water的混合模型,其中Length scale項設為6.46 ?魡,Mass Scale項設為54 Amu,Density項設置為3 g/cm3,點擊Build,就可得到水分子和MTX分子和PEI分子的混合分子的介觀模型。并進一步選用構建的DPD力場,對所構建的介觀模型進行優化。得到構象優化后的介觀模型后,基于DPD力場,進一步采用Mesocite模塊進行200 ns的耗散動力學模擬。
2 結果
2.1 PEI、MTX與水分子之間的分子間作用力分析
采用Autodock 4.2軟件,計算PEI、MTX與水分子之間的結合能、分子間作用力、范德華力與靜電作用力。從表1中可見,MTX與PEI之間的分子間作用力最大,為-12.98 kcal/mol,其中靜電作用力貢獻最大,達到了-11.36 kcal/mol,因此其結合到PEI上的結合能也遠大于PEI和水分子結合到PEI上的結合能,達到了-10 kcal/mol。見表1。
進一步對MTX結合至PEI的最低能量構象進行分析。MTX與PEI之間主要通過MTX中的羧基與PEI中的氨基形成靜電作用和氫鍵作用。見圖1。
2.2 PEI、MTX與水分子之間分子間混合能的計算結果
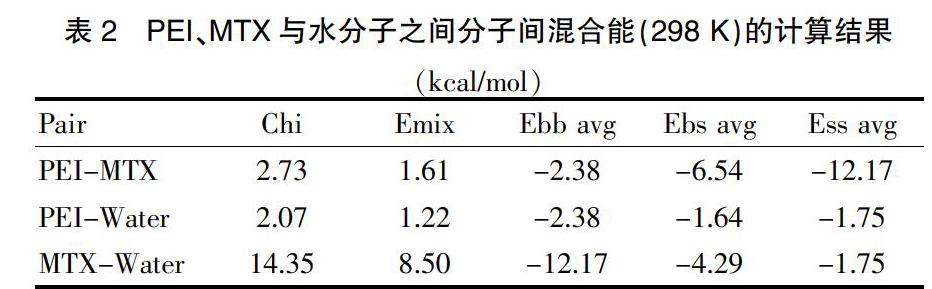
經計算,PEI與MTX之間的混合能為1.61 kcal/mol,遠低于MTX與水分子之間8.50 kcal/mol的混合能大小。見表2。
2.3 組裝體的介觀模擬結果
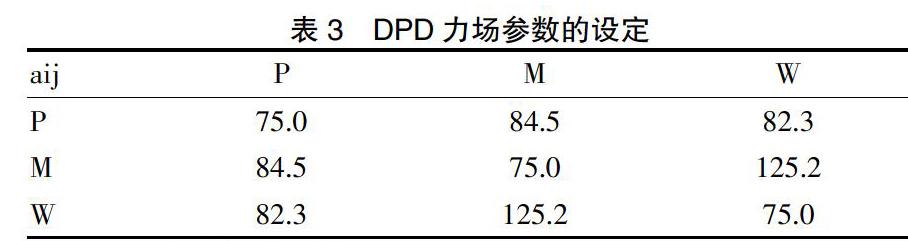
通過Blends模塊計算的Flory-Huggins參數(Chi),將PEI(n = 20)、MTX和3個水分子分別設定為P、M和W等3個珠子,并通過表1中Flory-Huggins參數,進一步計算得到珠子間的DPD排斥參數aij。見表3。隨后,基于珠子,分別構建了分子量為20 000的PEI的介觀分子(約25個珠子)模型,與MTX和Water的介觀分子模型。
進一步以PEI、MTX和水分子1∶1∶8的比例構建了水、MTX和PEI的混合的介觀體系,并基于設定的DPD力場,對其構象優化,獲得了其初始介觀體系。見圖2(封三)。
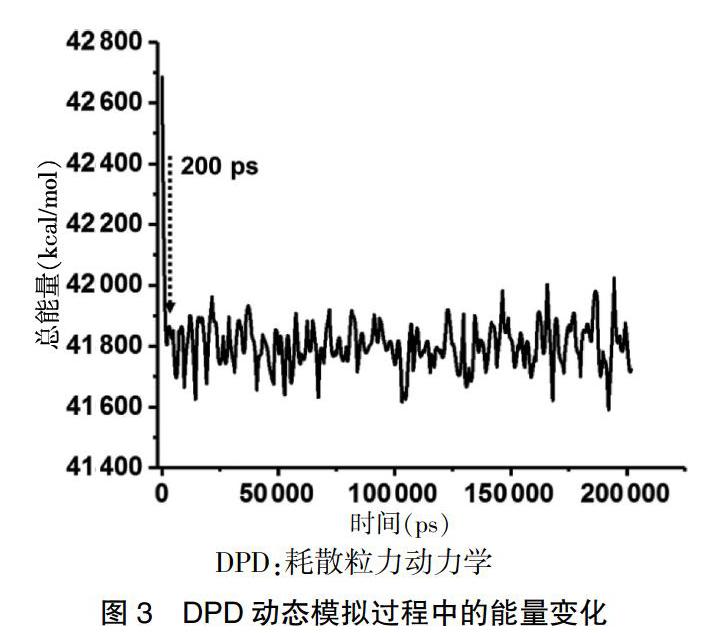
在得到初始介觀模型后,基于設定的DPD力場,進一步采用Mesocite中的DPD模塊進行了200 ns的DPD動態模擬。通過對DPD動態模擬過程中體系總能量變化的跟蹤。見圖3,可以發現體系的總能量在200 ps即發生了銳減,隨后就穩定在41 800 kcal/mol上下,提示200 ns的模擬時間足夠得到穩定的介觀組裝結構。
經過200 ns的分子模擬過程,最終獲得了一個球形的組裝體形態,其表面由桔色的PEI介觀分子呈網絡狀覆蓋。見圖4(封三)。
通過設置橫截面,可以清晰觀察到該介觀組裝體的內部結構。見圖5(封三)。由大量的MTX介觀分子填充形成內核,而其外圍由PEI介觀分子覆蓋形成外殼。
3 討論
本研究通過對MTX、PEI和水分子混合體系中分子間作用力、混合能以及DPD介觀模擬的計算與分析,成功揭露了MTX/PEI納米組裝體的組裝機制與內部結構。AutoDock分子對接結果提示,MTX與PEI之間較強的分子間作用力,特別是靜電作用力,是支持MTX/PEI納米組裝體組裝成功的原始動力。混合能的計算結果顯示,在水分子體系中,MTX與聚乙烯亞胺之間的混合相容性要優于于MTX與水分子之間的混合相容性。因此,在MTX、水分子和PEI的混合體系中,MTX分子更傾向于與PEI混合,而傾向于避免與水分子的接觸。隨后的DPD介觀模擬結果顯示,MTX/PEI納米組裝體是以MTX分子為內核,PEI分子為外殼的核殼結構納米粒。
隨著計算機技術的迅速發展,研究者基于計算機模擬技術已經大幅提高了對于生物大分子結構與功能的理解,但將計算機模擬技術應用于藥劑學領域的研究尚處于萌芽階段。特別是納米粒極小的納米尺寸導致其難以被充分表征,提高了通過傳統的實驗表征手段揭露其組裝機制與內部結構的難度。本研究創新性的將計算機分子模擬技術引入到納米粒的組裝機制與內部結構的表征中,實現了對PEI/MTX納米組裝體組裝機制與內部結構的分子模擬。
[參考文獻]
[1]? Chan ES,Cronstein BN. Methotrexate—how does it really work? [J]. Nat Rev Rheumatol,2010,6(3):175-178.
[2]? Chan ES,Cronstein BN. Mechanisms of action of methotrexate [J]. Bull Hosp Jt Dis(2013),2013,71 Suppl 1:S5-S8.
[3]? Tian H,Cronstein BN. Understanding the mechanisms of action of methotrexate:implications for the treatment of rheumatoid arthritis [J]. Bull NYU Hosp Jt Dis,2007,65(3):168-173.
[4]? Gutierrez JC,Hwang K. The toxicity of methotrexate in male fertility and paternal teratogenicity [J]. Expert Opin Drug Metab Toxicol,2017,13(1):51-58.
[5]? 蒙小麗,龍玲,陳小勇.基于聚乙烯亞胺構建pH響應性口服甲氨蝶呤納米遞送系統[J].中國當代醫藥,2018,25(4):20-24.
[6]? 陸小華,朱育丹,鄔新兵,等.基于分子間相互作用的納米尺度分子傳遞[C]//第十七屆全國化學熱力學和熱分析學術會議論文集,2014.
[7]? 徐筱杰,陳麗蓉.化學及生物體系中的分子識別[J].化學進展,1996,8(3):189.
[8]? Náray-Szabó G. Analysis of molecular recognition:steric electrostatic and hydrophobic complementarity [J]. J Mol Recognit,2010,6(4):205-210.
[9]? Kapetanovic IM. Computer-aided drug discovery and development(caddd):in silico-chemico-biological approach [J]. Chem Biol Interact,2008,171(2):165-176.
[10]? Talele TT,Khedkar SA,Rigby AC. Successful applications of computer aided drug discovery:moving drugs from concept to the clinic [J]. Curr Top Med Chem,2010,10(1):127-141.
[11]? Yang X,Wang Y,Byrne R,et al. Concepts of Artificial Intelligence for Computer-Assisted Drug Discovery [J]. Chem Rev,2019,119(18):10520-10594.
[12]? Yang B,Mao J,Gao B,et al. Computer-Assisted Drug Virtual Screening Based on the Natural Product Databases [J]. Curr Pharm Biotechno,2019,20(4):293-301.
[13]? Zhang C,Long L,Xiong Y,et al. Facile Engineering of Indomethacin-Induced Paclitaxel Nanocrystal Aggregates as Carrier-Free Nanomedicine with Improved Synergetic Antitumor Activity [J]. ACS Appl Mater Inter,2019,11(10):9872-9883.
[14]? Zhou X,Zhao Y,Chen S,et al. Self-Assembly of pH-Responsive Microspheres for Intestinal Delivery of Diverse Lipophilic Therapeutics [J]. Biomacromolecules,2016, 17(8):2540.
[15]? Che L,Liu Z,Wang D,et al. Computer-assisted engineering of programmed drug releasing multilayer nan-omedicine via indomethacin-mediated ternary complex for therapy against a multidrug resistant tumor [J]. Acta Biomater,2019,97:461-473.
[16]? Morris GM,Ruth H,William L,et al. AutoDock4 and AutoDockTools4:Automated docking with selective receptor flexibility [J]. J Comput Chem,2010,30(16):2785-2791.
[17]? Warren PB. Dissipative particle dynamics [J]. Curr Opin Colloid In,1998,3(6):620-624.
[18]? Hoogerbrugge PJ,Koelman JMVA. Simulating Microscopic Hydrodynamic Phenomena with Dissipative Particle Dynamics [J]. Europhys Lett,1992,19(3):155-160.
[19]? Espanol P,Warren P. Statistical mechanics of dissipative particle dynamics [J]. Europhys Lett,1995,30(4):191-196.
[20]? Moyassari A,Gkourmpis T,Mikael S,et al. Molecular dynamics simulation of linear polyethylene blends:Effect of molar mass bimodality on topological characteristics and mechanical behavior [J]. Polymer,2019,161:139-150.
(收稿日期:2019-08-12? 本文編輯:封? ?華)

