糖蛋白印跡二維光子晶體水凝膠傳感器的構建
李艷霞,黃 露,陳毅挺,婁本勇,繆 玲
(1.閩江學院 海洋學院 化學工程系,福建 福州 350108;2.閩江學院 藥物制劑研究與 測試中心,福建 福州 350108)
糖蛋白( Glycoprotein)由寡糖鏈與肽鏈中的一定氨基酸殘基以糖苷鍵共價連接而成,是生理功能的主要承擔者。糖蛋白與多種疾病的發生密切相關,并常用作臨床診斷的生物標志物和治療靶點。然而,在復雜的生物樣品中,糖蛋白的研究易受到其它蛋白的嚴重干擾。因此,在進行分析之前,糖蛋白的識別和分離就顯得尤為重要。目前,質譜已被證明是糖蛋白分析的強大工具,但其無法直接識別目標糖蛋白,需要進行繁瑣的樣品預處理,對于生物樣品來說,這一處理過程極易破壞蛋白質的結構與性質。因此,發展一種非破壞性、便捷、高敏感的糖蛋白分析方法具有重要意義。刀豆蛋白A(Concanavalin A,簡稱Con A),是一種植物血球凝集素,屬于糖蛋白,含一個糖結合部位,可高特異性和可逆地識別并可與含有糖基修飾的細胞或糖綴合物結合[1],已成為生物學、化學、免疫學、生物化學以及醫學等領域中有用的研究工具。
光子晶體是一種經典的光學材料,是一類在光學尺度上具有周期性介電結構的由人工設計和制造的晶體。光子晶體幾何形狀上的周期性使之具有光子能帶結構,但由于光子晶體中各個間隙位置的差異,導致其產生的反射光的顏色存在明顯的差別,該特點使光子晶體成為理想的光學傳感檢測材料[2-3]。
分子印跡技術是一種用于制備具有特殊識別功能的分子印跡聚合物的方式,是集材料化學、光學、高分子化學和生物學于一身的新興技術[4]。分子印跡凝膠光子晶體是分子印跡技術與凝膠光子晶體技術的有機結合,由于光子晶體周期性的介電結構可引起電磁波的布拉格衍射,當電磁波落在可見光測量波長范圍內時,水凝膠光子晶體即可產生肉眼可見的五彩斑斕的結構色[5];同時,分子印跡水凝膠可對外界的環境刺激產生響應而發生快速且可逆的溶脹收縮,進而引起光子晶體結構色的變化[6]。因此,結合分子印跡水凝膠的特異性識別能力和光子晶體的即時檢測功能,可實現目標物的定性與定量分析。迄今,基于分子印跡水凝膠光子晶體技術已經實現了L-色氨酸[7]、紅霉素[8]、磺胺二甲嘧啶[9]、葡萄糖[10]、三聚氰胺[11]、2,4,6-三氯酚[12]、滅多威[13]、乙基膦酸[14]等多種物質的檢測。此類檢測方法需滿足以下要求:①目標檢測物的分子可以被特異性吸附;②在吸附目標分子之后,光子晶體所發出的光信號會產生相應的變化,即可以對被檢測的物質產生響應。
本文選擇Con A作為糖蛋白印跡模板分子,以4-乙烯基苯硼酸為單體引入硼酸基團,并利用硼酸基團與糖蛋白中的鄰二羥基形成可逆共價鍵,制得能夠特異性識別Con A的糖蛋白印跡膜。以聚苯乙烯微球自組裝的光子晶體為載體,在光子晶體界面上制備Con A印跡的丙烯酰胺水凝膠。模板蛋白經洗脫,形成Con A分子印跡二維光子晶體水凝膠傳感器(MIPs)。當單色光垂直入射時,二維光子晶體的反面會出現德拜環,通過測量德拜環直徑變化,可以直觀地反映出印跡水凝膠對目標物的吸附效果,從而實現目標物檢測。整個過程快速、簡便,不需任何復雜的儀器設備,且可拓展到其它糖蛋白印跡。
1 實驗部分
1.1 儀器與試劑
載玻片(25.4 mm×76.2 mm×1 mm)、綠色激光筆(532 nm,1 000 mW)(西安市諾青激光有限公司);SU8000掃描電子顯微鏡(日本日立公司);Nicoler iS50傅立葉轉換紅外光譜儀(美國尼高力公司);TG-DSC分析儀(德國耐馳公司)。
甲基丙烯酸-2-羥乙酯、過硫酸鉀、丙烯酰胺、甲叉雙丙烯酰胺、過硫酸銨、乙酸、正丙醇(分析純),苯乙烯(化學純),均購于國藥集團化學試劑有限公司;4-乙烯基苯硼酸(純度96%)購于阿拉丁試劑有限公司;胎牛血清(FBS,優級純)、刀豆蛋白A(Con A,純度>95%)、卵清白蛋白(OVA,含量>95%)、胰蛋白酶(Try,含量>95%)購于北京鼎國生物技術有限責任公司;牛血紅蛋白(BHb,含量>95%)、溶菌酶(Lyz,含量>95%)購于源葉生物科技有限公司。實驗用水為Millipore超純水(18.2 MΩ·cm)。
1.2 聚苯乙烯微球的制備
采用無皂乳液聚合法制備粒徑為800 nm的單分散聚苯乙烯(PS)微球[15]:首先,向500 mL的三口圓底燒瓶中依次加入77.3 mL苯乙烯、1.865 mL 甲基丙烯酸-2-羥乙酯(HEMED)、0.18 g氯化鈉和205 mL超純水,在不斷攪拌的條件下,充氮除氧1 h,加熱至70 ℃;將0.11 g過硫酸鉀溶解在5 mL超純水中后加入到該三口圓底燒瓶中,回流24 h,得到乳白色溶液,反應結束,冷卻至室溫。用玻璃棉過濾,離心,取上清液,以超純水洗3~4次,再加入超純水純化PS微球,超聲30 min,以分散單個顆粒,保存備用。
1.3 二維光子晶體的自組裝
將制得的PS微球用去離子水稀釋成質量分數為20%的聚苯乙烯乳液,并與正丙醇以體積比2∶1混合,超聲20 min使其分散均勻。采取針尖注射法[16-17]在去離子水的表面制得一大片顏色鮮艷的單層聚苯乙烯光子晶體(PC),將制得的PC轉移至載玻片上,垂直放置,于空氣中風干,通過垂直沉降獲取具有一定規整排列的聚苯乙烯二維光子晶體。
1.4 Con A分子印跡二維光子晶體水凝膠的制備
A液:稱取12 g丙烯酰胺和0.4 g甲叉雙丙烯酰胺,加水溶解,定容至50 mL,并儲存在4 ℃冰箱中備用。
混合液的制備:取干凈的燒杯,向其中依次加入1 mL A液,0.006 g 4-乙烯基苯硼酸和10 mg Con A,充分混勻、溶解,再依次加入1 mL水,20 μL 10%的過硫酸銨和1 μL N,N,N′,N′-四甲基乙二胺(TEMED),攪拌混勻。

圖1 Con A分子印跡二維光子晶體水凝膠(MIPs)制備過程Fig.1 Schematic representation of the stepwise modification of MIPs
取一塊含有聚苯乙烯二維光子晶體的載玻片,移取200 μL上述混合液滴加在光子晶體表面,均勻鋪開,蓋上載玻片,在無氣泡條件下形成一種“三明治”結構,自聚合1 h,移去上層載玻片,將下層載有光子晶體水凝膠層的載玻片,浸泡在10%的乙酸溶液中洗脫1 h,倒出洗脫液,依次用洗脫液、水淋洗3遍,再將其浸泡在0.01 mol/L磷酸鹽緩沖液(pH 7.0)中,使水凝膠達到溶脹平衡狀態,即得到Con A印跡二維光子晶體水凝膠。
非分子印跡光子晶體水凝膠作為對照組,制備方法與上述步驟相同,但是混合液中不加Con A印跡分子。印跡分子水凝膠和非印跡分子水凝膠分別表示為MIPs和NIPs。MIPs吸附1.0 mg/mL Con A,標記為MIPs-Con A。制備過程示意圖如圖1所示。
2 結果與討論
2.1 分子印跡光子晶體水凝膠的表征
采用掃描電鏡(SEM)對PC和MIPs的形貌進行表征。圖2A為采用針尖注射法制備得到PC的SEM圖。可以看出,利用無皂乳液聚合方法制備的二維光子晶體粒徑約733 nm,為單層、有序的六方緊密堆積結構;PS小球呈圓形,微球粒徑均一,單分散性良好。實物照片表明該光子晶體色彩鮮艷豁亮,用肉眼即可觀測到表面由布拉格衍射引起的衍射色彩。圖2B為MIPs的SEM圖,由圖可見,形成水凝膠后的PS微球仍然規則地鑲嵌在水凝膠的表面,這種現象為后續德拜環的測量奠定了基礎。

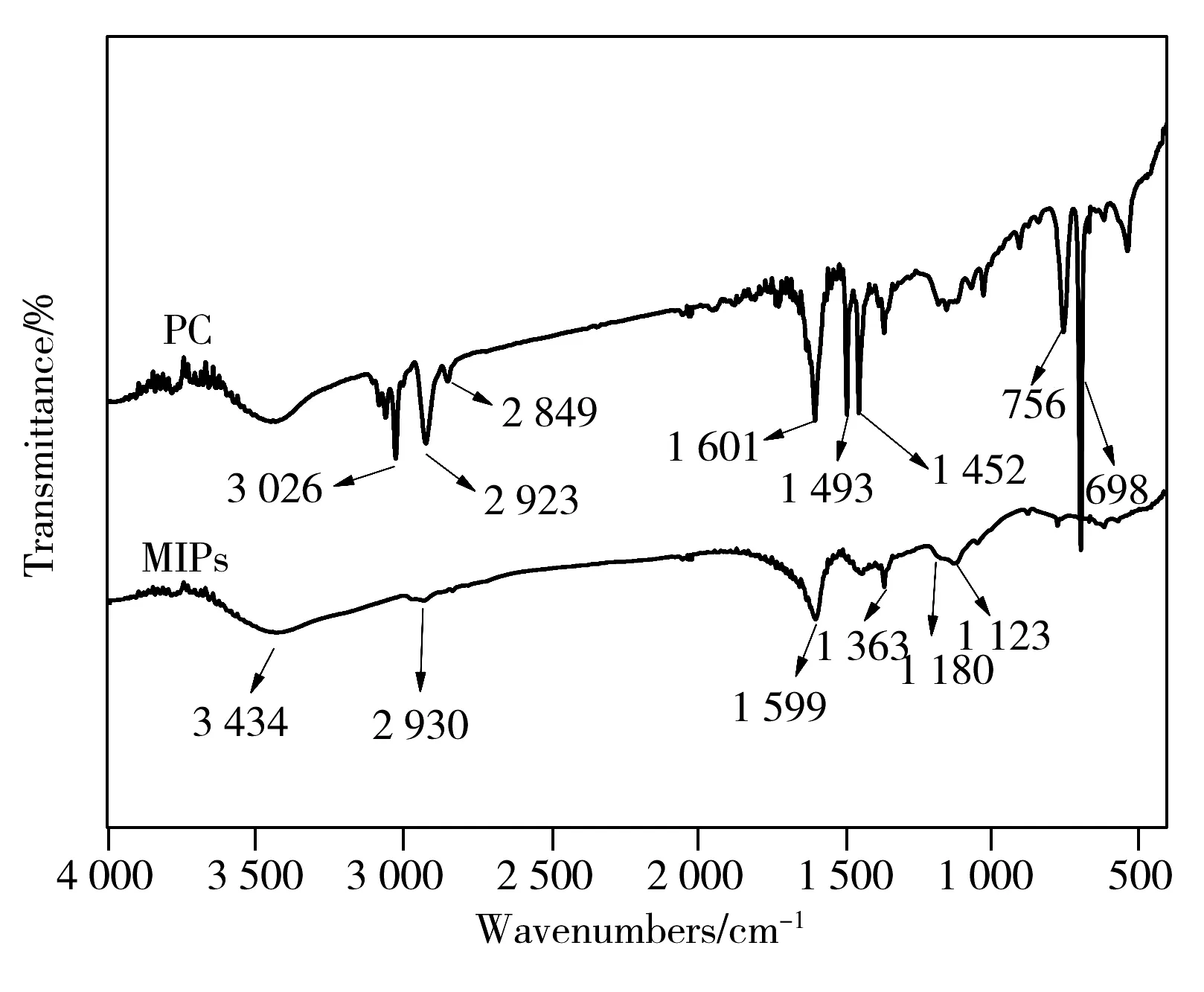
圖3 PC與MIPs的紅外光圖Fig.3 IR micrographs of PC and MIPs

圖4 德拜環測量示意圖(A)和激光照射MIPs后 產生的德拜環黑暗條件下的照片(B)Fig.4 Illustration of Debye diffraction ring measurement

2.2 MIPs的響應行為
通過測量二維光子晶體水凝膠對激光衍射產生的德拜環直徑的變化,探究 MIPs對 Con A的響應行為。德拜環直徑測量如圖4A所示,采用波長為532 nm的綠色激光筆垂直照射水凝膠,從而在二維光子晶體反面產生德拜衍射花環,該德拜環可用來表征二維光子晶體的晶格參數,進而反應緊密堆積的二維膠體晶體凝膠異質結構體積的改變。德拜衍射角α由單色入射光的波長λ和光子晶體球間距d共同決定。
(1)
采用綠色激光(λ=532 nm)光源,固定底部水平面與樣品之間的距離h,激光筆的位置也要固定。用最小刻度為1 mm的直尺測量德拜環直徑D,并根據下式求得衍射角α:
α=arctan(D/2h)
(2)
將衍射角α代入式(1),即可求得膠體晶體陣列的球間距d。
2.3 不同材料德拜環直徑差異
光子晶體表面修飾的材料不同,將使光子晶體中各個間隙位置產生變化,進而導致德拜環的差異。本文分別測定了PC、MIPs+Con A、MIPs和NIPs的德拜環直徑。結果如圖5A所示,PC德拜環直徑最小,說明PC中PS微球未受到其他物質影響,排列最緊密;當表面覆蓋一層水凝膠(NIPs)時,德拜環直徑略有增大,含有印跡空穴的MIPs可進一步增大德拜環直徑,而MIPs 飽和吸附 Con A后德拜環直徑最大。由此,可以得出,引入新的物質會引起光子晶體德拜環的增大。
2.4 MIPs的吸附等溫線
印跡分子的濃度會對水凝膠內的印跡孔腔數量產生影響,從而影響MIPs的響應行為。取洗脫后的MIPs和NIPs,分別滴加10 μL不同質量濃度的Con A溶液,吸附1 h, 洗去未被吸附的蛋白,測其德拜環的變化。圖5B可見,對于MIPs,當Con A質量濃度從0 mg/mL增大到0.5 mg/mL時,德拜環直徑逐漸增大;此后,隨著Con A質量濃度增大,德拜環直徑略有增加,但變化不大,說明吸附趨于飽和。而NIPs滴加Con A后未產生德拜環的顯著變化。說明MIPs由于分子孔穴的印跡效應,對Con A表現出了較高的吸附性能。這一動態響應過程可用于目標物的富集和即時檢測。
2.5 MIPs的吸附與洗脫效果
以MIPs和NIPs分別吸附1.0 mg/mL的Con A,德拜環直徑隨時間的變化情況如圖5C所示。由圖可知,隨著吸附時間的增加,兩者德拜環直徑的變化量都逐漸增大,當吸附60 min后,德拜環直徑趨于穩定,說明達到飽和吸附。但相同條件下,尤其是飽和吸附條件下,MIPs德拜環的直徑變化量遠大于NIPs,說明MIPs可以對Con A進行特異性吸附。
取上述分別飽和吸附Con A溶液的MIPs和NIPs,測其德拜環直徑后置于10%乙酸溶液中洗脫,測量德拜環直徑隨洗脫時間的變化情況。由圖5D可知,隨著洗脫時間的增加,MIPs和NIPs的德拜環直徑逐漸減小,60 min后無明顯變化,說明60 min 可以達到最佳的洗脫效果。




圖5 德拜環在不同條件下的變化情況Fig.5 Changes of Debye ring under different conditions diameter of Debye ring produced by different materials(A),curve of Debye ring changed with Con A concentration(B), adsorption time(C) and elution time(D)

表1 交聯度配方Table 1 Formula of crosslinking degree
2.6 交聯度對MIPs響應的影響
交聯度指溶液中交聯劑占單體和交聯體總量的百分數,是影響水凝膠強度、結構和溶脹率的一大因素[7],可通過德拜環的直徑變化來體現。本文在MIPs制備過程中,通過固定Con A(0.012 5 g)、乙烯基苯硼酸(0.007 5 g)、10%APS(0.025 mL)的用量,改變交聯劑(A液)的用量,考察了不同交聯度下MIPs對目標分子識別的敏感性。不同交聯度配方(表1)下德拜環直徑隨交聯度的變化曲線如圖6A所示。
由圖6A可知,當交聯度為10%時,德拜環的直徑變化最顯著,其最大的變化量為0.94 cm。這是因為當交聯度過小時,水凝膠交聯點較少,難以鎖定目標分析物,且印跡空腔容易溶脹變形,從而導致水凝膠的響應性能降低;隨著交聯度的逐漸增大,水凝膠結構中存在的交聯點增多,制得的水凝膠的結構更穩定,其剛性也逐漸增強,力學強度較高,收縮溶脹能力降低,故響應性能也降低;而當交聯度過高時,會使溶液的水溶性變差,溶脹度較低,水凝膠缺乏彈性,從而影響MIPs對目標物的識別能力。
2.7 MIPs的重復性
將同一片MIPs洗脫后測其德拜環,隨后在其上滴加10 μL質量濃度1.0 mg/mL 的Con A溶液,測德拜環直徑的變化,然后再用10%的乙酸溶液將Con A完全洗脫,結果如圖6B所示。經過4次吸附-洗脫過程,MIPs仍然保持良好的重復性。
2.8 MIPs的特異識別性
為驗證MIPs的特異識別性,選擇與Con A結構相似的牛血紅蛋白(BHb)、卵清白蛋白(OVA)、胰蛋白酶(Try)和溶菌酶(Lyz)進行對比實驗。由圖6C可以看出,MIPs在質量濃度均為1.0 mg/mL的BHb、OVA、Try和Lyz溶液中的德拜環直徑變化依次為0.60、0.53、0.30、0.21 cm,明顯小于MIPs在Con A(1.0 mg/mL)中的變化量(1.3 cm)。由此可見,MIPs對Con A有特異識別性。這種特異識別性主要是因為水凝膠印跡空穴與目標蛋白之間空間匹配,以及印跡空腔中富含的氨基和硼酸基團提供了多識別位點。
2.9 實際樣品檢測
本文進一步考察了Con A印跡二維光子晶體水凝膠在模擬生物樣品中的傳感性能。于胎牛血清原液(FBS)和稀釋20倍的FBS(1/20)中添加一定量的Con A,使其終濃度為1.0 mg/mL,測試基底血清樣品對目標分析物的干擾情況,結果如圖6D所示。MIPs在FBS(1/20)、Con A、FBS(1/20)+Con A、FBS和 FBS+Con A中德拜環的變化量依次為0.23、0.94、0.86、0.21、0.78 cm。這一結果表明,FBS溶液中MIPs對Con A仍然具有較高的靈敏性和選擇識別性,高濃度的干擾物質對目標分析物影響不大,所制備的MIPs表現出較強的抗干擾能力,有望用于FBS中Con A的快速檢測。

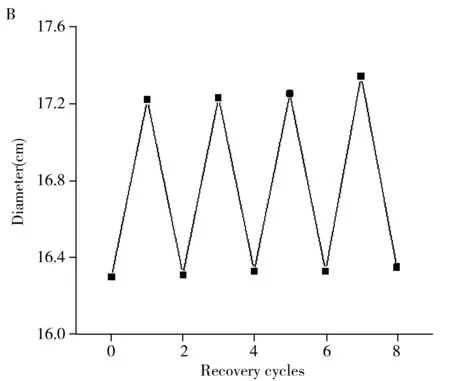


圖6 不同交聯度制備的MIPs吸附Con A后德拜環直徑的變化(A),MIPs的重復使用性(B), MIPs和NIPs的選擇性(C)及實際樣品分析(D)Fig.6 Debye ring diameter changes of adsorbed Con A by MIPs prepared with different crosslinking degrees(A),reusability of MIPs(B),selectivity of MIPs and NIPs(C) and actual sample analysis(D)
3 結 論
本文通過無皂乳液聚合的方法合成了粒徑733 nm的PS微球,采用垂直沉積法制備出色彩鮮艷的2D光子晶體,以糖蛋白Con A作為模板分子,于光子晶體表面制得一薄層印跡聚合物膜,通過引入苯硼酸基團,增加了目標糖蛋白的特異識別性能,實現了對Con A的特異性識別。所制備的MIPs具有可重復性和高選擇性,可快速響應目標分子,適用于目標物的富集和即時檢測。同時,水凝膠制備方法快捷方便,測量方式便利直觀,不需特殊設備,具有很強的普適性,該制備方法可拓展到其它糖類分子。

