挖掘圖表數(shù)據(jù)內(nèi)涵組織化學(xué)教學(xué)的若干啟示
孫立新


摘要:根據(jù)高中化學(xué)教材(人教版)中提供的圖表數(shù)據(jù)資料作分析和探討,闡述如何指導(dǎo)學(xué)生分析數(shù)據(jù)、質(zhì)疑數(shù)據(jù)、探索數(shù)據(jù)之間的關(guān)系等教學(xué)過程,為如何利用和挖掘教材中圖表數(shù)據(jù)的內(nèi)涵,進一步落實化學(xué)學(xué)科核心素養(yǎng)提供了教學(xué)實例。
關(guān)鍵詞:中學(xué)化學(xué)教學(xué);圖表數(shù)據(jù)內(nèi)涵;化學(xué)學(xué)科核心素養(yǎng)
《普通高中化學(xué)課程標準(2017年版)》(以下簡稱新課標)中指出:學(xué)科核心素養(yǎng)是學(xué)科育人價值的集中體現(xiàn),是學(xué)生通過學(xué)科學(xué)習(xí)逐步形成的正確的價值觀念、必備品格和關(guān)鍵能力。高中化學(xué)學(xué)科核心素養(yǎng)是高中發(fā)展核心素養(yǎng)的重要組成部分,是學(xué)生綜合素質(zhì)的具體體現(xiàn),反映了社會主義核心價值觀下化學(xué)學(xué)科育人的基本要求,全面展現(xiàn)了化學(xué)課程學(xué)習(xí)對學(xué)生未來發(fā)展的重要價值。
中學(xué)化學(xué)教材(人教版)中提供了不少的圖表數(shù)據(jù),這些數(shù)據(jù)反映了化學(xué)物質(zhì)之間的何種關(guān)系,向我們展示了化學(xué)物質(zhì)的哪些本質(zhì),需要引起我們的關(guān)注。讓學(xué)生了解這些數(shù)據(jù)所包含的內(nèi)涵,探索這些數(shù)據(jù)之間的關(guān)系,從而了解物質(zhì)的性質(zhì),對學(xué)習(xí)化學(xué)具有非常重要的意義。查閱有關(guān)資料,關(guān)于在中學(xué)化學(xué)課堂教學(xué)過程中,如何開展圖表數(shù)據(jù)的教學(xué)探討,落實化學(xué)學(xué)科核心素養(yǎng)的文章并不多見。范雷軍[1]曾對教材中數(shù)據(jù)類圖表的教學(xué)進行過初步探討,認為利用數(shù)據(jù)型圖表有利于培養(yǎng)學(xué)生的化學(xué)素養(yǎng),并提出利用數(shù)據(jù)型圖表的基本要求。占小紅[2]等對化學(xué)教材中圖表的認知難度也進行了分析和評價。
我們認為,高中化學(xué)教材(人教版)中圖表數(shù)據(jù)的教學(xué)蘊含著豐富的內(nèi)涵,其包括數(shù)據(jù)的查找、數(shù)據(jù)的推理、數(shù)據(jù)的內(nèi)在規(guī)律、數(shù)據(jù)的質(zhì)疑等多方面,在培養(yǎng)學(xué)生化學(xué)學(xué)科核心素養(yǎng)方面有很重要的價值和意義。
本文就如何利用教材中提供的有關(guān)圖表數(shù)據(jù),在“宏觀辨識與微觀探析”“證據(jù)推理與模型認知”以及“科學(xué)探究與創(chuàng)新意識”等三方面落實化學(xué)學(xué)科的核心素養(yǎng),談?wù)勎覀兊淖龇ê涂捶ā?/p>
1 挖掘圖表數(shù)據(jù)內(nèi)涵,落實“宏觀辨識與微觀探析”的核心素養(yǎng)教育
新課標關(guān)于“宏觀辨識與微觀探析”的教學(xué)要求是:能從元素和原子、分子水平認識物質(zhì)的組成、結(jié)構(gòu)、性質(zhì)和變化,形成“結(jié)構(gòu)決定性質(zhì)”的觀念;從不同層次認識物質(zhì)的多樣性等。如何從教材中所給出的圖表、數(shù)據(jù)等方面來落實“宏觀辨識與微觀探析”的核心素養(yǎng)教育?我們認為可從以下幾方面來落實。
1.1 學(xué)會查找數(shù)據(jù)
我們在選修3教材(人教版)中學(xué)習(xí)了金屬晶體的堆積方式,了解了金屬鈉是一種“體心立方堆積”后,不妨根據(jù)教材中提供的有關(guān)數(shù)據(jù)來計算一下鈉的原子半徑或密度大小,以此來慢慢感受查找數(shù)據(jù)、利用數(shù)據(jù)并用數(shù)學(xué)方法來處理數(shù)據(jù)的一般過程。
我們在必修2教材[3](人教版)中查得鈉的密度為0.97g/cm3,用這個數(shù)據(jù)來計算鈉原子的半徑會是多少?計算如下:
而我們在必修2教材[4](人教版)可查得鈉原子的半徑為186pm。顯然,計算結(jié)果與實驗結(jié)果高度一致!是不是很神奇?
1.2 學(xué)會利用數(shù)據(jù)進行推理與論證
類似地,我們還可以根據(jù)選修3教材[5](人教版)中提供的鈉離子半徑、銫離子半徑以及氯離子半徑來計算氯化鈉、氯化銫的密度,并證明氯化銫的配位數(shù)是8而不是6。
1.2.1 計算氯化鈉、氯化銫的密度
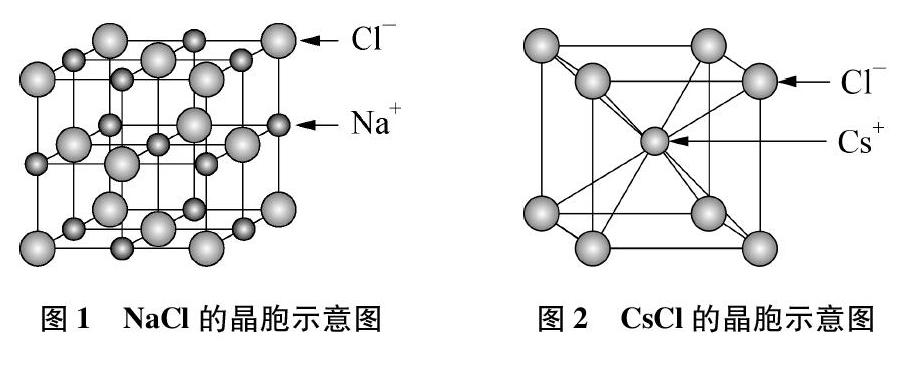
我們從教材中查得鈉離子半徑為95pm,銫離子半徑為169pm,氯離子半徑為181pm。 NaCl的晶胞和CsCl的晶胞如圖1、圖2所示。
我們知道,NaCl晶胞中有4個Na+和4個Cl-;晶胞的棱長應(yīng)是Na+和Cl-的直徑之和,即:晶胞的棱長=(95pm+181pm)×2=552pm。
所以,NaCl晶體的密度=4×(23+35.5)/〔6.02×1023×(552pm)3〕
=234g/101.25cm3
=2.31g/cm3
實際上,NaCl晶體的密度為2.165g/cm3。計算結(jié)果與實驗結(jié)果是不是相差不大?在化學(xué)學(xué)科里,這兩個數(shù)據(jù)我們可認為近似相等。
氯化銫的密度呢?我們也可以計算。從圖2中可以看出:每個CsCl的晶胞只有1個Cs+和1個Cl-;該晶胞的體對角線長應(yīng)是Cs+和Cl-的直徑之和,即:晶胞的棱長=(169pm+181pm)×2÷3=404.2pm。
所以,CsCl晶體的密度=(133+35.5)/〔6.02×1023×(404.2pm)3〕
=168.5g/39.74cm3
=4.24g/cm3
比實際值3.984g/cm3也要略大些,當(dāng)然,我們也可以近似地認為它們是相等的。
上述兩個計算結(jié)果都比實驗值略大。這是什么原因?原來,計算的結(jié)果只能是晶胞在“無隙并置”時的理想結(jié)果,而實際的NaCl晶體由晶胞“并置”時,并不是“無隙”的,而是常常留下“間隙”。也就是說,氯化鈉固體是由許多數(shù)目不定的晶胞組成的“集體”構(gòu)成的,這些“集體”與“集體”之間一定會有一些很小的“空間”,正是由于這些很小“空間”的存在,才導(dǎo)致了理論值(也就是計算值)比實驗值(也就是實際值)偏大。當(dāng)然,我們在使用NaCl晶體的密度時要用其實驗值,而不是理論值!
1.2.2 證明氯化銫的配位數(shù)是8而不是6
如果我們假定CsCl晶胞和NaCl晶胞的排列方式相同,那么此時CsCl晶體密度的理論計算值又會是多少?
仿照上述NaCl晶體密度的計算式,不難算出CsCl晶體的密度
=4×(133+35.5)/〔6.02×1023×(2×169pm+2×181pm)3〕
=674g/206.5cm3=3.26g/cm3
此時的理論值比實際值3.984g/cm3要小得多,這是不符合實際情況的。這是不是可以證明CsCl晶胞和NaCl晶胞的排列方式不同呢?當(dāng)然可以證明!
至此,學(xué)生的疑惑也就迎刃而解了。
1.3 “質(zhì)疑”數(shù)據(jù),是學(xué)習(xí)和思考過程中的一種思維習(xí)慣
1.3.1 養(yǎng)成關(guān)注教材中所給數(shù)據(jù)的習(xí)慣,是學(xué)習(xí)和思考過程中的一種思維方式
教材中給出的數(shù)據(jù)有許多,如果我們留意觀察,有時會發(fā)現(xiàn)同一種物質(zhì)的同一種數(shù)據(jù)有時會有些不同,這是什么原因?
其實這是一種正常的現(xiàn)象,因為化學(xué)數(shù)據(jù)都是實驗數(shù)據(jù)。不同的人,測定方法不同,所得的數(shù)據(jù)是不同的;不同的人,即使方法相同,所測得的數(shù)據(jù)也可能是不同的。當(dāng)然,即使是同一個人,用同一種方法測定,其結(jié)果也可能是不同的,也正是這個原因,我們在做定量實驗的時候,都必須做至少三次。例如,我們做酸堿中和實驗,用已知濃度的酸溶液滴定未知濃度的堿溶液時,我們至少應(yīng)做三次實驗,若這三次實驗的數(shù)據(jù)相差不大,在實驗的誤差范圍內(nèi),我們就可以不再重新實驗了;若有一個數(shù)據(jù)與其他兩個數(shù)據(jù)相差較大,不在誤差范圍內(nèi),我們就必須繼續(xù)實驗,且要找到那個誤差較大的數(shù)據(jù)產(chǎn)生的原因,否則,我們這次“中和滴定實驗”就是失敗的實驗。
同樣,科學(xué)家們的實驗方法不同,實驗儀器不同,所取的實驗材料不同等等,他們所測得的實驗數(shù)據(jù)也是不同的。比如:《物質(zhì)結(jié)構(gòu)與性質(zhì)》教材(人教版)的第80頁有NaF、 NaCl、 NaBr、 NaI的熔點分別為993℃、 801℃、 747℃、 661℃;而在該教材的第85頁卻指出它們的熔點分別為995℃、 801℃、 775℃、 651℃。我們不難發(fā)現(xiàn)這兩處的熔點是不同的,特別是NaBr的熔點竟相差28℃。
為什么會出現(xiàn)這樣的情況呢?顯然,這兩處的數(shù)據(jù)應(yīng)該是引自不同的資料,在同一本書中引用兩種不同的數(shù)據(jù)應(yīng)是不可取的,我們以后在用“數(shù)據(jù)”做推理或者做證據(jù)時,必須用同一個資料上的數(shù)據(jù),否則,我們的推理或論證就會缺少科學(xué)的嚴謹性和說服力。
1.3.2 “質(zhì)疑”數(shù)據(jù)要有理有據(jù),也是學(xué)習(xí)和思考過程中的一種思維方式
當(dāng)然,教材中給出的數(shù)據(jù),都是科學(xué)工作者用實驗的方法測得的,得到了絕大多數(shù)其他科學(xué)工作者的認可,到目前為止,這些數(shù)據(jù)應(yīng)該是大家公認的數(shù)據(jù)。隨著科學(xué)技術(shù)的不斷發(fā)展、科技手段的不斷更新,有些數(shù)據(jù)有可能會有更新,因此,教材中給出的某些數(shù)據(jù),我們是可以質(zhì)疑的。就像上述NaF、 NaCl、 NaBr、 NaI的熔點一樣,有著明顯的差異,我們能不懷疑嗎?
又如,選修4教材[6](人教版)第43頁給出了H2S的電離常數(shù),分別為K1=1.3×10-7,K2=7.1×10-15,它們相差108倍,其他多元酸的K1與K2相差都在104左右,H3PO4的K2、 K3也是相差104左右,我們是不是應(yīng)該“質(zhì)疑”它?我們可以用我們所學(xué)的知識來判斷它是否合理。
第一種證法是利用上述數(shù)據(jù),計算常溫下0.1mol/L硫化鈉溶液中硫離子的濃度,我們會發(fā)現(xiàn)硫化鈉溶液幾乎完全水解,也就是幾乎可以認為沒有硫化鈉溶液,或者說0.1mol/L硫化鈉溶液幾乎是不存在的。
從上述兩種證明,都可以說明H2S的電離常數(shù)K2=7.1×10-15是可以懷疑的,也是值得懷疑的!它應(yīng)該是多少呢?怎樣測得這個數(shù)值呢?需要我們每一個有興趣的同學(xué)努力學(xué)習(xí),積極思考。
2 挖掘圖表數(shù)據(jù)內(nèi)涵,落實“科學(xué)探究與創(chuàng)新意識”的核心素養(yǎng)教育
新課標關(guān)于“科學(xué)探究與創(chuàng)新意識”的教學(xué)要求是:認識科學(xué)探究是進行科學(xué)解釋和發(fā)現(xiàn)、創(chuàng)造和應(yīng)用的科學(xué)實踐活動;能發(fā)現(xiàn)和提出有探究價值的問題;能從問題和假設(shè)出發(fā),依據(jù)探究目的,設(shè)計探究方案,運用化學(xué)實驗、調(diào)查等方法進行實驗探究;能和同學(xué)交流實驗探究的成果,提出進一步探究或改進的設(shè)想;養(yǎng)成獨立思考、敢于質(zhì)疑和勇于創(chuàng)新的精神。
教材中給出了不少的實驗數(shù)據(jù),比如烷烴、烯烴的沸點數(shù)據(jù),直鏈一元醇的熔點、沸點數(shù)據(jù),堿金屬鹵化物的晶格能數(shù)據(jù)等等,卻沒有給出任何相關(guān)的規(guī)律。那么這些數(shù)據(jù)之間有無規(guī)律可循?或者說這些數(shù)據(jù)之間有沒有什么內(nèi)在的聯(lián)系呢?其實,有興趣的教師或?qū)W生是可以作些探索的。
例如,我們在講烷烴的物理性質(zhì)時,教材中給出了甲烷、乙烷、丙烷、丁烷、戊烷的沸點數(shù)據(jù):-164、 -88.6、 -42.1、 -0.5、 36.1(℃),我們查找有關(guān)資料,還得到了正己烷等的沸點:68.9、 98.4、 125.7、 150.8、 174(℃)。這幾個數(shù)據(jù)之間有沒有什么聯(lián)系呢?大家都知道:結(jié)構(gòu)和性質(zhì)相似的物質(zhì),相對分子質(zhì)量越大,其沸點會越高。也就是說,這些烷烴的沸點與它們的相對分子質(zhì)量會不會有定量的關(guān)系呢?這是我們可以探索的規(guī)律。當(dāng)我們計算了它們的絕對溫度后,發(fā)現(xiàn)它們之間還真存在著某種聯(lián)系。
通過描點法,我們發(fā)現(xiàn)這些絕對溫度數(shù)據(jù)與碳原子個數(shù)成近似拋物線的關(guān)系。于是我們提出了一個簡單的經(jīng)驗公式,即:T2=ax+b,式中T為直鏈烷烴的沸點,x為碳原子的個數(shù),a、 b為常數(shù)。我們通過計算,確定a=20885.41,b=-8739.39。計算結(jié)果如表1所示。我們可以看出實驗值與計算值較吻合。
我們從表中的計算結(jié)果不難發(fā)現(xiàn):影響直鏈烷烴沸點的決定因素是相對分子質(zhì)量,也就是范德華力;除了范德華力之外,還有其他因素(色散力、誘導(dǎo)力等),但這些因素都不是主要因素,對直鏈烷烴的沸點的影響不大。所以,我們在中學(xué)階段比較分子晶體的熔點、沸點的大小時,一般只需要比較相對分子質(zhì)量就可以了(含有氫鍵的分子其熔、沸點主要由氫鍵決定)。
我們還可以通過分析上述提出的計算公式,不難得出這樣的結(jié)論:對直鏈烷烴的熔沸點大小起決定作用的是其相對分子質(zhì)量。
3 挖掘圖表數(shù)據(jù)內(nèi)涵,落實“證據(jù)推理與模型認知”的核心素養(yǎng)教育
新課標關(guān)于“科學(xué)探究與創(chuàng)新意識”的教學(xué)要求是:要有證據(jù)意識;初步學(xué)會收集各種證據(jù),對物質(zhì)的性質(zhì)及其變化提出可能的假設(shè);基于證據(jù)進行分析推理,證實或證偽假設(shè);能解釋證據(jù)與結(jié)論之間的關(guān)系,確定形成科學(xué)結(jié)論需要的證據(jù)和尋找證據(jù)的途徑。
選修3教材[7](人教版)中提供了一些鍵能、鍵長的數(shù)據(jù),怎樣應(yīng)用這些數(shù)據(jù)呢?現(xiàn)摘錄一些加以說明(見表2)。
一般地,單鍵為σ鍵,雙鍵中有一個σ鍵,另一個為π鍵,叁鍵中只有一個σ鍵,另外兩個為π鍵。按照這個規(guī)律,再根據(jù)表中CC、 CC、 CC的鍵能大小,我們不難得出一個結(jié)論:碳碳鍵中π鍵的鍵能比σ鍵的鍵能小得多。
因為CC中一個σ鍵的鍵能和一個π鍵的鍵能之和為615kJ/mol,而CC的鍵能為347.7kJ/mol;
又因為CC的鍵長比CC的鍵長要短,因此,CC中σ鍵的鍵能應(yīng)比CC中σ鍵的鍵能大。
也就是說CC中π鍵的鍵能比σ鍵的能量要小得多!所以我們在有機化學(xué)的學(xué)習(xí)過程中介紹:CC易發(fā)生加成反應(yīng)完全合乎情理。
于是,有不少人就根據(jù)OO和OO的鍵能大小以及NN、 NN、 NN的鍵能大小得出另一個結(jié)論:氧氧鍵和氮氮鍵中π鍵的鍵能比σ鍵的鍵能大得多。
其實這個結(jié)論是不正確的!因為OO和OO以及NN、 NN、 NN的鍵長是不同的,也就是“電子云的重疊程度是不同的”,因而OO和OO以及NN、 NN、 NN中σ鍵的鍵能也是不同的。可以想象,NN的鍵長是最短的,σ鍵電子云的重疊是最多的,也就是NN 中的σ鍵的鍵能最大。不妨以NN 和NN的鍵能大小來作說明。
設(shè)NN中σ鍵鍵能為E1,NN中σ鍵的鍵能為E2,π鍵的平均鍵能為Eπ,則有
Eπ是否一定大于193kJ/mol呢?至少在數(shù)學(xué)上是不能確定的!當(dāng)然,我們也不能確定NN中π鍵的鍵能與σ鍵的鍵能大小,也就不能確定Eπ和E2的大小。而碳碳鍵中的σ鍵能大小和π鍵鍵能大小就沒有這種情況。
另外,我們還可以用OO和OO的鍵能數(shù)據(jù)來定性地推理:因為OO的鍵能為497.3kJ/mol,OO的鍵能為142kJ/mol,若OO中π鍵的鍵能比σ鍵的鍵能大,則OO 中σ鍵比π鍵更易斷裂,也就是說,鈉與O2(當(dāng)然,我們這里是將O2的結(jié)構(gòu)當(dāng)作是OO)反應(yīng)生成過氧化鈉時斷裂的是σ鍵而不是π鍵,即過氧化鈉中的氧氧鍵是π鍵而不是σ鍵!這當(dāng)然是不可以的。所以O(shè)O 中π鍵的鍵能大于σ鍵的鍵能是錯的!
在中學(xué)化學(xué)教學(xué)過程中落實化學(xué)學(xué)科核心素養(yǎng)是大勢所趨,而“化學(xué)數(shù)據(jù)”的處理,包括實驗“數(shù)據(jù)”的處理,利用“數(shù)據(jù)”的證實或證偽,利用“數(shù)據(jù)”探索物質(zhì)的結(jié)構(gòu)、性質(zhì)等都是化學(xué)教學(xué)的一個重要組成部分,甚至可以說沒有“數(shù)據(jù)”的證明是蒼白的證明!為此,我們在“數(shù)據(jù)”處理方面有了上述如是做法和看法,與大家共享。
參考文獻:
[1]范雷軍. 人教版高中化學(xué)新教科書中數(shù)據(jù)類圖表初探[J]. 現(xiàn)代中小學(xué)教育,2006,(5):24~26.
[2]占小紅,周少江. 化學(xué)教材圖表認知難度分析量表的設(shè)計及應(yīng)用[J]. 化學(xué)教學(xué),2015,(4):12~16.
[3][4]宋心琦主編. 普通高中課程標準實驗教科書·化學(xué)2[M]. 北京:人民教育出版社,2004:5,7.
[5][7]宋心琦主編. 普通高中課程標準實驗教科書·物質(zhì)結(jié)構(gòu)與性質(zhì)[M]. 北京:人民教育出版社,2004:31~32.
[6]宋心琦主編. 普通高中課程標準實驗教科書·化學(xué)反應(yīng)原理[M]. 北京:人民教育出版社,2004:43.

