長鏈非編碼RNA AC244502.3?201對甲狀腺乳頭狀癌細胞增殖和遷移的影響
向濤 梁巍巍 柯文 徐梓筠 修玲玲 衛國紅
中山大學附屬第一醫院內分泌科(廣州510080)
甲狀腺癌是內分泌系統中最常見的惡性腫瘤,近年來其發病率在全球范圍內持續升高,是全球增速最快的惡性腫瘤[1]。甲狀腺癌按組織形態學可分為起源于濾泡上皮細胞的甲狀腺乳頭狀癌(papillary thyroid cancer,PTC)、濾泡狀甲狀腺癌(follicular thyroid cancer,FTC)和未分化甲狀腺癌(anaplastic thyroid cancer,ATC)以及起源于濾泡旁C 細胞的甲狀腺髓樣癌(medullary thyroid cancer,MTC)[2]。PTC 在甲狀腺癌中約占90%[3],盡管大多數PTC 患者預后很好,但它具有較強的侵襲和定植能力,容易抵抗失巢凋亡發生淋巴結和遠處器官轉移,甚至會去分化演變為更惡性的癌癥[4]。因此研究PTC 惡性進展過程中的分子機制,尋找調控PTC 發生發展的關鍵因素和作用分子具有重要意義[5]。LncRNAs 是一類轉錄本長度超過200 nt 的不編碼蛋白的RNA 分子,它們可以通過對轉錄和轉錄后的調控、基因組印跡和染色質修飾等多種機制在腫瘤發生發展過程中發揮廣泛的調控作用[7],如LncRNA RP11?356I2.2 在胃癌中表達降低能抑制胃癌細胞增殖、遷移和成瘤[8]。在甲狀腺癌中,目前也發現多種異常表達的lncRNAs,其中部分lncRNAs 的功能得到了初步研究,例如一些在甲狀腺癌中表達下降的lncRNAs(如NAMA 等)具有抑癌作用[8],而表達增加的lncRNAs(如h19 等)則具有致癌作用[10],關于lncRNAs 調控甲狀腺癌功能的機制也有初步的研究,如LINC00377 在甲狀腺癌組織中低表達,在SW579 細胞中證實過表達LINC00377 能夠通過下調miR?29a?3p 表達促進ADAMTS9 基因的表達進而抑制細胞增殖和遷移[11]。AC244502.3?201 是一種長為844 nt 的lncRNA 分子,它位于14 號染色體22,415,362?22,418,657,由3 個外顯子組成。目前關于AC244502.3?201 在腫瘤發生發展中的作用還未被報道。
本研究旨在探討AC244502.3?201 在PTC 中的表達水平,并分析AC244502.3?201 對PTC 細胞增殖及侵襲遷移的影響以及可能的分子機制,為理解PTC 發生發展的分子機制及新的治療靶點提供依據。
1 材料與方法
1.1 臨床標本收集收集2019年在中山大學附屬第一醫院進行外科手術治療的10 例PTC 患者的癌組織及癌旁組織。取得的標本用無菌PBS(phosphate buffer saline)洗滌后快速放入液氮儲存待測。本研究通過中山大學附屬第一醫院倫理委員會審核批準。
1.2 細胞以及主要試劑Nthy?ori3?1、BCPAP 、TPC1、KTC1 和K1 細胞購自于北納生物(BNCC)細胞庫。DMEM(Dulbecco's Modified Eagle Medium)培養基和胎牛血清(Fetal Bovine Serum,FBS)購自美國Gibco 公司。BCA 蛋白定量試劑盒、核漿分離試劑盒、TRIzol 試劑及Lipofectamine 3000 購自美國Invitrogen 公司。Transwell 小室購自美國Corning 公司。RIPA 裂解液、CCK?8 試劑盒購自美國Sigma 公司。逆轉錄相關試劑購買于日本TaKaRa 公司。一抗和二抗均購自于美國CST 公司。qRT?PCR 引物于金唯智公司合成。EdU 試劑盒購自銳博公司,Smart Silencer 也由銳博公司設計合成。
1.3 RNA 提取和實qRT?PCR 檢測用TRIzol 試劑提取組織和細胞中的總RNA。采用MMLV 逆轉錄酶和隨機引物逆轉獲得互補脫氧核糖核酸(cDNA)。qRT?PCR 實驗采用SYBR Green 法,用CFX96 實時熒光定量PCR 儀運行標準程序。β?actin 用于標準內參,用2?ΔΔCt計算最終基因表達差異。相關引物序列如下:AC244502.3?201 上游引物:5'?GACAGGGAAGAAGATGAAT?3',下游引物:5'?CGTCTCCTTGTTGATGTA?3';β?actin 上游引物:5'?AGCCATGTACGTAGCCATCCA?3',下游引物:5'?TCTCCGGAGTCCATCACAATG?3';U1 上游 引物:5'?TCCCAGGGCGAGGCTTATCCATT?3',下游引物:5'?GAACGCAGTCCCCCACTACCACAAAT?3';CCND1上游引物:5'?GCTGCGAAGTGGAAACCATC?3',下游引物:5'?CCTCCTTCTGCACACATTTGAA?3';MYC 上游引物:5'?GGCTCCTGGCAAAAGGTCA?3',下游引物:5'?CTGCGTAGTTGTGCTGATGT?3';MMP9 上游引物:5'?TGTACCGCTATGGTTACAC?TCG?3',下游引物:5'?GGCAGGGACAGTTGCTTCT?3';VEGF 上游引物:5'?ATGGACCAGTGAAGCGAT?CAT?3',下游引物:5'?GTTCCTCCAAACTAGAAGC?AGC?3'。
1.4 核漿分離試驗核漿分離試劑盒用于分離細胞核和細胞漿的RNA 組分。qRT?PCR 實驗用于探測AC244502.3?201 的亞細胞定位。β?actin 用于細胞漿的參照標準,U1 用于細胞核的參照標準,引物序列見1.3。
1.5 細胞細胞培養和轉染細胞用含有10%FBS的DMEM 培養基,放置于在37 ℃的5%CO2恒溫孵箱中培養。為了敲低AC244502.3?201在細胞內的表達,由銳博公司設計合成特異性敲低AC244502.3?201 的Smart Silencer。Smart Silencer 由3 條siRNAs和3 條ASOs 構 成。3 條siRNAs 的靶 序 列為:5'?GCAAATCTTCACTGTGAAA?3';5'?TCACTCCTAAT?GGAATCAA?3';5'?GCGAGCAGAACAAATCAAA?3';3 條ASOs 的靶序列為:5'?CCCTATCCATGGT?GACTCCC?3';5'?CTTGCTGAGGTCCCTTCCAC?3';5'?TGATTTGTCTGGTGCACCCA?3'。其對照Nega?tive control(NC)也由銳博公司提供,是由不包含人、鼠和兔的同源序列的3 條siRNAs 和3 條ASOs 構成。Smart Silencer 和NC 的轉染均采用Lipofectamine 3000,按照試劑盒的標準操作進行轉染。
1.6 細胞增殖檢測將細胞接種于96孔板,CCK?8試劑孵育30 min 后,采用分光光度計測量450 nm處的吸光度,每24 h 檢測1 次細胞增殖水平。細胞接種于24 孔板,在EdU 試劑盒說明書的指導下對細胞進行孵育標記,通過計數熒光顯微鏡下能被EdU 標記的陽性細胞數目來檢測細胞增殖效率。細胞接種于6 孔板,10% FBS 培養7 d,4%多聚甲醛固定后采用結晶紫染色,漂洗后于顯微鏡下拍照并進行計數。
1.7 細胞侵襲遷移能力檢測運用8 μm 孔徑的Transwell 小室進行細胞侵襲能力檢測。提前在小室的上室中鋪50 μg 基質膠,加入含4×104個細胞的200 μL 無血清DMEM,下室加入500 μL 含有20%FBS 的DMEM,培養48 h 后,用4%多聚甲醛固定30 min,并用結晶紫染色30 min,漂洗后于顯微鏡下拍照并統計遷移入下室的細胞。細胞遷移實驗則不采用基質膠讓腫瘤細胞遷移24 h。
1.8 雙熒光素酶報告基因檢測實驗NF?κB 信號通路活性檢測采用報告質粒pNFκB?TA?Luc(Clon?tech)。該質粒在熒光素酶基因(Luciferase)前含有NF?κB順式作用增強元件(NF?κB cis?acting enhanc?er element),能夠檢測NF?κB 信號通路的活性。細胞接種于24 孔板,運用Lipofectamine 3000 共轉染Smart Silencer 或NC、pNFκB?TA?Luc 以及Renilla 內參基因,轉染6 h 后更換為含10% FBS 的DMEM 培養基,36 h 后根據Dual?luciferaseTMReport Assay Kit說明書檢測熒光素酶活性。
1.9 Western Blot 檢測采用RIPA 裂解液裂解細胞收集總蛋白,運用BCA 試劑盒測定蛋白濃度。制備蛋白樣品,經SDS-聚丙烯酰胺凝膠(SDS?PAGE)凝膠電泳,聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)轉膜后,用5%的脫脂牛奶封閉60 min。一抗4 ℃孵育過夜、二抗室溫孵育2 h,之后采用ECL 化學發光法進行顯影。
1.10 TANRIC(The Atlas of Noncoding RNAs in Cancer)數據分析TANRIC(https://bioinformatics.mdanderson.org/public?software/tanric/)分析了來源于TCGA(The Cancer Genome Atlas Program)的RNA?seq 數據,使得研究者能夠快速且直觀地分析感興趣的lncRNAs。為了鑒定在甲狀腺癌中具有差異表達的lncRNAs,筆者從TANRIC 中下載了497 例甲狀腺癌樣本及59 例癌旁非癌組織樣本的lncRNAs 數據。利用SPSS 20.0 軟件的成組t檢驗方法分析腫瘤組和癌旁組的差異表達的lncRNAs。
1.11 統計學方法所有統計分析均使用IBM SPSS Statistics 20.0 軟件,統計方法使用t檢驗。P<0.05 為差異具有統計學意義。
2 結果
2.1 AC244502.3?201在PTC 中高表達為了尋找在甲狀腺癌中具有差異表達的lncRNAs,本研究分析了TANRIC 下載的甲狀腺癌lncRNAs 表達數據。取差異倍數≥20倍且P<0.01的lncRNAs(共96個)進一步分析。筆者注意到其中AC244502.3?201 表達明顯升高(P< 0.05,圖1A),且在腫瘤中尚無相關研究報道,于是筆者選擇其進一步深入研究。在收集的10 對成對PTC 組織與相應癌旁組織中采用qRT?PCR 驗證其表達情況,結果顯示AC244502.3?201 在PTC 中的表達量相較癌旁組織明顯升高(P< 0.05,圖1B)。同時qRT?PCR 檢測人正常甲狀腺細胞(Nthy?ori3?1)和4 株PTC 細胞系(BCPAP、TPC1、KTC1 和K1)中AC244502.3?201 的表達量,結果顯示AC244502.3?201 在PTC 細胞系中的表達明顯升高(P<0.05,圖1C)。
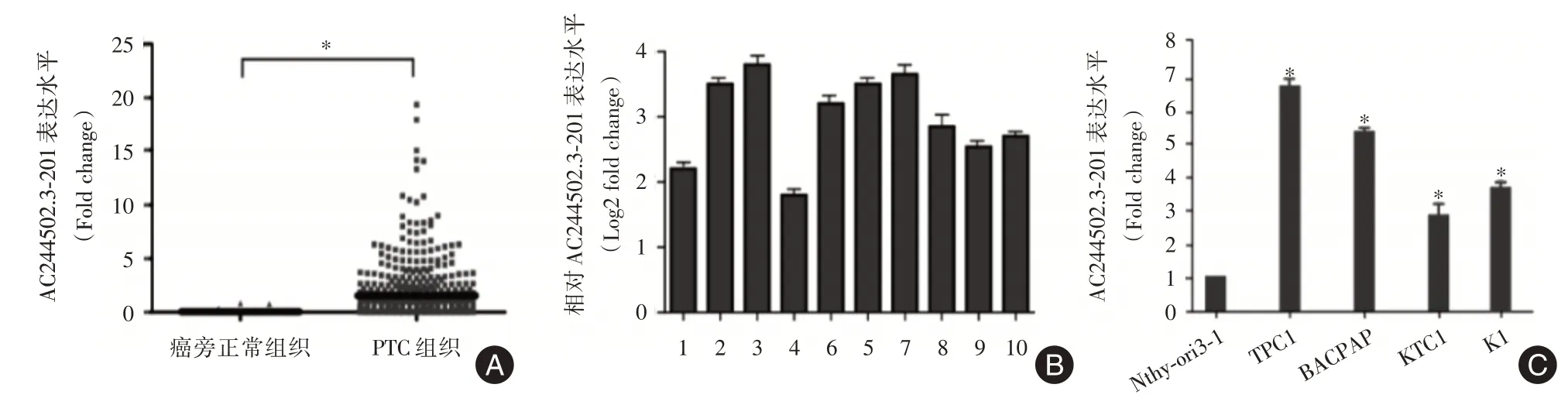
圖1 AC244502.3?201 在PTC 中表達明顯升高Fig.1 The expression of AC244502.3?201 is upregulated in PTC
2.2 AC244502.3?201 的基本生物學特征采用生物信息學軟件(CPC,http://cpc.cbi.pku.edu.cn/)預測AC244502.3?201 的編碼能力,結果表明其不具備蛋白編碼的能力(圖2A)。進一步利用ORF Finder(https://www.ncbi.nlm.nih.gov/orffinder/)分 析AC244502.3?201 的序列,結果顯示AC244502.3?201的序列中不含有>100 個氨基酸的開放閱讀框(圖2B),進一步證實AC244502.3?201 不具備編碼蛋白的能力。在PTC 細胞系(BCPAP 和TPC1)中,核漿分離RNA 實驗結合qRT?PCR 檢測AC244502.3?201細胞定位,結果顯示AC244502.3?201 主要定位于細胞漿(圖2C)。
2.3 細胞水平敲低AC244502.3?201 的表達抑制PTC 細胞的增殖前面結果已表明AC244502.3?201的表達量在BCPAP和TPC1中升高更為明顯,所以選擇BCPAP 和TPC1 細胞用來做敲低實驗驗證生物學功能。采用Smart silencer 敲低AC244502.3?201 的表達,qRT?PCR 實驗結果顯示Smart silencer能顯著降低細胞內AC244502.3?201 的表達(P<0.05,圖3A)。CCK?8檢測結果顯示敲低AC244502.3?201 表達后細胞活力較對照組明顯降低(P<0.05,圖3B)。EdU 實驗結果顯示敲低AC244502.3?201表達的細胞在24 h 之后EdU 標記的陽性細胞數目較對照組明顯減少(P<0.05,圖3C)。克隆形成實驗結果顯示敲低AC244502.3?201 表達之后細胞集落數目顯著低于對照組(P<0.05,圖3D)。
2.4 細胞水平敲低AC244502.3?201 的表達抑制了PTC 細胞的遷移和侵襲在PTC 細胞系(BC?PAP 和TPC1)中敲低AC244502.3?201 表達,Tran?swell 實驗證明敲低AC244502.3?201 表達后,無論是細胞的侵襲還是遷移能力都較對照組顯著下降(P<0.05,圖4A、4B)。
2.5 敲低AC244502.3?201 表達抑制了NF?κB 信號通路在PTC 細胞系(BCPAP 和TPC1)中敲低AC244502.3?201 表達后通過qRT?PCR 檢測增殖、侵襲相關基因的表達水平,發現MYC、CCND1、MMP9及VEGF的表達均明顯下調(P<0.05,圖5A,5B)。考慮這些基因是NF?κB 信號通路的下游效應分子,進一步通過NF?κB 信號通路報告質粒分析AC244502.3?201 是否調控NF?κB 信號通路,結果發現AC244502.3?201 敲低顯著抑制NF?κB 信號通路活性(P< 0.05,圖5C)。同時提取相應細胞的核蛋白,發現AC244502.3?201 敲低顯著抑制NF?κB p65 入核(P< 0.05,圖5D)。以上結果表明AC244502.3?201 調控NF?κB 信號通路。
3 討論
LncRNAs 本身不具有編碼蛋白的能力,長期以來被認為是不具有生物學功能的“轉錄噪音”[12]。近年來大量的研究發現lncRNAs 廣泛參與細胞的各種生物學行為如分化[13]、增殖[14]、衰老[15]、自噬[16]等,在基因轉錄翻譯及或轉錄后調控等個方面發揮重要的調控作用。在PTC 中已經證實多種lncRNAs 的差異表達并在PTC 的發生發展中發揮重要作用,如lncRNA HIT000218960 能夠增強HM?GA2 表達進而促進PTC 的惡性進展[17],而BANCR在PTC 中低表達起抑癌基因的作用[18]。然而這些差異表達的lncRNAs 中大部分的功能和分子機制還未被深入了解。
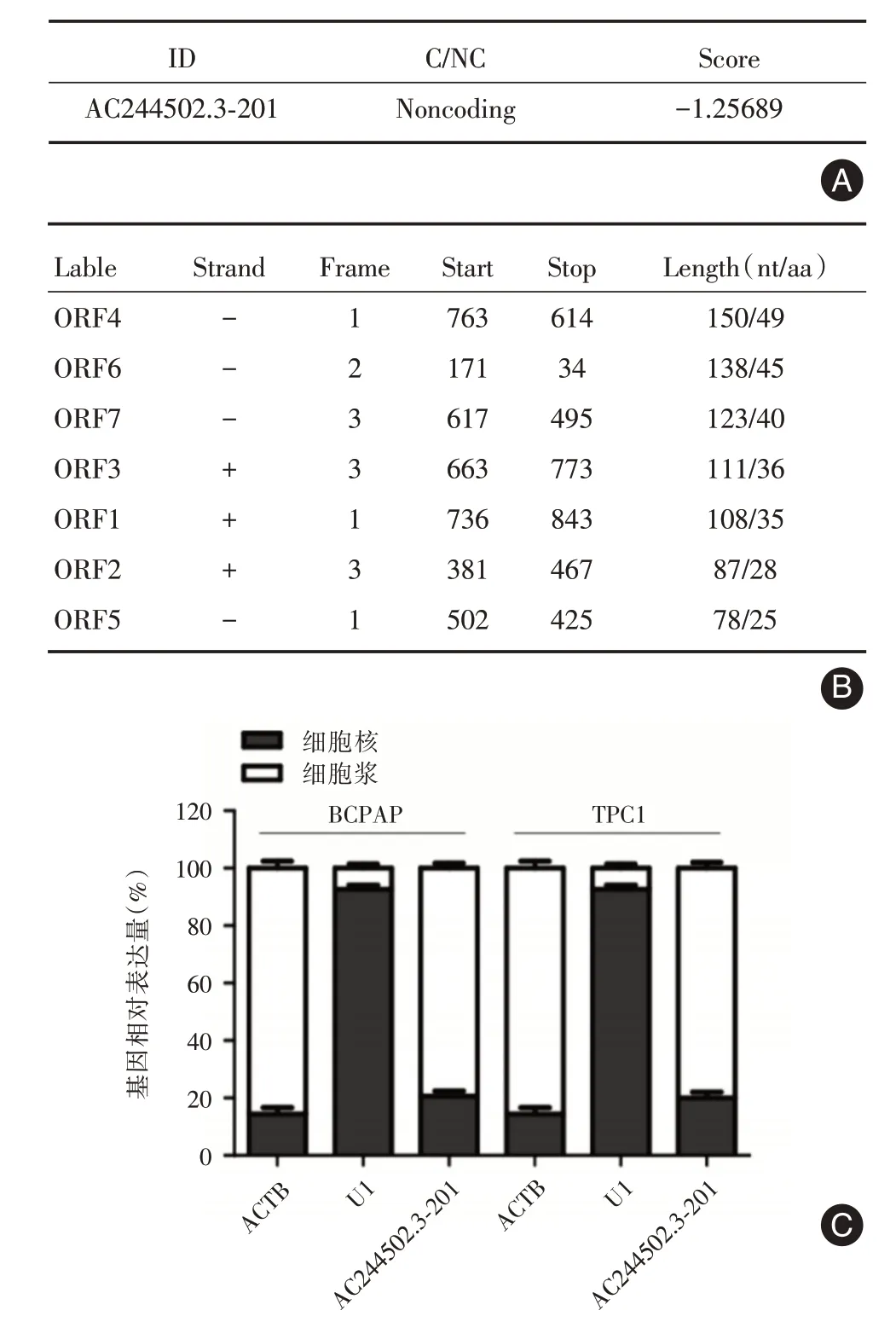
圖2 AC244502.3?201 的基本生物學特征Fig.2 Characters of AC244502.3?201
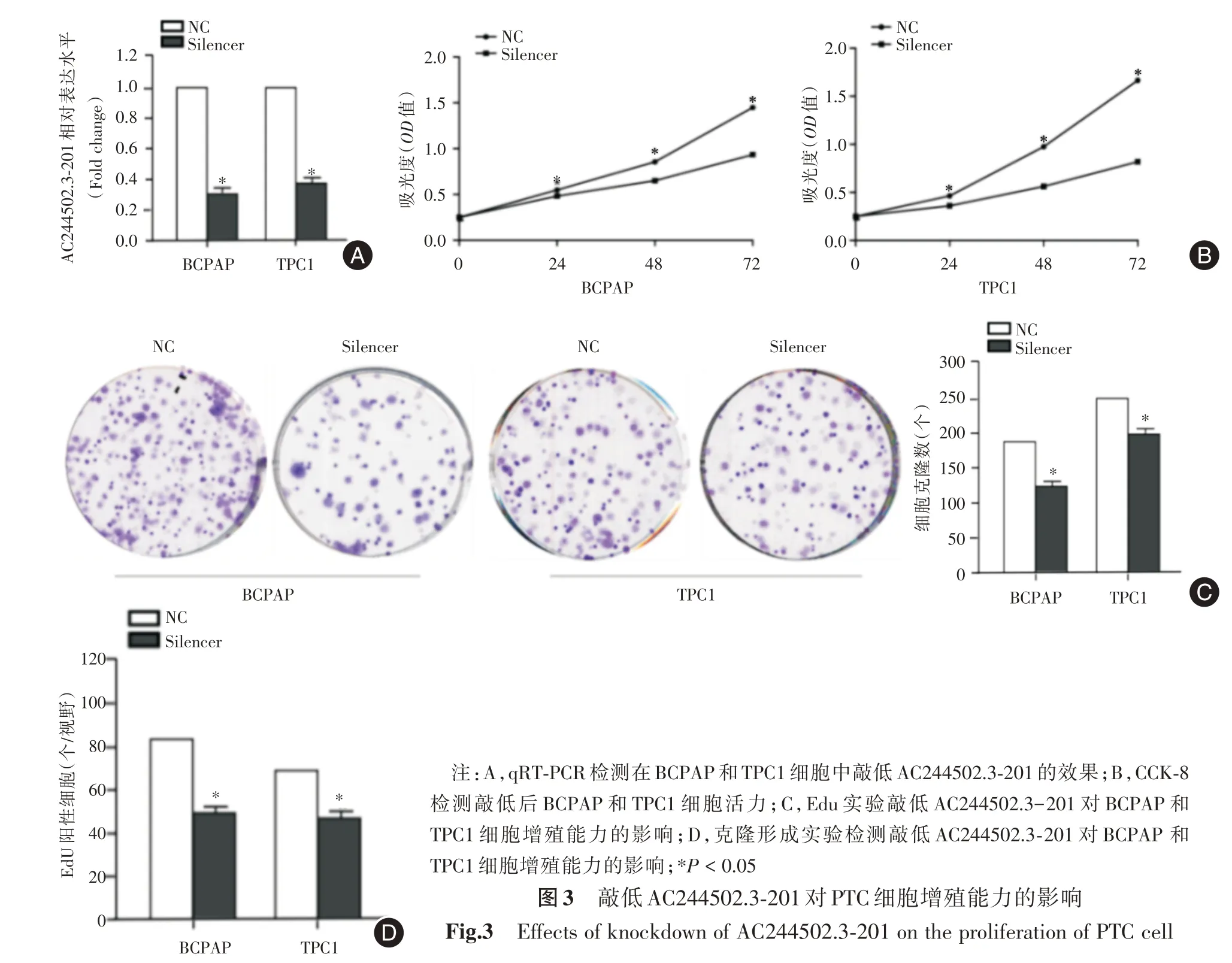
圖3 敲低AC244502.3?201 對PTC 細胞增殖能力的影響Fig.3 Effects of knockdown of AC244502.3?201 on the proliferation of PTC cell
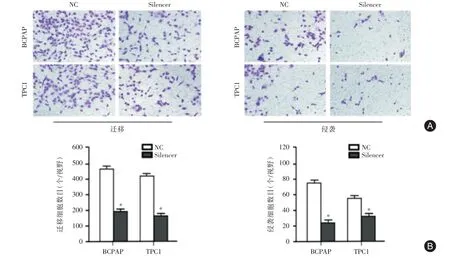
圖4 敲低AC244502.3?201 對PTC 細胞遷移和侵襲能力的影響Fig.4 Effects of knockdown AC244502.3?201 on the migration and invasion of PTC cell
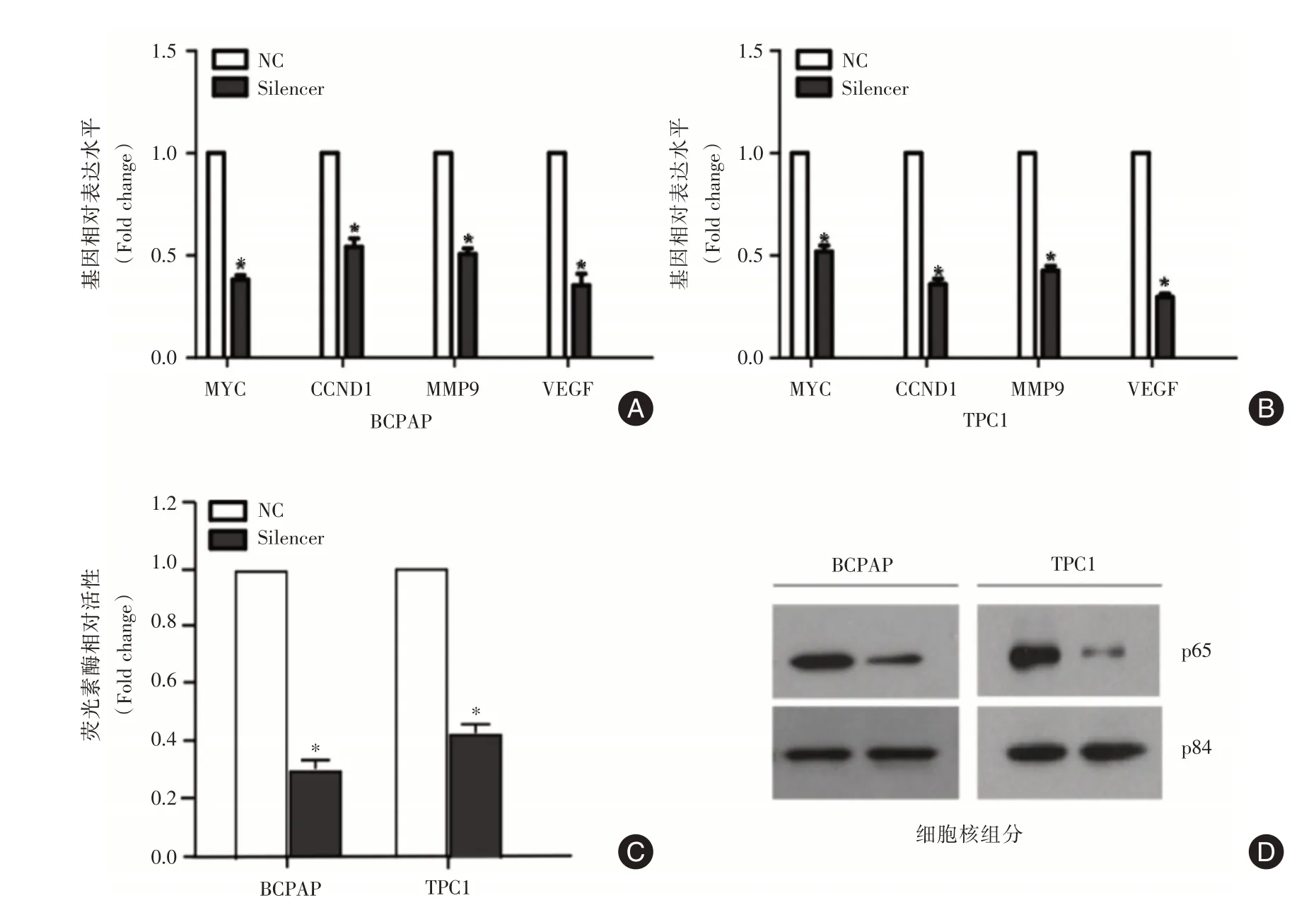
圖5 敲低AC244502.3?201 表達對NF?κB 信號通路的影響Fig.5 Effects of knockdown AC244502.3?201 on the NF?κB signal pathway
關于AC244502.3?201 在腫瘤中的作用目前尚無相關報道。本研究通過對TANRIC 的數據和收集的PTC 患者的癌及癌旁組織進行分析,發現AC244502.3?201 在PTC 組織中表達明顯上調。并進一步驗證了相較于人正常甲狀腺細胞,其在PTC 細胞系的表達也明顯上調。這些提示了AC244502.3?201 在PTC 的發生發展中可能具有重要作用。然后明確了其作為長鏈非編碼RNA 的生物學特性。并進一步通過多種體外實驗證實了敲低AC244502.3?201 能夠抑制PTC 細胞增殖、侵襲和遷徙能力,這證明了AC244502.3?201 能調控PTC 的生物學功能。既往研究證實NF?κB 信號通路參與PTC 的發生發展。如安石榴苷能夠通過NF?κB 信號通路抑制BCPAP 細胞的衰老[19]。也有報道證實了lncRNAs 是NF?κB 信號網絡中的重要一員[20]。然而在PTC 中lncRNAs 與NF?κB 信號通路的關聯尚未被深入研究。本實驗證實敲低AC244502.3?201 抑制了NF?κB 信號通路的活化,同時NF?κB 信號通路下游增殖及侵襲轉移相關的基因的表達也被抑制。這些結果表明AC244502.3?201 通過調控NF?κB 信號通路參與PTC 的惡性進展。本研究首次闡明了AC244502.3?201 在PTC 中的表達、生物學功能及相關分子機制,為PTC 發生發展的理論添加了新的內容,同時為尋找可能的PTC 新的治療靶點提供依據。
本研究的實驗結果證實了AC244502.3?201 參與PTC 的發生發展,本研究不足之處:首先缺乏過表達AC244502.3?201 的相關細胞實驗;其次缺乏體內動物模型的實驗證據;另外AC244502.3?201調控NF?κB 通路的具體分子機制還需要進一步深入研究。后續將通過AC244502.3?201 過表達的細胞模型及體內動物模型中進一步驗證其生物學功能,同時將深入探討明確AC244502.3?201 調控NF?κB 信號通路的具體分子機制。由于lncRNAs發揮生物學功能常常與其亞細胞定位相關,因此結合AC244502.3?201 位于細胞漿和此前報道的lncRNAs 發揮生物學功能的相關分子機制[21-22],AC244502.3?201 可能作為分子支架在細胞漿中與NF?κB 信號通路中的重要調控分子結合發揮作用;也有可能作為誘餌吸附調控NF?κB 信號通路的microRNA 發揮作用。還需相關研究(RNA?pull down 結合質譜分析等)進一步探討AC244502.3?201調控NF?κB信號通路的具體機制。
綜上所述,本研究證實了AC244502.3?201 在PTC 中高表達,在BCPAP 和TPC1 細胞中敲低AC244502.3?201 表達能夠抑制NF?κB 信號通路活性及下游相關基因的表達,最終抑制細胞增殖、侵襲和遷移。研究結果為理解PTC 發生發展的分子機制和可能治療靶點提供新的內容。

