子癇前期孕婦實驗室指標水平及其對妊娠結局的影響
侯書寧 程文國 劉 艷 李瑩瑩 朱新林
子癇前期(preeclampsia,PE)是妊娠期特有疾病,發病率約2%~8%,臨床主要表現為血壓升高并伴有蛋白尿,常累及多個重要器官致其損傷及功能衰竭,嚴重時會危及孕婦和胎兒安全[1-2]。子癇前期的發病機制尚未明確,主要與胎盤著床淺、免疫反應、血管內皮受損、遺傳因素、胰島素抵抗等有關[3-5]。已有研究[6]表明,血脂代謝異常可導致脂質介導的氧化應激和血管內皮損傷,從而引起子癇前期的臨床癥狀。維生素D作為廣泛生物學活性的脂溶性維生素,與妊娠子癇前期的關系也受到人們的關注。本研究選擇468例確診的子癇前期孕婦為研究對象,通過對其維生素D水平、血脂、腎功能、凝血功能指標進行對照分析,擬探討其在子癇前期診斷中的價值。
1 資料與方法
1.1 一般資料 選取2014年1月至2018年12月揚州市婦幼保健院產科定期產檢和分娩確診為子癇前期的孕婦468例為研究對象(觀察組),子癇前期診斷標準參照人民衛生出版社《婦產科學》(第9版)[7]。納入標準:①均為單胎;②孕婦年齡23~35歲;③采血時間10~12孕周;④孕期無特殊服藥史、無心臟病或肝及腎疾病史、無其他妊娠合并癥;本研究經院倫理委員會批準。排除標準:①孕前合并慢性心臟病、高血壓者;②孕前合并腎病、糖尿病者;③孕前存在甲狀腺功能亢進、自身免疫性疾病及血液病等慢性病史。468例子癇前期患者又分為慢性高血壓合并子癇前期組88例、重度子癇前期組380例,其中包括重度子癇前期合并HELLP綜合征16例;另選取同時間正常分娩孕婦375例為對照組,3組一般資料比較差異無統計學意義(P>0.05)。見表1。
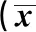
表1 3組孕婦一般資料比較s)
1.2 方法
1.2.1 實驗室指標檢測 研究對象在孕10~12周用分離膠采血管和含抗凝劑采血管抽取外周靜脈血3~5 mL,離心后待檢。①25-羥維生素D (25-dihydroxyvitaminD,25(OH)D)測定:采用ELISA法進行檢測,試劑購自于廣州菲康生物有限公司;②尿酸(uric acid,UA)、血尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine,Cr)、三酰甘油(triglyceride,TG)、總膽固醇(total cholesterol,TC)、低密度脂蛋白(low density lipoprotein,LDL)、鈣離子(calcium,Ca2+)、鎂離子(magnesium,Mg2+)測定:通過邁瑞生化儀BS2000進行檢測,腎功能為速率法,血脂為酶法,電解質為參比法;③纖維蛋白原(fibrinogen,FIB)、D-二聚體(D-dimer,D-D)檢測:通過希森美康CS5100進行檢測,D-D檢測為免疫比濁法,FIB檢測為凝固法。均按照說明書進行操作。
1.2.2 觀察指標 比較三組的25(OH)D、腎功能、血脂、電解質和凝血功能水平。比較慢性高血壓合并子癇前期組和重度子癇前期組不良妊娠結局(包括早產、低體質量兒、胎兒生長受限、新生兒窒息、胎兒窘迫和足月小樣兒)的發生率。

2 結果
2.1 3組25(OH)D、凝血功能和電解質比較 重度子癇前期組25(OH)D、Ca2+水平低于慢性高血壓合并子癇前期組和對照組,D-D、Mg2+濃度高于慢性高血壓合并子癇前期組和對照組,差異均有統計學意義(P<0.05);三組間FIB水平差異無統計學意義(P>0.05)。見表2。

表2 3組25(OH)D、凝血功能和電解質比較
注:與正常妊娠對照組比較,aP<0.05;與慢性高血壓合并子癇前期比較,bP<0.05
2.2 3組腎功能、血脂比較 重度子癇前期組與慢性高血壓合并子癇前期組的UA、BUN、Cr、TG、TC、HDL水平均高于對照組,差異均有統計學意義(P<0.05);重度子癇前期組的UA、BUN、Cr、TG均高于慢性高血壓合并子癇前期組,TC、HDL均低于慢性高血壓合并子癇前期組,差異均有統計學意義(P<0.05)。見表3。
2.3 兩組子癇前期產婦不良妊娠結局比較 兩組子癇前期產婦早產、胎兒生長受限和胎兒窘迫發生率差異有統計學意義(P<0.05),兩組低體質量兒、新生兒窒息和足月小樣兒發生率差異無統計學意義(P>0.05)。見表4。

表3 3組腎功能、血脂比較
注:與正常對照組比較,aP<0.05;與慢性高血壓合并子癇前期比較,bP<0.05
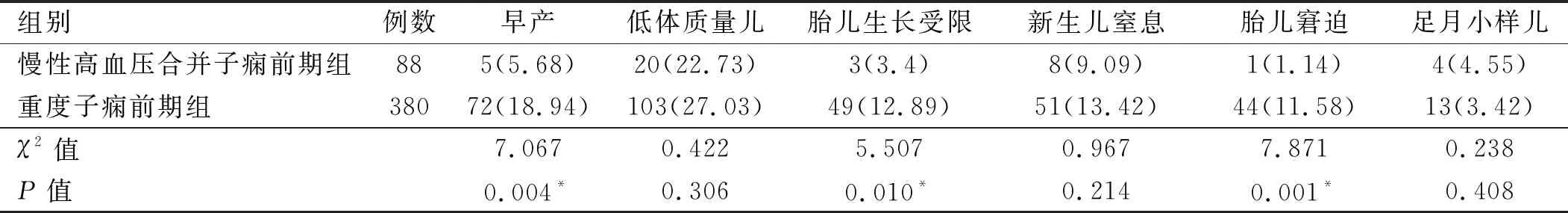
表4 兩組子癇前期產婦不良妊娠結局比較[例(%)]
注:*為Fisher確切概率法
2.4 實驗室指標對子癇前期發生的預測價值 以是否發生子癇前期為因變量(是=1,否=0),單因素分析中差異有統計學意義的指標為自變量,納入自變量的方法為逐步篩選法。結果顯示,血清TG、Mg2+和BUN是子癇前期發生的危險因素,而25(OH)D是保護因素。見表5。

表5 logistic回歸分析實驗室指標在子癇前期發生中的預測價值
2.5 實驗室指標診斷子癇前期的AUC 以靈敏度為縱坐標,1-特異度為橫坐標繪制ROC曲線,實驗室指標診斷子癇前期的AUC見圖1、表6。
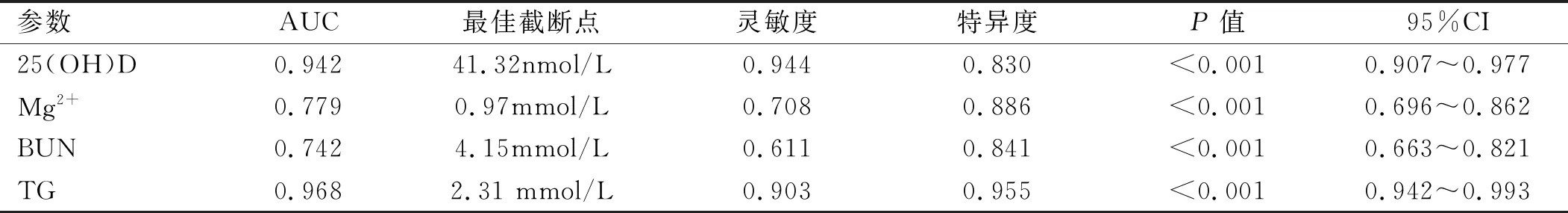
表6 血清25(OH)D、Mg2+、BUN和TG的ROC曲線分析

圖125(OH)D、Mg2+、BUN和TG診斷子癇前期的ROC曲線
3 討論
重度子癇前期是孕婦及胎兒死亡的主要原因之一,具有發病率高、發病時間早、病情重、并發癥多等特點[8]。發生重度子癇前期的孕婦存在全身小動脈痙攣并引起外周阻力增大,導致血壓升高甚至導致胎盤缺血缺氧損傷,且易累及多器官及系統功能障礙。
本研究發現,重度子癇前期組的25(OH)D水平顯著低于慢性高血壓合并子癇前期組和正常對照組,logistic回歸分析表明血清中高濃度的25(OH)D是子癇前期發生的保護因素,說明體內維生素D的缺乏與重度子癇前期的發生密切相關。近年來的研究[9]表明,25(OH)D除了能調節鈣磷代謝外,還具有影響激素分泌、調節免疫應答和控制細胞增殖、分化等作用。鈕玉潔等[10]研究發現,血清25(OH)D的降低能預示發生子癇前期的風險,這與本研究結果相一致。
子癇前期的發生可能與缺鈣有關,已有研究表明,孕期補鈣可使妊娠高血壓發生率下降。本研究發現,跟正常妊娠對照組比較,重度子癇前期組Ca2+降低、Mg2+顯著增高。表明可能由于重度子癇前期孕婦25(OH)D缺乏,腸道對Ca2+吸收率下降,血清鈣濃度失衡,從而促進機體對Mg2+的重吸收,導致血清鎂增高。
重度子癇前期的孕婦因妊娠高血壓導致血管內皮細胞破壞后暴露出膠原組織,可促進血小板聚集和血栓形成,導致血小板減少和凝血功能的紊亂[11]。本研究發現,與慢性高血壓合并子癇前期組和正常對照組相比較,重度子癇前期組的D-D明顯增高,而D-D的增高提示血栓形成,可能導致絨毛壞死和胎盤缺血,預示子癇前期的嚴重程度[12]。FIB是形成血栓的重要因素,本研究中未發現FIB在三組間有顯著變化,為探求原因需要進一步測定纖維蛋白原降解產物來確定子癇前期組的血栓狀態。
妊娠期高血壓除了引起凝血功能紊亂外,還會引起腎功能損傷,出現蛋白尿[13]。本研究發現,跟正常妊娠對照組和慢性高血壓合并子癇前期組比較,重度子癇前期組UA 、BUN 、Cr逐漸增高,差異有統計學意義,表明隨著病情進展,腎功能損傷越嚴重,Lisonkova 等[14]認為,腎功能更好反映PE的嚴重程度。
由于妊娠期的特殊生理需求,在妊娠的中期和晚期血脂水平升高明顯。已有研究[15]表明,血脂代謝水平異常、氧化應激與子癇前期發病關系密切。本研究發現,重度子癇前期血TC、TG和LDL明顯高于正常妊娠對照組,logistic回歸分析顯示血清中高濃度的TG是子癇前期發生的危險因素,表明TG在子癇前期發病起重要作用,這與Siddiqui等[16]研究相符。另外本研究發現,在選取的血清標志物中,TG診斷子癇前期的AUC大于25(OH)D、Mg2+和BUN,即TG代謝異常與子癇前期發生相關性更高,診斷PE價值更高。
妊娠子癇前期時,由于胎盤供血不足、胎盤功能減退,可發生胎兒窘迫、胎兒宮內發育遲緩等妊娠不良結局。本研究表明,相對于慢性高血壓合并子癇前期組,重度子癇前期組患者的早產、宮內生長受限和胎兒窘迫發生率顯著升高。
綜上所述,隨著子癇前期病情的發展,25(OH)D逐漸降低,而TG、BUN和Mg2+逐漸升高,因此分析血清25(OH)D、TG、BUN和Mg2可能對早期發現、早期干預子癇前期和減少不良妊娠的發生率有積極作用。但本研究尚未對正常妊娠組的孕中期、孕晚期實驗室指標進行分析比較,這些實驗室指標預測子癇前期發展仍需要進一步的深入探討。

