阿莫西林膠囊微生物計數方法適用性研究
劉南
(上海原能細胞生物低溫設備有限公司,上海201203)
阿莫西林膠囊是膠囊劑,填充物為白色或類白色粉末,主要成分是阿莫西林。阿莫西林膠囊成品以阿莫西林為主要原料,填充至藍黃色的膠殼中。本單位生產的阿莫西林膠囊的膠殼是藍黃色,型號1#,主要成分是食用級明膠。阿莫西林膠囊主要適用于敏感菌所引起的感染,即不能分泌β- 內酰胺酶的細菌。阿莫西林膠囊作為青霉素類的廣譜抗生素,其抗菌譜范圍較大,主要包括敏感性的球菌或桿菌所引起的上呼吸道感染、敏感菌所引起的泌尿系統感染、敏感菌侵染皮膚傷口造成的感染、敏感菌引起的急性支氣管炎和下呼吸道感染等。
2015 版《中國藥典》要求企業在對藥品進行微生物限度檢查時,應對微生物計數方法進行計數方法適用性試驗,確保微生物計數方法適合該產品的微生物計數。本次試驗的技術難點主要體現在對阿莫西林膠囊進行微生物限度檢查時,樣品中的抑菌物質可能會抑制樣品中微生物的生長,導致出現假陰性的可能性。阿莫西林膠囊作為β- 內酰胺類抗生素,對革蘭氏陽性菌和芽孢桿菌具有較強的抑制作用;對革蘭氏陰性菌也有一定的抑制作用,也就是說檢驗樣品存在抑菌性,需要在試驗過程中找到合適的方法消除抑菌性。根據2015 版《中國藥典》四部通則,對于β- 內酰胺類抗生素,可加入β- 內酰胺酶用于中和毒性。
在藥品的生產質量控制中要能夠準確地檢出樣品中的微生物,使藥品中的微生物檢驗不因檢驗方法的缺陷而出現明顯的偏差。為保證產品微生物檢驗結果的可靠性,微生物計數方法須進行適用性試驗,通過試驗數據的客觀性來判定方法的可靠性。
微生物回收時,如何去除樣品中的抑菌物質,保證樣品中的微生物能夠被檢出,避免出現假陰性的結果是一大難題。需要通過試驗證明這種去除抑菌物質的方法是可靠的,不僅能夠去除抑菌物質,還不影響微生物的檢出。試驗過程中注意設置合理的試驗組和對照以判定試驗是否存在系統誤差。
β- 內酰胺類抗生素是一種殺菌劑,它能抑制細菌細胞壁中肽聚糖的形成,從而殺滅細菌。真菌細胞壁的主要成分是幾丁質、脫乙酰殼多糖、葡聚糖、纖維素、半乳聚糖等。因此β- 內酰胺類抗生素對真菌無抑制作用。阿莫西林膠囊屬于β- 內酰胺類抗生素,因此對細菌的回收可以考慮在供試液中添加β-內酰胺酶,用來中和供試品中抑菌活性物質;霉菌和酵母菌則可以用平皿法回收。
1 試驗材料與儀器
1.1 樣品
阿莫西林膠囊,上海美優制藥有限公司,規格:0.25g,批號:150703。
1.2 儀器設備
生物安全柜(型號:BSC-02IIA2,蘇州安泰空氣技術有限公司);風熱消毒箱(BZF-50,上海博訊實業有限公司);生化培養箱(型號:LRH-70,上海一恒科學儀器有限公司);霉菌培養箱(型號:MJX-250B-Z,上海博訊實業有限公司);電熱恒溫培養箱(型號:SPX-250B,上海博訊實業有限公司);電子天平(BSA-8201, 德國賽多利斯公司);脈動蒸汽滅菌器(型號:SCM-D/JA,連云港千櫻醫療設備有限公司)。
1.3 菌種
白色念珠菌(Candida albicans)〔CMCC(F)98001〕、銅綠假單胞菌(Pseudomonas aeruginosa)〔CMCC(B)10104〕、金黃色葡萄球菌(Staphylococcus aureus)〔CMCC (B)26003〕、枯草芽孢桿菌(Bacillus subtilis)〔CMCC(B)63501〕、黑曲霉(Aspergillus niger)〔CMCC(F)98003〕。微生物計數方法適用性試驗,將上述的5 種菌株作為試驗菌,標準菌株從中國醫學細菌保藏中心采購且能溯源,工作菌株為第三代。
1.4 培養基
胰酪大豆胨瓊脂培養基(TSA)、沙氏葡萄糖瓊脂培養基(SDA)、胰酪大豆胨液體培養基(TSB)、沙氏葡萄糖液體培養基(SDB),干粉培養基均由上海盛思生化科技有限公司生產。
1.5 試劑
稀釋液:PH7.0 氯化鈉- 蛋白胨緩沖液,上海盛思生化科技有限公司生產。
中和劑:β- 內酰胺酶,杭州北望生物技術有限公司生產。
表面活性劑:聚山梨酯80,國藥集團化學試劑有限公司生產。
2 試驗方法
2.1 菌液制備
將金黃色葡萄球菌的第二代標準貯備菌株、銅綠假單胞菌的第二代標準貯備菌株、枯草芽孢桿菌的第二代標準貯備菌株,分別挑出一環新鮮培養于胰酪大豆胨液體培養基(TSB)中,33℃培養24 小時,得到第三代工作菌株;白色念珠菌的第二代標準貯備菌株挑出一環新鮮培養物,接種至沙氏葡萄糖液體培養基(SDB)中,23℃培養3 天,得到第三代工作菌株;黑曲霉的第二代孢子懸液挑出接種至沙氏葡萄糖瓊脂培養基斜面上,23℃培養7 天,用5ml 含0.05%(ml/ml)聚山梨酯80 的PH7.0 無菌氯化鈉- 蛋白胨緩沖液將黑曲霉孢子洗脫。分別取上述濃菌液1ml 加至9ml 的PH7.0 無菌氯化鈉- 蛋白胨緩沖液中,10 倍梯度稀釋至約為104cfu/ml。
2.2 供試液制備
稱取阿莫西林膠囊10g,分別加PH7.0 無菌氯化鈉- 蛋白胨緩沖 液 至100ml、200ml、500ml,37℃水浴,充分搖勻,使成1:10、1:20、1:50 供試液。
2.3 方法適用性試驗
2.3.1 平皿法
試驗組:取制備好的1:10、1:20、1:50 供試液分裝至無菌試管中,每管裝量9.9ml,分別加入金黃色葡萄球菌菌懸液、銅綠假單胞菌菌懸液、枯草芽孢桿菌菌懸液、白色念珠菌菌懸液和黑曲霉孢子懸液各 0.1ml (含菌量不超過104cfu/ml)。
菌液組:取PH7.0 無菌氯化鈉- 蛋白胨緩沖液分裝至無菌試管中,每管裝量9.9ml,分別加入金黃色葡萄球菌菌懸液、銅綠假單胞菌菌懸液、枯草芽孢桿菌菌懸液、白色念珠菌菌懸液和黑曲霉孢子懸液各 0.1ml (含菌量不超過104cfu/ml)。
供試品對照組:取制備好的1:10、1:20、1:50 供試液分裝中無菌試管中,每管裝量9.9ml,加PH7.0無菌氯化鈉- 蛋白胨緩沖液0.1ml。
回收率:取上述試驗組、菌液組、供試品對照組1ml,置直徑90mm 的無菌平皿中,注入15~20ml 溫 度 不 超 過 45℃ 的TSA/SDA,混勻,凝固,倒置培養。TSA:33℃培養3 天;SDA:23℃培養5 天,計數。供試品回收率=(試驗組菌落數- 供試品對照組菌落數)/菌液組對照數。供試品需進行3 次獨立平行試驗。
2.3.2 中和法
試驗組:分別將400 萬(800 萬、1200 萬)單位β- 內酰胺酶加至1:10、1:20、1:50 供試液中。將1:10、1:20、1:50 經中和的供試液分裝至無菌試管中,每管裝量9.9ml,分別加入試驗菌各0.1ml(含菌量不超過104cfu/ml)。
菌液組:分別將400 萬(800 萬、1200 萬)單位β- 內酰胺酶加于9.9ml 的PH7.0 無菌氯化鈉- 蛋白胨緩沖液中,分別加入試驗菌各0.1ml(含菌量不超過104cfu/ml)。
供試品對照組:分別將400 萬(800 萬、1200 萬)單位β- 內酰胺酶加于1:10、1:20、1:50 供試液中,每管裝量9.9ml,加PH7.0無菌氯化鈉- 蛋白胨緩沖液0.1ml。
回收率:取上述試驗組、菌液組、供試品對照組1ml,置直徑90mm 的無菌平皿中,注入15~20ml 溫度不超過45℃的TSA,混勻,凝固,倒置培養,33℃培養3 天,計數。供試品回收率=(試驗組菌落數- 供試品對照組菌落數)/菌液組對照數。供試品需進行3 次獨立平行試驗。
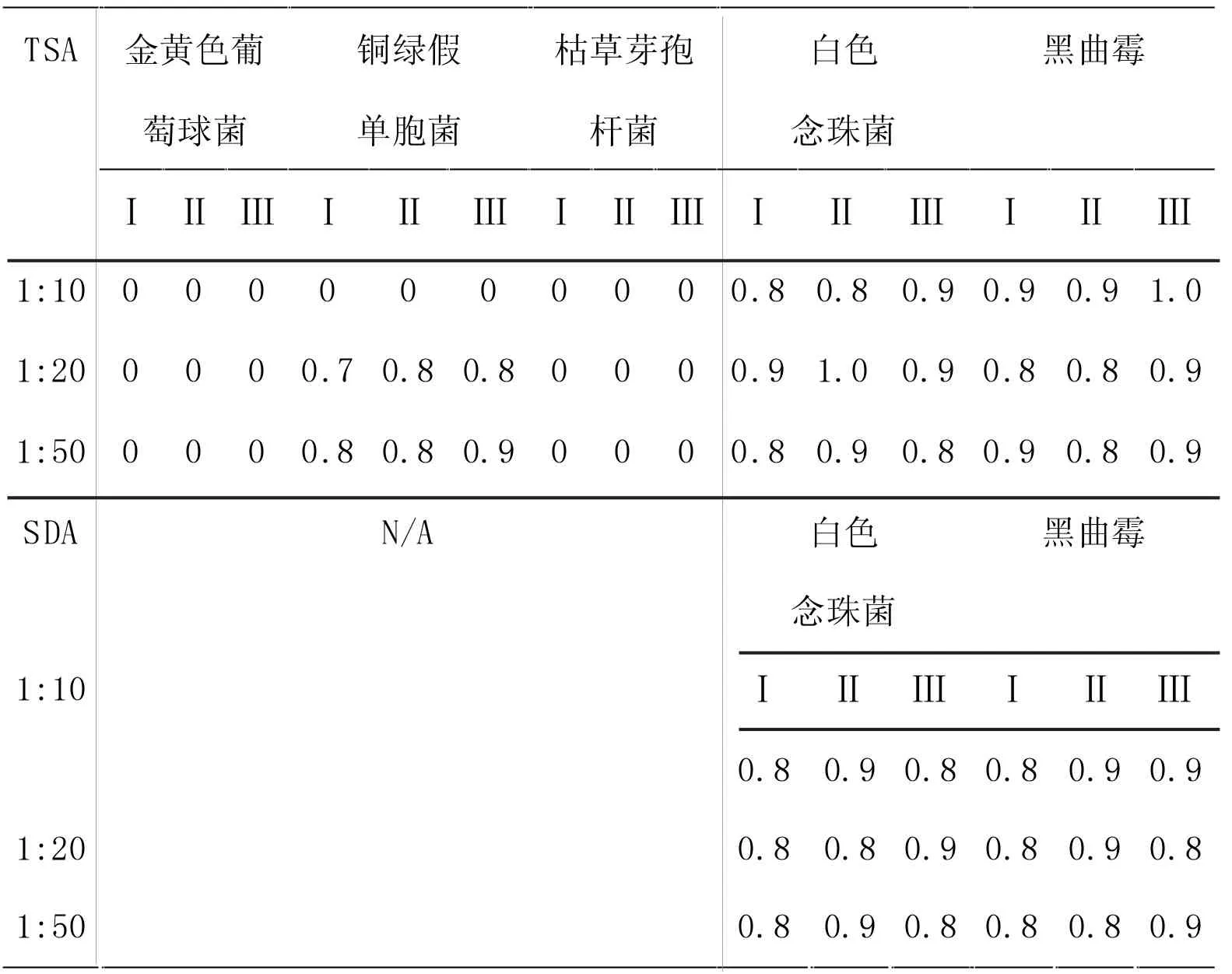
表1 平皿法進行微生物計數方法適用性的回收率

表2 中和法進行微生物計數方法適用性的回收率
3 試驗結果分析
阿莫西林膠囊采用平皿法進行需氧菌總數、霉菌和酵母菌總數計數方法適用性試驗,發現金黃色葡萄球菌和枯草芽孢桿菌的回收率為0,即金黃色葡萄球菌和枯草芽孢桿菌無法通過平皿法回收。銅綠假單胞菌在1:20 供試液下的回收率在0.5~2范圍內,即銅綠假單胞菌可采用平皿法(1:20 供試液)收回。霉菌和酵母菌在1:10 供試液下的回收率在0.5~2 范圍內,即霉菌和酵母菌可采用平皿法(1:10 供試液)收回。詳見表1。
阿莫西林膠囊采用中和法進行金黃色葡萄球菌和枯草芽孢桿菌計數方法適用性試驗,發現金黃色葡萄球菌和枯草芽孢桿菌在1:10 供試液加1200 單位的β- 內酰胺酶、1:20供試液加1200 單位的β- 內酰胺酶、1:50 供試液加400 單位的β- 內酰胺酶、1:50 供試液加800 單位的β- 內酰胺酶的回收率均不在在0.5~2 范圍內,無法回收。發現金黃色葡萄球菌和枯草芽孢桿菌在1:50 供試液加1200 單位的β- 內酰胺酶的回收率在0.5~2 范圍內,即金黃色葡萄球菌和枯草芽孢桿菌可采用稀釋法(1:50 供試液)和中和法加1200 單位的β- 內酰胺酶回收。詳見表2。
3.1 平皿法回收率
由表1 可知,霉菌和酵母菌總數計數可直接采用平皿法(1:10 供試液)。需氧菌總數計數(銅綠假單胞菌、白色念珠菌和黑曲霉)通過平皿法可以回收。
3.2 中和法回收率
由表2 可知需氧菌總數(金黃色葡萄球菌和枯草芽孢桿菌)計數,可采用中和法(1:50 供試液+1200 萬單位的β- 內酰胺酶)回收。結合表1 可知,需氧菌總數(金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌、白色念珠菌和黑曲霉)可采用稀釋法、中和法聯合使用,即1:50 供試液中,加1200 萬單位的β- 內酰胺酶回收。
4 結論
作為藥品微生物限度檢查的一種方法,微生物計數法應確保其可靠性,具體驗證方法可參考2015 年版《中國藥典》。通過對最終產品的微生物計數,從而判別其檢出結果是否符合相關國家標準或行業標準的要求以及企業產品質量要求。檢驗結果符合要求也能為藥品的出廠放行,提供微生物負載定量證據。
阿莫西林膠囊屬于β- 內酰胺酶類抗生素,本身會對部分細菌產生殺滅作用,也會使得部分致病菌處于損傷狀態或在檢驗培養體系中抑制致病菌的活性,但在適宜的條件下,這類被抑制的微生物可能會“復活”。如果這類被損傷的致病菌進入人體,它們可能會在血液中修補損傷從而恢復活性,“復活”后的致病菌會在血液中大量繁殖,從而危害人體健康。
微生物計數方法適用性試驗不僅是2015 版《中國藥典》的要求,更是確保企業微生物計數方法的可靠性,保證藥品中的微生物能夠被檢出,不會因為抑菌作用出現“假陰性”的可能性。
綜上所述,對阿莫西林膠囊這種β- 內酰胺類抗生素聯合使用稀釋法、中和法,即在1:50 供試液中加1200 萬單位的β-內酰胺酶回收需氧菌。采用平皿法,即1:10 供試液,直接回收霉菌和酵母菌。

