疝囊復發種植性黏液腺癌1例報告
楊勇 吳曉陽
黏液腺癌是一種好發于消化道的腫瘤,而疝囊復發種植性黏液腺癌在臨床上十分少見。我科收治1例病人,現報道如下。
1 病例介紹
病人,男性,83歲。因“右側腹股溝區復發難復性包塊20年”于2018年5月2日入院。病人曾于1998年發現右側腹股溝區一腫物,未予特殊重視,近半年病人自覺脹痛不適。查體:發育正常,營養中等,結膜未見明顯黃染;心肺無顯著變化;腹部平坦,無腹壁靜脈曲張,未見胃腸型及蠕動波,未觸及包塊;肝、脾肋下未觸及;腸鳴音正常;右側腹股溝區觸及一腫塊,約4 cm×5 cm 大小,質地偏韌,用手可將腫塊稍許回納。病人既往有“右側腹股溝疝”手術史30 年,有“血吸蟲”病史50 年,有“幽門螺桿菌感染史”10 年。無高血壓、DM、家族性腫瘤病史。B超示:右側腹股溝腫塊、腹腔積液。腹部CT 示:右側腹股溝疝(圖1)。術前擬診斷為:右側腹股溝復發疝。病人于2018年5月7日在手術室腰麻下行右側腹股溝疝無張力修補術[1]+右側睪丸切除術。術中見右側腹股溝區疤痕增生明顯,觸及質地偏韌腫塊,局部組織關系不清,遂于恥骨結節處解剖精索,探見疝囊頸位于腹壁下動脈外側,沿精索向內環口分離,分離過程中精索與疝囊致密粘連,無法分離。考慮病人年紀較大且既往手術瘢痕增生,分離疝囊易導致精索血管損傷斷裂而引起睪丸壞死,與家屬溝通后決定切除右側睪丸。離斷精索血管切除右側睪丸后,打開疝囊,見黃色液體流出,考慮腹腔滲出液,疝囊壁厚度約2 cm,中間夾雜著黃白色膠凍樣物質,未見腸管及大網膜,疝囊頸內側壁有粘連增生,較狹窄,但可與腹腔相通。術中考慮黏液瘤腹腔種植可能,保護術野,切除右側睪丸加全部疝囊及疝內容物送病理,探查右下腹腔內臟器,未見異常,用proline 線連續縫合腹膜關閉腹腔,于腹膜前創建間隙,將聚丙烯補片于間隙鋪平,逐層縫合腹壁,病人安返病房。術后6 d,病人恢復良好,無明顯不適出院。術后1 周病理回報:(右側)睪丸及附睪組織萎縮,(疝囊)纖維組織中見轉移性或浸潤性腺癌組織,部分為黏液腺癌。病人再次住院完善檢查,查消化道腫瘤指標稍有增高;行腹部增強CT 示:右下腹腸管糾集伴局部腸管管壁稍增厚,腹部網膜模糊增厚,伴不均勻強化;纖維結腸鏡檢查未發現腫瘤,傷口局部未見種植轉移,建議病人行PET-CT 檢查,病人及家屬拒絕。隨訪8 個月至今無明顯不適表現。
2 討論
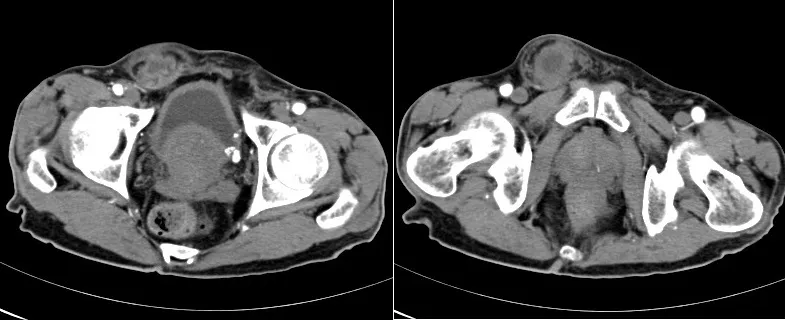
圖1 腹部CT
腹股溝疝是臨床中常見的疾病,術前診斷一般較為明確[2],也是中老年人群的常見病、多發病。隨著我國人口老齡化,此類病人數量會越來越多。有些老年病人會因各種原因長期帶疝生存,若此類病人出現腹腔腫瘤,發生腹腔種植轉移至疝囊,在理論上是可能存在的。黏液腺癌是一種好發于消化道、乳房、肺、卵巢、子宮等部位的腫瘤。黏液腺癌細胞來源于具有多向分化的潛能細胞,由于分化微環境的不同而產生不同的黏液類型[3]。癌細胞內外可見大量的黏液,細胞外黏液可形成大小不等且不規則的“黏糊狀”。黏液腺癌分為單純性黏液腺癌和混合性黏液腺癌,單純性黏液腺癌由于轉移少預后較好,而混合性黏液腺癌預后稍差。對于黏液腺癌的治療一般采用手術切除,如明確發生在消化道、肺、乳腺等部位包膜完整無轉移的黏液腺癌,手術切除是其不二的選擇;對于一些晚期黏液腺癌伴包膜潰破,發生廣泛的腹腔播散和盆腔種植性轉移時,臨床上是否行完全的減瘤術,獲得組織標本進行病理評估腫瘤分級,目前沒有統一標準。有資料表明,對于黏液腺癌伴腹腔大面積轉移,并出現嚴重腹脹、腹水、便秘、食欲減退等癥狀時可行最大程度減瘤術聯合最大區域化療(腹腔熱灌注化療)[4]。針對本病例,筆者經查閱文獻發現黏液腺癌轉移至疝囊的報道目前很少。臨床中對腹股溝疝常規行前入路腹股溝疝手術,通常采用腹膜前間隙填充修補材料的方法,為不造成腹膜局部缺損致腹膜局部張力升高,通常情況下疝囊并不切開,完整分離疝囊后,將其還納回腹腔。但有時發現病人疝囊或疝內容物有異常表現,多數為疝囊反復與周圍組織摩擦刺激造成的粘連增生。也有報道認為應對肉眼所見異常的疝囊行鏡檢,以免將隱匿性轉移癌漏診。本例病人因術中見疝內容物較堅韌,遂行切開探查,結果有陽性發現。此病人行前入路無張力腹股溝疝修補術,術中于腹膜前間隙填充人工修補材料,術后8 個月未見傷口局部有腫瘤種植轉移。但針對腹股溝疝囊內考慮惡性腫瘤時,是否可以填充修補材料,目前臨床上病例較少。若此病例選擇行經腹腹膜前疝修補術(TAPP),可進一步行腹腔探查,尋找腫瘤原發灶。但若行完全腹膜外疝修補(TEP),術中如何處理值得臨床醫生們思考。

