鈉離子電池磷酸鹽正極材料研究進展
曹鑫鑫,周江,潘安強,梁叔全
中南大學材料科學與工程學院,長沙 410083
1 引言
隨著高新科技的快速發展和城鎮化進程的不斷深入,能源和環境問題成為人類面臨的重大挑戰。目前人類消耗的能源主要是由煤炭、石油和天然氣等化石燃料提供的。但是,地球上的化石燃料是歷經上億年才演化而成的,其儲量有限且不可再生。同時,伴隨著傳統能源的大量消耗,衍生了一系列嚴峻的環境問題,如溫室氣體排放、酸雨、霧霾、熱污染等。因此,優化能源供給結構、探索和應用可再生清潔能源、提高能源儲存和轉化效率、控制三廢污染排放、改善氣候環境成為世界能源格局可持續發展的重要戰略目標。在新能源開發中,水能、太陽能、風能、潮汐能、生物能等綠色可再生清潔能源技術都具有重大的應用價值1。但這些能源供給的不穩定性和間歇性極大的限制了其并網使用。因此,開發與可再生新能源適配的高效儲能系統尤為重要。另一方面,新能源汽車的推廣是解決石油短缺和城市污染問題的有效途徑。動力電池技術是新能源汽車發展的核心,開發高比能、高安全、低成本、長壽命的動力電池已成為新能源汽車持續發展和市場推廣的瓶頸和關鍵所在。此外,隨著移動互聯網和通訊技術的高速發展,便攜式電子設備、人工智能裝備等正在迅速走進千家萬戶并改變著人們的生活方式,也推動著高能量密度、高安全二次電池技術的迅速發展。因此,開發二次電池儲能新技術關系到人類的可持續發展與生產生活方式的改變2。
現有的二次電池體系包括鉛酸電池、鎳鎘電池、釩液流電池、高溫鈉硫電池、鋰離子電池和鈉離子電池等3。其中鉛酸電池和鎳鎘電池能量密度低、污染環境且存在記憶效應。釩液流電池運行和維護的成本較高,且釩氧化物易析出破壞電池結構。高溫鈉硫電池需要較高的工作溫度,其安全問題不容小覷。鋰離子電池由于其自放電慢、循環壽命長、無記憶效應、能量/功率密度高等優勢在電化學儲能領域占據主導地位。自從索尼公司在上世紀九十年代將鋰離子電池成功商業化以來,鋰離子電池的應用已經從最初的消費類電子產品迅速擴張到新興電動/混合動力汽車、電網儲能、航空航天等領域。鋰離子二次電池如火如荼的迅速發展也使鋰資源短缺的問題日益突出。鋰在地殼中的含量約為0.0065%,其分布不均衡且提取難度大。這極大限制了鋰離子電池在大規模儲能領域的廣泛應用4。
鈉離子電池具有與鋰離子電池類似的電化學脫嵌機理,且鈉在地殼中的儲量豐富(約占地殼儲量的2.75%)、價格低廉(工業級碳酸鈉約250美元/噸),近些年受到廣泛關注5。但由于鈉的離子半徑比鋰大,使得鈉離子的擴散動力學遲緩,且易引起宿主材料體積應變,開發可穩定脫嵌鈉離子的材料成為鈉離子電池發展的關鍵6。另外,鈉與鋰相比原子質量更大且標準電極電勢更高,可見鈉離子電池的能量密度低于鋰離子電池。但是鈉離子電池以其成本和環保優勢有望替代鉛酸電池應用于低速交通和儲能領域。
目前針對鈉離子電池的研究主要集中在開發新型高能量密度電極材料、開發高安全性能的固態電解質、負極金屬保護技術及電池管理系統等。其中,正極材料是直接影響電池整體性能的核心因素,它既是鈉離子電池比能量提高的瓶頸,也是決定鈉離子電池成本的最重要因素(約占整個電池成本的35%–40%)7,8。因此,鈉離子電池技術能否取得新突破,其關鍵在于電極材料的創新研究。探索新型正極材料、調控材料結構、弄清電極結構與電化學性能之間的構效關系對發展高性能鈉離子電池具有重要的科學意義與實際應用價值。
2 鈉離子電池概述
2.1 鈉離子電池的組成和特征
鈉離子電池的結構與鋰離子電池類似,一般由正極、負極、電解液、隔膜、集流體和電池殼等組成,如圖1所示9。正極材料一般是電位較高的嵌鈉化合物,如過渡金屬層狀氧化物NaxMO2(M為過渡金屬)、聚陰離子型化合物和普魯士藍類似物等。負極材料一般是電極電位較低的碳材料、合金類材料及金屬氧化物、硫化物等。電解液一般用有機溶劑和鈉鹽配制而成,常用的有機溶劑有碳酸乙烯酯(EC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、乙二醇二甲醚(DME)、碳酸丙烯酯(PC)、碳酸甲乙酯(EMC)和氟代碳酸乙烯酯(FEC)等,常用的鈉鹽有高氯酸鈉(NaClO4)、六氟磷酸鈉(NaPF6)、雙(三氟甲基磺酰)亞胺鈉(NaTFSI)和三氟甲基磺酸鈉(NaCF3SO3)等。隔膜一般是玻璃纖維、聚丙烯(PP)或聚乙烯(PE)微孔膜,主要用于隔離正負極材料防止內部短路,同時確保鈉離子能夠自由穿梭。
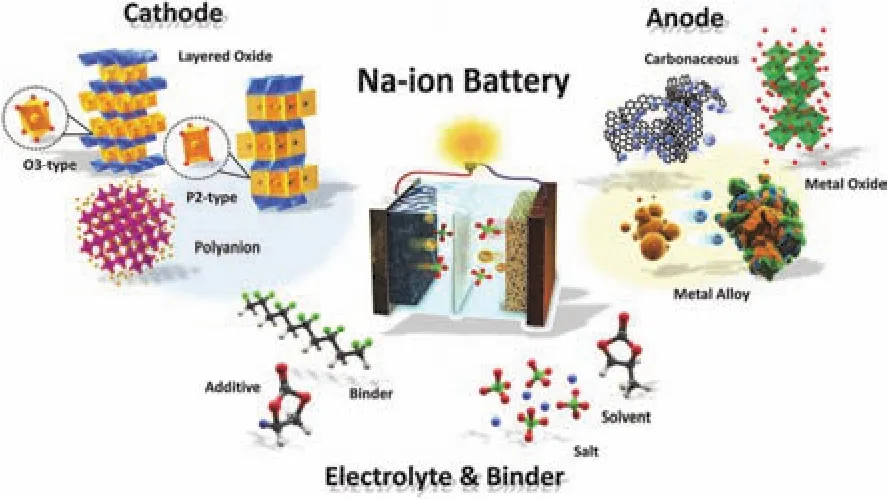
圖1 鈉離子電池的組成示意圖9Fig. 1 Schematic of the composition for sodium-ion battery system 9.
與商業化鋰離子電池相比,鈉離子電池具有許多潛在的優勢。首先是資源優勢,鈉是地殼中豐度排名第六的元素,大量存在于長石、方鈉石和巖鹽等礦物中。此外,海洋是一個巨大的鈉資源庫,其中氯化鈉的含量約為2.7%。因此,作為鈉離子電池原材料的鈉金屬和鈉鹽是非常廉價的。其次,鈉離子電池的集流體更便宜、輕便。鋁金屬與鋰容易發生反應生成二元合金,但對于鈉是穩定的。因此,在鈉離子電池中,鋁可以取代昂貴的銅作為負極的集流體,且鋁的密度低于銅,更有利于電池質量能量密度的提升。第三,金屬鈉比鋰更柔軟,可以通過機械壓力或者改進隔膜的機械性能來抑制鈉枝晶的形成10。但是鈉離子電池也存在致命的缺陷,金屬鈉的熔點較低,易產生熱失控現象。另一方面,鈉離子半徑比鋰離子大34%,使得鈉離子更難嵌入電極材料晶體結構中,發生化學反應。由于鈉離子的體積較大,儲鈉材料的比容量一般低于儲鋰化合物,且其晶體結構中需要足夠大的間隙來容納鈉離子。
2.2 鈉離子電池的工作原理
圖2為鈉離子電池的工作原理示意圖11。采用不同的正負極材料,其脫嵌鈉離子的機理有所不同。這里以層狀NaMnO2為正極材料、硬碳為負極材料的鈉離子電池為例闡述其工作原理,其正負極反應式如下:
正極反應:
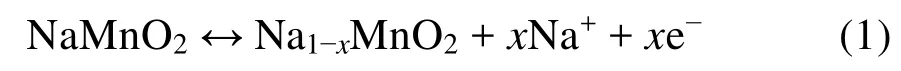
負極反應:
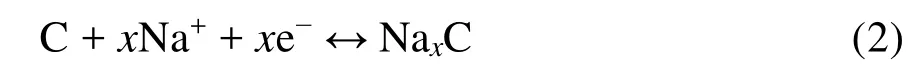
電池反應:
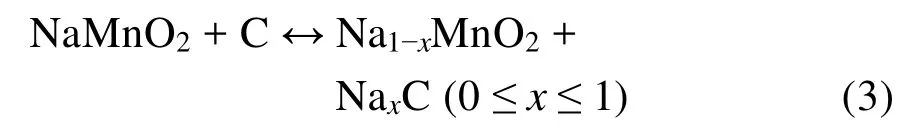
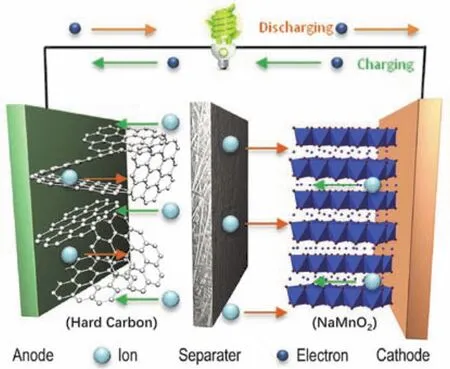
圖2 鈉離子電池的工作原理示意圖11Fig. 2 Schematic of mechanism illustration for sodium-ion battery 11.
充電時,在外電壓的作用下正極材料發生氧化反應同時伴隨著鈉離子從其晶格中脫出,鈉離子穿過電解液和隔膜到達負極并嵌入硬碳負極中。此時正極處于貧鈉狀態,而負極處于富鈉狀態,同時外電源提供的補償電荷流向負極使其發生還原反應。正負極之間形成電勢差,同時將電能轉化為化學能儲存于鈉離子電池中。放電過程恰好相反,鈉離子從負極材料中脫出,經過電解液的傳輸到達正極并嵌入正極材料晶格中。同時電子經外電路從負極流向正極,即形成驅動電流。可見,鈉離子電池的工作原理與鋰離子電池非常相似。所以鈉離子電池材料體系的創新探索可以借鑒鋰離子電池較為成熟的研究經驗。
2.3 鈉離子電池正負極材料概述
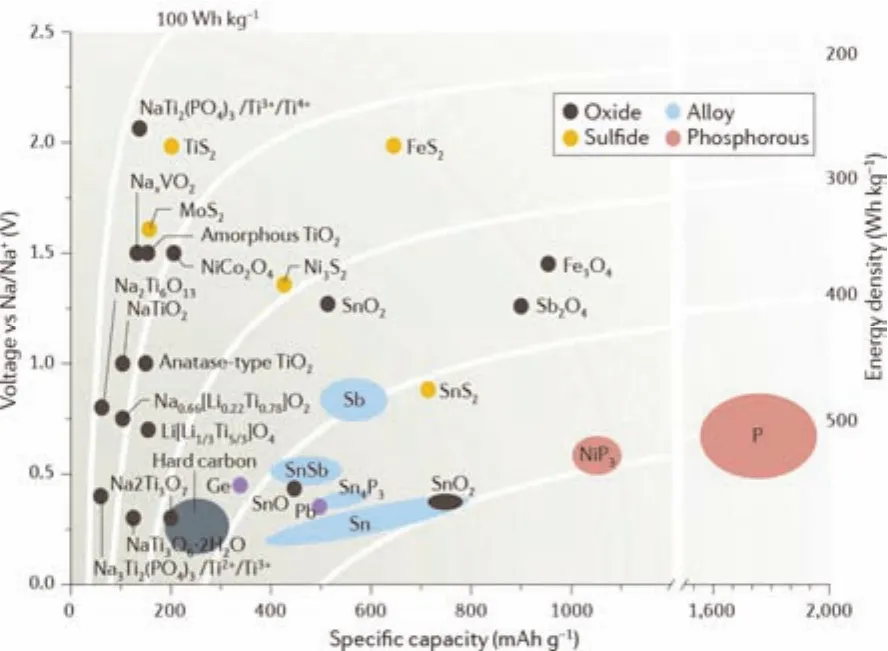
圖3 鈉離子電池負極材料的工作電壓和比容量對比12Fig. 3 Operation voltages versus specific capacities of sodium-ion battery anode materials 12.
對于鈉離子電池負極材料,一般要求較低的輸出電位,通常在0.0–1.0 V (vsNa+/Na)之間。理想的鈉離子電池負極材料應具有以下特征:高可逆的質量和體積比容量、相對正極更低的電位平臺、高倍率性能、長循環壽命、低成本、優異的穩定性和環境兼容性。圖3總結了鈉離子電池負極材料的工作電位和比容量特性12。主要包括三類:(1)碳基材料,包括硬碳、軟碳、石墨烯和碳納米纖維等;(2)合金類,許多金屬或非金屬元素,如錫、銻、鍺和磷等都可以和鈉金屬合金化,來充當鈉離子電池的負極材料;(3)過渡金屬氧化物和硫化物等。硬碳是鈉離子電池最受關注的負極材料,可以釋放出高達350 mAh·g-1的比容量,已非常接近石墨中的儲鋰容量。異質原子摻雜和結構優化可以有效提升碳材料的儲鈉性能,但是需要精準控制摻雜類型及摻雜量。對于大規模儲能應用,應該首選生物質碳材料。降低制備成本、提高儲鈉容量、提升首次庫倫效率和倍率性能是目前碳基負極材料亟需解決的關鍵問題。同時,需要對硬碳材料中的鈉離子存儲機制進行深入解析,研究表面含氧官能團如羧基、羰基與醛基等對電極過程的影響,揭示比表面、褶皺、雜原子、缺陷結構等對電化學行為的作用規律,為開發高性能、實用型的硬碳負極材料奠定理論基礎13。轉化反應類材料具有較高的可逆容量,但是循環穩定性和倍率性能有待進一步提升。電子導電性差和體積變化大嚴重影響了其性能的發揮。通過材料結構納米化和導電碳修飾可以克服部分缺陷。但轉化反應中結構重排引起的電壓滯后現象需更深入的研究和解決14。合金化反應類材料是一種極具潛力的高容量鈉離子電池負極材料,特別是錫、銻和磷。與鈉合金化過程中伴隨著巨大的體積膨脹會導致容量迅速衰減。通過碳包覆、納米化、金屬間復合可以有效提升材料的結構穩定性。探索合適的納米結構及復合金屬表界面儲鈉機制的解析仍存在巨大的挑戰15。此外,鈦基材料也受到一定的關注,但其儲鈉性能有待進一步提升,且需要深入理解鈦基材料與電解液之間的催化反應并尋求有效抑制方法16。
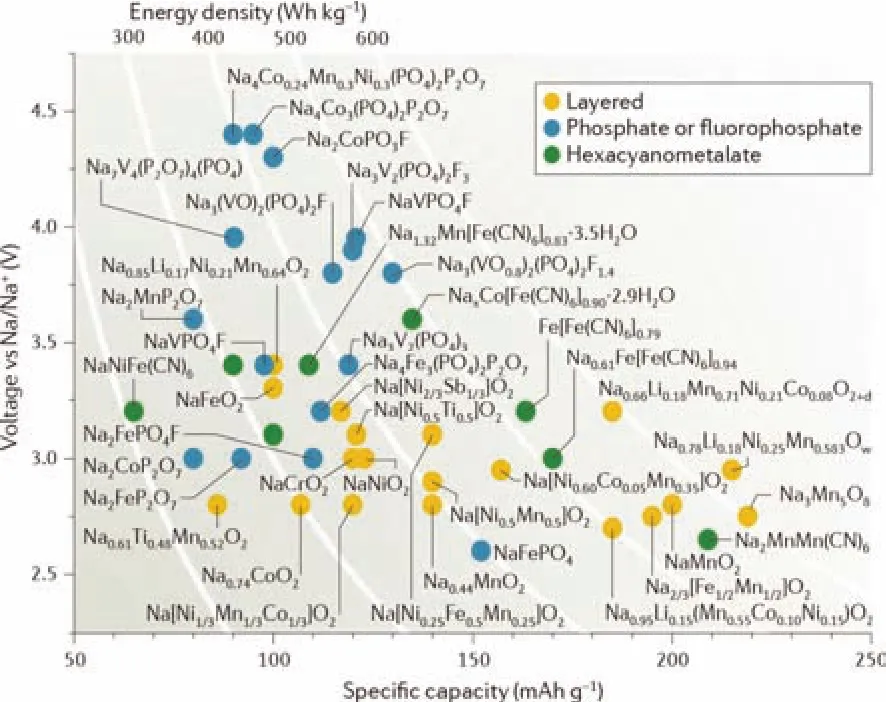
圖4 鈉離子電池正極材料的工作電壓和比容量對比12Fig. 4 Operation voltages versus specific capacities of sodium-ion battery cathode materials 12.
圖4總結了鈉離子電池正極材料的工作電位和比容量特性12。根據材料的晶體結構與化學成分可以將鈉離子電池正極材料分為三大類,它們都有合適的空間和通道供鈉離子存儲和輸運。其中包括:(1)過渡金屬氧化物類NaxMO2(M = Co、Mn、Fe或Ni),層狀過渡金屬氧化物具有α-NaFeO2型結構,氧原子為立方密堆積排列,結構中形成了供鈉離子擴散的一維、二維或三維通道。(2)普魯士藍類似物,這類材料具有一個立方體框架(KM2(CN)6),由于其開放的立方框架結構和充足的空間間隙位置,允許堿金屬離子可逆的脫出和嵌入。(3)聚陰離子化合物是另一類極具發展前景的正極材料,由于其結構穩定性好、安全性高、隨充放電體積變化小等優勢而受到廣泛關注。聚陰離子強烈的誘導效應可以調節過渡金屬氧化還原對的能量,從而產生較高的工作電壓。NASICON (Na Super Ionic Conductor)型化合物具有菱方晶胞結構,離子遷移速率快。這些化合物的分子通式為A3M2(XO4)3(A為堿金屬陽離子,M為過渡金屬,X為P、Si、As等),NASICON框架由XO4四面體與MO6八面體共享角原子組成。M2(XO4)3開放的框架結構可供鈉離子快速傳輸,其晶胞間隙至少可以容納4個堿金屬陽離子。因此,NASICON型化合物是一種很有前景的鈉離子電池正極材料。氟磷酸鹽類化合物,包括Na2MnPO4F、NaVPO4F、Na3V2(PO4)2F3、Na1.5VOPO4F0.5和Na2FePO4F等,堿金屬離子存在于MO4F2(M為過渡金屬)的隧道結構中。高電負性的F離子與磷酸根結合,由于氟離子的強誘導作用,使活性氧化還原對的電壓升高,形成了一類很有潛力的高能量密度正極材料。
3 影響鈉離子電池工作電壓的因素
鈉離子電池的工作電壓是由整個電池體系的多個組分共同決定的,包括正極、負極和電解液。通常正極和負極的化學勢差稱為工作電壓,即電池的開路電壓(Voc)17:

而在實際放電過程中的電壓又存在少量降低,這與離子在電解液和電極/電解液界面的輸運有關17:

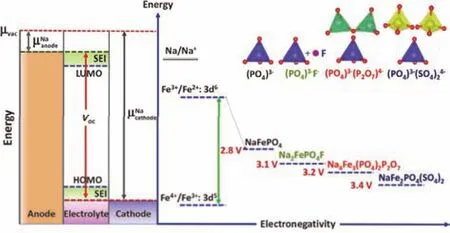
圖5 鈉離子電池鐵基聚陰離子正極材料的能量圖18Fig. 5 Schematic derivation of the energy diagram of iron-based mixed polyanion cathode materials for sodium-ion batteries 18.
其中電壓損失η稱為極化或過電勢。如圖5所示18,鈉離子電池的工作電壓受電解液的電化學窗口的限制,由最高占據分子軌道(Highest Occupied Molecular Orbital,HOMO)和最低未占分子軌道(Lowest Unoccupied Molecular Orbital,LUMO)的能量差決定。在選擇正負極材料時,正極材料的電化學勢μC需位于電解液HOMO上方,負極材料的電化學勢μA需位于電解液LUMO的下面。當正極材料的電化學勢μC低于電解液HOMO時,電解液中的電子會被正極材料俘獲,從而電解液被氧化和鈍化,導致正極材料表面形成固液界面層,加劇極化。當負極材料的電化學勢高于電解液LUMO時,負極材料的電子會被電解液奪取,因而電解液被氧化,反應產物在負極材料顆粒表面形成固液界面層(Solid Electrolyte Interface Film,SEI膜)。SEI膜的形成消耗的電解液中的鈉離子且增加了電池的內阻,導致電池的功率和容量降低19。研究表明,鈉離子電池中碳酸酯類電解液的最高穩定電壓上限約為4.2 V,而當正極材料如層狀氧化物的氧化還原電位超過電解液的HOMO極限時,將限制了其能量密度的發揮20。
影響鈉離子電池輸出電壓的另一個重要因素是正極材料的工作電壓。由于電池的能量密度取決于材料的比容量和工作電壓,因此,通過提升高比容量正極材料(如過渡金屬氧化物和磷酸鹽類)的工作電壓是一種提高電池的能量密度的有效途徑。正極材料的工作電壓和其過渡金屬氧化還原對的電勢直接相關,過渡金屬離子的電子結構(3d4s)中3d軌道電子的失去或獲得對應于充放電過程中的氧化或還原。通常對于相變反應機制的同系列材料MX (M為過渡金屬,X為F、O、S、N、P),其工作電壓的排序為:Cu > Ni > Co > Fe > Mn >Cr > V > Ti,而陰離子P軌道能級的位置會對電極材料的電壓產生影響,對于不同陰離子的化合物,其工作電壓的排序一般為:氟化物 > 氧化物 >硫化物 > 氮化物 > 磷化物21。此外,同樣的正極材料在不同的電池體系中的工作電壓也有所不同,一般遵循的規律為:Li電池> K電池 > Na電池 > Mg電池 > Al電池21。
在聚陰離子類化合物中,由于強電負性的聚陰離子基團誘導效應的不同,使得過渡金屬氧化還原對的電勢也有所區別。圖5中以鐵基聚陰離子化合物為例,分析了(PO4)3-、(PO4)3-F-、(PO4)3-(P2O7)4-、(PO4)3-(SO4)24-四種聚陰離子對Fe2+/Fe3+氧化還原對的費米能級的影響18。不同聚陰離子的組合可以通過結構的多樣性和不同程度的誘導效應來調節氧化還原電壓高度。這種通過聚陰離子組合調控氧化還原對能級進而調控電極材料工作電壓的方法也適用于其它的電化學氧化還原對,如Mn2+/Mn3+、V3+/V4+、Ni2+/Ni3+、Co2+/Co3+等19。
由此可見,鈉離子電池的工作電壓主要取決于正負極之間的電勢差,而普遍認為正極材料是提升鈉離子電池比能量的瓶頸,因此需要大力開發先進的正極材料。目前,對鈉離子電池正極材料的研究主要集中在三類化合物。第一類是鈉過渡金屬氧化物,這些材料具有高可逆容量和高工作電位,但它們中的大多數仍存在不可逆相轉變、空氣中不穩定和性能退化嚴重等問題。另一類是普魯士藍類似物,這些材料具有良好的工作電壓、循環穩定性和倍率能力,其實際應用的主要障礙是晶格缺陷、熱不穩定性和低振實密度。聚陰離子化合物是另一類極具發展前景的正極材料,由于其結構穩定性好、安全性高、隨充放電體積變化小等優勢而受到廣泛關注。迄今為止,許多鐵、釩和錳基聚陰離子化合物已經被廣泛和深入的研究。
4 鈉離子電池磷酸鹽正極材料
聚陰離子化合物是由強共價鍵構成的三維框架結構,因此具有較高的結構穩定性。其穩定的框架結構具有快速的鈉離子擴散速率且離子脫嵌過程中體積變化小、相變少,從而保障了在鈉離子電池中良好的循環穩定性和優異的安全性。但聚陰離子化合物中龐大的陰離子基團也會導致其比容量低且電子導電性差。聚陰離子化合物結構多變、種類繁多,包括磷酸鹽、氟磷酸鹽、焦磷酸鹽、混合磷酸鹽等。
4.1 正磷酸鹽類
4.1.1 NaFePO4
NaFePO4是最早被研究的鈉離子電池聚陰離子型正極材料,如圖6所示,它具有兩種不同的結構類型:磷鐵鈉礦相(Maricite phase,m-NaFePO4)和磷鐵鋰礦相(Triphylite phase,t-NaFePO4)。t-NaFePO4是由共頂點的FeO6八面體和PO4四面體共邊構成空間骨架,沿著b軸方向,t-NaFePO4具有一維的鈉離子擴散通道(圖6b)。而m-NaFePO4的結構是由共角的FeO6八面體和PO4四面體構成,其結構中沒有鈉離子的輸運通道(圖6a)。因此,通常認為磷鐵鈉礦相NaFePO4是一種沒有電化學活性的結構。
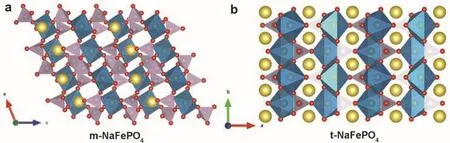
圖6 NaFePO4的兩種晶體結構:(a)磷鐵鈉礦相;(b)磷鐵鋰礦相Fig. 6 Crystal structures of (a) Maricite-type and (b) Triphylite-type NaFePO4.
NaFePO4的熱力學穩定相是磷鐵鈉礦相而非磷鐵鋰礦相,亞穩態的t-NaFePO4在480 °C以上就會相變為熱力學穩定的m-NaFePO422,因此傳統的高溫固相法難以合成t-NaFePO4。Baudrin等23最先發現LiFePO4結構中的鋰離子可以被鈉離子取代。之后,研究者們對t-NaFePO4的制備和表征進行了一系列研究。采用在有機溶液或者水溶液中的化學或電化學離子交換反應可以制得純相t-NaFePO424–26。Cao等26以LiFePO4/C為工作電極、活性炭作為對電極、Ag/AgCl為參比電極,在水溶液中通過的兩步電化學轉化過程制備了微球結構的磷鐵鋰礦相NaFePO4。得到的NaFePO4/C正極在0.1C的倍率下釋放出111 mAh·g-1的比放電容量和良好的循環穩定性,經過240此循環后容量可以保持90%。同時,他們采用傳統的電化學技術發現在放電時Na+嵌入的過程中存在一個中間相Na2/3FePO4,證實了在脫鈉和嵌鈉的過程中均存在相同的兩步相變反應。Pan等25采用類似的離子交換法成功制備了高純的橄欖石結構NaFePO4,通過從頭計算法和實驗相結合,證明了在水系電解液和陰極界面處的離子交換動力學與有機電解液相比更快。此外,他們采用原位同步輻射和非原位XRD研究了t-NaFePO4在脫嵌鈉時的相變過程。如圖7所示,在充電的過程中,NaFePO4首先完全轉變為中間相Na2/3FePO4,隨后進一步脫鈉形成FePO4。在放電時,FePO4首先部分轉變為中間相Na2/3FePO4,同時伴隨著NaFePO4的形成,隨著鈉離子的進一步嵌入,最終完全轉變為NaFePO4。Saracibar等27通過密度泛函理論(Density Functional Theory,DFT)計算結合高分辨同步輻射X射線衍射(XRD)發現NaxFePO4(0 ≤x≤ 1)存在兩個穩定的中間相Na2/3FePO4和Na5/6FePO4,計算得到NaFePO4和Na2/3FePO4的嵌鈉電壓差為0.16 V,這與實驗觀察到的電壓不連續相一致。Nazar等28報道了新型亞穩態橄欖石結構的金屬磷酸鈉鹽。他們采用在熔融鹽中的低溫(100 °C)固相反應將NH4[Mn1-xMx]PO4·H2O (M = Fe、Ca、Mg)轉化為Na[Mn1-xMx]PO4,將鈉離子電池橄欖石結構正極材料拓展到Na[Mn1-xMx]PO4(M = Fe、Ca、Mg)。與橄欖石型LiMPO4(M = Fe、Mn)不同,在Na1-xMn0.5Fe0.5PO4中觀察到了連續固溶過程的離子脫嵌機制。
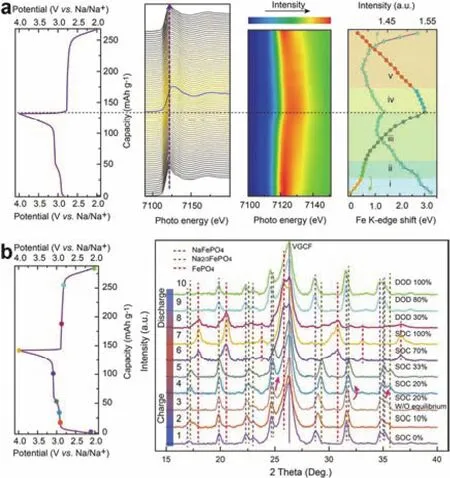
圖7 NaFePO4首圈循環過程中的(a)原位同步輻射鐵K邊X射線吸收近邊結構和(b)非原位XRD 25Fig. 7 (a) In situ synchrotron Fe K-edge XANES and (b)ex situ XRD studies of the NaFePO4 during initial cycles 25.
研究者們還對NaFePO4和LiFePO4的結構和電化學動力學行為進行了對比研究29–31。Wang等29通過實驗手段對比了NaFePO4和LiFePO4的熱力學和動力學行為,通過平衡電位、離子擴散系數和反應電阻的對比研究發現NaFePO4中的鈉離子擴散緩慢且接觸和荷轉移電阻更大,導致了其倍率性能較差。Nakayama等31通過第一性原理DFT計算發現NaFePO4和LiFePO4中的電子遷移能幾乎沒有區別,而NaFePO4中的鈉離子遷移能比LiFePO4的鋰離子遷移能更大。因此,研究者們通過導電聚合物包覆32、微鈉結構控制26,29及電解液優化33等手段對t-NaFePO4進行性能改性。
在很長一段時間里,人們認為磷鐵鈉礦相NaFePO4是不具有電化學活性的,這一定論被Kang等打破34。他們采用量子力學計算與實驗手段相結合首次證明m-NaFePO4結構中的鈉離子可以可逆脫出和嵌入。通過對m-NaFePO4中離子脫嵌機理的研究發現其結構中所有的Na+都可以脫出。非原位XRD和同步輻射分析結果表明鈉離子首次脫出后,m-NaFePO4轉化為非晶α-FePO4,使得鈉離子的傳輸勢壘大大減小。m-NaFePO4首次放電比容量為142 mAh·g-1,為理論值的92%,且具有優異的穩定性,經過200次循環后容量保持率為95%。最近,Fan等35采用靜電紡絲法成功制備了氮摻雜碳纖維封裝m-NaFePO4量子點復合材料(圖8a,b),這種獨特的微納結構可以有效增加活性材料的利用率、提升電子和離子的傳輸速率且穩定電極的結構。這種m-NaFePO4/C復合材料在0.2C的倍率下釋放出145 mAh·g-1高可逆容量,即使在高達50C的大倍率下仍可釋放61 mAh·g-1的比放電容量,且在5C的倍率下經過6300次循環后容量可保持89%(圖8c)。此外,研究者們通過增加m-NaFePO4的無序化程度36、構建快速電子傳輸網絡37,38和構筑協同優勢的復相材料39等手段來提升磷鐵鈉礦相NaFePO4的電化學性能。Huang等40通過水熱法合成了一種分級結構的Na0.67FePO4/CNT復合材料,其放電比容量為143 mAh·g-1,循環性能較穩定。但其首次充電容量非常低,這限制了其實際應用。
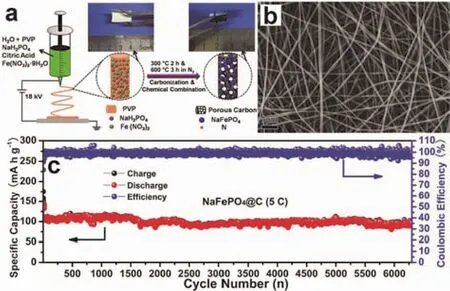
圖8 NaFePO4@C的(a)制備過程示意圖,(b) SEM圖像和(c)長循環性能35Fig. 8 (a) Schematic illustration of the preparation process, (b) SEM image, and (c) long-term cycling performance of the NaFePO4@C 35.
與NaFePO4類似,NaMnPO4也有兩種晶體結構:磷鐵鈉礦型結構和橄欖石型結構。據報道,采用高壓環境中的離子交換法可以制備出橄欖石型NaMnPO4,采用低溫(400 °C)固相法可以合成磷鐵鈉礦NaMnPO441。Johnson等42測試了NaCoPO4用于鈉離子電池正極材料時的性能表現。然而,目前報道的這兩種材料都沒有表現出很好的電化學性能,但通過結構優化和電解液改性等手段有望獲得更好的性能。
4.1.2 NASICON結構Na3V2(PO4)3
NASICON結構材料具有快速的鈉離子傳輸通道和穩定的三維框架結構,在電極材料、固態電解質等領域被廣泛研究。通常這種化合物以熱力學穩定的菱方晶胞結構(空間群:)存在。但是部分A3M2(PO4)3(A = Li、Na,M = Cr、Fe、Zr)類材料也以單斜結構存在,且在高溫條件下表現出可逆的結構相變43。Na3V2(PO4)3是一種代表性的NASICON結構材料,作為鈉離子電池正極材料受到廣泛的關注。如圖9a所示,NASICON結構中Na3V2(PO4)3是由VO6八面體和PO4四面體組成共價骨架[V2P3O12],骨架之間形成了三維互聯的隧道結構和兩種鈉離子分布間隙位置(M1和M2)。在鈉離子電池中,Na3V2(PO4)3基于V3+/V4+和V2+/V3+氧化還原對的工作電壓分別為3.4和1.6 V,因此Na3V2(PO4)3既可以用作正極材料又可以用于負極材料,對應的理論容量分別為118和50 mAh·g-144。
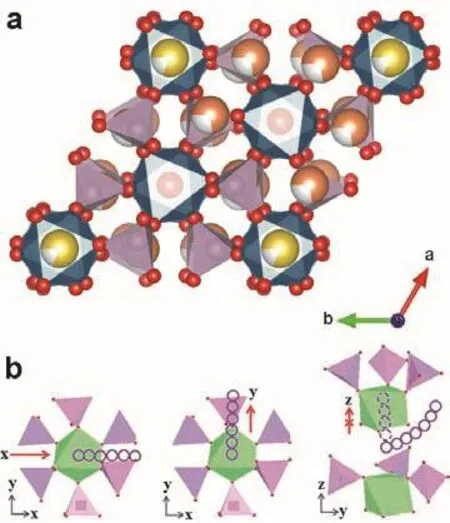
圖9 Na3V2(PO4)3的(a)晶體結構和(b)離子遷移路徑45Fig. 9 (a) Crystal structure and (b) ion migration paths of Na3V2(PO4)3 45.
研究者們采用多種譜學技術、電化學、理論計算等手段來探究Na3V2(PO4)3中鈉離子的儲存機理。為了解析Na3V2(PO4)3結構中的離子擴散通道,Ji等45通過第一性原理計算研究了其離子遷移活化能。結果表明,Na3V2(PO4)3結構中沿著x、y方向的兩條通道和另一條彎曲的遷移通道構成了其三維的離子輸運路徑(圖9b)。Hu等46采用電化學原位XRD技術研究了Na3V2(PO4)3中鈉離子的脫嵌機制(圖10a),隨著鈉離子的脫出,Na3V2(PO4)3的衍射峰逐漸變弱而NaV2(PO4)3的衍射峰逐漸增強,在嵌鈉后Na3V2(PO4)3的結構又能完全恢復,表明在3.4 V處的鈉離子脫出/嵌入是典型的兩相反應機制,而Na3V2(PO4)3和脫鈉相之間的體積變化僅為8.26%。他們還通過球差矯正環形明場相掃描電子顯微技術(ABF STEM)直接觀察到了鈉離子的脫出位置47。圖10b,c中顯示了Na3V2(PO4)3和NaV2(PO4)3的鈉原子的位置,其中Na3V2(PO4)3中鈉原子同時占據M1和M2位置,而NaV2(PO4)3中的鈉原子只占據M1位置,說明只有M2位置的鈉離子參與電化學脫嵌反應,與ABF圖像相對應的線型分布情況也驗證了這一結果(圖10c,d)。
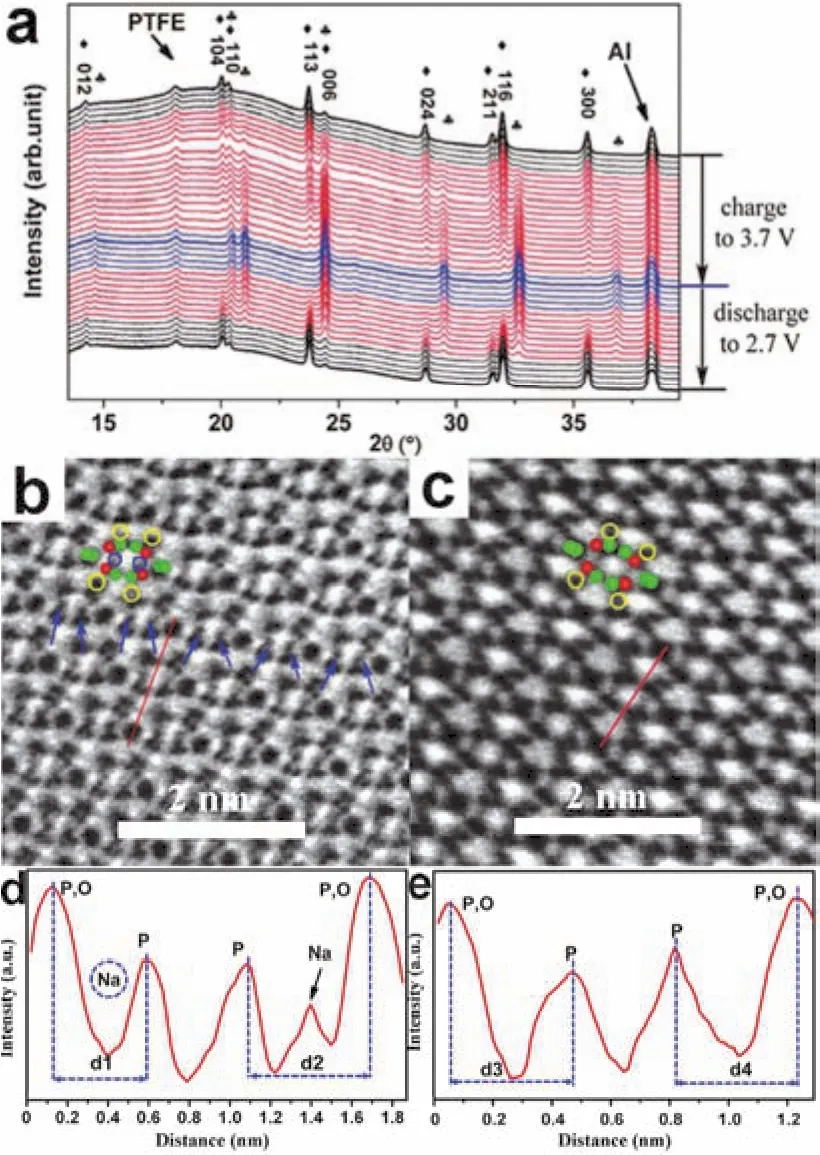
圖10 (a) Na3V2(PO4)3/Na電池的原位XRD譜,? Na3V2(PO4)3, ? NaV2(PO4)3 46;(b) Na3V2(PO4)3和(c) NaV2(PO4)3沿著[]晶帶軸的STEM ABF圖像47;(d) Na3V2(PO4)3和(e) NaV2(PO4)3沿著ABF圖像的線型分布47Fig. 10 (a) In-situ XRD patterns of the Na3V2(PO4)3/Na cell, ? Na3V2(PO4)3, ? NaV2(PO4)3 46; STEM ABF images of(b) Na3V2(PO4)3 and (c) NaV2(PO4)3 along the []projection 47; Line profiles along in the ABF images of(d) Na3V2(PO4)3 and (e) NaV2(PO4)3 47.
盡管Na3V2(PO4)3具有結構穩定、工作電壓較高等優點,但低電導率依然是其商業應用的主要阻礙。Chen的團隊48最先報道了一步固相法制備碳包覆Na3V2(PO4)3,在有機體系鈉離子電池中表現出3.4 V (vsNa+/Na)的電壓平臺。其首圈充放電比容量分別為98.6和93 mAh·g-1,表明碳包覆可以有效改善Na3V2(PO4)3的儲鈉性能。在過去的幾年中,研究人員采用了許多不同的方法來克服這個缺點,主要涉及微納結構調控、表面包覆改性、元素摻雜等49–51。為了優化Na3V2(PO4)3的微觀形貌,進一步提升其電子導電性和結構穩定性,研究人員嘗試了各種合成策略,如傳統的固相反應52、溶膠凝膠法53、靜電紡絲法54、水熱和溶劑熱法等55。Mai等56采用一種基于水熱反應的自犧牲模板法合成了三維Na3V2(PO4)3納米纖維,他們首次提出一種基于反應時間的由外向內的形貌演化機制。合成的Na3V2(PO4)3正極材料在鈉離子半電池和全電池中均表現出優異的循環穩定性和倍率性能。最近,Cao等55通過水熱反應法制備了一系列由納米片組裝的Na3V2(PO4)3/C分級微球,制備的Na3V2(PO4)3/C納米晶被氮摻雜碳緊密包覆。他們系統研究了水熱反應時間和前驅體濃度對Na3V2(PO4)3/C微納結構的影響并提出了結構生長機制(圖11)。作為鈉離子電池正極材料,Na3V2(PO4)3/C多孔微球表現出優異的倍率性能和循環穩定性,在100C倍率時可釋放99.3 mAh·g-1的放電比容量,在20C倍率下經過10000次長循環后容量保持79.1%。采用Na3V2(PO4)3/C為正極、SnS/C纖維為負極的鈉離子全電池能量密度可達223 Wh·kg-1。獨特的微納結構設計和氮摻雜碳包覆有效構筑了雙連續的電子和離子擴散通道,增加了電極和電解液的接觸面積同時增強了結構穩定性,進而造就了Na3V2(PO4)3/C多孔微球優異的電化學性能。
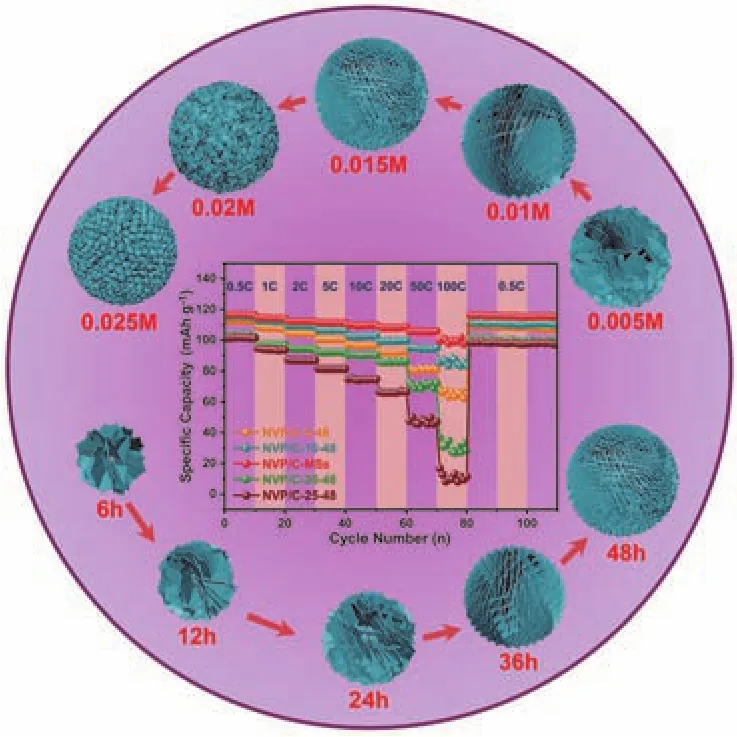
圖11 水熱反應法制備的Na3V2(PO4)3分級微球的形貌演化過程和倍率性能55Fig. 11 Morphological evolution process and rate performance of Na3V2(PO4)3 hierarchical microspheres prepared by hydrothermal reaction 55.
表面改性也被廣泛應用來提升Na3V2(PO4)3的電子導電性。碳包覆由于具有高電子導電性、成本低廉、化學穩定、在合成時或合成后都可以引入等優勢,成為最具吸引力并被廣泛使用的一種手段。研究者們采用了多種碳源和導電碳骨架來構筑碳包覆層。自從Balaya等57首次報道以陽離子表面活性劑作為碳源合成具有良好循環穩定性和優異倍率性能的Na3V2(PO4)3/C,研究者們開發了眾多不同的碳包覆技術。Cao等52設計了一種在熔融烴類化合物中的固態反應制備三維石墨烯籠包覆Na3V2(PO4)3納米片材料的方法(圖12a)。他們在合成過程中使用的油酸不僅作為碳源,而且作為陰離子表面活性劑引導晶體定向生長。Na3V2(PO4)3納米片被原位生成的3 nm厚的類石墨烯碳緊密覆蓋。作為正極材料,石墨烯包覆Na3V2(PO4)3納米片表現出優異的電化學性能,包括接近理論值的可逆容量(1C倍率下的可逆容量為115.2 mAh·g-1),優異的倍率性能(200C倍率下的比容量為75.9 mAh·g-1),并具有出色的循環穩定性(在50C倍率下30000圈循環后容量保持率為62.5%) (圖12b)。此外,刻蝕掉Na3V2(PO4)3后殘余的三維石墨烯籠也可作為鈉離子電池的負極材料,并在0.1 A·g-1時提供242.5 mAh·g-1的比容量。分別使用這兩種正極和負極材料的鈉離子全電池可提供高比容量和良好的循環穩定性(圖12c)。為了得到兼具高倍率性能和穩定性的Na3V2(PO4)3材料,另一種表面改性的有效策略是將Na3V2(PO4)3納米晶粒嵌入相互連通的高導電碳骨架中。由于有機碳源高溫熱解后的導電碳大部分是無定型碳,而化學氣相沉積法是一種制備一維石墨烯、二維碳納米管等高導電碳材料的有效手段。因此,Cao等58采用簡單、經濟的化學氣相沉積法構筑了分級結構碳骨架修飾的Na3V2(PO4)3。由類石墨烯包覆層和碳納米管交聯組成的分級碳骨架有效提升了Na3V2(PO4)3的電子傳輸效率,該材料在0.2C倍率時釋放出接近理論值的容量,在30C倍率下經過20000次循環后容量保持率為54%。此外,氧化物包覆、導電聚合物包覆等也可以有效地提升Na3V2(PO4)3的電化學性能59。
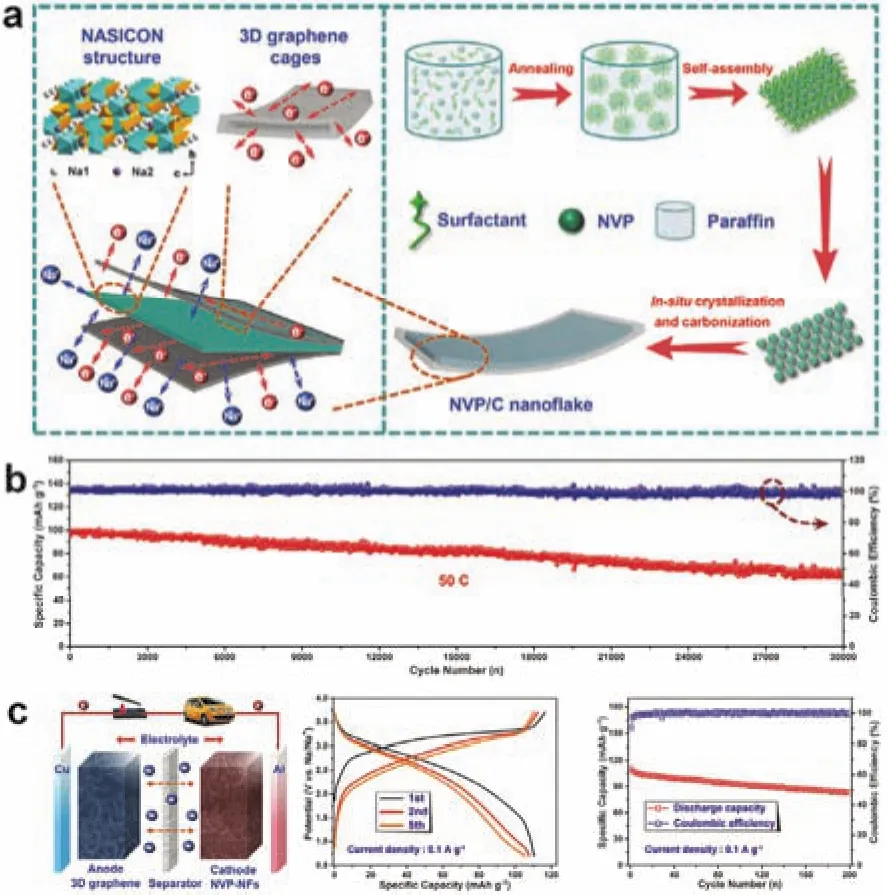
圖12 三維石墨烯籠包覆Na3V2(PO4)3納米片的(a)合成示意圖、(b)長循環性能和(c)全電池性能52Fig. 12 (a) Schematic illustration of the fabrication,(b) ultralong-life cycling performance, and (c) sodium-ion full-cell performance of 3D graphene capped Na3V2(PO4)3 nanoflakes 52.
元素摻雜是優化Na3V2(PO4)3電化學性能的另一種有效手段。Yang等60將較輕的Mg摻雜到Na3V2(PO4)3中V的位點,可以有效提升電極材料的性能。與未摻雜的Na3V2(PO4)3相比,采用簡單溶膠凝膠法制備的Mg摻雜Na3V2-xMgx(PO4)3/C復合材料在倍率性能和循環性能方面均有明顯提高。Goodenough等61設計并合成了一系列NASICON結構NaxMV(PO4)3(M = Mn、Fe、Ni) (圖13a),其中Na4MnV(PO4)3正極材料在3.6和3.3 V處顯示出兩個電壓平臺,分別對應于Mn3+/Mn2+和V4+/V3+氧化還原對。此外,Na4MnV(PO4)3正極材料表現出97%的首圈庫倫效率和長達1000次的循環壽命,是一種很有應用前景的高比能正極材料。最近,他們又開發出了一種具有更高電壓平臺的Na3MnZr(PO4)3鈉離子電池正極材料62(圖13b)。為了進一步提高碳包覆效果和其電子導電性,Wang等63在包覆碳層中引入氮摻雜。氮摻雜碳包覆Na3V2(PO4)3正極材料的電化學性能明顯提升,尤其是其倍率性能。此外,他們還詳細探討了不同位置的氮原子摻雜對電化學性能的影響,結果表明,氮摻雜可以在包覆碳層中引入一些缺陷,促進Na+的輸運和存儲。最近,Yu等64通過構筑氮、硫共摻雜的石墨烯多孔導電骨架來改善Na3V2(PO4)3的電子導電性。此外,在V位置的多價離子摻雜(如Ni2+、Cr3+、Al3+)和Na位置的單價離子摻雜(如Li+、K+)都可以調控Na3V2(PO4)3的電子結構和離子擴散通道65–67。
除了研究較多的釩基NASICON結構材料,還有很多其它的NASICON結構化合物也可以用于鈉離子電池,例如NaTi2(PO4)3、NaSn2(PO4)3、NaZr2(PO4)3、Na3Fe2(PO4)3、Na3Co2Fe(PO4)3、Na3TiFe(PO4)3、Fe2(MoO4)3、Na2Ni2(PO4)3等68,69。通過調整NASICON結構中過渡金屬原子的類型對可以調控其在鈉離子電池中的工作電壓,為高比能鈉離子電池正極材料的開發提供可能。
4.1.3 非晶型磷酸鹽
目前常用的二次電池正極材料都是晶體材料,晶體材料中的離子存儲受晶體結構、結晶性、擇優取向及結構穩定性等因素影響。通常晶體材料中的離子脫嵌受其晶格中的傳輸通道影響。而非晶材料與晶體材料中原子團簇的排列方式是不同的,非晶材料中的原子團簇是短程有序且它們隨機相連70,71。因此,非晶材料的XRD譜中沒有衍射峰,傳統的譜學技術很難表征。由于非晶材料具有長程無序而短程有序的特征,它們也具有一些獨特的優勢,例如各向同性、增強動力學、自由體積、利于調整晶格畸變等50。因此,非晶材料在鈉離子電池中具有一定的應用潛力。Kim等72研究了不同價態離子(一價、二價、三價)在非晶FePO4中的儲存性質(圖14),在鈉離子電池中,表現出高達179 mAh·g-1的比容量,同時他們發現在鈉離子嵌入的過程中非晶FePO4有向結晶NaFePO4轉變的趨勢。Zhang等73,74進一步研究了FePO4嵌鈉過程中的相變規律,他們發現非晶FePO4在嵌鈉過程中同時轉變為非晶NaFePO4和t-NaFePO4,而結晶FePO4在嵌鈉過程中相變為m-NaFePO4。
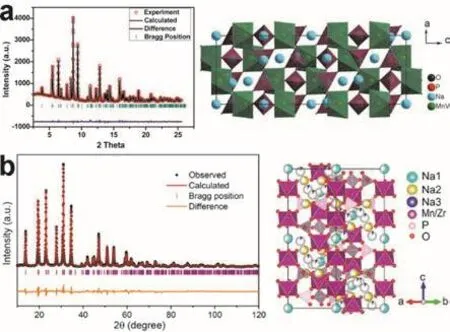
圖 13 (a) Na4MnV(PO4)3 61和(b) Na3MnZr(PO4)3 62的XRD譜和晶體結構Fig. 13 XRD patterns and crystal structures of (a)Na4MnV(PO4)3 61 and (b) Na3MnZr(PO4)3 62.
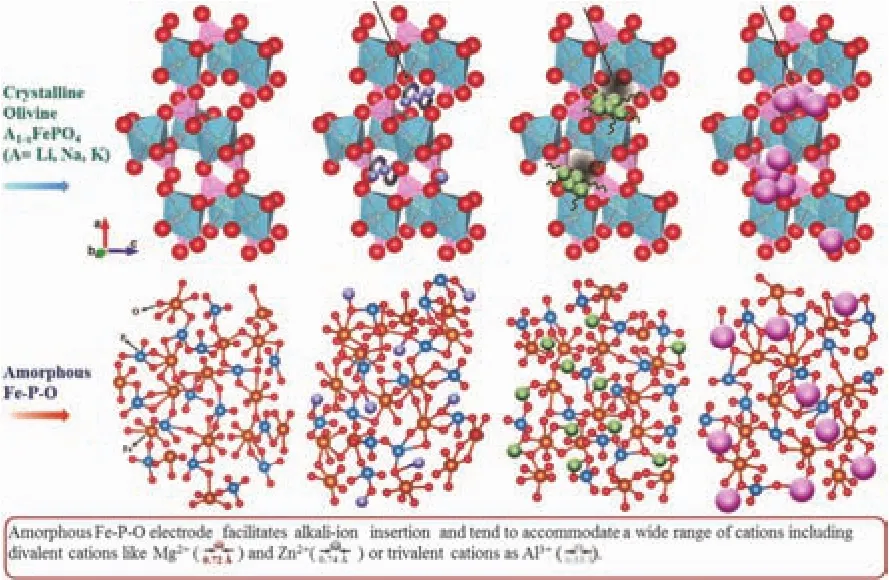
圖14 堿金屬離子嵌入結晶和非晶FePO4電極72Fig. 14 Schematic representation of alkali-ions(Li/Na/K) insertion in crystalline and amorphous FePO4 electrode hosts 72.
碳包覆/復合是提升非晶FePO4儲鈉性能的有效手段。Hu等75采用水熱法成功制備了一種單壁碳納米管連接多孔FePO4納米顆粒,在0.1C的倍率下可以釋放120 mAh·g-1的儲鈉容量。Cao等76采用簡單的化學誘導沉淀法制備了一種介孔碳骨架修飾的非晶FePO4,制備的FePO4/C在20 mA·g-1電流密度下的首次放電比容量為151 mAh·g-1,且經過200次循環后其容量仍可保持94%。此外,研究者們還采用石墨烯77、多壁碳納米管78、碳化聚苯胺79等構筑導電網絡來改性非晶FePO4的電化學性能。
形貌調控也可以有效改善非晶FePO4的電化學性能,低維尺寸或者分級多孔結構可以有效縮短離子的固相傳輸距離、提供更多的電化學活性位點。Pan等80制備了一種二維非晶FePO4納米片,由于其尺寸效應有效縮短了鈉離子的傳輸距離和較大的比表面積增加了電容的貢獻,非晶FePO4納米片在0.1C倍率下可以表現出168.9 mAh·g-1的首次放電比容量,在1C倍率下經過1000次循環容量保持率為92.3%。此外,研究者們通過多種物理或化學手段合成了不同形貌的非晶FePO4材料,包括納米球81、納米線82等。無鈉正極材料不利于實際產業應用,Tong等83通過模板法制備了中空結構的非晶NaFePO4,其首次放電比容量為152.1 mAh·g-1且經過300次循環其容量仍可保持94%,在高達10C的倍率下仍可釋放出67.4 mAh·g-1的比容量。非晶磷酸鹽正極材料的研究雖然取得了一些進展,但由于非晶材料結構的特殊性,關于其體相結構的熱力學和動力學特性以及與電化學性能之間的深層關系還有待深入研究。
4.1.4 其它正磷酸鹽 (VOPO4,NaVOPO4)
NaxVOPO4(x= 0, 1)也是一類很有潛力的鈉離子電池正極材料。VOPO4具有多種不同的晶體結構 (圖 15), 包 括 α/αI/αII-VOPO4, β-VOPO4, γ-VOPO4,δ-VOPO4,ε-VOPO4和ω-VOPO484。目前報道的NaVOPO4通常包括三種不同的結構(圖15),分別為α-NaVOPO4(三斜晶系,空間群:P21/c),β-NaVOPO4(正交晶系,空間群:Pnma),和αINaVOPO4(四方晶系,空間群:P4/nmm)85。Goodenough等86最先將單斜晶系NaVOPO4用于鈉離子電池正極材料,發現其工作電壓為3.6 V (vsNa+/Na)并可以釋放出90 mAh·g-1的可逆容量。Ong等84采用第一性原理計算對比研究了β、ε和αI三種VOPO4化合物的熱力學穩定性、工作電壓、能帶結構和擴散動力學行為,發現只有αI-VOPO4表現出較低的鈉離子擴散遷移勢壘。Aparicio等87結合密度泛函理論計算和分子動力學方法研究了α、β和αI三種NaVOPO4化合物的離子擴散、電子結構和離子摻雜特性。結果表明,α、β和αI相分別表現出二維、一維和三維的離子遷移路徑,其中αINaVOPO4表現出最優的離子擴散速率、通道和活化能,是一種很有潛力的鈉離子電池正極材料。
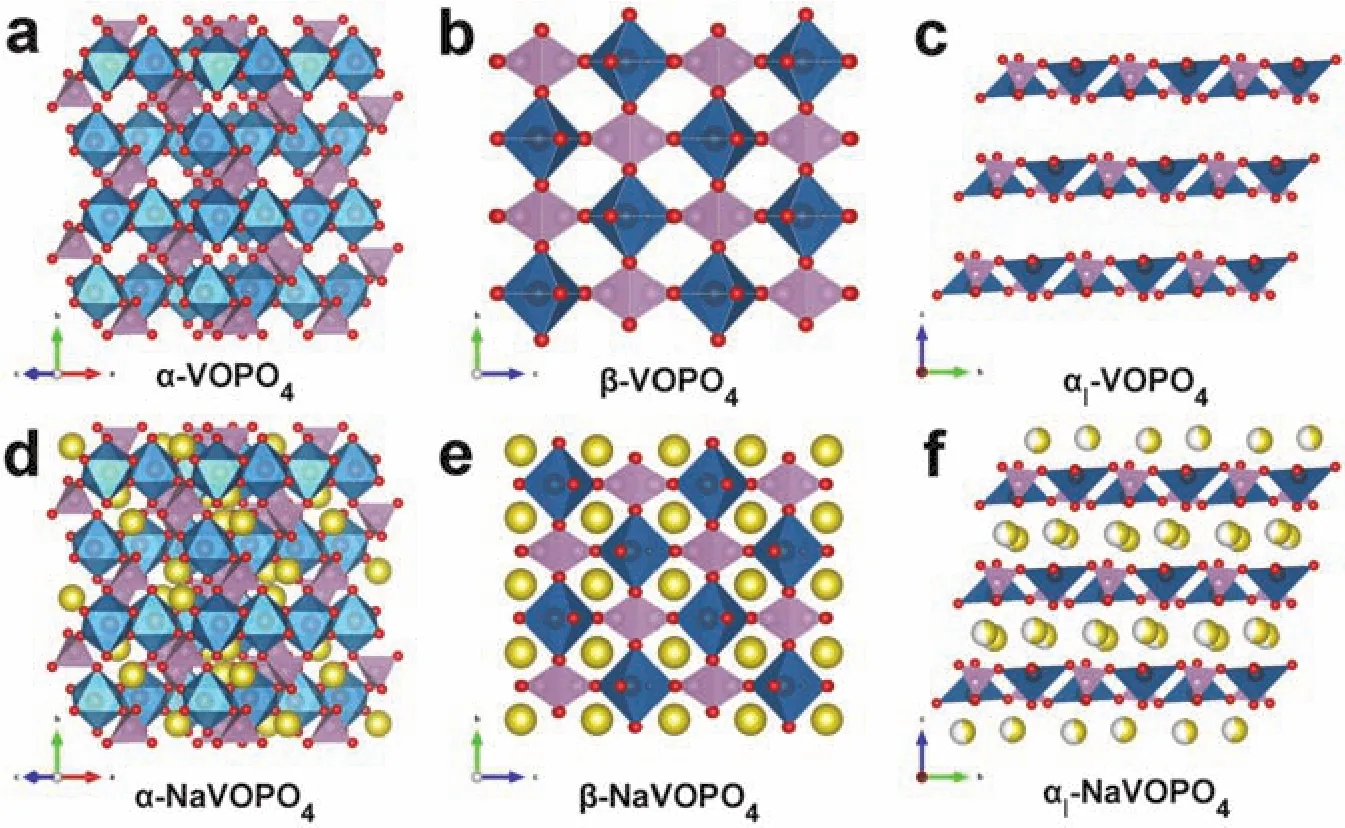
圖15 VOPO4和NaVOPO4的晶體結構Fig. 15 Crystal structures of VOPO4 and NaVOPO4.
Manthiram等88采用化學方法將四方晶系αILiVOPO4中的鋰離子脫出,制備了層狀結構αIVOPO4正極材料,基于V4+/V5+氧化還原對,αIVOPO4的工作電壓在3.5 V (vsNa+/Na)左右,且嵌鈉后可以轉變為層狀αI-NaxVOPO4。電化學測試結果顯示,純相αI-VOPO4表現出110 mAh·g-1的可逆容量,通過與rGO復合后,其放電比容量高達150 mAh·g-1。最近Ren等89通過水熱反應法直接制備了層狀結構NaVOPO4,這種層狀材料表現出3.5 V (vsNa+/Na)的工作電壓、高達144 mAh·g-1的比放電容量和良好的循環穩定性(經過1000次循環后容量保持67%),其優異的電化學性能歸因于層狀結構提供了快速的鈉離子遷移路徑、導電碳修飾利于快速的電子傳輸。此外,他們通過原位XRD和原位同步輻射技術詳細研究該層狀NaVOPO4中的儲鈉機制。最近,Whittingham等90研究了一種新型KVOPO4材料的儲鈉性能。Yu等91,92通過二維材料的層間工程制備了不同層間距的VOPO4材料,并研究了它們層間距對離子存儲的影響規律。此外,它們還將層狀VOPO4應用于鈉離子全電池中93,94,制備了一系列高比能且極具應用潛質的鈉離子全電池器件。
4.2 氟磷酸鹽類
4.2.1 NaVPO4F
如圖16a,b所示,通常認為NaVPO4F含有兩種不同的晶體結構:(1)低溫單斜晶系結構,與NaAlPO4F (ICSD#40522)的晶體結構相同,其空間群為C2/c;(2)高溫四方晶系結構,與Na2.82Al2(PO4)2F3(ICSD#88805)的晶體結構相同,其空間群為I4/mmm18。早在2003年,Barker等95就已經將四方晶系結構NaVPO4F應用于鈉離子電池中,采用NaVPO4F作為正極、硬碳為負極的鈉離子全電池顯示出兩對充放電電壓平臺且可以釋放出82 mAh·g-1的可逆容量。之后針對NaVPO4F的研究大部分集中在其單斜相,Zhang等96采用一種高溫熔融混合法合成了單斜結構NaVPO4F/C納米片,制備的復合材料具有優異的電化學性能(圖16c),在0.2C倍率下的首次放電比容量為135 mAh·g-1,在20C倍率下經過1500次循環后其容量仍能保持90.4%,他們還采用原位XRD技術證明了NaVPO4F中鈉離子的兩相反應存儲機制(圖16d)。
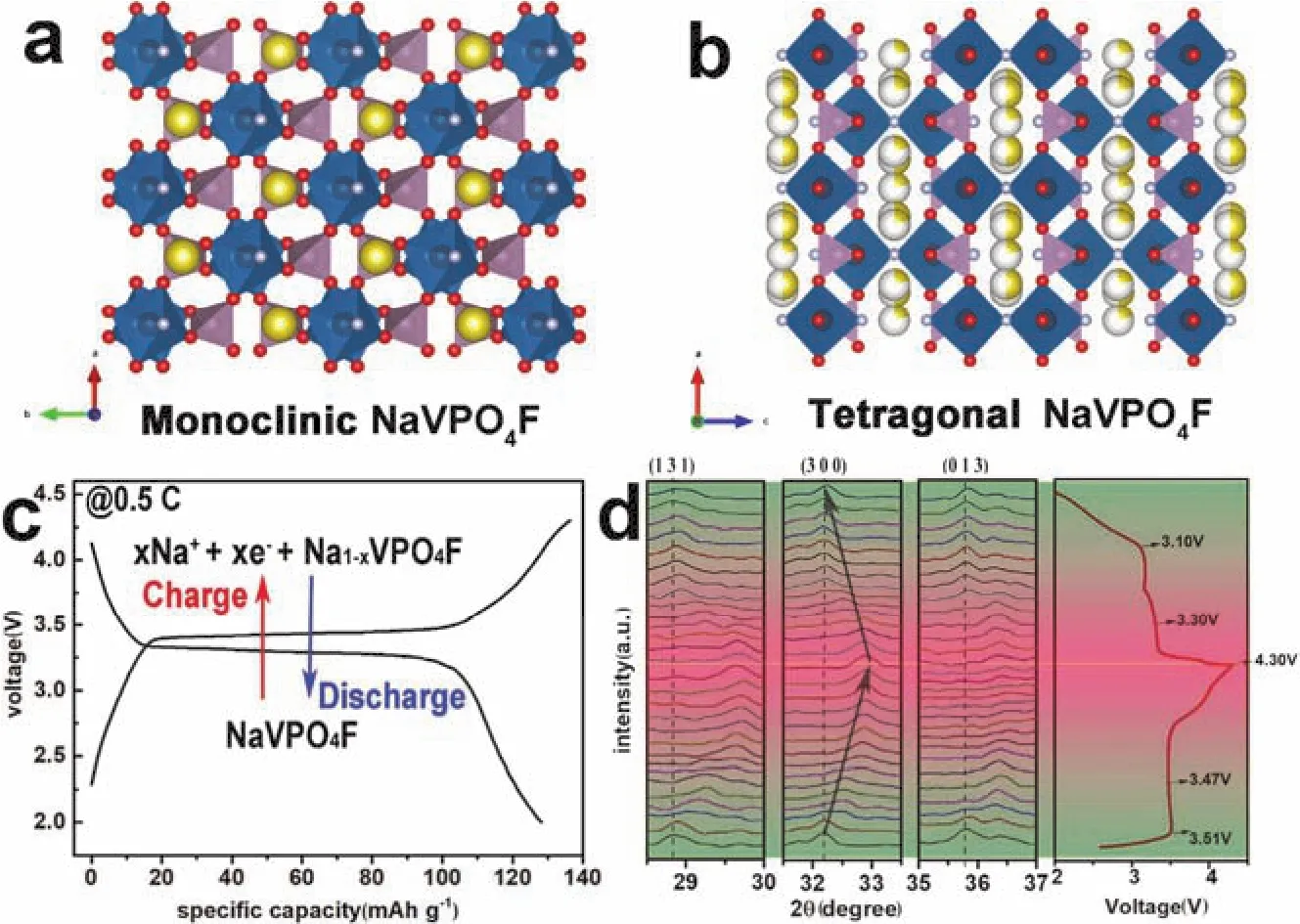
圖16 (a)單斜晶系和(b)四方晶系NaVPO4F的晶體結構;NaVPO4F的(c)充放電曲線和(d)原位XRD譜96Fig. 16 Crystal structures of (a) monoclinic and (b) tetragonal NaVPO4F, (c) charge-discharge curve and(d) in situ XRD pattern of NaVPO4F 96.
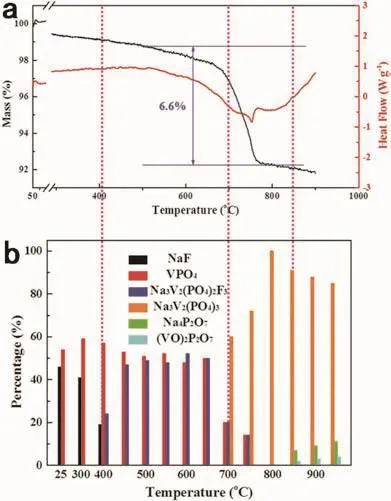
圖17 (a)原料在氬氣下加熱過程中的TGA/DSC曲線和(b)基于原位XRD譜半定量計算的成分變化情況106Fig. 17 (a) The TGA/DSC curves of raw materials upon heating in Ar fl ow; (b) The corresponding specific compositional changes calculated by semiquantitative calculation of in situ XRD patterns 106.
研究者們采用碳包覆、形貌調控和離子摻雜等手段進一步提升NaVPO4F的儲鈉性能。Ruan等97制備了石墨烯包覆NaVPO4F復合材料,其平均工作電壓高達3.95 V (vsNa+/Na)且首次放電比容量為120.9 mAh·g-1。之后研究者們采用多種碳包覆手段來提高NaVPO4F復合材料的電子導電性98–100。Jiao等101采用靜電紡絲技術制備了一維結構NaVPO4F/C納米纖維,NaVPO4F納米顆粒(約為6 nm)均勻地分散在導電碳纖維骨架中,基于形貌和微觀結構特征,復合材料表現出優異的電化學性能,在1C倍率下的放電比容量為126.3 mAh·g-1,在高達50C的倍率下仍可釋放61.2 mAh·g-1的容量,在2C的倍率下經過1000次循環后容量仍能保持96.5%。此外,研究者們還通過構筑三維多孔交聯網絡、三維多孔珊瑚狀結構等來改性NaVPO4F/C的儲鈉性能102,103。離子摻雜也可以調控NaVPO4F的電化學性能,Al和Cr被用于摻雜元素來改性NaVPO4F104,105。
盡管針對NaVPO4F的研究取得了一系列進展,但仍有研究者對NaVPO4F材料是否真實存在保持懷疑。最近,Li等106采用變溫原位XRD技術研究了摩爾比為1 : 1的NaF和VPO4在固相反應過程中的成分和結構變化情況(圖17),結果表明在不同溫區存在三種化學反應:
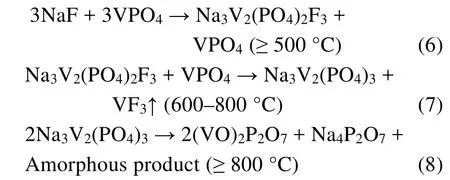
他們認為通過高溫固相燒結法是不可能合成單斜晶系和四方晶系結構的NaVPO4F。關于NaVPO4F材料存在性問題的爭論仍未終止,采用理論計算結合先進的分析表征技術進行深入研究不可或缺。
4.2.2 Na3(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1)
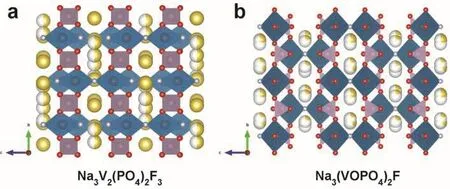
圖18 (a) Na3V2(PO4)2F3和(b) Na3(VOPO4)2F的晶體結構Fig. 18 Crystal structures of (a) Na3V2(PO4)2F3 and (b) Na3(VOPO4)2F.
Na3V2(PO4)2F3是一種很有前景的鈉離子電池正極材料,其結構中3個鈉離子脫嵌時具有高達192 mAh·g-1的理論容量。由于(PO4)3-基團的強誘導效應和F-離子的高電負性,Na3V2(PO4)2F3具有較高的工作電壓,其理論能量密度約為507 Wh·Kg-1,這個值與目前商業化LiFePO4的能量密度(530 Wh·Kg-1)非常接近。如圖18a所示,Na3V2(PO4)3F3的晶體結構屬于四方晶系的P42/mnm空間群,其中[V2O8F3]雙八面體和[PO4]四面體相互橋接構成三維框架,在[110]和[001]方向有鈉離子的快速遷移通道。Ji等107較早將Na3V2(PO4)3F3應用于鈉離子電池中,發現其在3.3、3.5和4.0 V處有三個放電平臺。Kang等108采用理論計算與實驗相結合進一步研究了Na3V2(PO4)3F3的相反應機理。結果表明,鈉離子是通過單相反應在宿主材料中可逆脫嵌且Na3V2(PO4)3F3脫鈉相的晶體結構非常穩定。研究人員進一步通過第一性原理計算揭示了Na3V2(PO4)3F3材料中鈉離子的遷移機制109,結果表明,Na3V2(PO4)3F3結構中的兩個鈉離子,即Na(1)和Na(2)通過兩步電化學過程可逆脫嵌,同時伴隨著V3+/V4+的氧化還原反應。圖19a,c進一步說明了氧化還原的相變過程及其晶體結構中鈉離子的分布情況110。普遍認為Na3V2(PO4)3F3結構中只有兩個鈉離子參與反應,而第三個鈉離子不具電化學活性。最近,Tarascon團隊111通過設計一種無序NaxV2(PO4)2F3材料成功激活了其結構中的第三個鈉離子的電化學活性。如圖19b所示,此材料在1–4.8 V的電壓范圍內可以可逆脫嵌3個鈉離子,最后一個是在1.6 V (vsNa+/Na)電壓處重新嵌入的。以此無序NaxV2(PO4)2F3材料作正極、硬碳作為負極的鈉離子全電池能量密度有望提升15%–20%。
如圖18b所示,基于體相結構設計研究者們還開發了一系列介于Na3V2(PO4)3F3(x= 0)和Na3(VO)2(PO4)2F (x= 1)之間的混合價態Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1)化合物,這里1-x代表材料中的氧含量,與Na3(VO1-xPO4)2F1+2x中的晶胞參數和晶胞體積密切相關。Na3(VO)2(PO4)2F的晶體結構屬于四方晶系的I4/mnm空間群。研究者們采用理論計算和原位/非原位譜學技術研究了Na3(VO1-xPO4)2F1+2x材料中的鈉離子脫嵌機制。Rojo等112,113研究了Na3V2O2x(PO4)2F3-2x和Na3V2O2(PO4)2F中的鈉離子存儲機制,發現了兩相反應和固溶反應并存的反應機制,且隨著成分的不同其電化學脫嵌機制也不盡相同。Kang等114采用理論計算結合實驗驗證的手段研究了Na3(VO1-xPO4)2F1+2x化合物中V3+/V4+和V4+/V5+氧化還原對的組合、鈉離子占位、F/O比例對工作電壓的影響(圖20a)及其鈉離子脫嵌機制。此外,他們發現通過體相結構調控,可以開發新型高能量密度的Nay(VO1-xPO4)2F1+2x正極材料,Kang等115設計了一種新型正極材料Na1.5VPO4.8F0.7,此材料的理論能量密度約為600 Wh·Kg-1,對應于V3.8+/V5+氧化還原對其每個晶胞單元中有1.2個離子能夠可逆脫嵌。電化學測試結果顯示此Na1.5VPO4.8F0.7正極材料具有優異的循環穩定性,經過100次循環容量保持率為95%,500次循環后可以保持84%的放電比容量。雖然Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1)化合物理論上具有很高的能量密度,但是由于電解液穩定電壓窗口的限制,其結構中的第三個鈉離子很難脫出,Goodenough等116通過理論計算預測采用Cl替換Na3V2O2(PO4)2F結構中的O形成的Na3V2Cl2(PO4)2F化合物有望實現第三個鈉離子的可逆脫嵌(圖20b),其理論能量密度高達758 Wh·Kg-1,但這一結論目前還沒有被實驗驗證。
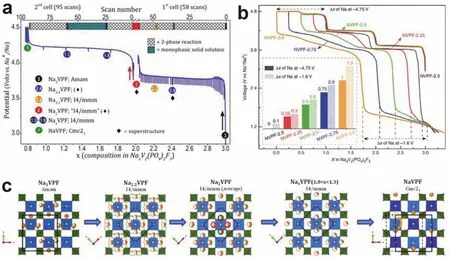
圖19 (a) Na3V2(PO4)2F3中Na+脫出過程中的電壓-成分曲線110;(b)無序相NaxV2(PO4)2F3中激發第三個Na+的電化學活性111;(c)基于Rietveld精修獲得不同Na3V2(PO4)2F3脫鈉相的鈉分布情況110Fig. 19 (a) Potential-composition electrochemical curves obtained upon Na+ extraction from Na3V2(PO4)2F3 110. (b) Trigger the activity of the third sodium electrochemically via the formation of a disordered NaxV2(PO4)2F3 phase 111. (c) Sodium distribution obtained from Rietveld refinement of the different phases upon sodium extraction from Na3V2(PO4)2F3 110.
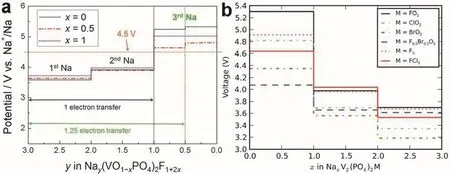
圖 20 (a)第一性原理計算的 Nay(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1; 0 ≤ y ≤ 3)的成分–電壓曲線 114;(b) NaxV2(PO4)2M中不同陰離子(M)摻雜對其電壓的影響116Fig. 20 (a) Voltage–composition curves for the Nay(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1; 0 ≤ y ≤ 3) electrodes from first-principles calculations 114. (b) Comparison of the voltage profiles of NaxV2(PO4)2M with different anion (M) substitutions 116.
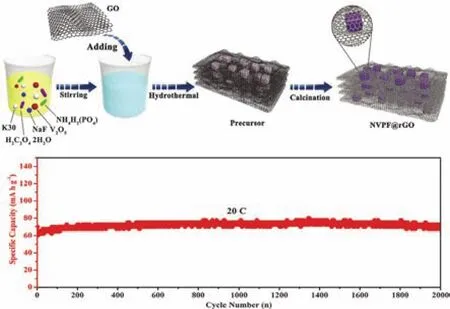
圖21 Na3V2(PO4)2F3立方體/石墨烯復合材料的制備過程及其在20C倍率下的長循環性能117Fig. 21 Preparation procedure of Na3V2(PO4)2F3 microcubes/graphene composite and its long cycling performance at 20C rate 117.
Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1) 類材料的本征電子導電性較差,嚴重影響了其電化學性能的發揮,研究者們采用導電層包覆/復合、摻雜和微納結構調控等手段進行改性研究。Liang等117制備一種Na3V2(PO4)2F3@rGO復合材料(圖21),表現出高達3.8 V (vsNa+/Na)的工作電壓平臺和優異的循環穩定性,組裝成全電池具有291 Wh·Kg-1的能量密度。研究發現三維石墨烯網絡可以提供連續的電子和離子傳輸通道,并緩解鈉離子嵌入和脫出過程中產生的應力以及體積變化,有助于提高材料的倍率性能和循環穩定性。此外,研究者們還采用有序介孔碳(CMK-3)118、三維石墨烯119、碳納米管120、石墨烯量子點121等導電材料包覆/復合手段來提升Na3(VO1-xPO4)2F1+2x化合物的電子導電性。Zhang等122研究了不同化合價的鈦離子(Ti2+、Ti3+、Ti4+)摻雜對Na3V2(PO4)2F3電化學性能的影響,發現合適的鈦離子摻雜可以有效提升Na3V2-xTix(PO4)2F3材料的電子導電性和離子傳輸速率,優化后的材料在0.2C的倍率下可以釋放出125 mAh·g-1的可逆容量,即使在40C的高倍率下仍可釋放104 mAh·g-1的容量。此外,研究者們還研究了Ru123、Mn124等元素摻雜對Na3(VO1-xPO4)2F1+2x類材料物理化學特性的影響。Xia等125通過微乳液調控的水熱反應法制備了一種RuO2包覆的Na3V2O2(PO4)2F納米線,其直徑約為50 nm,結合了導電層包覆和納米結構優勢,制備的復合材料在1C的倍率下可釋放出120 mAh·g-1的比容量,在20C的倍率下經過1000次循環后其放電比容量仍可保持95 mAh·g-1。此外,研究者們還采用多種物理或化學手段制備了Na3V2O2(PO4)2F/rGO微球126、Na3(VO)2(PO4)2F/C納米立方體121、Na3(VOPO4)2F多層微球127等結構來提升Na3(VO1-xPO4)2F1+2x正極材料的電化學性能。
4.2.3 Na2MPO4F (M = Fe、Mn、Co、Ni)
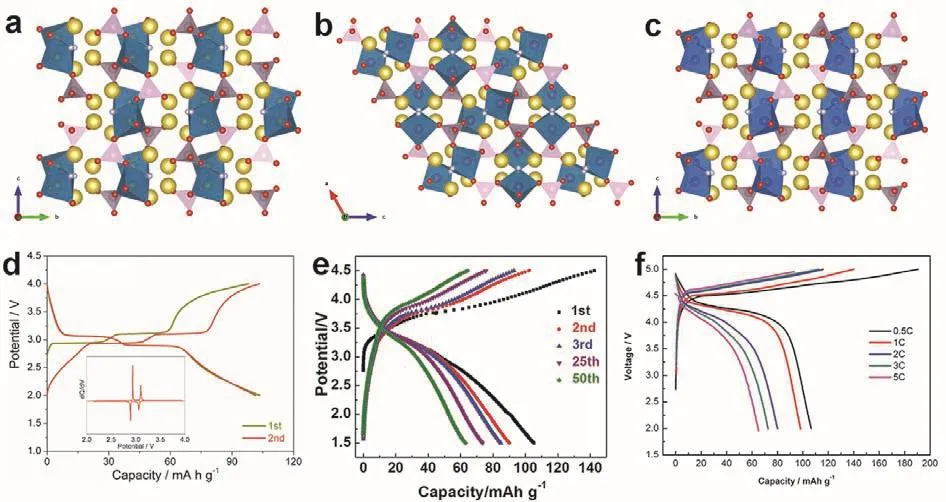
圖22 (a,d) Na2FePO4F、(b,e) Na2MnPO4F和(c,f) Na2CoPO4F的晶體結構和相應的充放電曲線131,137,138Fig. 22 Crystal structures and corresponding charge-discharge curves of (a, d) Na2FePO4F,(b, e) Na2MnPO4F, and (c, f) Na2CoPO4F 131,137,138.
研究人員一直都在尋找基于Fe2+/Fe3+氧化還原對的新型、環保的鐵基堿金屬氟磷酸鹽。Nazar團隊128首次報道了一種Na2FePO4F新材料。隨后,她們又報道了一種類似的新型Na2CoPO4F材料129。如圖22a,c所示,這兩種材料的晶體結構都屬于正交晶系Pbcn空間群,其結構中共面的MO4F2八面體通過F原子橋接形成M2O7F2單元,這些雙八面體M2O7F2單元和PO4四面體共角形成二維的框架結構,兩個鈉離子位于MPO4F層間。為了弄清原子尺度特征如何影響層狀Na2FePO4F的電化學性能,她們團隊采用原子模擬計算方法探索了鈉離子的傳導行為和固有缺陷特性130,結果表明,鈉離子更傾向于沿著層間能量較低的a面和c面方向遷移。Shao等131采用原位XRD技術研究了Na2FePO4F的儲鈉機制(圖23a),如圖22d所示131,在2.0–4.0 V (vsNa+/Na)電壓區間內,Na2FePO4F/C正極材料的充放電曲線顯示出兩對可逆的電壓平臺,對應于兩步可逆相變反應:Na2FeIIPO4F ? Na1.5FePO4F ?NaFeIIIPO4F,且Na2FeIIPO4F與其氧化物NaFeIIIPO4F之間的體積變化僅為3.7%,因此在鈉離子脫嵌過程中結構應變較小132。通過碳包覆和粘結劑優化,Na2FePO4F/C復合材料表現出優異的電化學性能,在4C的倍率下經過1000次循環后其容量保持率為84.7% (圖23b)。為了改善Na2FePO4F材料的儲鈉性能,研究者們嘗試了多種材料改性手段,包括碳包覆133,134和材料微納結構調控等135,136。
研究者們也將其它過渡金屬氟磷酸鹽化合物應用于鈉離子電池中,如Na2CoPO4F和Na2MnPO4F137,138,它們都可以通過高溫固相法、溶膠凝膠法和水熱法制備。Na2CoPO4F是高壓鈉離子電池良好的候選材料,在4.3 V (vsNa+/Na)附近有一個高電壓平臺(圖22f),基于單電子轉移其理論容量為122 mAh·g-1,對應理論能量密度為524 Wh·kg-1137。Na2MnPO4F也是一種潛在的鈉離子電池高壓正極材料,其晶體結構屬于單斜晶系P21/n空間群(圖22b)。Yang等138采用噴霧干燥法制備了一種Na2MnPO4F/C微球,其首圈放電比容量接近110 mAh·g-1(圖22e)。
此外,一些新型過渡金屬氟磷酸鈉鹽在鈉離子電池中也有很大的研究價值和應用潛力,包括:Na4NiP2O7F2139、Na2Mg(PO4)F140、Na3Ti2P2O10F141、Na7Fe7(PO4)6F3142等。目前關于一些新型高壓氟磷酸鹽正極材料的電化學反應機制解析及結構、性能優化的研究還比較少,在儲能機制解析和材料性能優化方面仍需努力。
4.3 焦磷酸鹽類
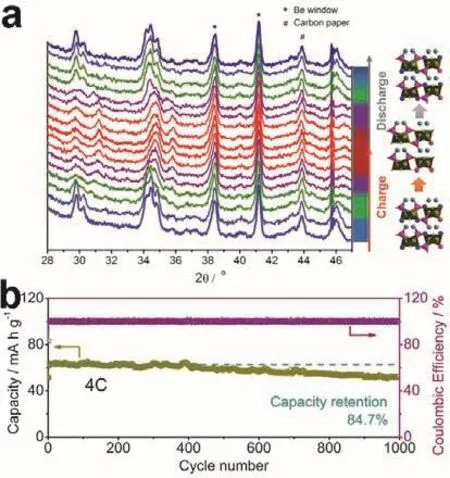
圖23 Na2FePO4F的(a)原位XRD譜和(b)循環性能131Fig. 23 (a) In situ XRD patterns and (b) cycling performance of the Na2FePO4F 131.
4.3.1 NaMP2O7 (M = Fe、Ti、V)
另一類很有潛力的鈉離子電池正極材料是焦磷酸鹽材料,如NaMP2O7(M = Ti、V、Fe),Na2MP2O7(M = Fe、Mn、Cu、Co),Na4-αM2+α/2(P2O7)2(2/3 ≤α≤ 7/8, M = Fe、Mn)等。它們具有不同的晶體結構,包括:三斜晶系(P1空間群)、單斜晶系(P21/C空間群)和四方晶系(P42/mnm空間群)。NaFeP2O7具有兩種不同的晶體結構,如圖24a,b所示,NaFeP2O7-I和NaFeP2O7-II都屬于單斜晶系P21/C空間群。NaFeP2O7-I是由共享角的FeO6八面體和PO4四面體構成,其結構中在[001]方向具有鈉離子遷移的通道。這種NaFeP2O7-I在高溫條件下(≥ 750 °C)很容易轉變為熱力學穩定的NaFeP2O7-II相。NaFeP2O7-II的晶體結構是由共享角的FeO6八面體和PO4四面體組成的籠狀結構,其中P-O-P的夾角為132.86°143。這種結構中的鈉離子位于細長的籠子中,在[101]方向有鈉離子的遷移路徑144。但是,目前還沒有針對NaFeP2O7儲鈉性能的研究報道。
此外,NaVP2O7和NaTiP2O7也被關注和報道145,146,它們的晶體結構和NaFeP2O7-II類似(圖24c)147。Okada等148采用高溫固相法制備了NaVP2O7并研究了其作為鈉離子電池正極材料的性能表現,其平均工作電壓為3.4 V (vsNa+/Na),理論容量為108 mAh·g-1,但在0.05C倍率下的首次放電比容量僅為38.4 mAh·g-1。最近,Kalaiselvi等149研究了AVP2O7/C (A = Li、Li0.5Na0.5、Na)化合物作為鈉離子電池負極材料的性能表現。
4.3.2 Na2MP2O7 (M = Fe、Co、Mn、Cu)
Na2MP2O7(M = Fe、Co、Mn、Cu) 是另一類焦磷酸鈉鹽化合物,它們的晶體結構通常以三斜、四方和正交結構存在。如圖25a所示,Na2FeP2O7是由共角的FeO6八面體二聚體[Fe2O11]通過共角或共邊的方式與PO4四面體連接而成,鈉原子存在于其框架結構中。Yamada組150最早將Na2FeP2O7應用于鈉離子電池中,他們測試了Na2FeP2O7材料的電化學性能,獲得了82 mAh·g-1的可逆容量,發現Fe2+/Fe3+的氧化還原電位位于2.5和3 V左右(圖25c)。他們還發現由于焦磷酸根穩定的結構,Na2FeP2O7材料和脫鈉相NaFeP2O7具有良好的熱穩定性,在600 °C時都不發生熱分解或析氧反應151。Choi等152采用理論模擬與實驗驗證相結合的方法深入研究了Na2FeP2O7材料的結構特征、電化學性能和熱力學行為。他們采用同步輻射X射線衍射譜結合DFT計算對Na2FeP2O7的晶體結構進行了深入研究。結果表明,其晶胞中含有8個鈉原子位點,DFT計算結果顯示,Na1位點的能量高于Na2–Na8位點,Na1沿[011]方向遷移的能量勢壘最低(0.48 eV)。因此,在動力學和熱力學方面,Na1都是最容易脫嵌的鈉原子位點。準平衡電勢結果和第一性原理計算結果一致表明,Na2FeP2O7的電化學過程包括兩種反應機制:一種是2.5 V左右的單相反應,另一種是2.5–3.0 V電壓范圍內的連續的兩相反應。
之后的一系列研究都旨在優化Na2FeP2O7材料的電化學性能。例如,通過碳納米管修飾的Na2FeP2O7材料表現出優異的倍率性能153。由于Mn2+/Mn3+電化學活性氧化還原對具有較高的工作電勢,通過錳摻雜可以將Na2FeP2O7材料的平均工作電壓提升至3.2 V (vsNa+/Na)154。非原位XRD和CV測試結果表明,由于鈉配位環境和鈉占位率的不同,Na2Fe0.5Mn0.5P2O7中發生的是單相反應。此外,研究者們也通過導電材料包覆/復合155、原子摻雜156、電解液優化157等手段進一步提升Na2FeP2O7的電化學性能。
Na2MnP2O7具有兩種不同的三斜晶系結構:Na2MnP2O7-I和Na2MnP2O7-II,它們具有類似的結構框架,但不同的晶胞大小和Mn-O-Mn、P-O-P鍵角(圖25a,b)。Choi和Yamada等158,159將Na2MnP2O7應用于鈉離子電池中,在3.8 V (vsNa+/Na)左右具有良好的電化學活性并釋放出90 mAh·g-1的可逆容量(圖25d)。他們采用第一性原理計算發現電化學性能提升的主要是由于原子的重排程度低,降低了電子傳導和離子相界遷移的障礙。通過石墨烯修飾可以有效提升Na2MnP2O7的電化學性能160。
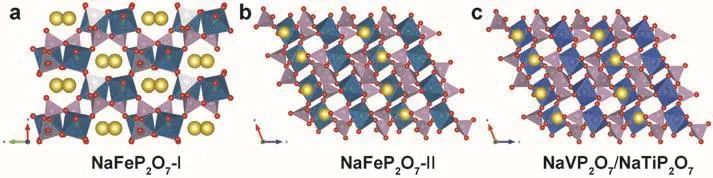
圖24 (a) NaFeP2O7-I、(b) NaFeP2O7-II和(c) NaVP2O7/NaTiP2O7的晶體結構Fig. 24 Crystal structures of (a) NaFeP2O7-I, (b) NaFeP2O7-II, and (c) NaVP2O7/NaTiP2O7.
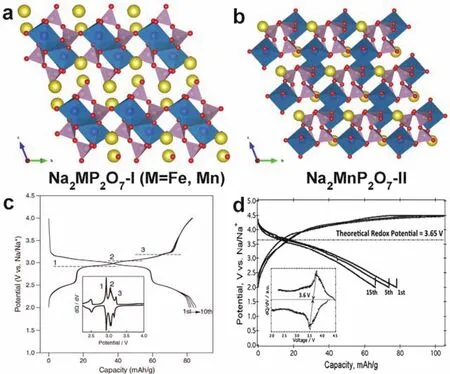
圖25 (a) Na2MP2O7-I (M = Fe, Mn)和(b) Na2MnP2O7-II的晶體結構;(c) Na2FeP2O7 150和(d) Na2MnP2O7 159的充放電曲線Fig. 25 Crystal structures of (a) Na2MP2O7-I (M = Fe, Mn) and (b) Na2MnP2O7-II.Charge-discharge curves of (c) Na2FeP2O7 150 and (d) Na2MnP2O7 159.
研究人員也對高壓正極材料Na2CoP2O7進行了研究。Na2CoP2O7具有三種不同的晶體結構,分別為正交晶系Pna21空間群、三斜晶系P1空間群和四方晶系P42/mnm空間群144。Yamada等161報道了一種正交結構(空間群Pna21)的Na2CoP2O7,此材料結構中具有二維的離子擴散通道,平均工作電壓為3 V。Jung課題組162成功制備了富含鈉缺陷的三斜晶系Na2CoP2O7,顯著提升其能量密度。通過引入缺陷來驅動電極材料電化學反應活性也為其它新材料的設計開發提供了新思路。
4.3.3 Na4-αM2+α/2(P2O7)2 (2/3 ≤ α ≤ 7/8,M = Fe、Mn)
非化學計量比的焦磷酸鹽Na4-αM2+α/2(P2O7)2(2/3 ≤α≤ 7/8,M = Fe、Fe0.5Mn0.5、Mn)也表現出良好的儲鈉性能163。圖26a為Na3.12Fe2.44(P2O7)2的晶體結構示意圖,屬于三斜晶系P1—空間群,其三維框架是由共角的Fe2P2O22和Fe2P4O20基本單元呈中心對稱連接而成,每個基本單元包含兩個FeO6八面體和兩個P2O7基團。Nazar等163發現Na3.12Fe2.44(P2O7)2正極材料的可逆容量約為90 mAh·g-1,平均工作電位為3.0 V (vsNa+/Na)左右(圖26b)。Chou等164采用原位同步輻射XRD技術和密度泛函理論計算揭示了Na3.32Fe2.34(P2O7)2中的離子存儲機理,結果表明在鈉離子脫嵌過程中,Na3.32Fe2.34(P2O7)2發生的是單相轉變且其結構中具有一維的離子遷移路徑。
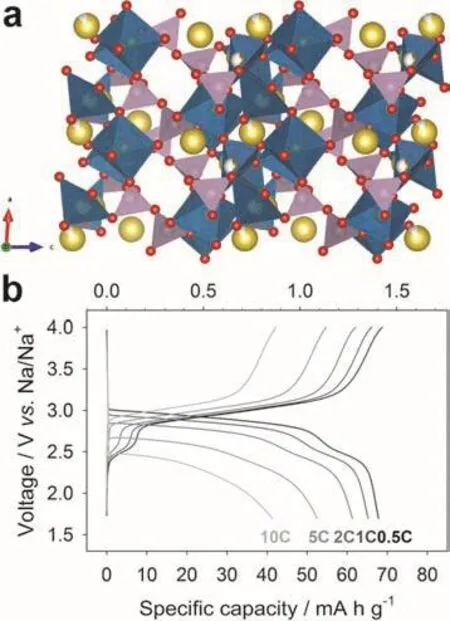
圖26 Na3.12Fe2.44(P2O7)2的(a)晶體結構和(b)充放電曲線163Fig. 26 (a) Crystal structure and (b) charge-discharge curves of Na3.12Fe2.44(P2O7)2 163.
研究人員采用多種材料改性策略對Na3.12Fe2.44(P2O7)2化合物的儲鈉性能進行研究。Li等165–167通過導電碳材料的包覆或復合有效提升了Na3.12Fe2.44(P2O7)2的電子導電性。Deng等168,169通過多種生物化學手段構筑了三維多孔結構的Na3.12Fe2.44(P2O7)2,有效縮短了鈉離子的遷移路徑且暴露了更多的電化學活性位點。
4.3.4 Na7V3(P2O7)4
具有不同結構的釩基焦磷酸鹽也得到了一些研究。如圖27a為Na7V3(P2O7)4的晶體結構,屬于單斜晶系C2/c空間群,其結構中VO6八面體和P2O7基團共角形成三維的鈉離子遷移路徑。Kang等170最先將Na7V3(P2O7)4作為正極材料應用于鈉離子電池中(圖27b),其氧化還原電位約為4.13 V (vsNa+/Na),在鈉離子脫嵌過程中,其晶胞變化僅為1%,在1C的倍率下充放電時,經過600次循環后其容量仍可保持75%。Deng等171–173通過生物化學手段構筑了多種不同三維微納結構的Na7V3(P2O7)4/C復合材料,其電化學性能得到了顯著提升。此外,在尋找鈉離子電池新型正極材料的進程中,其它過渡金屬焦磷酸鈉鹽也得到了初步研究,如Na1.82Mg1.09P2O7174、Na7Fe4.5(P2O7)4175、t-Na2(VO)P2O7176和δ-(MoO2)2P2O7等。
4.4 混合磷酸鹽類
4.4.1 Na4M3(PO4)2P2O7 (M = Mn、Fe、Co、Ni)
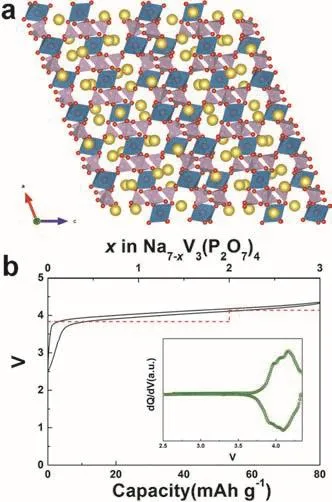
圖27 Na7V3(P2O7)4的(a)晶體結構和(b)充放電曲線170Fig. 27 (a) Crystal structure and (b) charge-discharge curves of Na7V3(P2O7)4 170.
將不同的聚陰離子結合在一起,可得到一系列結構新穎、電化學活性高的高壓正極材料。早期關于混合多價陰離子類化合物Na4M3(PO4)2(P2O7)(M = Fe、Mn、Co、Ni)的研究主要集中在材料結構解析。近年來,研究人員將它們應用于鈉離子電池中。如圖28a所示,這些材料中PO4四面體和MO6八面體共角組成雙鏈,層間通過焦磷酸根的P—O—P鍵橋接,相鄰的兩層之間形成沿著[010]和[001]方向延伸的離子擴散通道177。Kang等178使用第一性原理計算和實驗相結合的方法最先研究了Na4Fe3(PO4)2(P2O7)材料的儲Li/Na性能,其作為鈉離子電池正極材料釋放出129 mAh·g-1的可逆容量且平均工作電壓為3.2 V (vsNa+/Na)。Yang等179通過電化學原位XRD和核磁共振(NMR)技術研究了Na4Fe3(PO4)2(P2O7)中的相轉變機制(圖28b),Na4Fe3(PO4)2(P2O7)材料中鈉離子的脫出和嵌入過程是一種不完全的固溶反應,存在明顯的局部晶格畸變,固態NMR結果也印證了這一結論。電化學測試結果顯示(圖28c),制備的Na4Fe3(PO4)2(P2O7)/C復合納米材料在0.05C的倍率下首次放電比容量為110 mAh·g-1且平均工作電壓為3.1 V (vsNa+/Na)。
研究者們采用多種改性策略來優化Na4Fe3(PO4)2(P2O7)的結構,進而提升其儲鈉性能。最近,Chou等180采用溶膠-凝膠法制備了不同微納尺度的Na4Fe3(PO4)2(P2O7)/C復合材料,在0.05C和20C的倍率下分別釋放出113和80.3 mAh·g-1的放電比容量,在20C的倍率下經過4400次循環后其放電比容量仍能保持69.1%且表現出優異的高低溫特性。Cao等181,182采用三維石墨烯修飾、納米形貌控制的方法得到了性能優異的Na4Fe3(PO4)2(P2O7)正極材料。
Nose等183將Na4Co3(PO4)2P2O7作為正極材料應用于鈉離子電池中,其在4.1–4.7 V (vsNa+/Na)的電壓范圍內顯示出多步氧化還原反應(圖28d),可逆放電比容量為97 mAh·g-1。他們還報道了另一種多元混合磷酸鹽化合物Na4Co2.4Mn0.3Ni0.3(PO4)2P2O7,其在4.2和4.6 V左右出現兩對氧化還原電位184。Kang課題組185也將混合磷酸鹽材料的研究擴展到了Na4Mn3(PO4)2(P2O7),作為鈉離子電池正極材料,Na4Mn3(PO4)2(P2O7)中Mn2+/Mn3+氧化還原電位高達3.84 V (vsNa+/Na)且釋放出109 mAh·g-1的比放電容量(圖28e)。他們基于第一性原理計算和實驗相結合,證明了鈉離子在三維擴散通道中具有較低的活化能,因此該材料具有優異的倍率性能(20C),且Jahn-Teller效應引起的晶格畸變有助于打開鈉離子的擴散通道從而有效提升了離子遷移速率。此外,Passerini等186最先研究了Na4Ni3(PO4)2(P2O7)的儲鈉特性(圖28f),發現基于Ni2+/Ni3+氧化還原對的平均輸出電壓高達4.8 V (vsNa+/Na)。
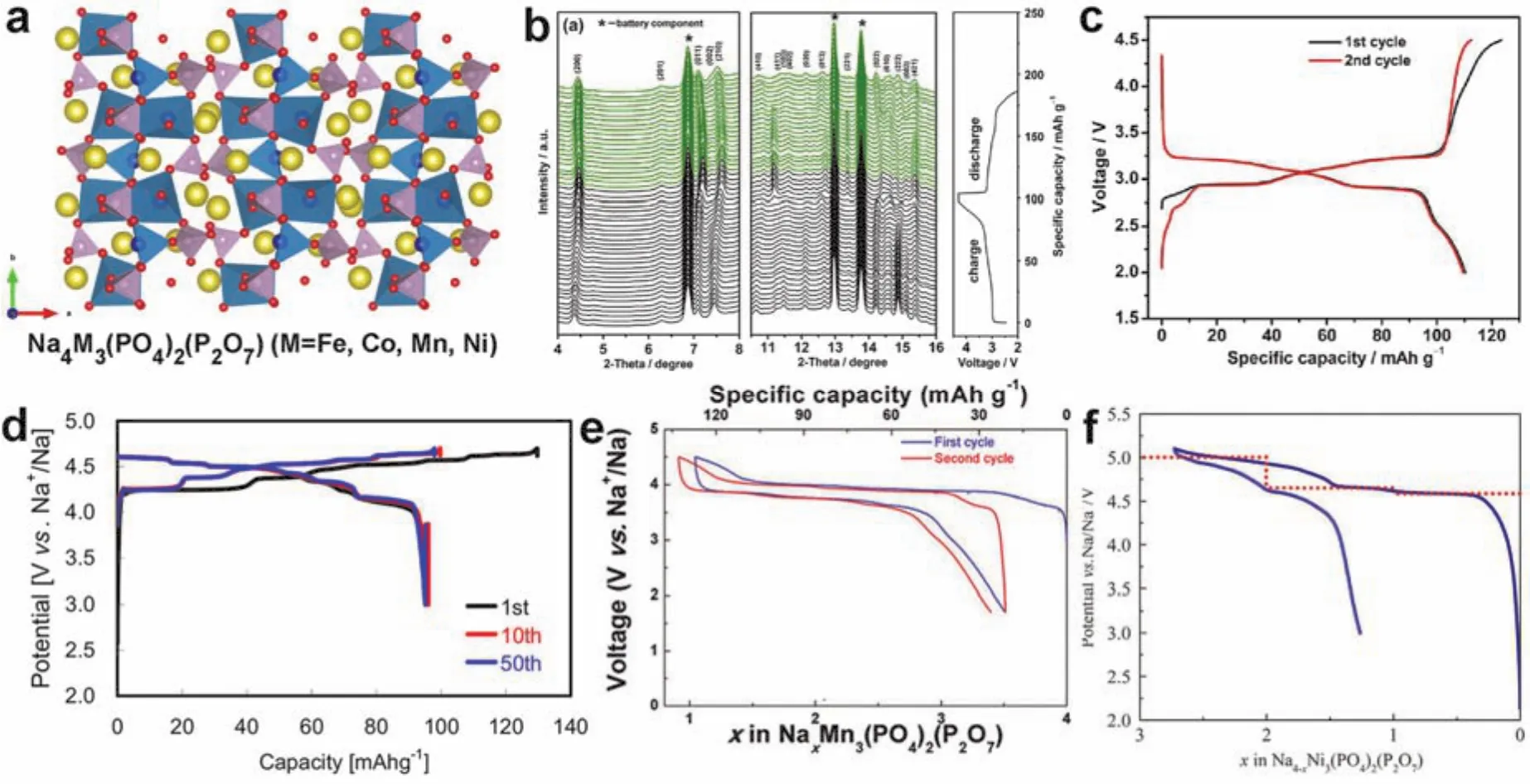
圖28 (a) Na4M3(PO4)2(P2O7) (M = Fe、Mn、Co、Ni)的晶體結構;Na4Fe3(PO4)2(P2O7)的(b)原位XRD譜和(c)充放電曲線179;(d) Na4Co3(PO4)2(P2O7) 183、(e) Na4Mn3(PO4)2(P2O7) 185和(f) Na4Ni3(PO4)2(P2O7) 186的充放電曲線Fig. 28 (a) Crystal structures of Na4M3(PO4)2(P2O7) (M = Fe, Mn, Co, Ni). (b) in situ XRD patterns and(c) charge-discharge curves of Na4Fe3(PO4)2(P2O7) 179. Charge-discharge curves of (d) Na4Co3(PO4)2(P2O7) 183,(e) Na4Mn3(PO4)2(P2O7) 185, and (f) Na4Ni3(PO4)2(P2O7) 186.
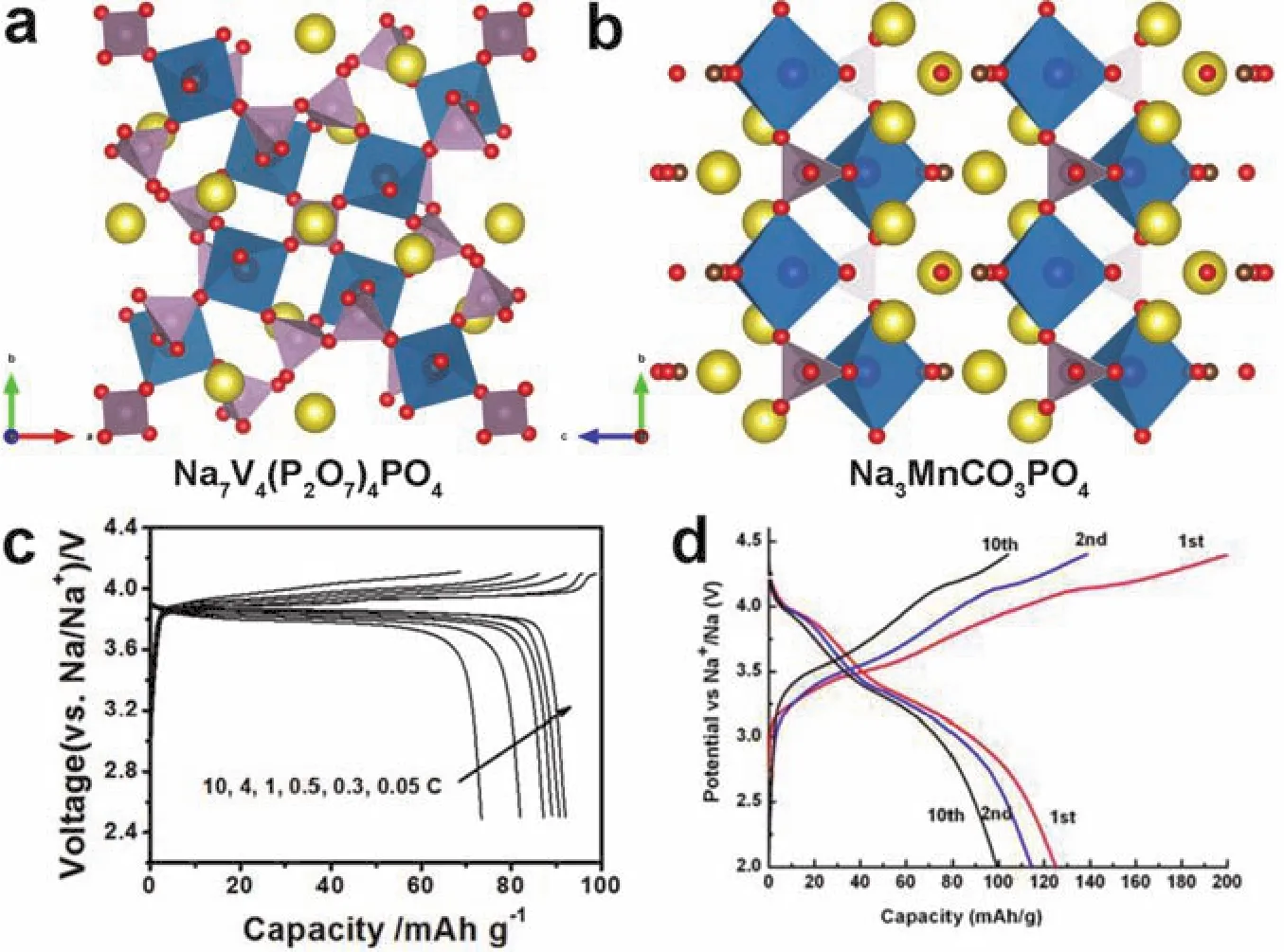
圖29 (a,c) Na7V4(P2O7)4PO4 187和(b,d) Na3MnCO3PO4 191的晶體結構和對應的充放電曲線Fig. 29 Crystal structures and corresponding charge-discharge curves of (a, c) Na7V4(P2O7)4PO4 187 and(b, d) Na3MnCO3PO4 191.
4.4.2 Na7V4(P2O7)4PO4
Na7V4(P2O7)4PO4也是一種廣受關注的混合磷酸鹽化合物,如圖29a所示,其晶體結構屬于四方晶系P21c。Choi等187研究了Na7V4(P2O7)4PO4的儲鈉性能,表現出高達3.8 V (vsNa+/Na)的工作電壓(圖29c),在0.5C倍率下經過1000次循環后其容量保持率為78%。Zhang等188通過恒電流間歇滴定(GITT)技術發現Na7V4(P2O7)4PO4在充放電過程中存在中間相Na5V3.5+4(P2O7)4PO4。此外,研究者們采用導電碳修飾189、構筑分級結構189、形貌調控190等手段進一步改善Na7V4(P2O7)4PO4的電化學性能。
4.4.3 Na3MPO4CO3 (M = Fe、Mn、Co、Ni、V)
5 總結與展望
鋰離子電池因為其高能量密度、長壽命等特點在電動汽車和儲能領域中得到了廣泛的應用。聚陰離子磷酸鹽電極材料相比于其它正極材料具有更好的安全性能和循環穩定性,在電動汽車等應用領域具有獨特的優勢。鈉離子電池因其具有原材料資源豐富、價格低廉等突出優點,近年來被視為是繼鋰離子電池之后可作大規模儲能系統應用的理想體系。因此,探尋資源豐富、經濟環保具有優良電化學性能的儲鈉電極材料已成為當前的一個研究熱點。聚陰離子型化合物因具有更穩定的結構和更大的離子擴散通道等特性備受各國科學家的青睞。雖然磷酸鹽正極材料在理論上具有很好的應用前景,但電子導電性差和容量偏低等缺陷極大的限制了其走向廣泛應用。
本文概述了鈉離子電池的組成、工作原理、正負極材料和面臨的問題,指出了提升鈉離子電池能量密度的關鍵在于正極材料的優化設計并總結了影響鈉離子電池正極材料工作電壓的內部和外部因素,詳細綜述了鈉離子電池磷酸鹽正極材料的最新進展,包括正磷酸鹽類、氟磷酸鹽類、焦磷酸鹽類和混合磷酸鹽類化合物,通過對磷酸鹽材料的晶體結構、儲鈉機理和改性策略等方面的綜述,揭示材料成分、結構與電化學性能之間的本征關系,為聚陰離子磷酸鹽正極材料的持續改性和新型磷酸鹽高壓正極材料的探索開發提供指導。
今后,在聚陰離子磷酸鹽體系正極材料方面還需要努力的方面包括:(1)開發新型高比能磷酸鹽正極材料。對新型高電壓、高容量聚陰離子正極材料進行設計和材料性能預測,通過理論計算分析離子類型、濃度、離子占位對聚陰離子型正極材料本征結構、儲鈉容量、儲鈉電位、離子輸運、電子結構等的影響,量化其特殊的體相結構與電化學本征特性關系。(2)磷酸鹽正極材料電化學機理研究。借助系列電池原位表征技術,分析電極材料工作過程中的相轉變、界面作用機制,探究微納米電極材料結構、成分和形貌與其電化學性能的內在關聯,為電極材料優化、電池系統優化提供更精準科學指導。(3)開發與磷酸鹽正極材料適配的耐高壓電解液。研究電解液成分、濃度、添加劑種類等對電解液活性、電化學穩定窗口的影響。探索制備耐高壓窗口穩定、儲能效率高的電解液新途徑。揭示電極/電解液異質界面作用機制,弄清界面快速荷質傳輸規律。(4)開發鈉離子全電池。綜合研究磷酸鹽正極與電解質、負極之間的相互作用,全電池系統在高低溫環境中的電化學表現,研究其相容性和匹配性。通過正交實驗尋找出最優的電池組合,優化電池組裝工藝,制備全電池單體,評估材料在全電池體系中的綜合表現。

