早期乳腺癌保乳術后動態與靜態調強放療技術的劑量學對比分析▲
鐘勝河 胡洪波 黎建緒
(1 廣西崇左市人民醫院腫瘤科,崇左市 532200,電子郵箱:258589859@qq.com;2 廣西醫科大學附屬腫瘤醫院放療科,南寧市 530021)
乳腺癌是我國常見的惡性腫瘤之一,其死亡病例數居全球第二位,嚴重地影響我國女性的健康[1]。臨床研究已證實,采用保留乳房手術(簡稱保乳術)聯合放射療法(簡稱放療)治療乳腺癌的效果與乳腺癌根治術相當[2]。目前臨床上使用的放療技術有普通放療、三維適形放療、逆向調強放療、電子線放療、容積旋轉調強放療、圖像引導放療以及自適應放療等,其中逆向調強放療使用最多。有研究顯示,調強放療在保乳術后放療中有明顯的優勢[3]。目前臨床使用的逆向調強放療分為靜態調強和動態調強。多葉光柵可通過采用step and shoot(SS)與sliding window(SW)兩種不同的模式來設計形成靜態調強和動態調強兩種放療的計劃。目前關于動態調強放療技術與靜態調強技術間的優劣勢尚未明確。本研究通過采用動態調強和不同子野數量的靜態調強技術設計不同的放療計劃,分析這兩種不同調強照射方式在乳腺癌靶區的劑量均勻性以及周圍危及器官的受照體積和劑量分布等方面的差異,探討適用于乳腺癌的調強治療方式,為臨床應用提供參考。
1 資料和方法
1.1 臨床資料 選取2018年2~8月在崇左市人民醫院行保乳術后放療的25例女性早期乳腺癌患者作為研究對象,其中病變位于左側19例,右側6例,年齡31~49(44.14±6.15)歲。所有患者術后病理均提示手術切緣無殘留,腋窩或前哨淋巴數量≥1個。放療照射范圍包括胸壁及鎖骨上下區,病理分期Ⅰ~Ⅲ期,卡氏評分≥80分。
1.2 CT定位及靶區勾畫 患者選擇仰臥體位,雙手臂十字交叉置于額頭,用真空袋固定患者體位,用激光燈線對體位,標記等中心點。體表用鉛絲標記乳腺下界(即平臥時乳腺褶皺位置下方2 cm)以及術后瘢痕位置。檢查前對患者進行自由平靜呼吸訓練,然后采用飛利浦Brilliance 16做CT定位掃描,掃描層厚為5 mm,范圍從環甲膜至肋膈角下3 cm,將全部乳腺及鄰近的危及器官完整掃描,通過醫院信息管理系統和瓦里安醫療系統(Area)將圖像傳至瓦里安(VARIAN)公司的Eclipse 13.5計劃系統。臨床靶體積(clinical target volume,CTV):參照鉛絲標記在CT圖像上勾畫,包括整個乳腺組織、胸肌間淋巴結和乳房下胸壁淋巴引流區;上界至胸鎖關節,下界至乳房褶皺下2 cm,內界為胸骨中線,外界為腋中線,前界在皮膚下2 mm,后界緊貼胸壁。計劃臨床靶體積(planning clinical target volume,PCTV)在CTV基礎上外放,頭頸方向外放1 cm,其余方向外放5 mm,皮膚不外放。每例患者均由同一名醫師勾畫靶區,并由同一名主任醫師審核,以確保靶區的一致性。本研究中的危及器官包括雙側肺、心臟及脊髓。
1.3 計劃設計 采用瓦里安(VARIAN)公司的Eclipse 13.5計劃系統進行逆向調強放療計劃設計,射線源采用Varian CX直線加速器。所有放療計劃的處方均為靶區劑量50 Gy,2 Gy/次,5次/周;對危及器官劑量限制為:患側肺V20<30%,V30<20%,心臟V30<40%、V40<30%(V為處方劑量的百分比),脊髓最大劑量<45 Gy,對側肺平均受照量<2.5 Gy。放療計劃設計時若以上均滿足劑量學要求時,則著重考慮降低肺受照劑量。先對計劃進行通量計算,得到滿意的通量圖后,計算兩種多葉光柵運動方式下的劑量分布情況。動態調強直接選擇SW模式計算(即SW組)。在計算靜態調強時,將子野強度水平設置為:7、10、13、16、19、22這6個等級水平,形成6個靜態調強計劃(分別為SSL07、SSL10、SSL13、SSL16、SSL19、SSL22共6組)。所有的計劃均采用AAA算法計算,劑量計算網格設為2.5 mm,使用的劑量率為400 MU/min。
1.4 計劃評估 計劃完成后,分別對等劑量分布靶區和正常組織器官劑量體積直方圖進行評估。靶區劑量的分析指標包括PCTV的最大劑量、平均劑量及V95、V100、V107、適形度指數(conformity index,CI)、均勻性指數(heterogeneity index,HI)等指標。其中CI[4]的計算公式為:CI=(Vt.ref*Vt.ref)/(Vt*Vref),其中Vt為靶區體積,Vt.ref為參考等劑量線包括的靶區體積,Vref為參考等劑量線包括的體積,CI值的范圍是0~1,值越大,適形度越好。HI[5]的計算公式為:HI=(D2%-D98%)/D,式中D2%和D98%分別是指2%、98%靶區體積所受到的照射劑量,D是指計劃給予的處方劑量,HI值越接近0,靶區劑量的均勻性越好,HI值越大說明超過處方劑量越大,靶區內劑量分布越不均勻。危及器官的保護程度主要根據患側肺、健側肺和心臟的劑量分布情況評估,包括患側平均劑量,接受10 Gy、20 Gy、30 Gy、40 Gy照射的體積百分比(V10、V20、V30、V40),心臟最大劑量。采用脊髓和健側肺平均劑量來評價危及器官的保護程度,機器跳數評價治療時間及對機器損耗情況。
1.5 統計學分析 采用SPSS 20.0軟件進行統計分析。符合正態分布的計量資料以(x±s)表示,比較采用配對t檢驗。以P<0.05認為差異有統計學意義。
2 結 果
2.1 靶區劑量分析 各組的PCTV-HI、PCTV-CI、PCTV最大劑量、PCTV平均劑量、PCTV-V95、PCTV-V107差異均有統計學意義(均P<0.05)。其中,SSL07組的PCTV-HI、PCTV最大劑量、PCTV-V107均高于SW組,PCTV-CI、PCTV平均劑量、PCTV-V95均低于SW組(均P<0.05);SSL10組的PCTV-HI高于SW組,PCTV-CI低于SW組(均P<0.05);SSL16、SSL19、SSL22組的PCTV-V107均低于SW組(均P<0.05);除上述外,SW組其他參數與靜態調強各組比較差異均無統計學意義(均P>0.05)。見表1。
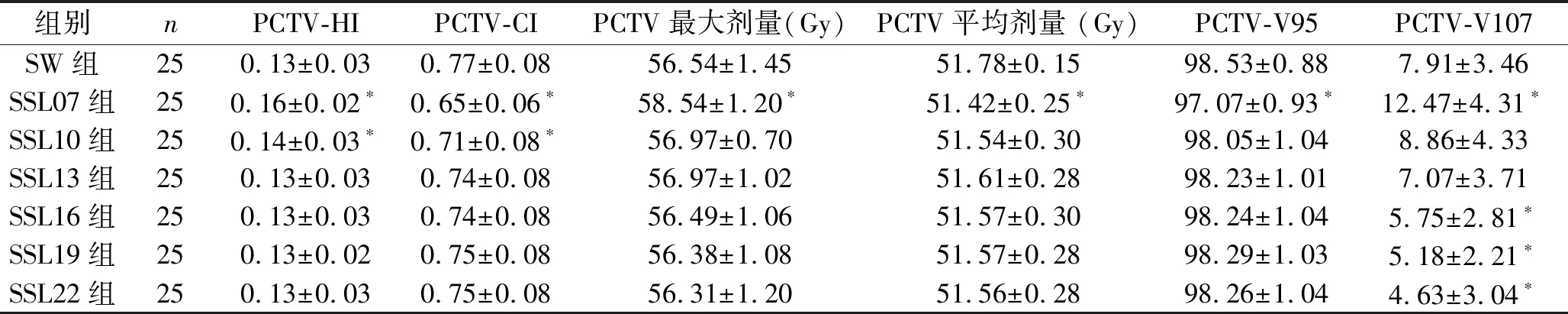
表1 靶區劑量學參數(x±s)
注:與SW比較,*P<0.05。
2.2 危及器官劑量分析 危及器官方面,SW組患側肺V40、V30、V20、V10、健側肺、心臟、健側乳腺最大劑量均高于各靜態調強組,但差異均無統計學意義(均P>0.05)。見表2。
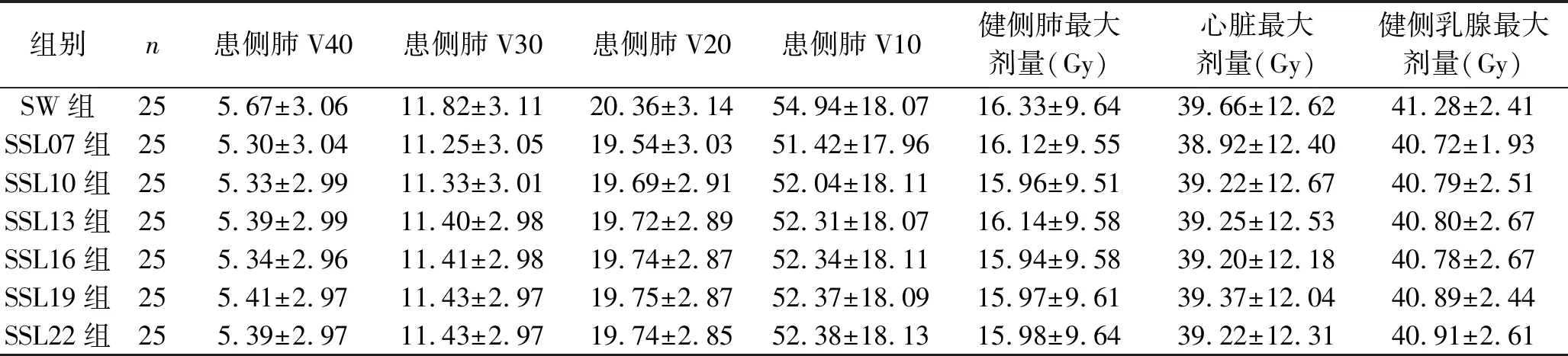
表2 危及器官劑量學參數(x±s)
2.3 各組間的機器跳數及執行時間比較 靜態調強各組機器跳數和計劃執行時間均低于SW 組(均P<0.05),而靜態調強各組間的機器跳數和計劃執行時間差異均無統計學意義(均P>0.05)。見圖1、圖2、表3、表4。
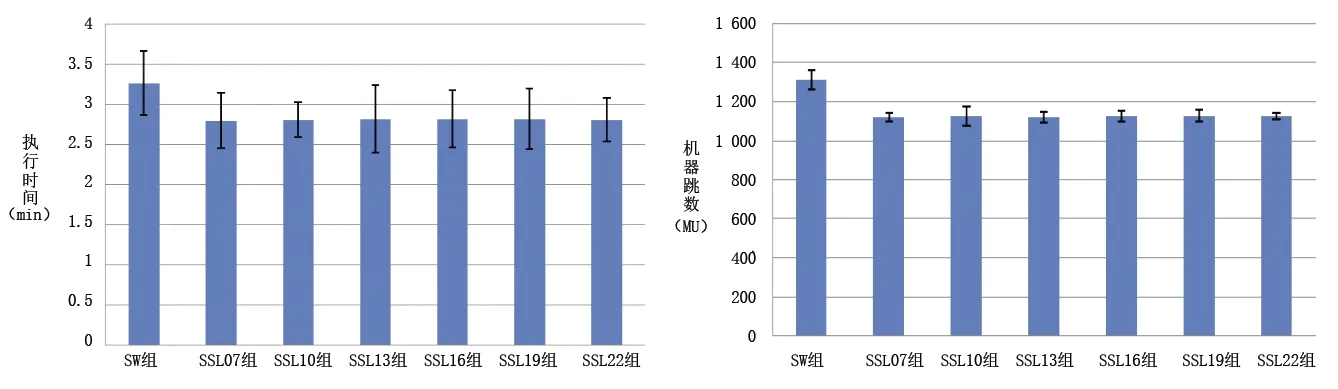
圖1 各組計劃執行時間直方圖 圖2 各組機器跳數直方圖
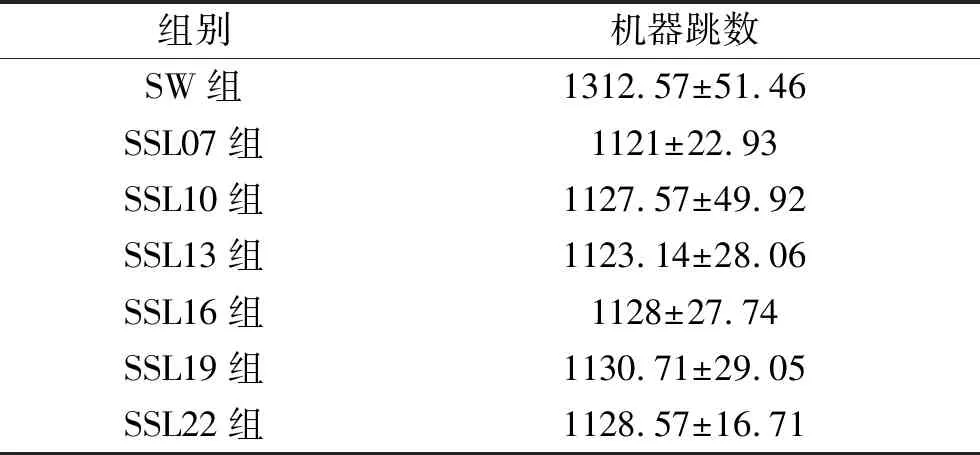
表3 各組機器跳數(x±s,MU)
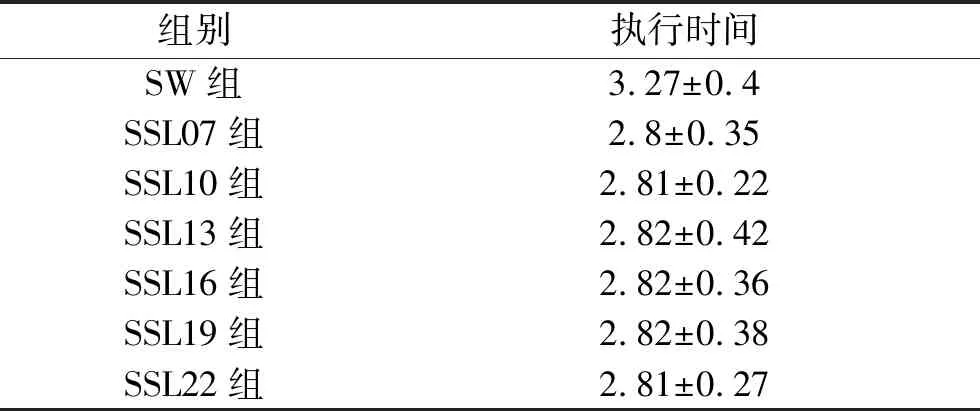
表4 各組執行時間(x±s,min)
3 討 論
乳腺癌是常見的女性惡性腫瘤之一,全球范圍內乳腺癌的發病率和死亡率僅次于肺癌[6]。近年來我國乳腺癌發病率及死亡率呈現逐年升高的趨勢,是45歲以下女性最常見的癌癥死因[1]。保乳術已成為早期乳腺癌的首選治療方式,術后多數患者需要行輔助放療、化療、內分泌治療、靶向治療等綜合治療[7]。有研究顯示,放療是乳腺癌保乳術后的必要治療手段,可延長患者生存期[8]。
朱健等[9]研究發現,放療中使用完全相同的射野參數并優化函數可形成相同的射野通量,但是選擇兩種不同的多葉光柵調強模式得到的靶區劑量無差異,均可以將處方劑量體現到靶區內,且靜態調強模式在三維空間中等劑量線的靶區適形度更優,能更好地保護靶區周圍的正常組織,降低危及器官的受照劑量。肖鋒等[10]研究發現,在早期鼻咽癌患者中,動態調強放療靶區內劑量分布優于靜態調強,靜態調強子野數量越多靶區適形度越好;CI、HI等各項指標顯示動態調強各個靶區的適形度、均勻度均優于或等于靜態調強;兩者的危及器官受量大體相當,靜態調強更有利于保護腮腺等正常組織。總體上講,鼻咽癌使用動態調強放療略優于靜態調強。
本研究中,瓦里安醫療公司Eclipse計劃系統在治療乳腺癌過程中使用的動態調強與靜態調強實施方法和步驟,以及計劃設計的時間均完全相同,結果顯示:(1)動態調強需要的機器跳數多于靜態調強各組(均P<0.05),而靜態調強的機器跳數隨著子野強度水平增加而增多但差異均無統計學意義(均P>0.05);從治療時間看,動態調強的治療時間最長,靜態調強治療時間隨著子野強度水平增加而縮短,但差異均無統計學意義(均P>0.05),與相關研究結果[10-11]相似。分析其原因為,從機器性能方面看,由于動態調強模式是在多葉光柵持續運動過程中,通過調節葉片的運動速度來形成不同形狀的子野,因此動態調強相較于靜態調強對葉片的走位精度以及葉片的響應時間都有較高的要求;而靜態調強模式下射線只有在葉片到位之后才能出束,所以靜態調強模式對葉片的到位精度要求相對較低。由此可見,靜態調強模式在降低機器損耗、延長多葉光柵等相關備件的壽命方面比動態調強模式更有優勢[11]。(2)從靶區劑量學方面分析,在形成靶區劑量通量圖后,動態調強模式下多葉光柵連續運動,劑量能過渡更加圓滑,更加接近優化形成的通量圖;而靜態調強模式下,由于多葉光柵走到位后才出束,劑量分布容易出現階梯現象。本研究中,由各靜態調強組與動態調強的靶區HI、CI等各項指標的差異可以看出,動態調強適形度、均勻度均優于或等于靜態調強,同時靜態調強子野數量強度水平越低靶區的適形度、均勻度越差,究其原因可能為動態調強模式下多葉光柵運動方式能更好地實現優化通量圖。(3)從周圍危及器官方面分析,乳腺癌放療考慮的正常器官有患側肺、健側肺、健側乳、心臟和脊髓等。本研究中,SW組患側肺V40、V40、V20、V10、健側肺、心臟、健側乳腺最大劑量均高于各靜態調強組,但差異均無統計學意義(均P>0.05)。這提示靜態調強模式下各項正常器官受到的輻射劑量小于動態調強模式,且子野數量越多正常器官受照射量越大。因此,在相同的優化劑量通量下靜態調強方式能有效地降低危及器官的受照劑量,更好地保護靶區周圍的正常組織,在不影響靶區劑量的情況下或可提高腫瘤患者的生存質量,但總體上動態調強模式周圍危及器官的受照量仍在可接受的范圍內,臨床運用時應綜合考慮。
綜上所述,在對早期乳腺癌保乳術后患者的調強放療過程中,動態調強和靜態調強各有優勢,在不考慮直線加速器損耗的情況,動態調強的靶區適形度、均勻性等各項參數優于靜態調強,雖然其周圍危及器官的受照量較動態調強略高,但仍在可接受的范圍內,建議優先考慮使用動態調強。但是本文研究未考慮多葉光柵的厚度,未對放療計劃進行劑量驗證以及未考慮呼吸運動對放療計劃的影響,這些問題是否會對靜態調強和動態調強產生影響有待進一步的研究。

