磷石膏礦化CO2反應體系調控碳酸鈣晶型的過程參數研究
謝安帝,李 季,朱家驊,葛 敬,吳 林,彭玉鳳,盧 蔚
(四川大學 化學工程學院,四川 成都 610065)
濕法磷酸工業產生大量固廢磷石膏,嚴重污染環境,磷石膏的資源化利用亟待解決[1]。CO2的過度排放引發溫室效應,對全球氣候和環境的影響愈發明顯[2]。利用磷石膏礦化CO2,生產高附加值(NH4)2SO4和CaCO3,以廢治廢,是實現CO2減排和磷石膏資源化利用的綠色低碳技術路線[3]。該過程的主要反應發生在CaSO4· 2H2O-NH3-CO2-H2O 三相反應體系中:

產物CaCO3有方解石、文石、球霰石3 種可能的結晶形態,其熱力學穩定性依次降低[4]。目前產物CaCO3呈方解石、球霰石等混合晶型,僅可作為水泥原料,經濟效益較低。球霰石型碳酸鈣通常為球形多孔顆粒,比表面積大,粒徑分布均勻,所以常用來改善產品物理性能和填充性能[5];同時,其良好的生物相容性和可降解性,在藥物控釋載體、仿生材料制備等生物醫學領域顯示出巨大的發展潛力[6-7]。如能實現球霰石型碳酸鈣的定向結晶,可以大大提升產物CaCO3的經濟附加值。
目前,球霰石型碳酸鈣的制備方法主要有仿生礦化法[8]、單分子膜法[9]、復分解法[10]、超聲分散法[11]等。但這些制備方法過程較為復雜,實驗條件要求較高,且產率較低,工業應用成本高,難度大。對于磷石膏礦化CO2體系,薛瀟[12]等通過添加不同濃度的乙二胺(EDA),成功合成了球霰石型碳酸鈣。SONG X F[13]等以脫硫石膏礦化CO2為基礎,向體系中加入聚丙烯酸(PAA),控制CaCO3晶型為方解石。雖然體系產物晶型得到了控制,但添加劑的使用,增加了成本和后續分離難度,不利于工程化應用。在類似體系的研究中,CaCO3的晶型與形貌會受反應過程參數影響,如:溫度、pH 值、壓力、溶液飽和度等[14-17]。如果利用磷石膏礦化CO2反應體系自身特點,實現產物晶型調控,將有工程實際應用價值。
研究磷石膏礦化CO2三相反應體系的溫度、氨濃度、CO2流量等過程參數對碳酸鈣晶型的影響,為不外加添加劑的前提下直接制備純凈球霰石型碳酸鈣提供基礎數據和實驗依據。
1 實驗材料和方法
1.1 實驗試劑與儀器
試劑:二水硫酸鈣、氨水、二氧化碳、無水乙醇、去離子水。
儀器:電熱恒溫水浴鍋(SINO TECH, XOSC-15D);懸臂式攪拌器(IKA? EUROSTAR 20 digital);蠕動泵(Kamoer, KCP-C);pH 計(Rex,PHSJ-4F);pH 電極(Rex, E-301-D);電子天平(SHANGPING, FA1004N); 電 熱 恒 溫 干 燥 箱(BOXUN, GZX- 9146MBE); X 射 線 衍 射 儀(SHIMADZU,XRD-6000);掃描電子顯微鏡(JEOL,JSM-6360LV);可見分光光度計(YUANXI,723N)。
1.2 樣品制備與表征

圖1 實驗裝置
實驗裝置見圖1。在原料罐中配制w(CaSO4·2H2O)為1%,w(NH3)分別為2%、4%、6%、8%的原料。將容積為1 L 的連續反應容器置于超級恒溫水浴中。循環水溫度設置為15 ~35 ℃,設置攪拌轉速500 r/min,調節CO2流量100 ~350 mL/min。以停留時間60 min 調節漿液體積流量為16.66 mL/min。反應穩定后取樣,利用真空泵過濾得到產物碳酸鈣,經去離子水和無水乙醇洗滌后,放入60 ℃恒溫干燥箱中干燥2 h,然后于干燥器中保存。
采用Malvern 型激光粒度分析儀分析樣品粒度。采用掃描電子顯微鏡(SEM)觀察樣品的形貌與結構。采用D/Max2500型轉靶X射線多晶衍射儀(XRD)分析樣品的物相晶型。采用可見分光光度計測定反應液中硫酸根含量。
2 結果與討論
2.1 氨濃度對產物碳酸鈣晶型的影響
在CaSO4· 2H2O-NH3-CO2-H2O 三相反應體系下,改變氨濃度會生成不同形貌和結構的碳酸鈣晶體,見圖2。由圖2可知,當w(NH3)為2%時,產物主要是立方體型小顆粒的團聚物,說明產物主要為方解石型碳酸鈣;當w(NH3)為4%時,立方體型顆粒群大量消失,晶體呈球狀團聚物,晶體表面粗糙并且伴隨著立方體型顆粒;當w(NH3)為6%時,表面立方體型顆粒進一步減少,表面趨于平整;當w(NH3)升高至8%時,晶體完全表現為球狀顆粒的團聚物,顆粒表面平整,說明產物主要為球霰石型碳酸鈣。

圖2 不同氨濃度下碳酸鈣結晶SEM圖
產物碳酸鈣的XRD譜圖如圖3所示。將樣品的譜圖與標準譜圖進行比對,發現樣品譜圖和標準譜圖的峰一一對應,沒有其他的衍射峰,說明樣品中只含有方解石和球霰石,純度較高。球霰石的(110)晶面對應的衍射角2θ=24.90°,方解石的(104)晶面對應的衍射角2θ=29.40°。

圖3 不同氨濃度下碳酸鈣結晶XRD圖
晶體中球霰石和方解石的質量分數可以根據XRD數據計算得到[18]。通過計算得到對應條件下球霰石和方解石的質量分數如表1所示。

表1 不同氨濃度下碳酸鈣產物晶型特征
由表1可知,當CO2流量為250 mL/min、溫度為25 ℃時,若w(NH3)大于4%,球霰石的質量分數均大于90%。由此可得出在CaSO4·2H2O-NH3-CO2-H2O三相反應體系下,氨濃度會影響產物碳酸鈣的晶型,且隨著氨濃度的增加,球霰石的含量增加。
2.2 溫度對產物碳酸鈣晶型的影響
在CaSO4· 2H2O-NH3-CO2-H2O 三相反應體系下,不同的溫度也會誘導形成不同形貌和結構的碳酸鈣晶體,通過計算得到對應條件下球霰石和方解石的質量分數如表2所示。

表2 不同溫度下所得碳酸鈣產物晶型特征
由表2 可知,當w(NH3)為6%、CO2流量為250 mL/min、溫度為15 ℃時,產物碳酸鈣中球霰石占比超過97%;當溫度升至25 ℃時,球霰石含量略微減少,仍超過95%;但當溫度為30 ℃時,球霰石質量分數迅速減少,小于40%;當溫度升至35 ℃,球霰石質量分數小于5%,方解石為產物碳酸鈣的主要晶型。
2.3 CO2流量對產物碳酸鈣晶型的影響
在CaSO4· 2H2O-NH3-CO2-H2O 溶解-結晶耦合反應體系下,不同的CO2流量也會誘導形成不同形貌和結構的碳酸鈣晶體,其中球霰石和方解石的質量分數如表3 所示。

表3 不同CO2流量下所得碳酸鈣產物晶型特征
由表3可知,當w(NH3)為4%、溫度為25 ℃、CO2流量為100 mL/min 時,產物中沒有球霰石,為單純的方解石;當CO2流量為150 mL/min 時,球霰石開始出現,但占比小于30%;當CO2流量增大至250 mL/min 時,球霰石占比接近95%;當CO2流量繼續增大至350 mL/min 時,球霰石占比略有下降,但仍超過90%,可能是因為當CO2流量大于250 mL/min時,CO2的吸收率降低[19]。
2.4 最佳實驗條件
在溫度為25 ℃、w(NH3)為8%、CO2流量為250 mL/min時成功制備出球霰石占比達到99%、表面平整的球形微孔球霰石型碳酸鈣,如圖4 所示。表征結果表明這種球霰石顆粒是由尺寸更小的球霰石顆粒聚集而成,粒徑在5 μm左右。
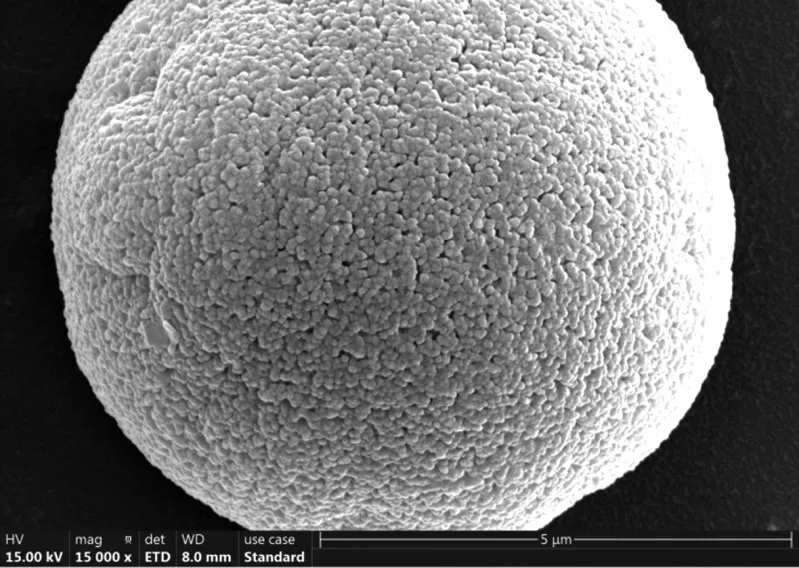
圖4 溫度25 ℃、w(NH3)8%、CO2流量為250 mL/min時制備的碳酸鈣
3 結論
在CaSO4· 2H2O-NH3-CO2-H2O 三相體系中,研究體系的溫度、CO2流量、氨濃度等反應參數對CaCO3結晶形貌的影響規律。當溫度大于30 ℃、CO2
流量小于150 mL/min 或w(NH3)低于2%時,主要產物為方解石型碳酸鈣。在溫度為25 ℃、w(NH3)為8%、CO2流量為250 mL/min 時,成功制備純度99%的球形微孔球霰石型碳酸鈣,為磷石膏礦化CO2反應體系直接制備純凈球霰石提供了基礎數據和實驗依據,證實了磷石膏礦化CO2反應體系直接制備純凈球霰石的可行性。

