生物材料肝素固定化結合方式專利技術綜述
鄭瓊娟 薛發珍

摘要:本文闡述了專利申請中生物材料肝素固定化結合方式,主要包括物理混合、離子鍵合和化學鍵合,并對不同的方法進行了比較。對生物材料領域科學研究、產業發展、專利申請以及審查工作等方面具有一定的指導作用。
關鍵詞:生物材料;肝素;固定化;物理混合;離子鍵合;化學鍵合
中圖分類號:R973 文獻標識碼:A 文章編號:1003-5168(2020)09-0080-03
1 引言
肝素的生物學作用主要是通過與抗凝血酶Ⅲ相互作用,肝素分子含有硫酸化殘基,其允許多糖以高親和力與抗凝血酶結合,從而加速凝血因子的失活。存在于動物體內的肝素具有良好的抗凝血作用,但其在體內停留的時間不長,通過固定化可以延長肝素在體內的作用時間,其中肝素固定化就是肝素大分子在生物材料表面上的固定化。通過肝素化來提高生物材料抗凝血性,是公認的改進生物材料抗凝血性能最好的方法之一。本文統計了專利申請中肝素固定化生物材料主要的結合方式:物理混合、離子鍵合和化學鍵合。
2 物理混合
物理混合主要利用物理包埋作用、分子鏈的纏繞和滲透、多孔材料的吸附作用等原理將肝素固定到生物材料表面。肝素在上述固定化的過程中未發生任何化學作用,因此保留了原始構象,能夠較好地發揮抗凝血性能。
常用來與肝素共混的主要是具有較高生物相容性的天然高分子:專利JPH01124465A[1]采用膠原或明膠與肝素進行共混成膜,用于人造血管等生物材料的抗凝血用;專利US2003161938A1[2]將低分子量肝素或硫酸乙酰肝素等,與多聚賴氨酸或肽混合進行涂層,其中所述肽優選具有精氨酸-賴氨酸-天冬氨酸-絲氨酸序列的四肽或者具有精氨酸-賴氨酸-天冬氨酸-賴氨酸序列的四肽,這些肽一方面可以抑制血小板聚集并可提高溶栓治療的功效和效力,另一方面具有很快粘附到表面上的能力,可以顯著減少接觸時間,以便在醫療裝置如心臟麻痹單元,氧合器或支架上獲得不可逆涂層;專利CN101879330A[3]將絲素蛋白與肝素制備成混合液,注入復合體中層的內表面,經冷凍干燥處理后,在復合體內層形成絲素多孔材料等。
物理混合方法簡便易行,但由于物理固定具有穩定性差和可控性差,故實用性較低,在三種主要固定方式中占比最低。
3 離子鍵合
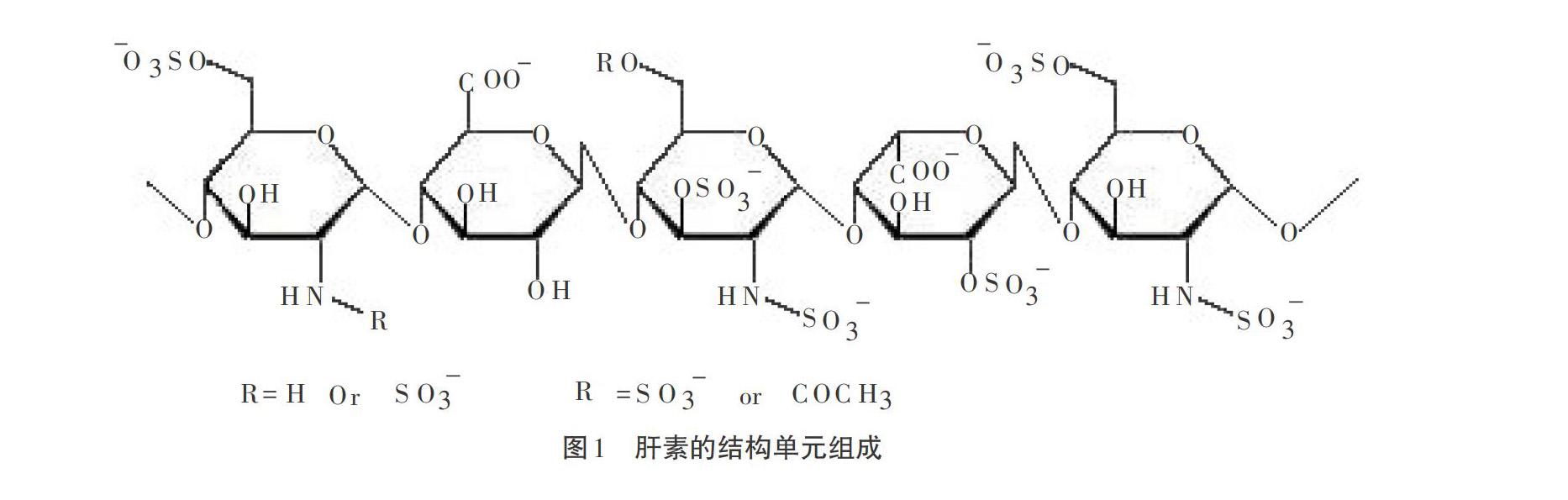
離子鍵合是利用正、負電荷之間的相互作用將帶有負電荷的肝素固定在生物材料的表面上。由于肝素分子上含有大量的負電性基團:羥基、羧基、磺酸基,具體如圖1所述,可以引入帶正電性的季銨基團偶聯劑或陽離子表面活性劑與肝素發生靜電吸附,如圖2所示,從而實現肝素的固定,如GERALD A、GRODE等[4]采用偶聯劑TDMAC通過兩步法,將偶聯劑與生物材料進行反應,從而在生物材料表面上引入陽離子基團,再利用季銨根離子與肝素分子的正負電荷吸附作用,將肝素吸附固定在生物材料上;專利JP2000202031A[5],將TDMAC與肝素優先形成TDMAC化肝素溶液,再利用AC段與生物材料的親和力進行結合;專利JPS4813341B2B1[6]設計了一種通過用由肝素和陽離子表面活性劑組成的有機溶劑可溶的共沉淀材料或包含溶解在有機溶劑中的這種共沉淀材料和塑料材料的液體組合物涂覆制品而在制品上提供抗凝血表面的方法,然后干燥如此處理的制品,可應用于任何與血液接觸的物品,如人工心臟,人工心臟瓣膜等。
離子鍵合還可以合成帶有陽離子基團如氨基等的高聚物,再與肝素作用,通過離子鍵合形成肝素涂層。如專利JPS498583A[7]在十二烷基硫醇和溴仿的存在下使丙烯腈和丙烯酸聚合,然后接枝甲基丙烯酸二甲基氨基乙酯,季銨化后吸附肝素形成肝素涂層。
為了進一步提高離子鍵合的結合力,可通過多層離子鍵結合以固定肝素,如CN1836743A[8]先用芯材材料聚乳酸、或聚乙醇酸及其共聚物、或聚己內酯制成多孔的支架,然后用帶有正電荷的殼聚糖或膠原,與帶有負電荷的硫酸軟骨素或硫酸肝素組裝材料交替按順序一層一層自組裝在多孔支架芯材外層,重復自組裝步驟直到設計的組裝層數,而后快速冷凍和真空冷凍,即得到多孔、分層、三維空間多級結構的組織支架材料。
總體而言,離子鍵合較物理混合穩定,能夠維持肝素的原始構象,最大限度地保留抗凝血效果。但通過離子鍵合多層結合并不能很好的暴露抗凝血酶結合序列,導致抗凝血活性不能得到較好發揮,加之肝素易被血液中其它陰離子置換或因離子鍵的斷裂而快速釋放,使得生物材料表面較快失去抗凝血活性。
4 共價鍵合
共價鍵合利用生物材料表面上固有的,或者改性后具有的功能基團,如-NH2、-COOH、-NCO、-OH、等基團與肝素分子上的-OH、-COOH、-NH或共價結合,如專利US2005244453A[9]通過處理包括粘附聚合物和肝素的涂層組合物形成的涂料化合物,其中粘附聚合物和生物相容性藥劑通過光敏部分偶聯,如使用聚(丁基)甲基丙烯酸酯通過光敏部分與肝素發生光發生化學反應實現偶聯;或通過交聯劑如戊二醛、EDC的交聯反應,實現對肝素的共價固定,如EP0352330A1[10]通過交聯劑碳二亞胺或戊二醛實現肝素在絲素蛋白上的固定,并可根據需要進行成型,如流延成膜用于制備血液容器等。
相比于離子鍵合,共價鍵合具有更高的穩定性,由此獲得的肝素化生物材料在臨床上可長期使用。然而,更為穩固的固定結構,一定程度上反而限制了肝素分子的原始構象,導致被固定化肝素分子的生物活性被削弱。相應的,其抗凝血性能也受到一定的影響,上述問題是共價鍵合最大的缺陷。
為了解決共價鍵合后帶來的肝素活性下降的問題,可通過以下兩種手段進行改善:
第一,在生物材料表面與肝素分子之間連接一“空間臂”以增加肝素分子的自由性,如專利JPH09108331A[11]將肝素分子通過與半縮醛部位線性結合而延伸的尿素結合和烷基的懸垂支路接枝聚合并固定在生物材料上,構成樹枝部分的烷基有3~6個碳,通過上述改性方法可以實現防止肝素由于離子鍵合洗脫流失的同時,肝素與高分子材料之間的間隔可以確保肝素的柔軟運動性,進而能夠長時間保持持續優異的抗血栓性;專利US2005266038A1[12]通過胺封端的PEG偶聯到醛封端的肝素上,隨后除去第二胺上的t-BOC保護基團,然后可以使用第二氨基將肝素間隔部分接枝到聚合物或底物表面上,由此可使肝素分子具有柔性,從而使肝素分子的結合位點能夠被結合蛋白接近。采用連接“空間臂”法一方面可以提高肝素分子的自由性,顯著提高共價鍵合肝素的抗凝血活性;另一方面,相對離子鍵合,具有較強的結構穩定性,可滿足實際應用要求。因此,上述方法成為肝素固定化研究中未來最值得重點研究和完善的技術。
第二,控制肝素分子與生物材料表面的鍵合量,如終點固定法,專利CN102600515A[13]將高分子材料浸泡在高錳酸鉀的硫酸溶液中,進行酸化處理;將材料置于聚乙烯亞胺溶液中,以得到氨基化修飾的表面;將肝素鈉溶于去離子水中,加入亞硝酸,低溫重氮化處理肝素鈉,得到多糖片段A;氧化處理海藻酸鈉,使得海藻酸片段末端暴露醛基,得到多醛基海藻酸鈉,即多糖片段B;配置多糖片段A和B的反應液,將氨基化修飾表面的材料置于反應液中,通過終點固定法得到復合涂層。所得涂層中海藻酸鈉和肝素集團固定在材料的表面,增大與血液接觸的面積,有效發揮性質;終點固定法實施方便,結合牢固,空間構象好,能有效增加生物相容性和抗凝活性。
就穩定性而言,通過共價鍵合法遠較離子鍵合法和物理混合法的高,但就固定化肝素的抗凝血性來說,一般卻正相反。因此,如何提高共價鍵合固定化肝素的抗凝血性,同時又不影響生物材料的本體性能,一直是肝素化生物材料領域研究的重點內容。為了平衡上述問題,出現了同時使用離子鍵和共價鍵結合的方式,如US4118485[14],首先用伯胺試劑處理,使得肝素基本上所有陰離子基團被烷基銨離子封閉,然后用二醛處理生物材料表面,這種穩定化處理肝素具有完全的生理活性,并且在與血液或血漿接觸時不從表面釋放。
5 結語
基于固定化肝素的穩定性和生物材料的抗凝血性的抗衡,共價鍵合法和離子鍵合法成為固定化肝素的兩種主要方式。今后的研究重點應放在肝素固定化技術的改進上,研制出抗凝血性良好,同時其他生物學性能優良的新型抗凝血生物材料。
參考文獻:
[1] ?KANEGAFUCHI CHEM KK.COMPOSITION FOR ARTIFICIAL BASEMENT MEMBRANE AND IMPLANTATION DEVICE WITH ARTIFICIAL BASEMENT MEMBRANE:JPH01124465A[P].1989.
[2] Bo Johnson,等.Compositon and method for coating medical devices:US2003161938A1[P].2003.
[3] 趙薈菁,等.一種小口徑絲素蛋白管狀材料及其制備方法:CN101879330A[P].2010.
[4] GERALD A . GRODE等.Biocompatible Materials for Use in the Vascular System [J].J. BIOMED. MATER. RES. SYMPOSIUM,1972(3):77–84.
[5] AMANO KENICHI,等.ANTICOAGULANT INTRODUCER SHEATH:JP2000202031A[P].2000.
[6] Eiichi Masuhara,等.METHOD FOR PROVIDING ANTICOAGULANT SURFACES ONTO ARTICLES:US3717502A[P].1973.
[7] Heparin plastic anticoagulant coating - based on heparin-cationic surfactant complexand polymethacrylates, polyepichlorohydrin or polyurethane:JPS498583A[P].1974.
[8] 閆玉華,等.多孔、分層、三維空間多級結構的組織支架材料及其制備方法:CN1836743A[P].2006.
[9] Sean M Stucke,等.Composition and method for preparing biocompatible surfaces:US2005244453A[P].2005.
[10] HIRABAYASHI,等.FIBROIN MOLDINGS, PROCESS FOR THEIR PREPARATION, HEPARIN-IMMOBILIZING CARRIER,AND PROCESS FOR ITS PREPARATION:EP0352330A1[P].1990.
[11] NIPPON SHERWOOD KK,等.High polymer material having persistent anti-platelet activity - contains heparin molecule polyvinylidene chloride chloropolyethylene, chloropolypropylene and copolymer:JPH09108331A[P].1997.
[12] ThierryGlauser,等.Antifouling heparin coatings:US2005266038A1[P].2005.
[13] 李彤,等.一種多糖分子片段復合涂層的制備方法:CN102600515A[P].2012.
[14] ERIKSSON JAN CHRISTER,等.Non-thrombogenic medical article and a method for its preparation:US4118485[P].1978.

