大棚甜瓜枯萎病病原鑒定及其生物學特性
王先挺, 曾立紅, 王 斌, 張曉萌, 俞賢瓊
(寧波市鄞州區農業技術推廣站, 浙江 寧波 315100)
近10年來,寧波市試驗推廣哈密瓜型甜瓜種植,取得了良好的經濟效益,并已形成一定的產業,全市春季種植總面積為0.1萬hm2以上,單季產值1.2億~1.5億元。甜瓜的主要病害是蔓枯病,2012年后甜瓜枯萎病的發生日益嚴重,嚴重年份發病率達30%~50%,直接影響甜瓜的產量和質量,給生產帶來嚴重損失。甜瓜枯萎病在整個生長周期都可發病,以開花期、坐果期和果實膨大期3個階段為高發期,發病初期可有1~2枝蔓失水萎蔫,隨后根莖腐朽變褐色,引起整株萎蔫枯死。抽樣調查顯示,寧波地區大棚種植地塊甜瓜枯萎病的平均發病率在40%以上,主要發生在開花坐果以后,特別是在持續多日陰雨天轉晴,大棚內溫濕度驟然升高,不及時降溫降濕的情況下更易發生。發病初期,葉片從基部開始逐漸向上萎蔫,中午明顯,早晚恢復正常,幾天后葉片全部凋萎,根莖部縊縮,維管束變褐,整株枯死。
枯萎病是制約農業產業化發展的一種世界性土傳真菌病害,嚴重危害棉花、甘蔗、香蕉、番茄、瓜類、四季豆及辣椒等[1-2]經濟作物。尖孢鐮刀菌甜瓜專化型(Fusariumoxysporumf.sp.melonisW.C. Snyder &H.N. Hans)是甜瓜枯萎病主要病原菌,其病原菌菌絲和孢子可在土壤或未腐熟肥料中存活,從根部傷口或根尖組織侵染植物組織,在植株體內定殖[3]。目前,國際上已經鑒定出4種甜瓜專化型枯萎病生理小種,而且不同地區甜瓜專化型生理小種的分布存在差異[4];楊來新等[5]研究表明,甜瓜根腐病與枯萎病病原菌發病癥狀及病原形態相似。明確病原菌的種類及其生物學特性是進行病害防治的基礎,但是目前尚未見有關寧波地區甜瓜枯萎病病原菌的研究報道。因此,以寧波大棚典型甜瓜枯萎病病株為試材,采用組織分離法結合科赫氏法則 (Koch’s postulates)、形態學觀察及rDNA-ITS區序列檢測等方法,研究甜瓜枯萎病病原及其生物學特性,以期為甜瓜枯萎病的預防與防治奠定基礎。
1 材料與方法
1.1 材料
1.1.1 感病植株 新發病的甜瓜枯萎病病株,采自寧波市鄞州區農業科學研究所試驗基地甜瓜大棚。
1.1.2 試劑 0.1%升汞,馬鈴薯葡萄糖瓊脂(PDA)培養基,葡萄糖、蔗糖、乳糖、麥芽糖和可溶性淀粉,L-酪氨酸、脯氨酸、甘氨酸、硝酸鈉、L-谷氨酰胺、L-絲氨酸、L-白氨酸和L-天冬氨酸、(0.2 mol/L Na2HPO4-0.1 mol/L檸檬酸緩沖液、0.05 mol/L Na2HPO4-0.1 mol/L NaOH緩沖液,SDS購于上海生工生物公司。
1.1.3 儀器設備 恒溫培養箱,離心機,Mastercyclerpro 銀制梯度 PCR擴增儀。
1.1.4 其他 甜瓜種子,品種為紅妃哈密瓜,上海菲托種子有限公司;培養土,購于花圣園藝科技公司。
1.2 方法
1.2.1 病原菌分離 2015年5月12日從寧波市鄞州區農業科學研究所試驗基地甜瓜大棚采集試樣用于分離枯萎病病菌。田間調查發現,該基地2012年甜瓜枯萎病平均發病率17.9%,2015年為31.6%。參照文獻[6]的方法,采集新發病的甜瓜枯萎病病株,取病株莖段病健組織交界處上方5 cm取樣,經自來水沖洗,切成5 mm左右長度,用0.1%升汞表面消毒3 min,無菌水沖洗3遍,然后將組織塊置于馬鈴薯葡萄糖瓊脂(PDA)培養基上,于28℃恒溫培養箱中培養36~48 h,待組織塊周圍長出菌絲時,挑取邊緣單根菌絲轉接培養,即獲得純分離菌株。
1.2.2 病原菌致病性檢測 采用蘸根法、浸種法、澆根法和菌絲塊接莖基部法接種病菌,以空白處理為對照,每個處理接種10株甜瓜,3次重復。操作步驟: 1) 將分離所得的真菌在PDA培養基上培養7 d,用滅菌水洗下分生孢子,顯微計數檢測孢子濃度,分別制成5×105個/mL的孢子懸浮液備用。2) 空白對照處理,將培養土滅菌后裝入預先消毒的直徑為15 cm的花盆中澆水備用。將甜瓜種子在清水中浸泡12~14 h,挑選露嘴的種子插入培養土中(大約1/3),每盆5粒,在25~30℃的溫室內正常培育管理,觀察病情。3) 蘸根法,挖取盆中子葉完全展開的甜瓜幼苗,洗凈其根部,采用浸根接種法接菌[7],即將其根系浸入孢子懸浮液中10 min,以無菌水浸根作對照。接菌后的幼苗定植于營養缽內,在溫室內正常管理,觀察病情。4) 浸種法,將種子浸泡到孢子懸浮液種12~14 h,挑選露嘴的種子插入(大約1/3)到培養土中,其他同空白對照。5) 澆根法,當盆中甜瓜幼苗真葉完全展開時,用5×105個/mL的孢子懸浮液滴澆甜瓜幼苗根部,每株滴澆1 mL,其他同空白對照。6) 菌絲塊接莖基部法,當盆中甜瓜幼苗子葉完全展開時,切取3 mm×3 mm的PDA培養基上培養5 d的病原菌菌絲塊和分生孢子(培養基一同切取),粘帖在離培養土1 cm左右的甜瓜幼苗莖基部,3 d后去掉菌絲塊,其他同空白對照。選取回接試驗顯示萎焉癥狀的植株離培養土5~10 cm主莖,菌絲塊接莖基部法離病部5~10 cm主莖再作分離,分離到的真菌參照BOOTH[8]的方法和標準進行培養,同時進行形態學和分子生物學鑒定。
1.2.3 病原菌鑒定
1) 形態學鑒定。將供試菌株和經致病性測定后再分離獲得的菌株接種到PDA培養基上,28℃、12 h光照/12 h黑暗恒溫培養4 d后觀察菌落培養性狀,測量菌落大小,待產孢后,通過制玻片、顯微鏡觀察病原菌分生孢子形態特征。根據病菌生長速度、菌落形態特征和產孢特征,查閱真菌分類資料確定病原菌種類。
2) 分子生物學鑒定。采用PDA培養基培養待鑒定菌株,收集菌絲體,采用SDS法提取菌體基因組DNA[9]。瓊脂糖凝膠電泳檢測基因組DNA分子的大小、完整性及電泳條帶的清晰度。DNA樣品在-20℃冰箱保存備用。然后,擴增檢測基因組PCR。采用ITS1 5′-TCCGTAGGTGAACCTGCG
G-3′和ITS4 5′-TCCTCCGCTTAT TGATATGC -3′對提取的真菌基因組全長ITS區序列進行PCR擴增。PCR退火溫度58℃。將擴增出來的目的核酸片段送杭州華大基因生物工程有限公司純化后進行測序。采用MEGA 4構建系統發育樹,將核酸片段測序結果提交NCBI的GENBANK數據庫進行BLAST比對,選取相似度高的序列和一外族序列作為構建進化樹的序列;采用ClusterX進行比對分析,將比對結果導入MEGA 4中,采用Neighbor-Joining方法構建系統發育樹。
1.2.4 病原菌生物學特性測定 考察不同碳源、氮源、生長溫度和pH對病原菌生長的影響及病原菌的致死條件。將回接分離確定的病原菌代表性菌株在PDA平板上28℃培養3 d,用滅菌的內徑5 mm的打孔器切取菌落邊緣菌餅,分別移至不同培養基中央,28℃黑暗培養3 d。3次重復,3 d后用直尺測量菌落生長直徑。
1) 碳源。設5個處理,以葡萄糖、蔗糖、乳糖、麥芽糖和可溶性淀粉等為碳源,基本培養基為PDA,其他處理則將PDA中的葡萄糖替換成相同濃度的其他碳源。
2) 氮源。設8個處理,以L-酪氨酸、脯氨酸、甘氨酸、硝酸鈉、L-谷氨酰胺、L-絲氨酸、L-白氨酸和L-天冬氨酸等為氮源,基本培養基為蔡氏培養基,其他處理則將蔡氏培養基中的硝酸鈉轉換成相同濃度的其他氮源。
3) pH。設8個處理,用磷酸鹽緩沖液(0.2 mol/L Na2HPO4-0.1 mol/L檸檬酸緩沖液和0.05 mol/L Na2HPO4-0.1 mol/L NaOH緩沖液)將滅菌的PDA培養基調節pH分別為3.0、4.0、5.0、6.0、7.0、8.0、9.0和10.0。
4) 生長溫度。設8個處理,試驗溫度為5℃、10℃、15℃、20℃、25℃、28℃、30℃和35℃,培養基為PDA,分別置于不同溫度的培養箱內培養。
5) 致死條件。將經致病性測定后再分離獲得的菌株接種到PDA培養基上培養5 d,用滅菌水洗下分生孢子制成濃度為4.6×104個/mL的孢子懸浮液,分別裝在無菌的10 mL離心管內,在46℃、48℃、50℃和52℃的水浴鍋中處理10 min,再用移液槍吸取100 μL分別涂布在PDA培養基上,于28℃黑暗培養3 d,3次重復,3 d后測量生長情況和菌落直徑。
1.3 數據統計分析
數據分析采用SPSS 15.0進行方差分析和多重比較(Duncan法)。
2 結果與分析
2.1 甜瓜枯萎病菌的分離及其致病性
從甜瓜病株莖蔓組織中分離獲得1株真菌,將分離到的菌株采用蘸根法、浸種法、澆根法和菌絲塊接莖基部法回接至健康甜瓜苗上,其發病癥狀與自然發病癥狀基本一致(圖1)。其中,蘸根法,病菌回接10 d,2株甜瓜出現輕微萎焉癥狀,15 d時有5株甜瓜出現明顯萎焉癥狀,21 d共有21株甜瓜出現萎焉癥狀,回接發病率為70.0%。菌絲塊接莖基部法,病菌回接5 d后有12株甜瓜莖部出現病斑,15 d時病斑擴大并且明顯溢縮,病部長灰白色菌絲體和分生孢子,21 d時共有22株甜瓜出現萎焉癥狀,回接發病率為73.3%。浸種法,病菌回接10 d時有3株甜瓜在下部葉上出現輕微萎焉癥狀,上部葉仍然正常,21 d時共有11株甜瓜的下部葉出現明顯枯萎癥狀,回接發病率為36.7%。澆根法,回接發病癥狀同浸種子法一致,回接發病率為33.3%。從所有回接試驗中采集顯示枯萎癥狀的植株,在其離培養土5~10 cm的主莖中均再次分離到相同的真菌菌株。
2.2 病原菌鑒定
2.2.1 形態學觀察 分離獲得的真菌經25℃培養4 d后,在PDA培養基上形成直徑為41.3 mm的菌落,并產生大量的小型分生孢子,未見大型分生孢子;培養10 d后,偶見大型分生孢子。小型分生孢子從單個瓶狀小梗上產生,粘附在一起,不鏈生。單孢,橢圓或略彎,大小為(2.9~3.4)μm×(3.5~7.4)μm;1個分隔的大小為(3.0~3.3)μm×(3.5~8.2)μm(圖2)。大型分生孢子著生在單瓶梗上,多數2~3個分隔;2個分隔的大小為(4.3~6.4)μm×(22.6~31.0)μm;3個分隔的大小為(4.8~6.4)μm×(16.0~35.4)μm。參照BOOTH[8]的鐮刀菌專著(The Genus Fusarium),初步鑒定寧波甜瓜枯萎病的病原為Fusariumoxysporum。
2.2.2 分子鑒定 使用ITS1和ITS4引物對病原菌基因組進行PCR擴增后測序獲得455 bp大小的PCR片段。使用Clustalx和MEGA 4生物信息軟件以Neighbor-Joining方法構建的系統發育樹表明,該片段DNA序列與鐮刀菌Fusariumoxyspor-umstrain A0654 ITS區段相似性高達98%(圖3),二者處于同一分支,同源性很高。
2.3 鐮刀菌的生物學特性
2.3.1 碳源對病原菌生長的影響 從表1看出,碳源對病原菌生長(菌落直徑)的影響差異顯著,不同碳源病原菌的菌落直徑為葡萄糖>蔗糖>α-乳糖=可溶性淀粉>麥芽糖。其中,葡萄糖為最佳碳源,其菌落直徑最大,為38.3 mm,極顯著高于其余碳源;蔗糖其次,菌落直徑為34.7 mm,與其他碳源差異顯著;其余碳源間差異不顯著。
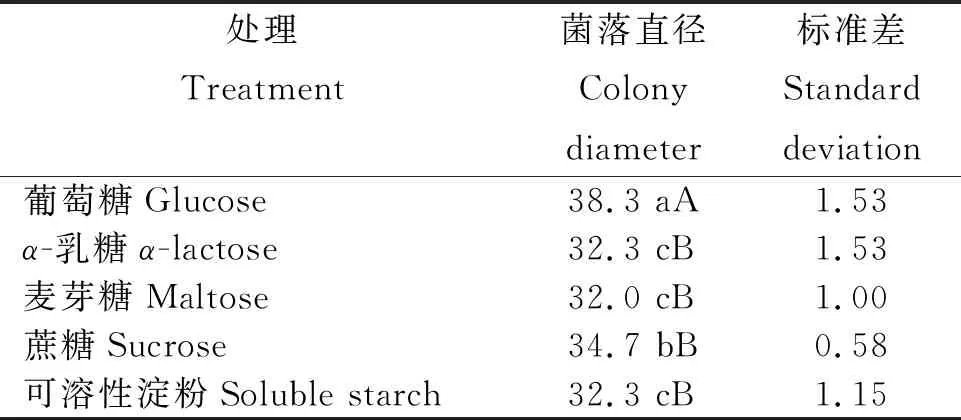
表1 不同碳源處理病原菌的菌落直徑
2.3.2 氮源對病原菌生長的影響 從表2看出,氮源對病原菌生長(菌落直徑)的影響差異顯著,不同氮源病原菌的菌落直徑為硝酸鈉>甘氨酸>白氨酸=酪氨酸>脯氨酸>谷氨酰胺>絲氨酸>天冬酰胺。其中,硝酸鈉為最佳氮源,其菌落直徑為40.3 mm,與甘氨酸差異顯著,極顯著高于其余氮源;甘氨酸其次,其菌落直徑為37.3 mm,顯著高于脯氨酸,極顯著高于谷氨酰胺、絲氨酸和天冬酰胺,與其余氮源差異不顯著;白氨酸、酪氨酸、脯氨酸和谷氨酰胺間差異不顯著,但均極顯著高于絲氨酸和天冬酰胺。
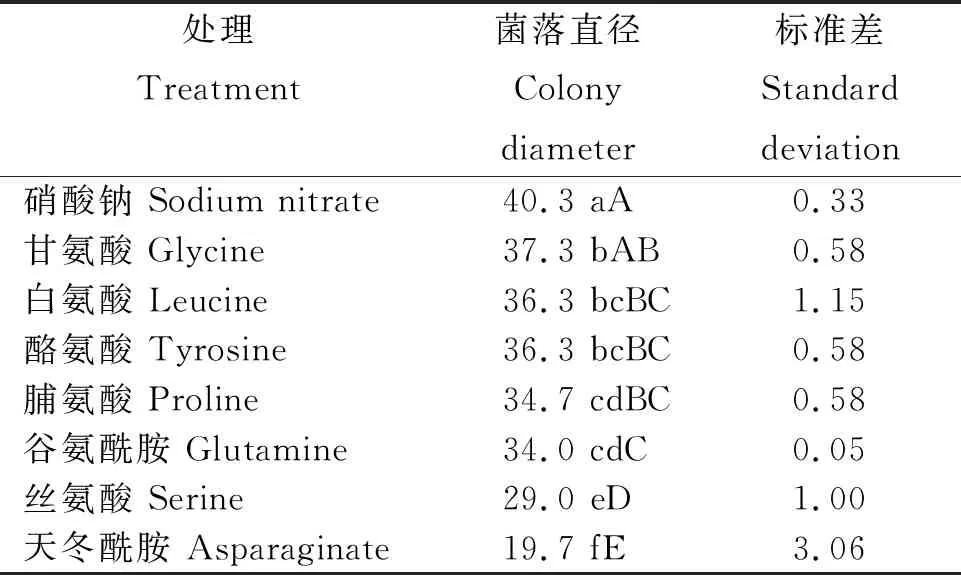
表2 不同氮源處理病原菌的菌落直徑
2.3.3 溫度與pH對病原菌生長的影響 從圖4看出,隨著培養溫度和pH升高,菌落直徑分別呈先增后減和先增后減再增再減趨勢,溫度和pH對病原菌生長(菌落直徑)的影響存在差異。其中,病原菌在15~35℃均能生長,25℃生長最佳,25℃菌落直徑最大,為41.7 mm,顯著高于其余溫度;25~30℃生長較好,菌落直徑顯著高于其余溫度;溫度大于30℃生長受到明顯抑制。病原菌對pH改變有較強的耐受性,在培養基pH 5.0~10.0均生長較好,且菌落大小無顯著差異(pH 8除外);培養基pH為4時,病原菌生長受到顯著抑制。
2.4 病原菌的致死條件
試驗結果顯示,病原菌孢子在46℃和48℃處理10 min后仍存活且在培養基上形成大量菌落;50℃處理后僅觀察到少量的小菌落形成;52℃處理后未形成菌落。表明,該病原菌分生孢子的致死條件為52℃ 10 min。
3 結論與討論
研究結果表明,寧波春季大棚甜瓜枯萎病病原菌為尖孢鐮刀菌(Fusariumoxysporum),與邵元健等[10]的研究一致,但與康鋒等[11]報道的新疆甜瓜枯萎病病原菌為腐皮鐮孢菌〔Fusariumsolani(Mart.) Sacc.〕不同。可見,不同地區甜瓜枯萎病的病原種類、致病機理存在一定差異。已報道的甜瓜枯萎病菌的生理小種有4個,分別為小種0、1、2和1.2[12]。總體上,具有地區針對性的枯萎病病原篩選和鑒定工作對于當地甜瓜枯萎病發生的防治具有重要指導意義。寧波春季大棚甜瓜枯萎病病原菌的生理小種有待進一步探明。
研究表明,葡萄糖和蔗糖、硝酸鈉和甘氨酸分別為該菌生長的較好碳源和氮源;病原菌在15~35℃均能生長,25~30℃生長較好,25℃生長最佳;病原菌對pH變化有很強的適應性,在pH 5.0~10.0均生長良好,表明,改變土壤pH并不能有效遏制該病原菌生長。病菌分生孢子的致死溫度為52℃ 10 min,與前期在西瓜枯萎病菌上的報道類似[13],同時一定程度上證明南方伏天灌水覆單層白膜提高大棚溫度能夠有效防治大棚甜瓜枯萎病的發生。
試驗結果表明,蘸根法、浸種法、澆根法和菌絲塊接莖基部法均能導致發病,蘸根法和菌絲塊接莖基部法發病率高,回接發病率分別為70.0%和73.3%;浸種子法和澆根法的回接發病癥狀不典型,只在下部葉上出現枯萎癥狀,上部葉仍然正常,但是再次分離發病病株莖仍能得到相同的鐮孢菌。表明,種子帶菌可以作為病害的初侵染來源,病菌可以通過胚根侵染發芽的種子,與前人的研究結果一致[14]。

