順鉑聯合培美曲塞治療表皮生長因子受體突變晚期非小細胞肺腺癌的臨床療效
陳東堂,冉秀榮
1商丘市第三人民醫院藥劑科,河南 商丘 476000
2商丘市第一人民醫院全科醫學科,河南 商丘 476000
肺癌是最常見的惡性腫瘤,非小細胞肺癌(nonsmall cell lung cancer,NSCLC)占所有肺癌的70%~85%[1]。肺癌起病隱匿,多數患者診斷時已為晚期,失去手術的機會[2],在無任何治療干預情況下患者的中位生存期僅5~10個月[3]。表皮生長因子受體(epidermal growth factor receptor,EGFR)突變與腫瘤細胞的增殖、分化、侵襲、轉移和血管生成密切相關[4]。研究顯示,與含鉑兩藥聯合化療方案相比,攜帶EGFR敏感突變的晚期NSCLC患者小分子酪氨酸激酶抑制劑(tyrosine kinase inhibitor,TKI)的療效更好且不良反應更低,已成為EGFR突變晚期NSCLC的一線化療選擇[6-7],但EGFR基因敏感突變的NSCLC患者的一線治療方案尚未確定。本研究比較順鉑+培美曲塞與順鉑+吉西他濱治療的EGFR突變晚期NSCLC的療效和安全性,現報道如下。
1 資料與方法
1.1 一般資料
選取2016年1月至2018年7月商丘市第三人民醫院收治的EGFR突變晚期NSCLC患者。納入標準:①均經病理學檢查確診為NSCLC;②TNM分期為Ⅲb或Ⅳ期;③生存期>3個月;④美國東部腫瘤協作組(Eastern Cooperative Oncology Group,ECOG)體力狀況評分(performance status,PS)為0~2分。排除標準:①有EGFR-TKI類藥物治療史;②肝腎功能及血常規異常;③病灶不能客觀測量。依據納入和排除標準,本研究共納入112例EGFR突變晚期NSCLC患者,根據治療方案分為觀察組(n=57)和對照組(n=55),對照組患者接受順鉑+吉西他濱治療,觀察組患者接受順鉑+培美曲塞治療。對照組中男30例,女25例;平均年齡為(59.80±9.11)歲;ECOG PS評分:0~1分32例,2分23例;TNM分期:Ⅲb期36例,Ⅳ期19例。觀察組中男35例,女22例;平均年齡為(60.14±8.45)歲;ECOG PS評分:0~1分30例,2分27例;TNM分期:Ⅲb期32例,Ⅳ期25例。兩組患者性別、年齡和TNM分期等臨床特征比較,差異均無統計學意義(P>0.05),具有可比性。
1.2 治療方法
對照組患者接受順鉑+吉西他濱方案化療:第1天,順鉑25 mg/m2加入500 ml生理鹽水中,靜脈滴注;第3天,吉西他濱1000 mg/m2加入100 ml生理鹽水中,靜脈滴注;觀察組患者接受順鉑+培美曲塞方案化療:第1天,順鉑25 mg/m2加入500 ml生理鹽水中,靜脈滴注;第3天,培美曲塞500 mg/m2加入150 ml生理鹽水中,至少10 min靜脈滴注;培美曲塞使用前1周開始補充維生素B12和葉酸;用藥期間口服4 mg地塞米松,每天2次。兩組患者均每3周重復,均至少完成2個療程。化療前后應用5-HT3抑制劑,必要時使用重組人粒細胞集落刺激因子防止白細胞下降。
1.3 隨訪方法
治療期間記錄所有可能與治療相關的不良反應及合并用藥情況,直至患者疾病進展或出現不可耐受的不良反應,每治療2個周期進行1次療效評價。治療結束后或化療3個周期完成后,采用電話或定期醫院復查的方式隨訪,隨訪時間8.2~14.3個月,中位隨訪時間11.5個月,截止至2019年3月。
1.4 觀察指標和評估標準
治療2個周期后,依據實體瘤療效評價標準(response evaluation criteria in solid tumour,RECIST)[9]評估兩組患者的臨床療效,包括完全緩解、部分緩解、病情穩定和疾病進展。總有效率=(完全緩解+部分緩解)例數/總例數×100%,疾病控制率=(完全緩解+部分緩解+病情穩定)例數/總例數×100%,比較兩組患者的無進展生存時間(progression-free survival,PFS)和總生存時間(overall survival,OS)。
治療前和治療3個月后,采用酶聯免疫吸附測定(enzyme-linked immunosorbent assay,ELISA)檢測兩組患者血清腫瘤標志物,包括癌胚抗原(carcinoembryonic antigen,CEA)、糖類抗原125(carbohydrate antigen 125,CA125)、血管內皮生長因子(vascular endothelial growth factor,VEGF)水平,操作步驟嚴格按照說明書進行。
依據美國國立癌癥研究所常見毒性分級標準3.0版(National Cancer Institute common toxicity criteria version 3.0,NCI-CTC v3.0)比較兩組患者的不良反應,分為0~4級。
1.5 統計學方法
采用SPSS 22.0軟件對所有數據進行統計分析,計量資料以均數±標準差(±s)表示,組間比較采用兩獨立樣本t檢驗,組內比較采用配對樣本t檢驗;計數資料以例數和率(%)表示,組間比較采用χ2檢驗;等級資料的比較采用秩和檢驗;采用Kaplan-Meier法繪制生存曲線,生存率的比較采用Log-rank檢驗;以P<0.05為差異有統計學意義。
2 結果
2.1 近期療效的比較
入組的112例晚期NSCLC患者均可進行療效評價,中位隨訪時間為11.5個月(8.2~14.3個月)。觀察組患者的臨床療效優于對照組患者,差異有統計學意義(Z=2.098,P=0.036)。觀察組患者的疾病控制率為73.68%(42/57),高于對照組患者的54.55%(30/55),差異有統計學意義(χ2=4.466,P=0.035)。觀察組患者的總有效率為43.86%(25/57),高于對照組患者的29.09%(16/55),差異無統計學意義(χ2=2.631,P=0.105)。(表1)
2.2 腫瘤標志物水平比較
治療前和治療后3個月,兩組患者CEA、CA125和VEGF水平比較,差異均無統計學意義(P>0.05)。治療后3個月,兩組患者CEA、CA125和VEGF水平均低于本組治療前,差異均有統計學意義(P<0.05)。(表2)
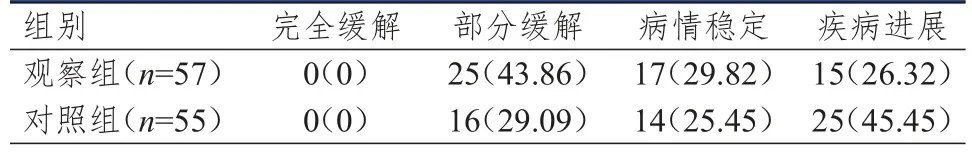
表1 兩組患者的臨床療效[n(%)]*
表2 治療前和治療后3個月兩組患者血清腫瘤標志物水平的比較(±s)
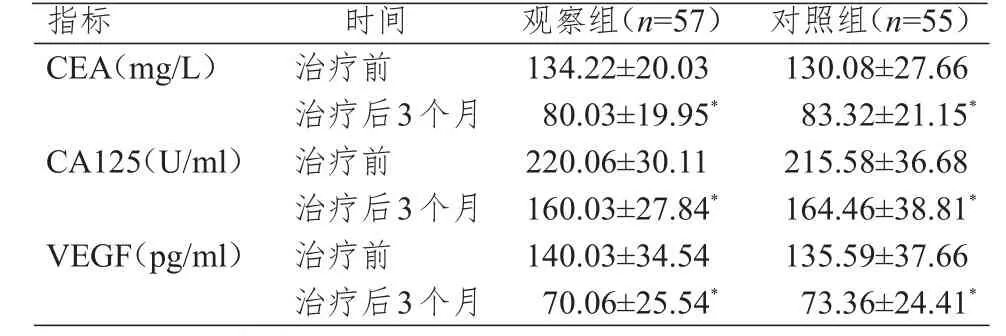
表2 治療前和治療后3個月兩組患者血清腫瘤標志物水平的比較(±s)
注:*與本組治療前比較,P<0.05
指標C E A(m g/L)C A 1 2 5(U/m l)V E G F(p g/m l)治療前治療后3個月治療前治療后3個月治療前治療后3個月1 3 4.2 2±2 0.0 3 8 0.0 3±1 9.9 5*2 2 0.0 6±3 0.1 1 1 6 0.0 3±2 7.8 4*1 4 0.0 3±3 4.5 4 7 0.0 6±2 5.5 4*1 3 0.0 8±2 7.6 6 8 3.3 2±2 1.1 5*2 1 5.5 8±3 6.6 8 1 6 4.4 6±3 8.8 1*1 3 5.5 9±3 7.6 6 7 3.3 6±2 4.4 1*時間觀察組(n=5 7)對照組(n=5 5)
2.3 生存情況的比較
觀察組患者的中位PFS為15.00個月(95% CI:12.80~17.15個月),長于對照組患者的12.00個月(95% CI:10.08~14.10個月),差異有統計學意義(χ2=19.734,P<0.05)。觀察組患者中位 OS為22.00個月(95% CI:20.03~23.64個月),長于對照組的17.00個月(95% CI:15.50~19.55個月),差異有統計學意義(χ2=19.459,P<0.05)。(圖1、圖2)
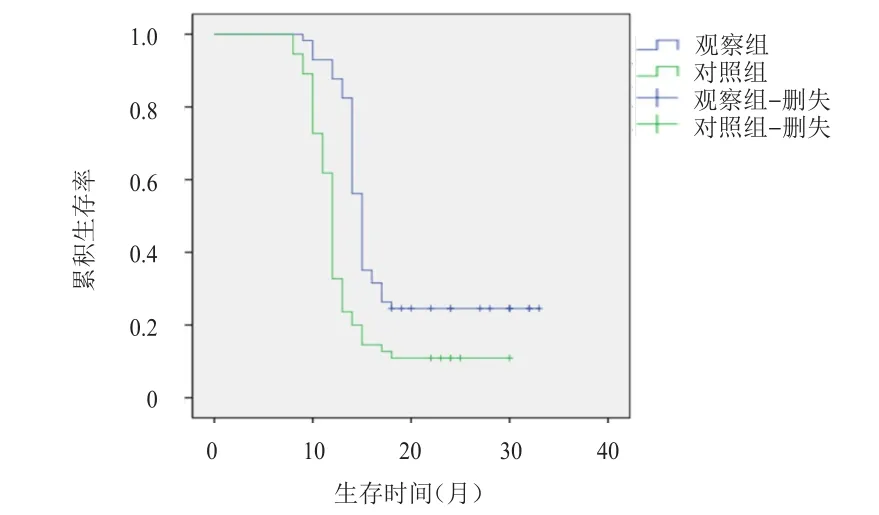
圖1 觀察組(n=57)和對照組(n=55)EGFR突變晚期NSCLC患者的無進展生存曲線
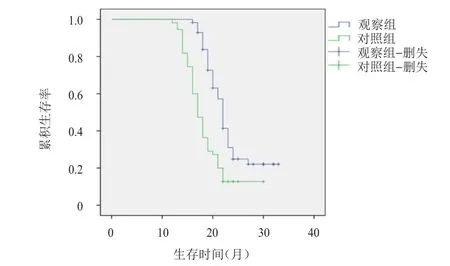
圖2 觀察組(n=57)和對照組(n=55)EGFR突變晚期NSCLC患者的總生存曲線
2.4 不良反應情況的比較
兩組患者的不良反應主要表現為血液毒性、消化道反應和肝腎功能損傷,胃腸道反應主要表現為惡心、嘔吐,均為1~2級。觀察組患者中性粒細胞減少的發生率最高,其次為貧血;對照組患者血小板減少發生率最高,其次為中性粒細胞減少。兩組患者中性粒細胞減少、貧血、血小板減少、胃腸道反應和肝腎功能損害發生率的比較,差異均無統計學意義(P>0.05)。(表3)

表3 兩組患者的不良反應情況[n(%)]
3 討論
肺癌發病率和病死率均均全球首位,且中國肺癌的發病率仍呈逐年上升趨勢。以鉑類藥物為基礎的兩藥聯合化療是晚期NSCLC患者的主要治療手段之一,常見的一線標準化療方案包括順鉑+紫杉醇、順鉑+吉西他濱、順鉑+培美曲塞等[8],這些化療方案的總體療效類似,但針對不同人群化療方案的優選仍是當前臨床治療中亟待解決的問題。
EGFR是細胞膜表面的糖蛋白受體,屬于絡氨酸激酶受體家族成員,NSCLC細胞膜表面陽性表達率達40%~80%[9],EGFR通過與其受體結合介導下游信號通路,主要包括磷脂酰肌醇-3-羥激酶(phosphatidylinositol 3-hydroxy kinase,PI3K)/蛋白激酶B(protein kinase B,PKB,又稱AKT)和大鼠肉瘤癌基因(rat sarcoma oncogene,RAS)/促分裂原活化的蛋白激酶(mitogen-activated protein kinase,MAPK)通路活化,誘導EGFR自身酪氨酸的磷酸化,從而促進腫瘤細胞的生長、增生、轉移。EGFR突變多見于del19缺失突變、L858R替換突變和G719X替換突變等,這些突變因未存在相應的配體而使激酶本身的活性強化,打破激酶的激活和非激活平衡,使非激活狀態的EGFR向激活狀態轉化,使腫瘤增殖分化狀態更劇烈,因此,與EGFR突變NSCLC患者相比,EGFR突變的NSCLC患者的預后效果更差。尋找抑制腫瘤細胞周期進程,增加耐受性降低不良反應的化療藥物至關重要。
培美曲塞是一種含吡咯嘧啶集團的抗葉酸劑,進入細胞通過多谷氨酸合成酶的作用將其轉化成多谷氨酸的形式,通過破壞腫瘤細胞內葉酸依賴性的代謝過程,抑制細胞復制,發揮抗腫瘤作用。培美曲塞代謝物在腫瘤細胞中半衰期較長,間接增加了培美曲塞在腫瘤細胞中的作用時間,增強了藥效,降低了劑量相關性不良反應的發生程度[10]。體外研究顯示[11],培美曲塞廣泛應用于結腸癌、乳腺癌、白血病、胰腺癌、肺癌、胃癌等多種惡性腫瘤中,且具有較好的抗腫瘤活性。美國食品藥物管理局(FDA)于2008年9月30日批準葉酸酯類似物代謝抑制劑培美曲塞的適應證,并將其與順鉑的聯用作為伴有非鱗狀組織學特征特性的局部晚期和遠處轉移的NSCLC患者的一線治療方案[12]。一項大型隨機Ⅲ期臨床研究比較培美曲塞和多西他賽類藥物在晚期NSCLC治療中的效果和毒性分析,結果發現,二者具有相似的有效率和生存率,但培美曲塞骨髓抑制的發生率及嚴重程度明顯低于多西他賽[13],表明培美曲塞與鉑類藥物聯用較其他鉑聯合方案具有相似療效但毒性反應發生率明顯較低。本研究結果顯示,與順鉑+吉西他濱相比,順鉑+培美曲塞的近期有效率更好,中位無進展生存時間、總生存時間較長,與既往研究報道一致[14]。李遠航和白維君[15]回顧性分析了100例晚期非鱗狀NSCLC患者的臨床資料,給予培美曲塞聯合鉑衍生物治療,結果顯示,無進展生存期和總生存期均較高,分別為127天和191天,效果優于其他含鉑聯合方案的治療效果相比,中位總生存期也明顯長于其他含鉑聯合方案(781天vs360天)。本研究結果顯示,兩種化療方案不良反應發生率無明顯差異,這與Manegold等[16]研究報道并不一致,可能與樣本量和研究對象的選擇差異有關。
此外,本研究未發現兩種治療方案對腫瘤標志物血清CEA、CA125、VEGF水平無明顯影響,二者在抗腫瘤細胞的增殖、侵襲和新血管生成等方面并無明顯差別,與既往研究報道并不一致[17-18]。尚需擴大樣本進行多中心隨機對照實驗以確定順鉑+培美曲塞對腫瘤標志物水平的影響。
綜上所述,順鉑聯合培美曲塞治療EGFR突變晚期NSCLC療效較好,值得臨床使用。

