改良擴(kuò)皮送鞘法在超聲引導(dǎo)下經(jīng)外周中心靜脈置管術(shù)中的應(yīng)用效果
婁海林 呂 利 周軼芳
經(jīng)外周靜脈置入中心靜脈導(dǎo)管(peripherally inserted central venous catheters,PICC)因創(chuàng)傷小、并發(fā)癥少、留置時間長等優(yōu)點(diǎn)已廣泛應(yīng)用于臨床[1-2]。超聲引導(dǎo)下的PICC極大地提高了PICC置入成功率,減少了置管出血量,且留置時間延長[3],但其操作過程中手術(shù)刀擴(kuò)皮時易損傷置入處組織、毛細(xì)血管或淋巴管,導(dǎo)致穿刺點(diǎn)滲血、滲液,增加感染概率和導(dǎo)管維護(hù)的次數(shù)。目前臨床常用的擴(kuò)皮手段有撕裂鞘與擴(kuò)張器組裝直接擴(kuò)張穿刺點(diǎn)后送鞘法、盲穿針外鞘與擴(kuò)張器組裝擴(kuò)張穿刺點(diǎn)后送鞘法,此兩種擴(kuò)皮送鞘法雖然可以降低皮膚和血管的損傷,減少穿刺點(diǎn)滲血、滲液的發(fā)生,但在實(shí)際操作中仍有部分人群因皮膚角質(zhì)層厚實(shí)導(dǎo)致送鞘失敗[4]。為此,筆者對擴(kuò)皮送鞘法進(jìn)行了改良。本文通過比較上述兩種擴(kuò)皮送鞘法與改良擴(kuò)皮送鞘法在超聲引導(dǎo)下PICC中的應(yīng)用效果,探討超聲引導(dǎo)下PICC的合適擴(kuò)皮送鞘方法。
1 資料與方法
1.1 一般資料 選擇2018年1月至2019年12月合肥市第一人民醫(yī)院血液腫瘤科符合PICC置管條件的血液腫瘤患者75例,按隨機(jī)數(shù)字表法分為A、B、C三組,各25例。納入標(biāo)準(zhǔn):①所有患者年齡在18周歲以上,能正常交流并配合研究;②患者均符合PICC置管適應(yīng)證[5],且是首次置管,置管后一周內(nèi)均在本病區(qū)進(jìn)行導(dǎo)管維護(hù);③患者知情同意并簽署同意書。排除標(biāo)準(zhǔn):①凝血功能異常者;②穿刺部位皮膚有瘢痕或破潰者;③有心臟支架或起搏器者。3組患者年齡、性別、疾病種類及穿刺靜脈比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。見表1。

表1 3組患者一般資料比較
1.2 方法 所有患者均采用4Fr三向瓣膜式單腔PICC管(美國巴德公司生產(chǎn)),SiteRite5超聲儀、MST微插管鞘套件、PICC置管專用穿刺包、巴德導(dǎo)引穿刺套件,寶萊特心電監(jiān)護(hù)。三組超聲引導(dǎo)下PICC操作均由2名具有PICC置管資質(zhì)并成功置管200例以上的護(hù)士完成,且由同一名固定的助手(具有臨床工作經(jīng)驗(yàn)12年、取得院級維護(hù)資質(zhì)護(hù)士)負(fù)責(zé)PICC患者的臨床觀察及記錄。 PICC按照美國輸液護(hù)士協(xié)會2016版《輸液治療實(shí)踐標(biāo)準(zhǔn)》[6]及我國2013版《輸液治療護(hù)理實(shí)踐指南與實(shí)施細(xì)則》[7]制定的超聲引導(dǎo)下結(jié)合塞丁格技術(shù)行PICC置管流程進(jìn)行,置管部位均為肘上,血管盡量選擇貴要靜脈。穿刺前測量時均采用“一字法”確定患者導(dǎo)管長度[8]。
1.2.1 A組 置管中采用可撕裂外鞘與擴(kuò)張器組件直接擴(kuò)張穿刺點(diǎn)后送鞘鈍性分離。操作:①確定穿刺針進(jìn)入血管后,立即將導(dǎo)絲沿穿刺針?biāo)腿胙埽w外保留10 cm以上;②擴(kuò)張穿刺點(diǎn)前,分離血管鞘的擴(kuò)張器和可撕裂外鞘,先將擴(kuò)張器沿導(dǎo)絲左右旋轉(zhuǎn)并推進(jìn)血管擴(kuò)張穿刺點(diǎn),見回血后立即取出擴(kuò)張器并用生理鹽水沖凈其血液后套上可撕裂外鞘,沿導(dǎo)絲左右旋轉(zhuǎn)再次推進(jìn)血管,同時撤出導(dǎo)絲及擴(kuò)張器后送入導(dǎo)管至預(yù)測長度[4,9];③腔內(nèi)心電圖確認(rèn)導(dǎo)管位置、修剪導(dǎo)管并安裝減壓套管及無針接頭、固定導(dǎo)管、X線定位。
1.2.2 B組 置管中采用盲穿針外鞘與擴(kuò)張器組裝擴(kuò)張穿刺點(diǎn)后送鞘的鈍性分離法。操作:①同A組;②擴(kuò)張穿刺點(diǎn)前,分離血管鞘的擴(kuò)張器和可撕裂外鞘,分離PICC導(dǎo)管套裝內(nèi)的盲穿針針芯和外鞘,把擴(kuò)張器放入盲穿針的外鞘內(nèi),后沿導(dǎo)絲左右旋轉(zhuǎn)并推進(jìn)血管擴(kuò)張穿刺點(diǎn),待見回血并且盲穿針的外鞘前端全部沒入皮下后,同時撤出導(dǎo)絲及擴(kuò)張器后送入導(dǎo)管至預(yù)測長度;③同A組。
1.2.3 C組 置管中采用改良擴(kuò)皮送鞘法,即采用盲穿針外鞘、擴(kuò)張器與可撕裂外鞘組件擴(kuò)張穿刺點(diǎn)后送鞘的鈍性分離。操作:①同A組;②擴(kuò)張穿刺點(diǎn)前,分離血管鞘的擴(kuò)張器和可撕裂外鞘,分離PICC導(dǎo)管套裝內(nèi)的盲穿針針芯和外鞘,把擴(kuò)張器放入盲穿針的外鞘內(nèi),后沿導(dǎo)絲左右旋轉(zhuǎn)并推進(jìn)血管擴(kuò)張穿刺點(diǎn),待見回血后即刻取出盲穿針外鞘和擴(kuò)張器,分離擴(kuò)張器和盲穿針的外鞘,用生理鹽水沖凈擴(kuò)張器血液后套上可撕裂外鞘,沿導(dǎo)絲左右旋轉(zhuǎn)再次推進(jìn)血管,同時撤出導(dǎo)絲及擴(kuò)張器后送入導(dǎo)管至預(yù)測長度;③同A組。上述3種鈍性分離擴(kuò)皮不成功者,均再次采用手術(shù)刀擴(kuò)皮。

1.3 統(tǒng)計(jì)學(xué)方法 采用SPSS 23.0進(jìn)行統(tǒng)計(jì)分析,偏態(tài)分布計(jì)量資料以M(P25,P75)表示,采用非參數(shù)H檢驗(yàn);計(jì)數(shù)資料以例數(shù)或百分比表示,采用χ2檢驗(yàn)或秩和檢驗(yàn),以P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 3組一次性擴(kuò)皮成功率和送鞘成功率比較 B組和C組一次性擴(kuò)皮成功率均為100%,A組一次性擴(kuò)皮成功率為80%(20/25),差異有統(tǒng)計(jì)學(xué)意義(P=0.009)。A組和C組一次性送鞘成功率均為100%,B組一次性送鞘成功率為92%(23/25),但差異無統(tǒng)計(jì)學(xué)意義(P=0.324)。
2.2 3組擴(kuò)皮后即刻出血量、擴(kuò)皮后24 h出血量比較 擴(kuò)皮后B組即刻小量出血率為86.9%,高于A組的60.0%、C組的48.0%,B組擴(kuò)皮后24 h穿刺點(diǎn)小量出血率91.3%,高于A組的70.0%、、C組的52.0%,A、B、C三組間即刻及24 h出血量差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表2。其中,B組即刻(P<0.01)及24 h出血量(P<0.05)相比C組差異有統(tǒng)計(jì)學(xué)意義,A組與B組、A組與C組的即刻、24 h出血量未見統(tǒng)計(jì)學(xué)差異(P>0.05)。

表2 3組穿刺點(diǎn)出血量比較[例(%)]
2.3 3組置管后7天維護(hù)次數(shù)和穿刺點(diǎn)感染情況比較 3組置管后7天維護(hù)次數(shù)、穿刺點(diǎn)感染次數(shù)比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。見表3。3組置管后均未發(fā)生穿刺點(diǎn)滲液。
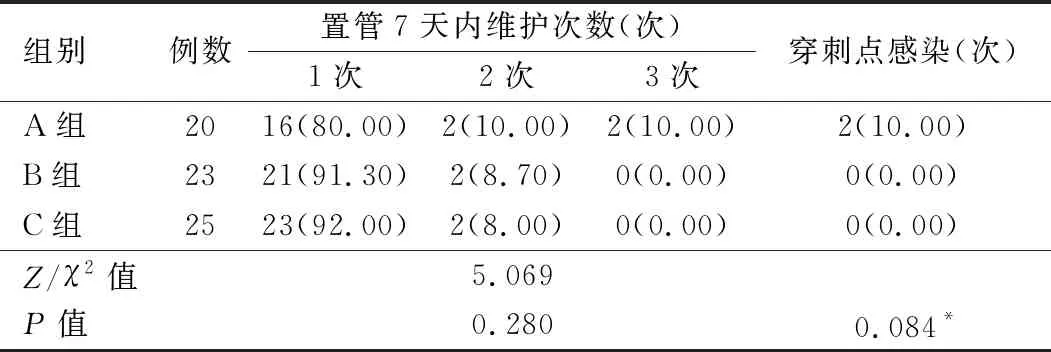
表3 3組置管后7天維護(hù)及穿刺點(diǎn)感染情況比較[例(%)]
3 討論
3.1 改良擴(kuò)皮送鞘法一次性擴(kuò)皮成功率及一次性送鞘成功率較高 本研究中,C組改良擴(kuò)皮送鞘法的一次性擴(kuò)皮成功率明顯高于A組(P<0.05)。可能是由于在改良擴(kuò)皮送鞘法中盲穿針外鞘管壁較薄,與擴(kuò)張器的貼合度高,鞘前端與鞘身過渡段約2 mm ,在推進(jìn)過程中可減小皮膚阻力[11],降低了患者疼痛,從而提高了一次性擴(kuò)皮成功率。而A組擴(kuò)皮時會因?yàn)榛颊咂つw緊致,皮下組織厚,需要用很大的力氣推進(jìn)擴(kuò)張器,造成患者疼痛致擴(kuò)皮失敗,不得不再次用手術(shù)刀進(jìn)行擴(kuò)皮,這已經(jīng)被多個研究者[4,12]證實(shí)。
在本研究中,改良擴(kuò)皮送鞘組和A組的一次性送鞘成功率均為100%,高于B組,但差異無統(tǒng)計(jì)學(xué)意義(P>0.05),而有臨床研究[11]表示,采用盲穿針外鞘與擴(kuò)張器組裝鈍性分離比可撕裂外鞘與擴(kuò)張器組裝鈍性分離一次性送鞘成功率高。這可能與B組中一次性送鞘失敗的2例患者均肥胖,皮下脂肪厚有關(guān)。由于肥胖或血管過深的患者,血管深度超過3.2 cm,鞘前端與鞘身過渡段約2 mm,盲穿針外鞘未能穿透血管,退出內(nèi)部擴(kuò)張器后,導(dǎo)致送鞘失敗[11]。另外因本研究中每組樣本量較少,無法凸顯出改良擴(kuò)皮送鞘法在一次性送鞘成功率方面的優(yōu)勢。
3.2 改良擴(kuò)皮送鞘法在出血量及7天內(nèi)維護(hù)次數(shù)等方面無明顯優(yōu)勢 本組資料顯示,B組的穿刺點(diǎn)即刻出血量及24 h出血量均比A組和C組明顯減少(P<0.05),表明改良擴(kuò)皮送鞘方法在超聲引導(dǎo)下PICC不能夠降低即刻出血量和24 h出血量。采用改良擴(kuò)皮送鞘法時,C組中的可撕裂鞘長度較B組中的盲穿針長,進(jìn)入血管的部分亦長,對血管的損傷較大從而引起出血量增加,這已被研究[11]證實(shí)。同時,由于可撕裂鞘比盲穿針外鞘硬,在送入時對血管的摩擦力比較大,對血管的損傷程度較盲穿針大,因此出血量比較多。另外改良法擴(kuò)皮時需兩次擴(kuò)張穿刺點(diǎn),對皮下組織及血管產(chǎn)生2次創(chuàng)傷,故在擴(kuò)皮后即刻出血量和術(shù)后24 h穿刺點(diǎn)出血量上會明顯增多[12]。C組在7天內(nèi)維護(hù)次數(shù)方面無明顯優(yōu)勢可能與出血量有關(guān),出血量直接影響7天內(nèi)維護(hù)次數(shù)。
綜上所述,在PICC置管前通過B超檢查患者判斷血管深度,若患者血管深度≤3 cm,宜采取B組的鈍性分離方法;若患者血管深度>3 cm,則可采取改良擴(kuò)皮送鞘鈍性分離的方法以提高一次性擴(kuò)皮成功率,筆者認(rèn)為如果采用改良擴(kuò)皮送鞘法時可以在預(yù)防出血方面加強(qiáng)護(hù)理,比如使用藻酸鹽敷料、局部加壓包扎等,也可采用王佳等[13]的準(zhǔn)確送入導(dǎo)管鞘長度來減少出血。在日常PICC置入中,結(jié)合B超評估血管,根據(jù)血管的深度靈活選用合適的鈍性分離方法,針對肥胖、血管深度>3 cm的患者,采用改良擴(kuò)皮送鞘法在保證高置管成功率的同時,可減少PICC置入相關(guān)并發(fā)癥的發(fā)生,提高一次性擴(kuò)皮成功率,這一改良方法值得臨床推廣應(yīng)用。

