43例吡咯生物堿相關(guān)肝竇阻塞綜合征臨床特征及預(yù)后分析
徐 楠 李 江 謝琴秀
肝竇阻塞綜合征(hepatic sinusoidal obstruction syndrome,HSOS)是由各種原因?qū)е赂胃]內(nèi)皮細胞損傷,紅細胞滲入肝竇內(nèi),導(dǎo)致肝竇阻塞進而使門靜脈壓力增高的一種肝臟血管性疾病,既往又被稱為肝小靜脈閉塞病(hepatic veno-occlusive disease,HVOD)。我國病因以服用含吡咯生物堿(pyrrolidine alkaloid,PA)的中草藥為主[1-3],如“土三七”等,稱為吡咯生物堿相關(guān)肝竇阻塞綜合征(pyrrolidine alkaloid-related hepatic sinusoidal obstruction syndrome,PA-HSOS)。該病表現(xiàn)為腹脹、腹痛、肝大、腹水等,與其它病因?qū)е碌募甭愿窝住⒏斡不Т鷥斊谂R床表現(xiàn)類似,易導(dǎo)致誤診、漏診,報道病死率高達20%~70%[4-5]。本研究回顧性分析43例PA-HSOS患者的臨床資料,總結(jié)臨床特征,評估不同治療方案的療效,為臨床診治提供參考。
1 資料與方法
1.1 一般資料 回顧性分析2015年1月至2019年2月安徽醫(yī)科大學(xué)第一附屬醫(yī)院收治的PA-HSOS患者臨床資料。所有患者診斷均符合PA-HSOS診斷和治療專家共識意見(2017年南京)[6]:有明確服用PA中草藥史,排除其它已知病因所致的肝損傷,且有以下3項臨床表現(xiàn),①腹脹和/或肝區(qū)疼痛、肝大和腹水;②血清總膽紅素升高或其它肝功能異常;③有典型的影像學(xué)或肝臟病理表現(xiàn)。本研究通過安徽醫(yī)科大學(xué)第一附屬醫(yī)院倫理委員會審核批準(zhǔn),所有患者各項侵入性操作前均簽署知情同意書。
1.2 資料收集 記錄并分析納入患者的基本資料、臨床表現(xiàn)、實驗室及影像學(xué)檢查結(jié)果、病理結(jié)果、治療方案及預(yù)后。出院后每半年對患者進行門診或電話隨訪,隨訪終點為死亡或由內(nèi)科保守治療轉(zhuǎn)換為肝移植、經(jīng)頸靜脈肝內(nèi)門體靜脈內(nèi)支架分流(transjugular intrahepatic portosystemic shunt,TIPS)術(shù),或為出院后第365天。根據(jù)隨訪終點時預(yù)后,將所有患者分為死亡組及改善組。根據(jù)有無使用抗凝劑,分為抗凝組及非抗凝組。
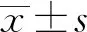
2 結(jié)果
2.1 基本情況 43例PA-HSOS患者,女性14例,男性29例,年齡33~77歲,平均(59.2±10.6)歲。所有患者發(fā)病前均有服用“土三七”病史,服藥時間為3 d~3年,其中1例為間斷服藥(共服藥5次,每次10 d,最后一次為服藥前3個月),所有患者病程為0.1~13個月。服藥方式以泡水、泡酒為主,分別為24例、17例,有2例患者服用“土三七”粉末。至隨訪終點,死亡15例,占34.9%,28例患者病情改善。
2.2 臨床表現(xiàn) 腹脹是最常見的癥狀(93.0%, 40/43例),部分患者有腹痛(32.6%, 14/43例)、肝大(25.6%, 11/43例),12例有雙下肢水腫,15例出現(xiàn)黃疸,其它癥狀還包括乏力、納差、惡心、嘔吐等非特異表現(xiàn),所有患者均無發(fā)熱。
2.3 實驗室檢查特點 43例患者均有不同程度的肝損害,以谷氨酸氨基轉(zhuǎn)移酶(alanine aminotransferase, ALT)、天門冬氨酸氨基轉(zhuǎn)移酶(aspartate aminotransferase,AST)、堿性磷酸酶(alkaline phosphatase,ALP)、γ-谷氨酰轉(zhuǎn)肽酶(γ-glutamyl transpeptidase, GGT)升高為主,31例患者ALT、AST小于5倍正常值上限(upper limit of normal , ULN),16例患者總膽紅素(total bilirubin, TB)水平在1~2倍ULN,88.4%(38/43例)的患者總膽紅素小于5倍ULN,最高達428.31 μmol/L。36例(83.7%)患者出現(xiàn)凝血功能異常,凝血酶原活動度(prothrombin time activity, PTA)為(59.48±16.61%),國際標(biāo)準(zhǔn)化比值(international normalized ratio,INR)為1.40(1.22, 1.62)。有6例患者癌胚抗原(carcinoembryonic antigen,CEA)升高、8例甲胎蛋白(alpha-fetoprotein,AFP)升高,41例患者糖類抗原125(Carbohydrate antigen125,CA125)升高明顯。圖1顯示INR、TB、ALT、CA125各指標(biāo)不同范圍的分布。死亡組與改善組各實驗室指標(biāo)差異無統(tǒng)計學(xué)意義(P>0.05),見表1。
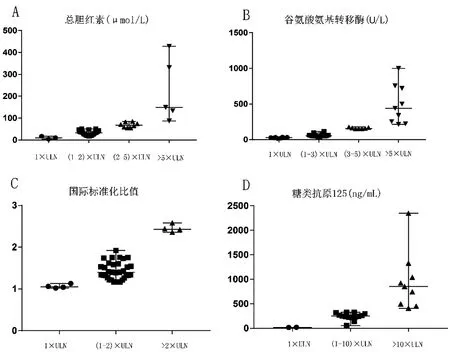
圖1 重要實驗室指標(biāo)在不同范圍的分布圖

表1 不同預(yù)后患者實驗室檢查結(jié)果比較
2.4 影像學(xué)特點 35例患者影像學(xué)存在彌漫性肝臟病變,23例肝腫大,6例脾腫大,34例存在不同程度的腹水,44.2%(19/43例)的患者動脈期、門靜脈期及延遲期可見肝實質(zhì)強化不均,呈地圖樣或斑片狀強化,48.8%(21/43例)的患者有下腔靜脈狹窄,62.8%的患者肝靜脈顯示不清。典型PA-HSOS肝臟增強CT及MRI的特點見圖2。
2.5 胃鏡及病理學(xué)檢查特點 10例患者行胃鏡檢查,3例存在輕-中度食管胃底靜脈曲張,1例門脈高壓性胃病。6例患者行肝穿刺活組織檢查,病理損傷以肝腺泡Ⅲ區(qū)為重,表現(xiàn)為肝竇內(nèi)皮細胞腫脹、損傷、脫落,肝血竇內(nèi)擴張淤血,肝內(nèi)小靜脈管腔狹窄甚至閉塞,炎性細胞浸潤不明顯,匯管區(qū)無纖維化或僅輕度纖維增生,見圖3。

圖2 典型PA-HSOS患者的CT及MRI表現(xiàn)

圖3 典型PA-HSOS患者肝臟病理表現(xiàn)(HE×100)
2.6 治療及預(yù)后 43例患者均接受了內(nèi)科治療,包括補充白蛋白、保肝、降酶、退黃、改善微循環(huán)、利尿等。根據(jù)有無使用抗凝劑,將患者分為抗凝治療組及非抗凝治療組,非抗凝組的隨訪時間為230 d (41 d,365 d),抗凝組隨訪時間為282 d(151 d,365 d)。對于內(nèi)科保守治療不佳,出現(xiàn)頑固性腹水或肝衰竭的患者,有轉(zhuǎn)換治療方案的指征,根據(jù)病情、相關(guān)科室會診意見等,選擇TIPS術(shù)或肝移植術(shù)。
24例患者接受抗凝治療,為低分子肝素鈉或華法林,其中70.8%(17/24例)的患者癥狀緩解、病情好轉(zhuǎn),7例患者癥狀加重,其中2例患者死亡,5例接受外科干預(yù),包括4例TIPS術(shù),1例肝移植術(shù),術(shù)后病情好轉(zhuǎn)。抗凝序貫手術(shù)治療的緩解率達91.7%(22/24例)。19例患者未接受抗凝治療,57.9%(11/19例)的患者癥狀緩解,8例病情加重,其中7例死亡,1例行TIPS術(shù)后好轉(zhuǎn)。使用Kaplan-Meier方法計算抗凝序貫外科治療組及非抗凝組患者累積生存率,圖4可見隨著隨訪時間延長,抗凝序貫外科治療組的生存率高于非抗凝組,差異有統(tǒng)計學(xué)意義(P= 0.021)。

圖4 PA-HSOS患者不同治療方案的生存曲線圖
注:隨著隨訪時間延長,抗凝序貫外科治療組的生存率顯著高于非抗凝組
3 討論
引起HSOS的病因有:服用含PA的中草藥、骨髓造血干細胞移植術(shù)(hematopoietic stem cell transplantation, HSCT)、實體腫瘤化療藥物以及肝移植術(shù)后免疫抑制劑[7-9]。PA進入人體后經(jīng)細胞色素酶P450(cytochrome P450,CYP450)的催化,生成中間代謝產(chǎn)物,與蛋白結(jié)合形成有肝毒性的吡咯蛋白結(jié)合物(pyrrole protein adducts,PPAs),造成肝竇內(nèi)皮損傷[10-11]。民間所稱的“土三七”是多種植物的統(tǒng)稱,通常認(rèn)為導(dǎo)致PA-HSOS的是菊三七,因具有活血化瘀、消腫止痛的功效,常被用于治療關(guān)節(jié)疼痛、高血壓等。本研究患者發(fā)病前均有服用“土三七”的病史,服用方式以泡水、泡酒為主。除此之外一些中藥成方制劑也含有PA,如千柏鼻炎片、川貝雪梨膏、橘紅顆粒、小兒肺熱平膠囊、紫草軟膏、花紅顆粒、小兒寶泰康顆粒等,甚至常見食物如茶葉、野生蜜源植物的蜂蜜也含有PA[12-14]。盡管上述中藥成方制劑PA含量較低,但患者特別是嬰幼兒若長期攝入,則可能導(dǎo)致PA蓄積風(fēng)險。因此,應(yīng)加強科普教育,避免藥物、保健品濫用,盡量減少PA-HSOS的發(fā)生。
本研究中所有患者均存在肝功能損害,但72.1%的患者轉(zhuǎn)氨酶小于5 ULN,88.4%患者總膽紅素僅輕-中度升高,提示PA-HSOS患者肝功能損害并不重。83.7%(36/43例)的患者PT延長,提示凝血功能受損,這導(dǎo)致抗凝劑使用存在風(fēng)險,可能會延誤治療時機。本研究絕大部分患者存在CA125的異常升高,該指標(biāo)是跨膜黏蛋白16(mucin 16,MUC16) 的胞外片段,生理狀態(tài)下可在腹膜和女性生殖系統(tǒng)等多種組織中表達,臨床上多作為婦科腫瘤標(biāo)志物。有研究[15]表明,CA125可作為肝硬化腹水的標(biāo)志物,并可用于預(yù)測腹水的轉(zhuǎn)歸。本研究患者CA125升高原因可能為大量腹水導(dǎo)致腹膜微循環(huán)障礙,腹膜上皮細胞表面脫落的CA125被吸收進入血液循環(huán),導(dǎo)致血CA125升高。該指標(biāo)異常升高可能會導(dǎo)致PA-HSOS誤診為惡性腫瘤、肝硬化等。影像學(xué)提示超過一半患者存在肝腫大、腹水,44.2%(19/43例)患者肝臟CT或MRI增強呈不均勻強化,病變范圍與預(yù)后不良呈正相關(guān)[16],48.8%患者有下腔靜脈狹窄,可能為腫大的肝臟壓迫了下腔靜脈近肝段。與肝硬化門靜脈高壓不同,PA-HSOS患者并沒有顯著的胃食管靜脈曲張或脾腫大,這可能與門脈高壓進展較快,側(cè)支循環(huán)未及代償有關(guān)。
除了保肝及對癥支持治療外,HSOS最主要的治療在于抗凝和抗血栓形成。盡管肝素、低分子肝素等具有很強的抗凝作用,但對HSCT-HSOS患者并沒有明顯的治療作用[17]。本研究的24例患者接受了低分子肝素和/或華法林的抗凝治療,緩解率達到70.8%,高于非抗凝組的57.9%。抗凝組內(nèi)科治療未緩解的患者,在序貫外科治療后,預(yù)后進一步改善。7例抗凝組未緩解的患者4例進行了TIPS術(shù),1例進行肝移植,病情均得到控制,抗凝序貫外科干預(yù)使得治療緩解率達到了91.7%(22/24例)。抗凝序貫外科治療對PA-HSOS的療效可能因為這部分患者沒有嚴(yán)重的基礎(chǔ)疾病,肝功能損害較輕,而HSCT-HSOS患者存在白血病等血液系統(tǒng)腫瘤,移植后機體免疫力低下,不能耐受手術(shù)治療。
本研究是回顧性,且患者數(shù)量較少,結(jié)果存在一定的局限性。PA-HSOS作為特殊的藥物性肝損害,需要通過增加科普教育,盡量減少該病的發(fā)生,臨床醫(yī)生需要加強對該病的認(rèn)識,仔細詢問病史,盡早做出正確診斷,選擇合適的治療時機及方案,抗凝序貫外科治療可以顯著改善PA-HSOS患者預(yù)后。

