高壓脈沖電場(chǎng)輔助提取紫薯酒渣花色苷
馬懿 ,陳曉姣,古麗珍,包文川
1.四川輕化工大學(xué)生物工程學(xué)院(自貢 643000);2.固態(tài)發(fā)酵資源利用四川省重點(diǎn)實(shí)驗(yàn)室(宜賓 644000)
花色苷屬于天然的水溶性色素,其廣泛存在于水果、蔬菜等植物中,具有抗氧化、抗癌、抗心血管疾病等諸多生物學(xué)活性[1-3]。因此,花色苷資源的開(kāi)發(fā)利用具有重要的科學(xué)價(jià)值。紫薯作為一類重要谷物和食品加工材料,富含大量花色苷等營(yíng)養(yǎng)成分。Clifford[4]研究發(fā)現(xiàn)紫薯花色苷含量明顯高于黑米、藍(lán)莓、草莓、紫甘藍(lán)、葡萄皮。相關(guān)研究還發(fā)現(xiàn),利用紫薯為主要原料生產(chǎn)的紫薯酒具有比葡萄酒更高的抗氧化活性[5]。這對(duì)于加速紫薯產(chǎn)業(yè)的發(fā)展奠定較好的理論基礎(chǔ)。紫薯酒在日本成為暢銷產(chǎn)品[6]。然而,以紫薯為原料生產(chǎn)紫薯酒過(guò)程中必然產(chǎn)生大量富含花色苷的紫薯酒渣副產(chǎn)物。這些副產(chǎn)物僅被用于飼料喂養(yǎng)或植物肥料,利用率較低,經(jīng)濟(jì)價(jià)值不高。因此,將紫薯酒渣進(jìn)行資源的循環(huán)利用,可有效增加其附加值,具有重要的經(jīng)濟(jì)價(jià)值和社會(huì)效應(yīng)。
高壓脈沖電場(chǎng)輔助提取作為一種非熱的提取技術(shù)[7-8],對(duì)于提取花色苷等穩(wěn)定性差的天然產(chǎn)物具有重要作用,這可能與細(xì)胞壁的破壞,通透性的改變有關(guān)。該方法能有效降低活性物質(zhì)的損失,具有操作簡(jiǎn)單、耗時(shí)短的優(yōu)點(diǎn)[9],被廣泛應(yīng)用于活性物質(zhì)提取,但國(guó)內(nèi)外直接利用紫薯發(fā)酵酒副產(chǎn)物,提取花色苷的研究還鮮有報(bào)道。
因此,試驗(yàn)以紫薯酒渣為研究對(duì)象,通過(guò)高壓脈沖電場(chǎng)輔助提取紫薯酒發(fā)酵副產(chǎn)物中花色苷,并通過(guò)響應(yīng)面設(shè)計(jì)優(yōu)化提取工藝,對(duì)于紫薯的深加工和資源利用具有重要應(yīng)用價(jià)值。
1 材料與方法
1.1 材料與儀器
紫薯酒渣(實(shí)驗(yàn)室自制);矢車菊素-3-葡萄糖苷標(biāo)準(zhǔn)品(純度≥98%,南京景竹生物有限公司);無(wú)水乙醇、鹽酸(均為分析純,成都科龍?jiān)噭┯邢薰荆?/p>
UV-Vis光度計(jì)(北京普析);精密pH計(jì)FE20型(瑞士Mettler-Toledo公司);電子天平(瑞士Mettler-Toledo公司);Milli-Qadvantage超純水系統(tǒng)(德國(guó)Millpore公司);高壓脈沖電場(chǎng)提取裝置[10](實(shí)驗(yàn)室自制)。
1.2 試驗(yàn)方法
1.2.1 花色苷相對(duì)含量的測(cè)定
pH示差法能簡(jiǎn)便、快速的進(jìn)行花色苷含量測(cè)定[11-12]。其計(jì)算方法如下:
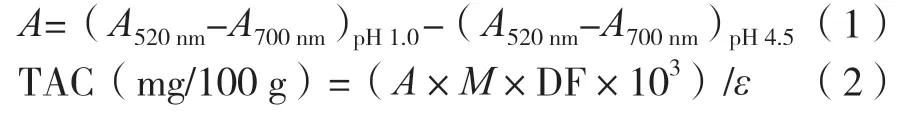
式中:M為矢車菊素-3-葡萄糖苷的摩爾質(zhì)量,449.2 mg/mol;DF為稀釋倍數(shù);ε為摩爾吸光系數(shù),26 900。
1.2.2 花色苷提取方法
在室溫條件下,利用體積分?jǐn)?shù)60%酸性乙醇(pH 3.5),以不同液料比值,通過(guò)高壓脈沖電場(chǎng)輔助提取紫薯酒渣中的花色苷。考察電場(chǎng)強(qiáng)度、脈沖數(shù)及液料比值等3個(gè)因素對(duì)花色苷提取率的影響。試驗(yàn)選擇的電場(chǎng)強(qiáng)度為5,10,15,20和25 kV/cm;脈沖數(shù)為4,6,8,10和12;液料比值為5,10,20,30和40(mL/g)。
1.2.3 響應(yīng)面試驗(yàn)優(yōu)化
根據(jù)單因素試驗(yàn)結(jié)果,以液料比值、脈沖數(shù)以及電場(chǎng)強(qiáng)度等3個(gè)因素為變量,以紫薯酒渣花色苷含量為響應(yīng)值,使用Design-Expert優(yōu)化高壓脈沖電場(chǎng)提取工藝。響應(yīng)面設(shè)計(jì)如表1所示。
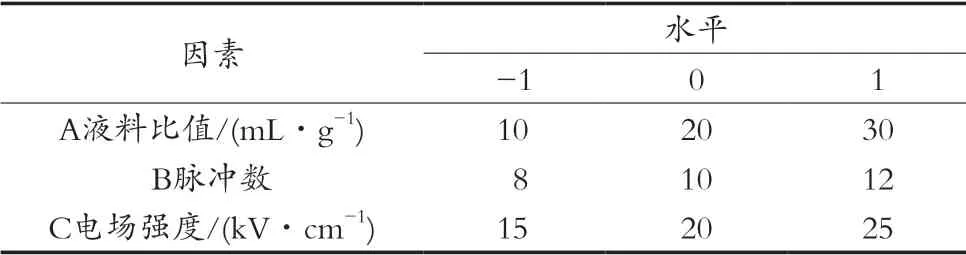
表1 響應(yīng)面試驗(yàn)因素水平表
1.2.4 DPPH自由基清除能力試驗(yàn)
根據(jù)Kahkonen[13]的自由基清除能力試驗(yàn)設(shè)計(jì)方法,測(cè)定VC、紫薯花色苷和紫薯酒渣花色苷清除DPPH自由基的能力。分別將2 mL樣品溶液(0.625~1 mg/mL)分別與2 mL 0.2 mmol/L DPPH乙醇溶液或2 mL蒸餾水混合均勻,避光靜置1 h,測(cè)定其在最大吸收時(shí)的吸光度As和Ab;再將2 mL DPPH乙醇溶液與2 mL蒸餾水混勻,以相同方法測(cè)定Ac。DPPH自由基清除能力根據(jù)如式(3)計(jì)算。
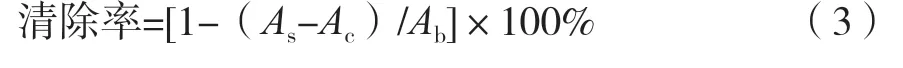
2 結(jié)果與討論
2.1 紫薯酒渣花色苷提取的單因素試驗(yàn)
2.1.1 電場(chǎng)強(qiáng)度對(duì)提取效果的影響
電場(chǎng)強(qiáng)度對(duì)紫薯酒渣花色苷提取效果的影響如圖1所示。隨著電場(chǎng)強(qiáng)度加強(qiáng),紫薯酒渣花色苷含量逐漸增大,電場(chǎng)強(qiáng)度為20 kV/cm時(shí),花色苷的提取效果最好,花色苷含量達(dá)到62.1 mg/100 g。這可能是由于較大電場(chǎng)強(qiáng)度導(dǎo)致細(xì)胞壁迅速受損,加速花色苷的溶出。然而,當(dāng)電場(chǎng)強(qiáng)度繼續(xù)增大時(shí),過(guò)大的電場(chǎng)強(qiáng)度可能破壞花色苷分子結(jié)構(gòu),影響其穩(wěn)定性,從而導(dǎo)致花色苷的提取效果呈現(xiàn)下降趨勢(shì)。
2.1.2 液料比值對(duì)花色苷提取影響
不同液料比值對(duì)紫薯酒渣花色苷提取效果的影響如圖1所示。液料比值低于20(mL/g)時(shí),花色苷的提取效果隨著提取液量的增加而增加,而液料比值超過(guò)20(mL/g)時(shí),花色苷提取率顯著降低。由此可見(jiàn),液料比值為20(mL/g)時(shí),提取效果較好。這可能是由于溶液中花色苷含量飽和,而液料比值超過(guò)臨界值后,花色苷溶解在溶液中較多,花色苷濃度降低。
2.1.3 脈沖數(shù)對(duì)花色苷提取影響
脈沖數(shù)對(duì)紫薯酒渣花色苷提取效果的影響如圖1所示。隨著脈沖數(shù)增加,紫薯酒渣花色苷的提取效果逐漸增加,脈沖數(shù)10時(shí),花色苷的含量達(dá)到62.4 mg/100 mg,這可能與電子脈沖促進(jìn)細(xì)胞壁加速破壞有關(guān)。脈沖數(shù)直接影響高壓脈沖電場(chǎng)的作用時(shí)間,當(dāng)作用時(shí)間在一定的范圍內(nèi)持續(xù)增加時(shí),有助于花色苷的提取。
2.2 回歸模型的建立與分析
通過(guò)單因素試驗(yàn),以液料比值(A)、脈沖數(shù)(B)和電場(chǎng)強(qiáng)度(C)等3個(gè)因素為自變量,花色苷含量為響應(yīng)值,利用Design-Expert軟件,根據(jù)Box-Behnken模型進(jìn)行響應(yīng)面試驗(yàn)優(yōu)化設(shè)計(jì),試驗(yàn)設(shè)計(jì)及結(jié)果如表2所示。
表3為紫薯酒渣花色苷含量的方差分析結(jié)果。建立的回歸方程為:Y=63.1+1.84A+1.21B+1.85C+1.7AB-0.73AC-0.28BC-6.28A2-0.97B2-2.8C2。
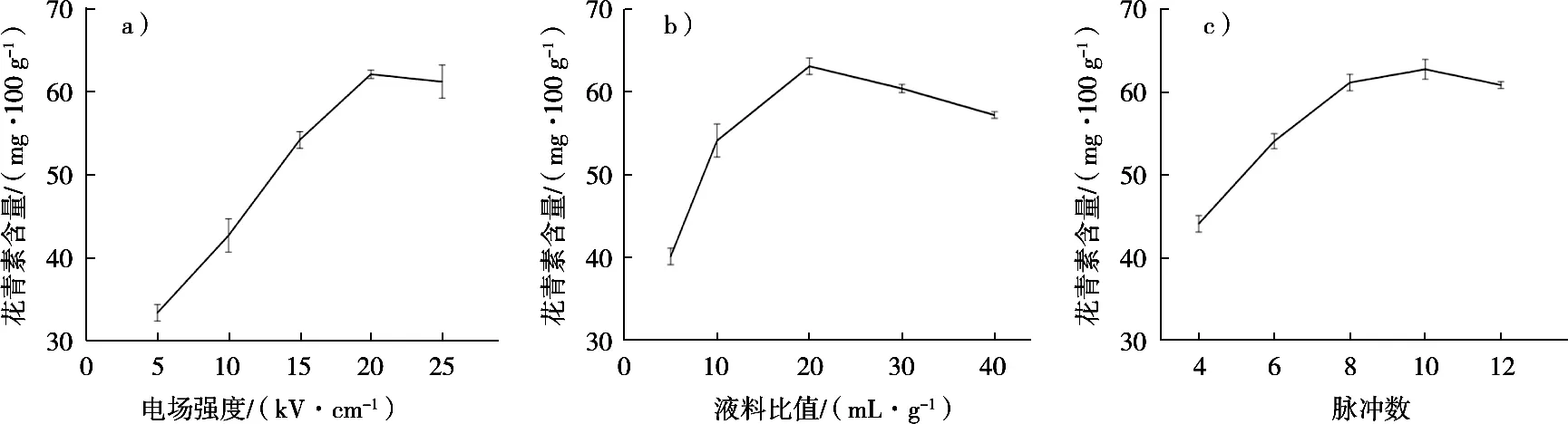
圖1 單因素對(duì)紫薯酒渣花色苷提取率的影響
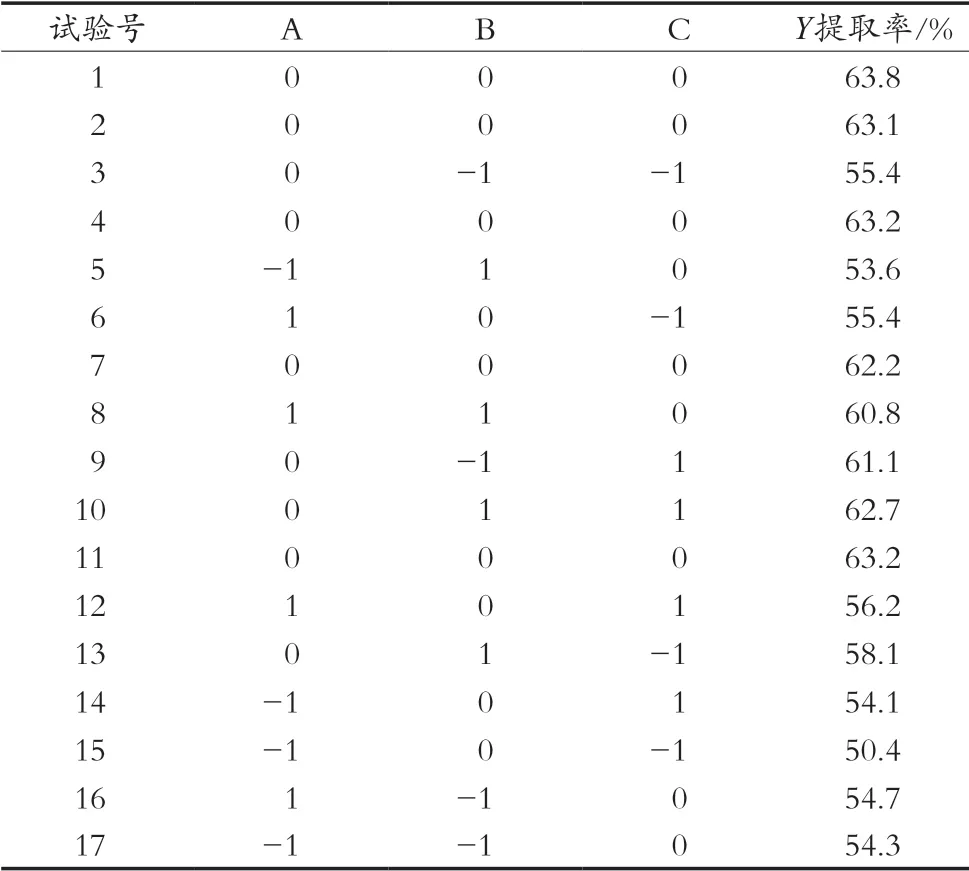
表2 Box-Behnken試驗(yàn)設(shè)計(jì)及結(jié)果
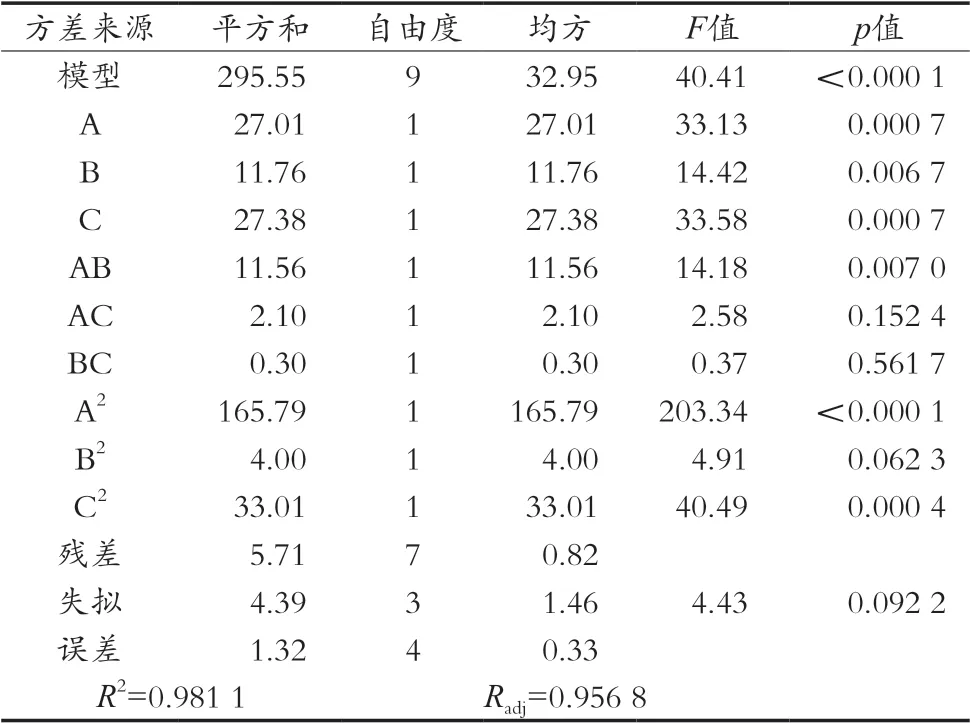
表3 方差分析表
該數(shù)學(xué)模型達(dá)到極顯著水平(p<0.001),而失擬項(xiàng)不顯著(p=0.092 2>0.05),說(shuō)明模型的擬合度高,可用于預(yù)測(cè)紫薯酒渣花色苷的含量。回歸方程的相關(guān)系數(shù)(R2)為0.981 1,說(shuō)明各變量與響應(yīng)值的相關(guān)性顯著。3個(gè)因素對(duì)紫薯酒渣花色苷含量的影響極顯著(p<0.01),影響順序?yàn)殡妶?chǎng)強(qiáng)度>液料比值>脈沖數(shù)。各因素的二次項(xiàng)及其交互作用對(duì)花色苷含量的影響達(dá)到顯著水平。
2.3 交互作用分析
因素交互作用的三維響應(yīng)面圖如圖2所示。響應(yīng)面表示在一個(gè)自變量為零水平時(shí),另外兩自變量交互作用對(duì)紫薯酒渣花色苷含量的影響情況。如圖2所示,液料比值20(mL/g),隨著脈沖數(shù)和電場(chǎng)強(qiáng)度增加,花色苷加速?gòu)淖鲜砭圃腥艹觯妶?chǎng)強(qiáng)度超過(guò)20 kV后,提取的花色苷含量出現(xiàn)下降趨勢(shì),這可能與過(guò)大電場(chǎng)強(qiáng)度破壞花色苷穩(wěn)定性有關(guān)[14]。由圖2可見(jiàn),盡管隨著電場(chǎng)強(qiáng)度增加,紫薯酒渣花色苷的含量先增加,之后稍微減少,但其交互作用應(yīng)主要?dú)w功于液料比值的增加[15-16]。這可能是由于提取溶劑的增加,增強(qiáng)導(dǎo)電性,從而加速物質(zhì)的溶出。由圖2可見(jiàn),紫薯酒渣花色苷的提取率受液料比值和脈沖數(shù)的交互作用影響較為明顯。
根據(jù)預(yù)測(cè)分析,響應(yīng)面的最優(yōu)條件為:液料比值21(mL/g)、電場(chǎng)強(qiáng)度18.3 kV/cm、脈沖數(shù)9.3。此時(shí)預(yù)測(cè)響應(yīng)值為64.02 mg/100 g。在該條件下,紫薯酒渣花色苷的提取含量為63.9 mg/100 g,與理論預(yù)測(cè)值接近,表明響應(yīng)面優(yōu)化模型可用于確定最佳工藝條件。
2.4 紫薯酒渣花色苷清除DPPH能力
圖3展示紫薯酒渣花色苷和紫薯花色苷的DPPH自由基清除能力,并用VC的測(cè)定結(jié)果作為對(duì)照。紫薯花色苷質(zhì)量濃度為1 mg/mL時(shí),清除DPPH能力達(dá)到90.1%。紫薯酒渣花色苷清除DPPH能力也呈現(xiàn)出相似趨勢(shì),隨著紫薯酒渣花色苷濃度增加,其抗氧化能力迅速增加,質(zhì)量濃度達(dá)到1 mg/mL時(shí),其對(duì)DPPH的清除率可達(dá)81.9%。盡管紫薯酒渣花色苷清除DPPH能力弱于紫薯花色苷,但其與VC的DPPH清除能力相近,說(shuō)明紫薯酒渣花色苷仍具有較好的抗氧化活性。這可能是因?yàn)樽鲜淼陌l(fā)酵過(guò)程使花色苷的分子結(jié)構(gòu)發(fā)生改變,從而引起抗氧化活性的變化。
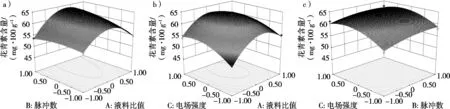
圖2 各因素交互作用對(duì)紫薯酒渣花色苷提取率的響應(yīng)曲面圖
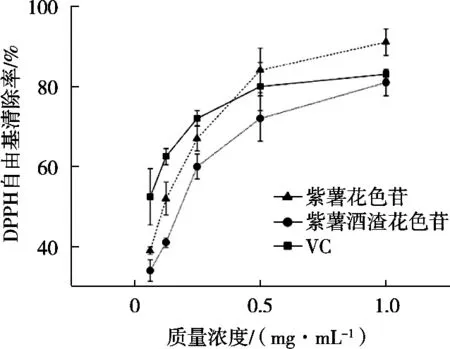
圖3 紫薯花色苷、紫薯酒渣花色苷和VC清除DPPH自由基能力(n=3)
3 結(jié)論
通過(guò)響應(yīng)面設(shè)計(jì)對(duì)紫薯酒渣花色苷的提取工藝進(jìn)行優(yōu)化,其最優(yōu)提取工藝為:液料比值21(mL/g)、電場(chǎng)強(qiáng)度18.3 kV/cm、脈沖數(shù)9.3。此時(shí)預(yù)測(cè)響應(yīng)值為64.02 mg/100 g。經(jīng)試驗(yàn)驗(yàn)證,實(shí)際含量為63.9 mg/100 g,表明模型能用于預(yù)測(cè)紫薯酒渣花色苷的提取工藝。DPPH清除能力試驗(yàn)表明紫薯酒渣花色苷具有較強(qiáng)的抗氧化能力。因此,紫薯酒渣可作為花色苷開(kāi)發(fā)利用的潛在資源。

