艾葉揮發(fā)油-環(huán)糊精包合物研究概述
周瑤 ,陳崗 ,詹永,楊勇,吳振 ,譚紅軍*
1.重慶市中藥研究院(重慶 400065);2.重慶市中藥健康學重點實驗室(重慶 400065)
艾葉為菊科蒿屬植物艾(Artemisia argyi Lévt. et Vant)的干燥葉,可入藥[1]。艾的生長適應能力強,常見于荒野、荒坡草地和丘陵地帶,也可人工種植。在世界上主要分布于亞洲東部,我國的東北、華北、西南、陜西及甘肅等地均有分布。從艾葉中提取出的揮發(fā)油是一種具有揮發(fā)性且氣味濃郁的物質,其成分以小分子揮發(fā)性的桉葉素、樟腦、龍腦、檸檬烯等萜類化合物為主,主要是單萜類、單萜類衍生物、倍半萜類及其衍生物三類有效物質,艾葉揮發(fā)油具有多種藥理作用,包括平喘止咳、鎮(zhèn)靜、消炎、利膽、抗過敏、抗癌,止血等[2-5]。體外研究發(fā)現(xiàn),艾葉揮發(fā)油能使酪氨酸酶活性下調,揮發(fā)油濃度越高,黑色素下降越多,具有美白肌膚的功效[6]。因此艾葉揮發(fā)油在醫(yī)藥、保健品、化妝品等方面的應用和開發(fā)越來越受重視,但由于其具有水溶性差,易揮發(fā),遇光、熱、氧化易降解等特點,極大限制了在各個方面的深度開發(fā)應用。為擴大其在藥物及其他領域的應用,通常采用環(huán)糊精包合技術,以克服其在各個領域應用上的局限。
環(huán)糊精(CD)是直鏈淀粉在由芽孢桿菌產生的環(huán)糊精葡萄糖基轉移酶作用下生成的一系列環(huán)狀低聚糖的總稱,通常含有6~12個D-吡喃葡萄糖單元,其中最常見的自然形成的環(huán)糊精包括α-、β-、γ-這3種構型,值得注意的是,葡萄糖單位的數(shù)量決定CDs的空腔直徑(圖1)[7]。環(huán)糊精包合物又稱分子膠囊,是指具有空間結構的主體分子全部或部分包裹另一個客體分子。環(huán)糊精包合技術有許多優(yōu)點:揮發(fā)油被環(huán)糊精包合后,可以增加揮發(fā)油溶解度和溶出度,降低刺激性;環(huán)糊精疏水腔可以避免揮發(fā)油的揮發(fā),可明顯提高有效成分的保留率,增加儲存過程中的穩(wěn)定性;揮發(fā)油被嵌入環(huán)糊精分子中,可控制和延緩揮發(fā)油的釋放,達到緩釋、靶向的目的;組成的揮發(fā)油包合物還可以提高制劑的生物利用度,減少服藥劑量,改善藥物在體內的吸收,減輕毒副作用;同時,包合技術還能將性狀進行轉變,如通過合理加工,能夠將液態(tài)的中藥轉化成為粉末狀,可掩蓋中藥比較特殊的一些氣味,在防止藥性揮發(fā)基礎上,大幅提高藥物的純度及治療效果[8]。國內外對艾葉揮發(fā)油環(huán)糊精包合物的研究仍不多,由于青蒿素是從青蒿中提取的一種天然倍半萜類化合物,因此綜述青蒿素環(huán)糊精包合物的部分研究,以期為艾葉揮發(fā)油環(huán)糊精包合物的深入研究和實際應用提供思路。
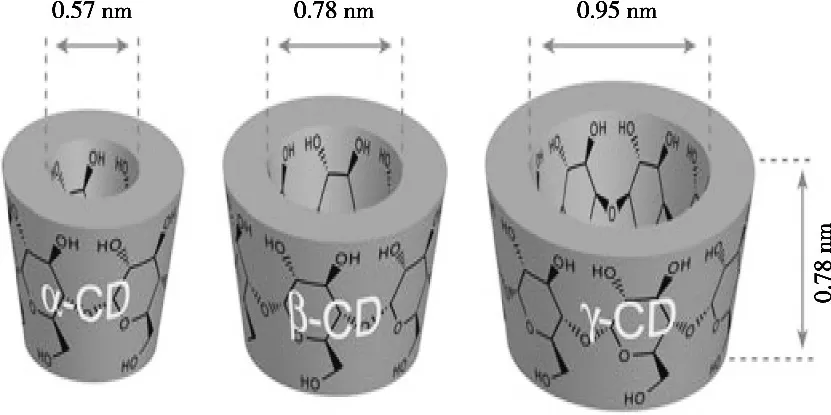
圖1 α-,β-和γ-環(huán)糊精幾何結構及尺寸
1 艾葉揮發(fā)油-環(huán)糊精包合物的制備方法
環(huán)糊精包合物的制備方法有飽和水溶液法(重結晶或共沉淀法)、微波法、超聲波法、研磨法、冷凍干燥法、噴霧干燥法等。
1.1 飽和水溶液法
艾葉揮發(fā)油研究中采用最多的制備方法是飽和水溶液法(圖2)[9],即稱取一定量環(huán)糊精,溶于適當溫度蒸餾水,磁力攪拌一段時間,配制成飽和溶液,再將揮發(fā)油滴加到飽和環(huán)糊精溶液中,包合、過濾、干燥,即得包合物。沈德鳳等[10]使用飽和水溶液法,從艾葉揮發(fā)油利用率、包合物得率和含油率3個指標優(yōu)化試驗,結果表明,在環(huán)糊精和油比例8∶1、包合溫度60 ℃、包合時間2 h條件下,艾葉揮發(fā)油利用率和包合物收得率為最佳。方法方便簡捷,包合率較高,是實驗室常用的包合物制備方法,且適用于工業(yè)化生產,但是此法可能會因儀器和個人的試驗差異造成試驗誤差,且存在溶劑殘留的問題。包合過程中的包合溫度、包合時間等均對包合率的影響較大。對溫度的控制尤為重要,溫度過高,包合物溶解度增大,揮發(fā)油易從分子中逸出,過低則環(huán)糊精易析出,包合機會減少,造成包合率較低,艾葉揮發(fā)油的包合溫度一般以60 ℃為佳。
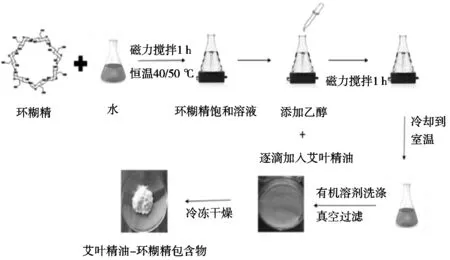
圖2 使用共沉淀法制備環(huán)糊精包合物
1.2 超聲波法
將揮發(fā)油的有機溶劑(如乙醇)溶液加入環(huán)糊精的飽和水溶液中,用超聲儀在優(yōu)化的超聲強度和時間下進行包合,包合完成后冷藏,將析出的沉淀過濾、洗滌、干燥,即得包合物。超聲法較飽和水溶液法簡單快捷,適用于大量生產。鄒新城[11]對艾葉揮發(fā)油用β-環(huán)糊精進行包合,超聲法制備的最佳包合工藝條件是:β-環(huán)糊精與揮發(fā)油比率6∶1、超聲時間30 min、超聲溫度40 ℃。
1.3 冷凍干燥法
在環(huán)糊精飽和溶液中加入揮發(fā)油,混合攪拌使藥物包合,再通過冷凍干燥技術揮去溶劑,可制成粉針劑。對于某些在低溫加熱干燥時容易分解、揮發(fā)或變色的包合物,可以使用冷凍干燥法對包合物進行干燥。詹國平等[12]在羥丙基-β-環(huán)糊精的水溶液中加入乙醇溶解的艾葉揮發(fā)油,攪拌2 h后過濾,-35 ℃下冷凍干燥48 h,研磨后得疏松、溶解性能好的淡黃色粉末。張志等[13]將艾葉揮發(fā)油滴加到羥丙基-β-環(huán)糊精飽和水溶液中,攪拌至規(guī)定時間后用少量乙酸乙酯萃取未包合的揮發(fā)油,水相冷凍干燥36 h,即得溶解性好的凍干粉。
1.4 研磨法
在環(huán)糊精中加入一定量的水混合均勻,加入揮發(fā)油的有機溶劑溶液,充分研磨,干燥后得包合物。由于此方法實驗室手工操作較費時費力,不適用于大量生產,但采用工業(yè)膠體磨等制備環(huán)糊精包合物較快速、簡便。鄒新城[11]通過研磨法制備β-環(huán)糊精艾葉揮發(fā)油的包合物,發(fā)現(xiàn)影響環(huán)糊精包合的主要因素是加水倍數(shù)、環(huán)糊精與揮發(fā)油比例以及研磨時間。加水倍數(shù)100,環(huán)糊精與揮發(fā)油比例8∶1、研磨時間30 min是最佳工藝條件。
艾葉揮發(fā)油環(huán)糊精包合物的制備方法的選擇取決于包合率、包合速度、簡便性及產品最終的特性。傳統(tǒng)常見的環(huán)糊精包合物制備方法耗時都比較長,難以滿足工業(yè)及商業(yè)化制備要求,且存在溶劑殘留問題。為解決上述問題,一些新型的技術手段也被應用于制備環(huán)糊精包合物。如微波法反應速率比傳統(tǒng)的加熱方法快數(shù)倍甚至上千倍,具有操作簡單、收率高、后處理方便等特點。超臨界CO2法由于其包合溫度低,適用于對濕熱敏感的物質,且有效解決溶劑殘留問題,與飽和水溶液法相比,客體分子在CO2中比在水中有更高的溶解度,這種技術最大的優(yōu)勢能擴大商業(yè)應用。高壓均質包合法,可使處理樣品在高壓下產生強烈的剪切、撞擊和空穴作用,使液態(tài)的揮發(fā)油呈現(xiàn)超微細化狀態(tài),將微細化狀態(tài)的揮發(fā)油包合到環(huán)糊精所提供的空穴結構中,可提高包合率和增加穩(wěn)定性。
2 環(huán)糊精包合技術對艾葉揮發(fā)油理化及生物學特性的影響
2.1 環(huán)糊精包合技術對艾葉揮發(fā)油理化特性的影響
2.1.1 增強溶解性和生物利用度
艾葉揮發(fā)油被環(huán)糊精包合后,能增加其在水中的溶解度和溶出速率,進而改善揮發(fā)油的生物利用度。一般通過相溶解度來評估環(huán)糊精對客體溶解度的影響,相溶解度以客體分子濃度為縱坐標,環(huán)糊精濃度為橫坐標,獲得環(huán)糊精包合物的相溶解度的線性函數(shù)曲線。此法不僅用于測定包合常數(shù),同時還有助于了解包合物的溶解行為和環(huán)糊精對客體分子的增溶效果。Zime-diawara等[14]通過測定青蒿素在不同濃度β-環(huán)糊精、γ-環(huán)糊精、羥丙基-β-環(huán)糊精、羥丙基-γ-環(huán)糊精等的溶解度,繪制相溶解度曲線,試驗結果表明所有類型的環(huán)糊精都可以增強青蒿素的溶解度。Balducci等[15]制備的β-環(huán)糊精包合的青蒿素口服粉劑與未包合的粉劑相比,大鼠血液中青蒿素水平增加約3.2倍,極大提高了青蒿素的生物利用度。
2.1.2 保留
艾葉揮發(fā)油制成藥物制劑可能有不良氣味及苦澀味,輕微低毒性讓其有一些刺激性,影響制劑應用。環(huán)糊精包合后可掩蓋不良氣味,降低刺激性,控制和降低其有效成分的揮發(fā),并延緩藥物的釋放。沈德鳳等[16]制備一種艾葉揮發(fā)油β-環(huán)糊精包合物口含片,口中含化時間達15 min以上,口感較好。Balducci等[15]通過噴霧干燥制備一種青蒿素/β-環(huán)糊精口服粉劑,經體外溶出度測定顯示,10 min內約70%的藥物從粉劑中釋放出來,而空白粉劑釋放出來的青蒿素低于10%。
2.1.3 增強穩(wěn)定性
艾葉揮發(fā)油易揮發(fā),遇光、熱、氧化易降解等特點,嚴重影響了其在生產中的應用和實際的療效。揮發(fā)油可以通過包封來防止其逸散,環(huán)糊精將揮發(fā)油包入其空腔能避免其直接與光、氧氣等不利環(huán)境接觸,能提高制劑的穩(wěn)定性。如羥丙基-β-環(huán)糊精(HP-β-CD)對羅勒和龍蒿揮發(fā)油的包合,改善其在紫外線照射下的穩(wěn)定性。李麗華等[17]對艾葉-連翹揮發(fā)油環(huán)糊精包合物和混合物進行熱穩(wěn)定性試驗、抗光解試驗、濕穩(wěn)定性試驗。結果表明,包合物含量均無明顯的變化,而混合物含量下降,證明艾葉-連翹揮發(fā)油包合物在光熱濕等因素下穩(wěn)定性能良好。鄒新城[11]對艾葉揮發(fā)油-β-環(huán)糊精包合物和混合物進行強光照射、高溫、高濕試驗,結果發(fā)現(xiàn)艾葉揮發(fā)油-β-環(huán)糊精包合物具有一定抗光解性,熱穩(wěn)定性和濕穩(wěn)定性明顯優(yōu)于單純艾葉揮發(fā)油。孫艷等[18]研究艾葉揮發(fā)油和艾葉揮發(fā)油-β-環(huán)糊精包合物的反應時間,后者相比前者提高111.8%,說明艾葉揮發(fā)油經β-環(huán)糊精包合后,其有效期得到延長。
2.2 環(huán)糊精包合技術對艾葉揮發(fā)油生物學特性的影響
環(huán)糊精包合揮發(fā)油不會干擾其生物活性,能充當滲透促進劑,增加活性劑的溶解和透過生物膜濃度,通常認為其促進藥物吸收的機理是由增溶作用引起的。沈德鳳等[19]結合透皮給藥系統(tǒng),以左氧氟沙星為模型藥物,研究艾葉揮發(fā)油β-環(huán)糊精包合物對左氧氟沙星透皮吸收的促進作用。透皮給藥系統(tǒng)是20世紀80年代發(fā)展起來的第三代制劑,但由于其透皮吸收率低的缺點限制其廣泛應用,因此提高藥物的透皮吸收率是研究透皮系統(tǒng)的關鍵。該試驗結果表明艾葉揮發(fā)油的β-環(huán)糊精包合物對左氧氟沙星有顯著的透皮吸收促進作用。高金波等[20]考察艾葉揮發(fā)油的β-環(huán)糊精包合物對鹽酸環(huán)丙沙星透皮吸收的影響,顯示0.8%的艾葉揮發(fā)油的β-環(huán)糊精包合物對鹽酸環(huán)丙沙星有顯著的透皮吸收促進作用。
3 影響艾葉揮發(fā)油-環(huán)糊精包合物的因素
制備艾葉揮發(fā)油或其活性成分的環(huán)糊精包合物,了解包合過程中各種可能的影響因素是很有必要的。影響環(huán)糊精包合的因素主要有以下幾方面。
3.1 環(huán)糊精類型
環(huán)糊精的類型可能會影響環(huán)糊精艾葉揮發(fā)油包合物的包合。環(huán)糊精有各種類型,其中β-環(huán)糊精是研究較多的類型,但因β-環(huán)糊精存在的空腔內徑小,水溶性差,非胃腸道給藥有腎毒性的缺點,導致其使用范圍的局限。因此有學者在β-環(huán)糊精基礎上對其進行結構改造和化學修飾,獲得一些性能優(yōu)良的環(huán)糊精衍生物。如一氯均三嗪-β-環(huán)糊精(MCT-β-CD)是β-CD的醚化衍生物,具有和β-CD類似的分子結構,基本不溶于有機溶劑,可溶于水,其溶解度隨著溫度的升高而增大,穩(wěn)定性好,無毒,可生物降解,也可被人體所吸收。此外還有甲基-β-環(huán)糊精(Me-β-CD)、羥丙基-β-環(huán)糊精(HP-β-CD)、磺丁基醚環(huán)糊精[21]。Jiang等[22]研究β-環(huán)糊精、2,6二甲基-O-β-環(huán)糊精及羥丙基-β-環(huán)糊精對艾蒿揮發(fā)油的包合,使用熒光光譜法評估β-環(huán)糊精及其衍生物的包合作用,結果表明微膠囊形成能力β-環(huán)糊精>2,6二甲基-O-β-環(huán)糊精>羥丙基-β-環(huán)糊精。在青蒿素研究中,由于β-環(huán)糊精水溶性較差的特性,導致它對青蒿素的增溶能力有限,它的衍生物羥丙基-β-環(huán)糊精能更好地增溶青蒿素,且比甲基化衍生物的增溶效果強。環(huán)糊精類型的選擇前提條件是要求客體分子幾何形狀、尺寸、極性與環(huán)糊精的空腔尺寸和性質相匹配。
3.2 主客體比率
主客體比率可能會影響包合率,包合率是制備包合物的一個重要參數(shù),大部分研究揮發(fā)油或其有效成分被包合時,都會優(yōu)化揮發(fā)油環(huán)糊精主客體比例對包合率的影響。李冬梅等[23]制備的艾葉揮發(fā)油β-環(huán)糊精包合物,當環(huán)糊精用量超過揮發(fā)油的10倍以上時,包含率不再有明顯增加,試驗中最優(yōu)主客體比例8∶1。主客體包合比例過小,艾蒿提取液不能充分被包合;比例過大,不能充分發(fā)揮環(huán)糊精的包合作用。
3.3 制備技術
艾葉揮發(fā)油環(huán)糊精包合物可使用不同技術制備,選擇的制備方法會直接影響環(huán)糊精對揮發(fā)油的包合率。鄒新城[11]考察3種包合技術對艾葉揮發(fā)油環(huán)糊精包合物的包合作用,研磨法、飽和水溶液法、超聲法的平均包合率分別為50%,93%和55%,在此試驗中飽和水溶液攪拌法在包合揮發(fā)油上顯示出更好的結果。
4 新興的以環(huán)糊精為基礎的技術對揮發(fā)油的包合
環(huán)糊精包合技術還能與其他新興的技術結合創(chuàng)造出新的技術形式,如微膠囊技術、納米技術、脂質體裝載的環(huán)糊精包合物等。葛玲艷等[24]以艾葉揮發(fā)油和甘油為芯材,以多孔淀粉和β-環(huán)糊精為壁材,利用艾葉揮發(fā)油微囊化研制出艾葉揮發(fā)油糧食防蟲劑,針對玉米象和雜擬谷盜進行防治。王輝[25]以明膠和阿拉伯樹膠為壁材,艾草揮發(fā)油為芯材,通過復合凝聚法制備的艾草揮發(fā)油微膠囊呈圓球形,表面較粗糙,沒有裂縫和空隙,表面連續(xù)、多空,囊壁具有半透性,艾草揮發(fā)油可以通過囊壁緩慢釋放,不致在較短時間內釋放完畢,從而達到緩慢釋放、抗菌持久的效果。
5 結語
艾葉揮發(fā)油的不穩(wěn)定性、刺激性、低毒性、溶解性差以及生物利用度低等問題阻礙其在臨床上的應用,使用環(huán)糊精包合艾葉揮發(fā)油則有望解決這些問題,環(huán)糊精自發(fā)現(xiàn)以來,不僅適用于食品行業(yè),也適用于制藥及化妝品等行業(yè),隨著更多環(huán)糊精衍生物的出現(xiàn),包合技術將會有更大發(fā)展空間。國內外對艾葉揮發(fā)油環(huán)糊精包合技術的研究還處于初級階段,尚有很多問題需要深入研究,環(huán)糊精類型、主客體比例、制備方法是獲得最大包合率的最重要的參數(shù),需要更系統(tǒng)地進行研究,以β-環(huán)糊精研究為主,對其衍生物的研究很少。包合物的制備方法只是單一研究,沒有進行更多的比較研究以尋找到更適當?shù)闹苽浞椒ā-h(huán)糊精空腔包合客體分子主要依賴于其與空腔的匹配度,客體分子的尺寸、結構及特性均會影響空腔包合作用,因此需要對揮發(fā)油與環(huán)糊精的作用機制進行研究,艾葉揮發(fā)油環(huán)糊精包合物的作用機制幾乎未得到研究。某些測定包合率及揮發(fā)油使用率的技術還有缺陷,實際應用中可能需要幾種表針方法共同驗證。

