乳腺癌病人靜脈血栓栓塞癥風險預測模型的構建
李 靜,強萬敏*,張方圓,李笑陽,任佳蕾
(1.天津醫科大學腫瘤醫院,天津300060;2.大連大學;3.天津中醫藥大學)
靜脈血栓栓塞癥(venous thromboembolism,VTE)包括深靜脈血栓形成(deep vein thrombosis,DVT)和肺血栓栓塞癥(pulmonary thromboembolism,PTE)兩種類型,在癌癥人群中的發病率為4%~20%,是非癌癥人群的6~7 倍[1]。相對于胰腺、胃和肺部的惡性腫瘤,乳腺癌病人VTE 的風險較低,為0.16%~0.30%,但乳腺癌作為全球女性發病率最高的癌癥,VTE 病人的絕對值和由此產生的醫療消耗是龐大的[2-3]。研究發現,發生VTE 的乳腺癌病人死亡風險增加1 倍以上,其中13%的病人會出現血栓后綜合征,表現為長期疼痛、水腫和潰瘍癥狀[4]。美國國家綜合癌癥網絡的癌癥相關性靜脈血栓栓塞性疾病指南和我國預防和治療腫瘤相關靜脈血栓栓塞專家指南均認為,應用高質量的血栓風險評估工具識別高危病人,并據此采取分層預防措施可有效降低血栓的發生。目前,國際上存在多種癌癥病人VTE 風險的評估模型,如通用的Caprini評分、Wells 量表和基于癌癥人群開發的Khorana 模型(Khorana Score,KS)及其后來的多個修訂版(CATS、PROTECHT 和CONKO 模型)。然而,目前KS 已被證實并不適用于住院乳腺癌病人[5],尚未發現其他模型在獨立的乳腺癌隊列進行驗證的研究,因此其預測價值仍有待探討。本研究通過系統地回顧文獻和Meta 分析,篩選出乳腺癌病人VTE 形成的危險因素并計算其綜合危險度,構建乳腺癌專科VTE 風險預測模型,以期指導臨床更好地預防VTE 發生。
1 資料和方法
1.1 文獻檢索 計算機檢索英文數據庫:PubMed、EMbase、Web of Science、CINAHL、Cochrane Library,檢索詞為“thrombosis/deep vein thrombo*/venous thrombo*/thrombus/embolism/blood clot/phlebothrombosis”“breast neoplasm/breast cancer/breast tumor*/mammary cancer/breast malignant neoplasm*”“factor*/risk factor/influence factor/relevant factor”;中文數據庫:中國知網、萬方數據庫、中國生物醫學文獻數據庫、維普數據庫,檢索詞為“乳腺癌/乳腺腫瘤”“靜脈血栓/VTE”“危險因素/影響因素/相關因素/發病因素/原因”。同時,采用滾雪球法對納入文獻的參考文獻進行追蹤檢索。檢索時限均為從建庫至2019 年5 月31 日。
1.2 文獻納入與排除標準 納入標準:①研究對象為年齡18 歲以上經病理診斷為乳腺癌病人;②觀察終點包括客觀診斷的VTE 事件;③研究類型為隊列研究或病例對照研究;④可直接或者通過數據轉換能夠獲取影響因素的風險值(risk ratio,RR)及95% 置信區間(confidence interval,CI);⑤暴露組(病例組)和非暴露組(對照組)基線具有可比性;⑥各研究假設及研究方法類似,均衡性一致。排除標準:①研究對象除納入乳腺癌人群外,另有其他類型的癌癥人群;②涉及因素僅限醫學檢測的生物因子或基因層面研究;③試驗設計不嚴謹,混雜偏倚多的病例對照研究;④不同的數據庫交叉或者重復發表的研究,僅納入最新的報道;⑤統計描述不全面或違反統計分析原則的研究。
1.3 資料提取與質量評價 對納入的文獻進行資料提取,主要包括兩方面資料。①納入研究的基本資料:作者、發表年份、研究設計類型、調查地點與時間、年齡、樣本量、隨訪時間、血栓事件和確診檢查等;②VTE 發生的危險因素、對應RR 及95%CI。使用紐卡斯-渥太華量表(Newcastle-Ottawa Scale,NOS)對納入文獻進行質量評價。量表包括研究人群的選擇(4分)、組間可比性(2 分)、結局的測量(4 分)3 部分,共10分。以上工作均由2 名研究者獨立完成后交叉核對結果,若有分歧由小組成員共同協商解決。
1.4 統計學分析
1.4.1 Meta 分析 使用RevMan 5.3 進行Meta 分析。納入研究結果間的異質性的大小采用χ2檢驗和I2定量判斷;當I2≤50%,使用固定效應模型進行Meta 分析;當I2≥50%,且有明顯的臨床異質性,進行亞組分析或敏感性分析。如不能發現明顯的臨床異質性,則使用隨機效應模型。使用Stata15.0 軟件,采用Begg's 秩相關檢驗法和Egger's 回歸分析法對納入大于10 篇以上研究的危險因素評價發表偏倚。檢驗水準均為0.05。
1.4.2 風險預測模型的建立
1.4.2.1 Logistic 回歸預測模型
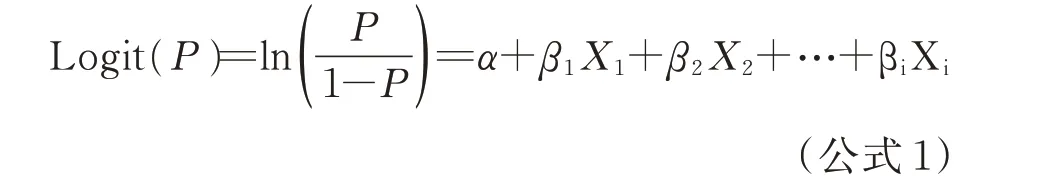
其中,P表示個體發病概率,X1、X2…Xi分別是1,2,…,i 個危險因素;α是常數項,β1、β2...βi是偏回歸系數,計算公式如下:
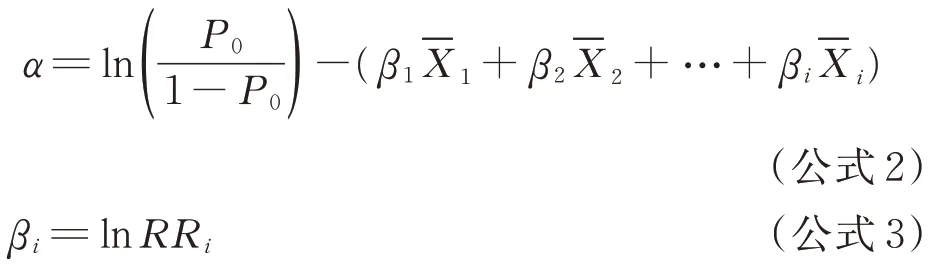
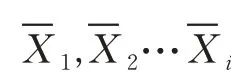
1.4.2.2 風險評分系統的具體步驟 公式1 中各回歸系數βi值同時除以最小回歸系數βm;將新的系數按四舍五入法取整數,即各自變量對應的危險分數為Si,總危險分數為Sc為各危險分數的和,得出僅有1 個自變量的新的評分預測模型,即:
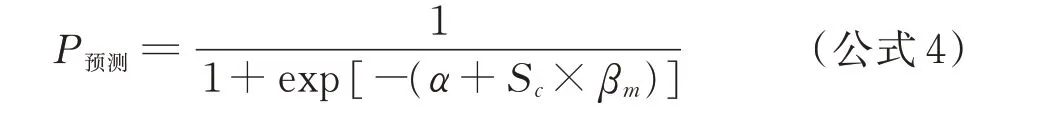
根據估算的平均暴露率和VTE 發病率(2.3%),使用R 軟件模擬10 000 例病例,繪制概率分布曲線并劃分危險等級。
2 結果
2.1 文獻檢索及篩選 初檢獲得文獻2 854 篇,通過追蹤參考文獻獲取8 篇文獻。經EndNote 去重520 篇,獲得2 342 篇文獻;閱讀題目和摘要進行初篩,剔除2 284 篇;納入58 篇,閱讀全文進行復篩,排除12 篇無法找到全文的研究、3 篇數據有交叉的研究、21 篇無法提供有效數據的研究,最終納入22 篇文獻。
2.2 納入分析文獻的一般狀況與質量評價結果 本研究共納入22 篇文獻,包括13 篇回顧性隊列研究[6-18]、6 篇病例對照研究[5,19-23],2 篇前瞻性隊列研究[24-25]和1篇巢式病例對照研究[26],研究時間范圍1998 年1 月1日至2018 年12 月31 日。回顧性研究共納入526 205例乳腺癌病人,其中有22 456 例發生VTE;前瞻性研究共納入864 例,其中有222 例發生VTE;有7篇[5,19-23,26]研究采用了配對的方法來消除部分重要的混雜因素。采用NOS 量表對納入的文獻研究進行質量評價,其中10 篇評分≥7 分,12 篇評分為4~6 分。
2.3 Meta 分析結果 本研究納入的22 篇研究中共涉及研究因素104 個,其中研究次數4 次以上的影響因素共15 個,分別是年齡、體質指數(body mass index,BMI)、吸煙、高血壓、糖尿病、冠心病、既往血栓史、遠處轉移、浸潤性導管癌、“三陰型”癌、乳腺手術、化療、內分泌治療、服用他莫昔芬和中心靜脈置管(central vena catheterization,CVC)。其中高血壓、冠心病、遠處轉移和內分泌治療合并的數據有較大異質性,進行了亞組分析或敏感性分析;Meta 分析結果及異質性分析詳見表1。其他因素異質性均低于60%,說明各因素研究間的RR 值趨于一致。對研究數量在10 個以上的危險因素(高血壓和糖尿病),進行Begg's 秩相關法和Egger's 直線回歸法檢驗,結果顯示均無發表偏倚。

表1 Meta 分析結果及異質性分析
2.4 風險預測模型的構建及分層
2.4.1 風險預測模型的構建 將Meta 分析合并效應量差異有統計學意義的10 個因素作為預測因子納入模型。
Logistic 回歸模型如下:
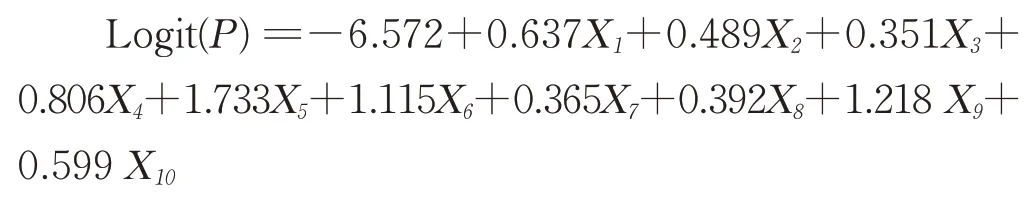
其中,X1、X2…X10分別代表BMI、高血壓、糖尿病、冠心病、既往血栓史、浸潤性導管癌、乳腺手術(3 個月內)、化療、他莫昔芬類藥物和CVC。根據建立的Logistic 回歸模型,糖尿病的βm=0.351 為最小回歸系數,建立危險評分模型,得出:
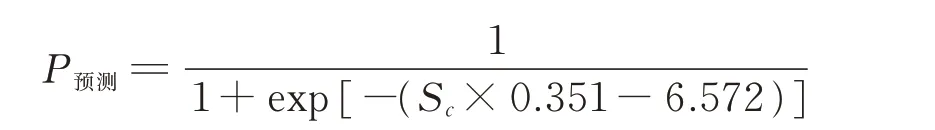
模型各預測因子的危險分值,最低為1 分,最高為5 分,總分為0~21 分。見表2。
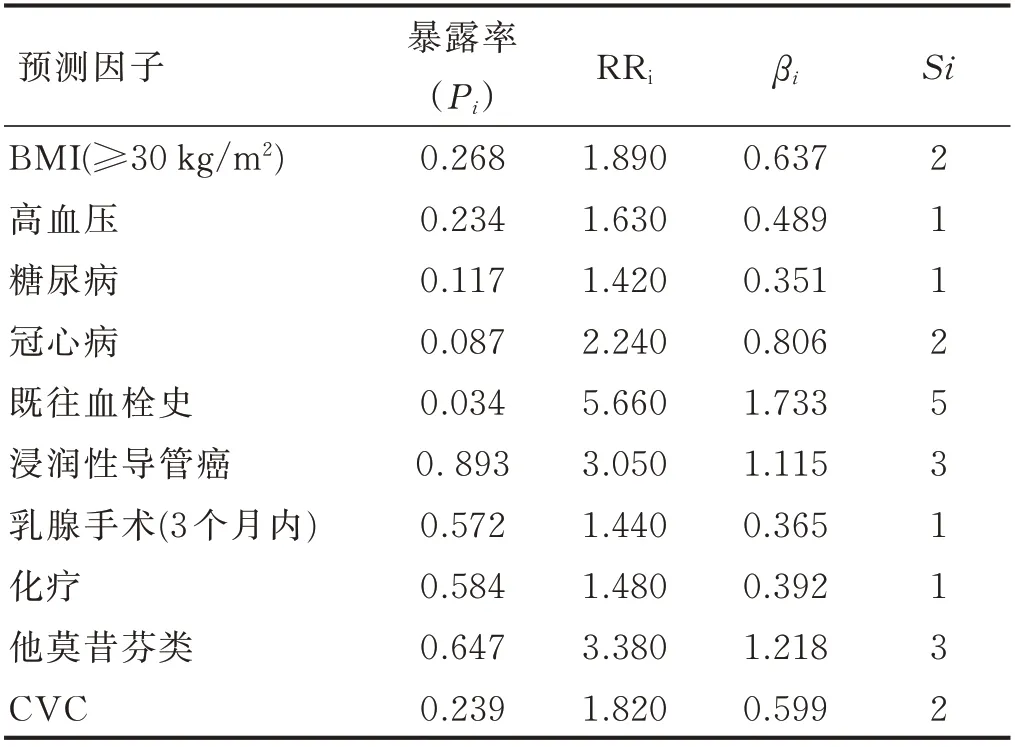
表2 風險預測模型各預測因子參數及轉換分值
2.4.2 風險評分系統的等級劃分 根據乳腺癌病人VTE 的10 個危險因素的暴露率,使用R 軟件以rbinom(n,size,prob)為基礎R 語言編寫代碼,模擬10 000 例病例并繪制概率分布曲線。最終將乳腺癌病人VTE的發生率2.3%的1.5 倍即3.45%對應點的發病危險作為發生VTE 的中危與高危的分界,即第9 655 位的A 點,對應發病概率是0.095 7,分值是13 分;2.3%的8倍即18.4%對應點的發病危險作為VTE 的低危與中危劃分界限,即第7 800 位為B 點,對應發病概率是0.018 0,分值是9 分。危險等級的劃分節點詳見圖1。因此,該模型的危險分層是低于9 分為低危,9~<13分為中危,≥13 分為高危。
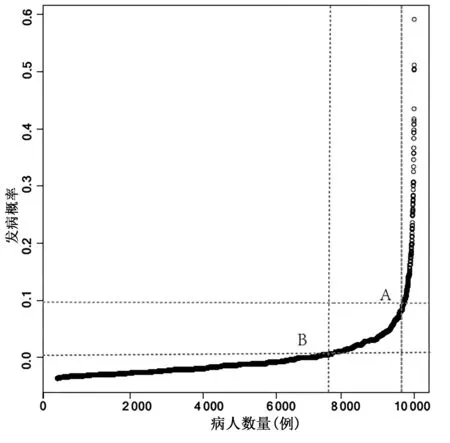
圖1 預測模型危險等級劃分節點圖
3 討論
本研究構建的風險預測模型包括病人特征、疾病診斷和治療相關因素在內的10 個預測因子。KS 及其修訂版CATS、PROTECHT 評分模型均將BMI≥35 kg/m2作為VTE 的預測因子之一,但歐美人群BMI 整體水平偏高,考慮到亞洲人種的差異,將分層界值為30 kg/m2的亞組納入模型。最新發布的COMPASS-CAT評估模型基于1 023 例門診癌癥病人構建,其中乳腺癌占61%,對預測乳腺癌病人VTE 的風險具有重要的參考價值[27],它將心血管類疾病數量作為重要的預測因子評為6 分,總分28 分。而本研究將高血壓、糖尿病、冠心病分別作為獨立的預測因子,總分為4 分。與其他多個廣泛應用的模型如Caprini 評分、Wells 量表一致,此模型中既往血栓史作為最重要預測因子,評分為5 分;浸潤性導管癌次之,評分為3 分。多項研究表明,手術是發生VTE 的獨立危險因素,且術后3 個月內發生率最高,這一時期確診的VTE 事件占所有事件的70%左右[14,28];乳腺癌病人常用的化療藥物有環磷酰胺、5-氟尿嘧啶、蒽環類和紫杉醇類等,這些藥物均可直接或間接抑制血管內皮生長因子的活性,損傷血管壁,促進血栓形成[29-30];COMPASS-CAT 模型將含蒽環類藥物的化療作為預測因子之一[RR=2.33,95%CI(1.02~5.33)]。服用他莫昔芬可增加靜脈血栓的風險,且與化療藥物聯用時發病風險會更高[31]。但目前,他莫昔芬類藥物增加血栓發生的機制仍未明了。
通過評估乳腺癌病人是否存在以上10 個危險因素,來估算個體VTE 的發病概率、危險評分和分級。例如:1 例65 歲乳腺癌術后2 個月的住院病人,即將使用CVC 行第6 周期的化療,BMI 為30.5 kg/m2,高血壓病史10 年,冠心病史3 年,無糖尿病和既往血栓史,病理診斷是浸潤性導管癌,未服用他莫昔芬類進行內分泌治療。試預測該病人化療期間發生靜脈血栓的風險有多少?將危險因素BMI(2 分)、高血壓(1 分)、冠心病(2 分)、浸潤性導管癌(3 分)、乳腺手術(1 分)、化療(1 分)和CVC(2 分)的評分相加,為12 分,血栓發生風險為中危;計算發生概率P預測=8.63%,該病人發生VTE 概率是一般人群(2.3%)的4 倍。因此,可以考慮對該病人采取機械性物理措施,強化血栓預防的健康教育并增加下肢的評估頻率。在實際應用中需要注意的是,該模型構建使用的常數項和10 000 例模擬病例均是根據文獻報道的VTE 平均發病率和文獻中各危險因素的對照組暴露率進行估算的,如目標醫院或地區以上兩方面數據與本研究差距過大,可能使得估算的個體發病概率(P預測)和危險分層出現偏差。因此,盡管本研究在綜合分析已有數據的基礎上建立了乳腺癌病人VTE 形成風險預測模型,但仍有待臨床實踐對其穩定性和適用性進行外部驗證。
本研究系統地檢索和回顧了乳腺癌VTE 相關的危險因素,通過Meta 分析的方法,結合Logistic 回歸模型構建了乳腺癌病人VTE 的個體化風險預測模型。這種大樣本的累積不僅克服了因乳腺癌人群VTE 發病率低、病例收集難的問題,同時避免了單中心研究樣本缺乏代表性的問題,保障了各危險因素綜合危險度的可靠性;通過邏輯評分法將復雜的公式轉化成評分,增加了預測模型臨床的可操作性,而且這種評分轉換方法在其他風險評估模型構建中已廣泛應用,其科學性和可靠性已得到了驗證[29-31];通過計算機模擬數據集劃分了3 個危險等級,以期指導臨床有針對性地采取物理或藥物預防,以達到最佳風險/獲益比。此外,該模型除了對乳腺癌病人VTE 形成有預防的現實意義外,還可為下一步建立其他疾病發病的風險預測模型提供新的思路。但由于Meta 分析本身是基于原始研究的二次分析,致使本研究存在不可規避的不足。例如提取數據時雖優先采用多因素校正后的RR 值,但仍有部分僅提供單因素分析的結果,這有可能使合并效應量摻有混雜因素的效應;由于與癌癥病人VTE發生相關的生物標志物,如D-二聚體、血細胞參數等多是連續性數據并未納入Meta 分析,直接導致了預測因子的不全面性,使構建的風險預測模型存在一定缺陷;除高血壓和糖尿病這2 個危險因素外,其他13 個危險因素研究文獻數量不足10 個,未檢測發表偏倚,無法明確這些因素的合并效應量是否受發表偏倚的影響。另外,模型的驗證是檢驗模型區分度、一致度和分類度的重要手段。由于本研究是基于原始研究的定量綜合,數據集并不是來自單一的研究隊列,所以也無法使用重抽樣法、交叉驗證等方法進行內部驗證。目前,該模型被用于我科室預測乳腺癌術后病人的VTE 風險,詳細結果將會繼續報道。

