Wnt信號通路調控衰老相關疾病的研究進展*
樊廷俊,鄭明月,徐 彬
(中國海洋大學海洋生命學院,山東 青島 266100)
人口老齡化已成為世界各國日益突出的社會問題。據文獻報道,截止到20世紀末,全球65歲以上人口從約7%上升到20%以上,80歲及以上人口有1.25億[1]。老齡化帶來的相關疾病也呈指數增長,如2型糖尿病、神經退行性疾病、心血管疾病和癌癥等[2-5]。
老齡化導致的疾病為個人和社會帶來了巨大的經濟負擔。統計數據顯示,一個人年滿45歲后所花費的醫療費用占其一生總醫療費用80%以上[6]。因此,研究老齡化的干預措施變得越來越重要。在過去的幾十年里,衰老領域的研究取得了重大進展,包括建立了各種衰老研究模型,以及衰老機制及壽命延長研究等方面。繼mTOR信號通路后[7],研究發現Wnt信號通路在衰老過程中發揮關鍵的調控作用[8]。因此,本文就常見的衰老模型以及Wnt信號通路在衰老相關疾病中的作用方面的研究進展進行綜述。
1 衰老
衰老表現為機體生理完整性的逐漸喪失,導致機體功能受損并更易死亡。衰老細胞的形態扁平且擴大,并出現多種分子標志物,包括端粒功能異常誘導的聚集(Telomere-dysfunction-induced foci,TIF)、衰老相關的異染色質聚集(Senescence-associated heterochromatin foci,SAHF)、脂褐素顆粒、DNA疤痕和基因表達改變等[9]。衰老細胞的另一個重要特征是釋放衰老相關分泌表型(Senescence-associated secretory phenotype,SASP)因子[10]。此外,衰老細胞還表現出特殊的生化特性,例如,增殖性Ki-67蛋白表達缺失、較高的衰老相關β-半乳糖苷酶活性(SA-β-gal)以及腫瘤抑制因子和細胞周期抑制劑表達升高[11]。細胞核及線粒體DNA損傷會加速細胞衰老,雖然細胞內存在修復機制,但是修復機制一旦失效,受損的DNA則會積累,阻礙細胞功能并導致其衰老。衰老有很多誘因,如端粒縮短、有毒物質或癌基因等,會導致SAHF的形成,其標志性蛋白包括異染色質形成蛋白(例如,異染色質蛋白1)、組蛋白H3K9Me2/3和組蛋白H2A變異體中的macroH2A[12]。
2 常見衰老模型
衰老是許多人類疾病的最大危險因素,了解衰老過程可能會促進衰老相關疾病新療法的開發和發展[13]。雖然體外培養細胞能夠提供有價值的信息,但是無法完全模擬體內的生物學過程。因此,建立衰老模型研究相關疾病能更加深入和全面地研究衰老。常見的衰老模型主要包括以下幾類:
2.1 酵母模型
釀酒酵母(Saccharomycescerevisiae)是一種生物醫學研究領域中常用的衰老模型[14]。酵母細胞參與神經退行性過程的基本代謝途徑是比較保守的,因此常用于此類疾病的研究,包括肌萎縮、帕金森綜合癥和亨廷頓病[14]。
2.2 無脊椎動物模型
秀麗隱桿線蟲(Caenorhabditiselegans)是一種適用于研究衰老的臨床前實驗模型,主要是因為其體型小,壽命較短(約20天),全基因組已知,且與人類基因的相似度超過65%,適用于探索衰老及神經退行性疾病,例如阿爾茲海默癥、帕金森綜合癥等的可能機制[15]。有研究者發現脂質在亞細胞和組織解剖位置的分布會影響衰老的速率。此外,線蟲衰老過程中的脂肪再分配和異位積聚可能會造成脂肪毒性進而導致衰老相關組織功能下降[16]。這表明肥胖能夠加速衰老進程。
無論是理論研究還是應用研究,果蠅(Drosophilamelanogaster)都是一種比較理想的抗衰老藥物評價模型[17]。鑒于蛋白功能的高度保守性和果蠅的生命周期長度,果蠅也被廣泛應用于衰老分子機理的研究,尤其是代謝與衰老之間的關系,例如,有研究發現胰島素/IGF-1樣信號通路在衰老中起到重要作用[18]。此外,果蠅還被應用于許多神經系統疾病的病理機制研究,尤其是阿爾茲海默癥[19]。
近年來,也有研究者將不同種類的海膽作為衰老模型用于研究延長壽命和可忽略衰老(Negligible senescence),發現可忽略衰老過程常伴有細胞氧化損傷的積累,維持正常抗氧化能力及蛋白酶活性能夠延緩衰老[20]。
2.3 脊椎動物模型
水生脊椎動物是研究人類疾病的理想模型。2017年,第八屆人類疾病的水生動物模型大會重點介紹了包括斑馬魚、假鰓鳉、青鳉等多種研究模型。主要涉及13種人類相關疾病,包括癌癥、心血管疾病、代謝紊亂、神經疾病、衰老等[21]。其中,斑馬魚(Daniorerio)自1870年代以來作為經典模型用于發育生物學相關領域的研究,是研究機體衰老的理想動物模型,其衰老過程與人類相似,衰老的生理變化包括肌肉萎縮導致脊椎彎曲,眼睛出現白內障及視覺障礙[22]。此外,斑馬魚具有非常強的再生能力,多用于組織修復和延緩衰老的機理研究[23]。鳉魚(Nothobranchiusfurzeri)是壽命最短的脊椎動物[24],其衰老過程表現出多種哺乳動物衰老特征,是一種比較廉價且理想的衰老干預模型[24-25],可用于高通量篩選抗衰老藥物[26]。鳉魚不僅可以作為快速探索衰老及相關疾病的平臺,而且能夠用作發育機理研究,例如胚胎停止發育、早期性染色體進化等[25]。
鳥類作為一種獨特的衰老模型,多用于代謝和衰老相互作用的跨物種比較研究。例如,日本鵪鶉(Coturnixjaponica)是一種常見的實驗室飼養鳥類,壽命最長為6 a,它對卡路里限制反應類似于哺乳動物,因此多用于哺乳動物衰老代謝相關研究[27]。
嚙齒類動物中,實驗用小鼠(Musmusculus)和大鼠(Rattusnorvegicus)是研究衰老和年齡相關疾病的常見模型。小鼠模型多用于誘發型和自發型衰老模型[28],是應用最廣泛且最成熟的衰老模型。大鼠模型則被廣泛應用于衰老誘發的多種疾病的研究,包括心血管疾病、神經紊亂、行為神經、癌癥易感性和腎臟疾病以及行為認知等[29]。裸鼴鼠(Heterocephalusglaber)是迄今為止發現的壽命最長的嚙齒類動物,最長壽命達30 a,通常被用于衰老相關行為、神經和生理方面的研究[30]。
馴化物種例如犬和貓也是一種獨特的衰老模型。其中,犬的壽命多為10~12 a,會自發地發展出許多衰老有關的表型,如肌肉和神經功能的衰退,以及心血管疾病[31],因此,犬多被用于認知惡化和年齡相關神經退行性疾病的研究[32]。家貓壽命為12~14 a,正常生長過程中易發展衰老相關疾病,包括腎臟疾病、關節炎、肌少癥和神經功能衰退等,因此也常被用做衰老模型[33-34]。
從理論上講,非人類靈長類動物是研究衰老和年齡相關疾病最合適的模型,其中恒河猴(Macacamulatta)一直是研究衰老的主要模型,因為其與人類在遺傳學、內分泌學、生理學、神經解剖學和認知功能等方面極為相近[35]。另外一種應用廣泛的非人類靈長類衰老模型是狨猴(Callithrixjacchus),它壽命短且體型較小,并且表現出一些與人類相似的衰老相關疾病,例如神經系統疾病、癌癥和糖尿病等[36]。此外,灰鼠狐猴(Microcebusmurinus)常用做飲食限制衰老模型,常用于長期的飲食限制及抗衰老藥物的篩選研究[37]。
3 Wnt信號通路
Wnt蛋白家族包括以下成員Wnt1、Wnt2、Wnt2B、Wnt3、Wnt3A、Wnt4、Wnt5A、Wnt5B、Wnt6、Wnt7A、Wnt7B、Wnt8A、Wnt8B、Wnt9A、Wnt9B、Wnt10A、Wnt10B、Wnt11和Wnt16[38]。Wnt信號分子借助7次跨膜受體蛋白Frizzled家族蛋白和單次跨膜的輔助受體LRP5/6或ROR1/2共同作用,進而激活下游的經典或非經典Wnt信號通路[39]。
經典Wnt信號通路是Wnt通過與Frizzled和LRP5/6受體作用,進而導致胞質破壞復合體[復合體包括糖原合成酶激酶3β(glycogen synthase kinase-3β,GSK3β)、Axin和APC]解聚,抑制GSK3β對β-catenin的磷酸化降解,使β-catenin處于穩定狀態,并由胞質進入細胞核,促進β-catenin依賴的受體T細胞因子/淋巴細胞增強-結合因子(TCF/LEF)下游靶基因的轉錄(Wnt/β-catenin信號通路)[40];同時抑制β-catenin非依賴的FOXM1、NRF2、YAP和其他蛋白質的表達(Wnt/穩定蛋白信號通路)[41]。相反地,非經典Wnt信號通路是通過Frizzled或ROR受體激活Dishevelled依賴的Rho-ROCK和Rac-JNK級聯反應(Wnt/PCP信號通路)[42];G蛋白依賴的鈣通道蛋白-NFAT、CAMK2-NLK和PKC級聯反應(Wnt/G蛋白偶聯受體信號通路)[43]。
Wnt信號調控細胞自我更新、代謝、存活、增殖及上皮間充質轉化[44-46],此外還與FGF、Hedgehog、Notch及TGF-β信號通路之間有交互作用(Crosstalk)[47-49]。最新研究發現Wnt信號通路在細胞衰老及衰老相關疾病中發揮著至關重要的作用。
4 Wnt信號通路在衰老相關疾病中的調控作用
衰老是人類主要疾病包括糖尿病、神經退行性疾病、心血管疾病和癌癥的主要誘因。利用衰老模型研究發現,Wnt信號通路在衰老過程中發揮著關鍵的調控作用(見圖1)。
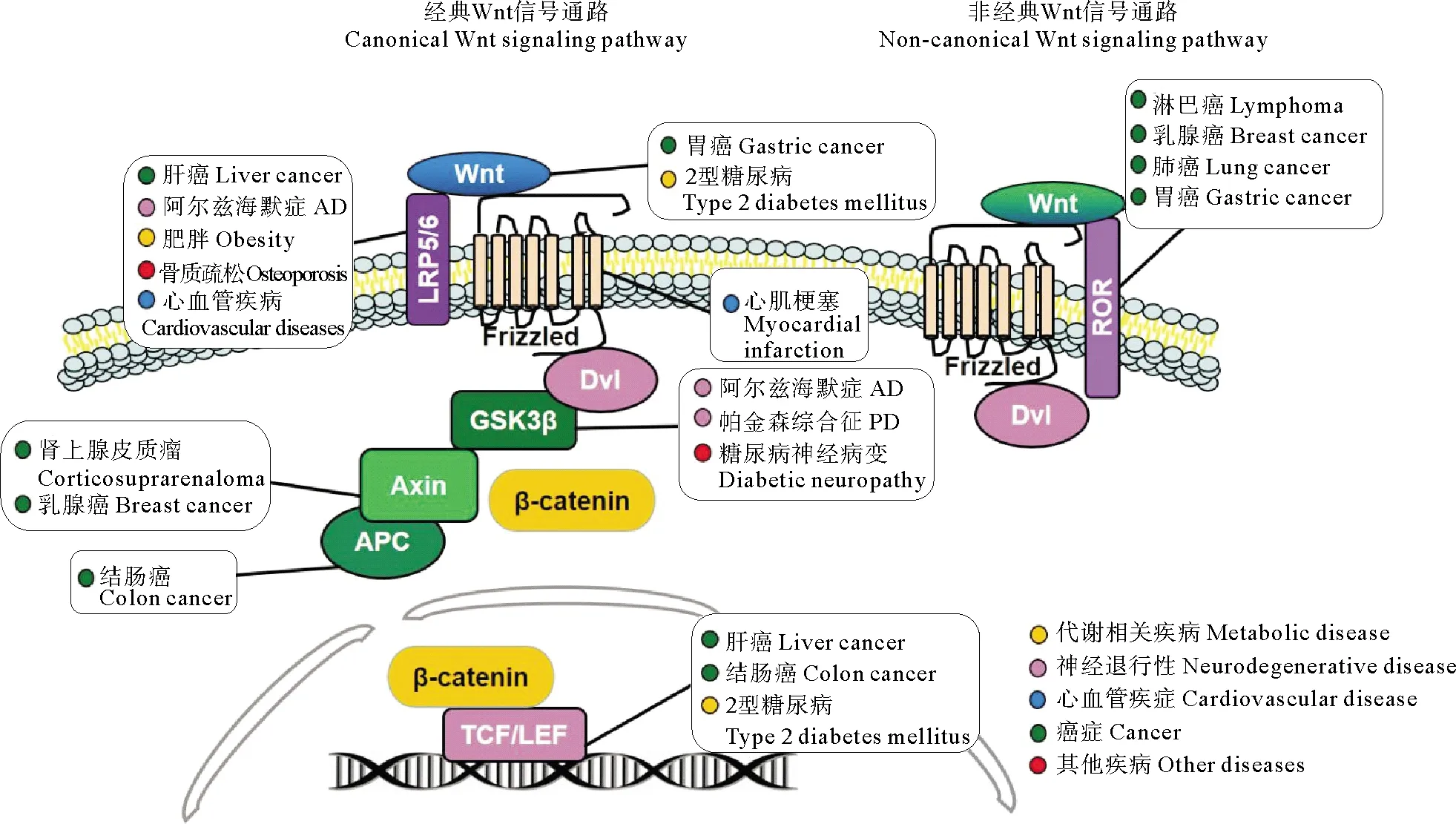
圖1 Wnt信號通路及與其相關的衰老疾病
4.1 2型糖尿病
全世界確診的糖尿病患者共有4億多人,預計到2035年將超過5億人,這種快速增長主要歸因于衰老、不健康的飲食、缺乏運動、超重和肥胖[50]。在衰老的過程中,糖耐量受到損害,并表現出一些明顯的糖尿病特征,如餐后高血糖[51]。研究表明,Wnt信號通路參與胰腺β細胞增殖、脂質代謝和葡萄糖誘導的胰島素分泌過程[52-53]。研究還發現,Wnt5B基因單核苷酸發生變異與2型糖尿病有關[54]。此外,Wnt通路在糖尿病神經病變中也起到重要作用,例如,GSK3β與糖尿病神經病變受試者中胰島素受體磷酸化水平升高之間具有相關性[55]。經典Wnt信號通路與糖尿病腎病的發生也存在聯系[56]。這些研究共同指出了Wnt信號在糖尿病病理生理學中的重要性。因此,Wnt信號通路有望成為治療該類疾病的有效作用靶點。
4.2 神經退行性疾病
神經退行性疾病的特征是動態和進行性神經元細胞損傷和神經元丟失,典型的疾病主要是阿爾茲海默癥(Alzheimer disease, AD)和帕金森綜合征(Parkinson’s disease,PD)。
4.2.1 阿爾茲海默癥 AD是一種常見的年齡相關神經退行性疾病,其主要特征是:淀粉樣β肽在細胞外積累形成老年斑;神經元纏結(主要是由高度磷酸化的tau蛋白組成)[57]。Wnt信號通路是中樞神經系統發育的基礎,與AD發病機制密切相關[58]。該信號通路在成人大腦中起著重要作用,此外還參與調節突觸可塑性和記憶過程[59]。已有大量的AD動物模型和臨床研究顯示AD疾病中的Wnt信號通路是被破壞的,例如,LRP6單核苷酸多態性與遲發性AD有關,因此LRP6被視為AD的易感基因[60]。最新研究發現,與年齡匹配的對照相比,Wnt活性缺失的AD患者中,β-catenin水平下降,他們的腦皮質中GSK3β磷酸化水平上升[61]。另外,研究還發現Wnt抑制劑因子Dickkopf-1(DKK1)也與AD有關。當AD腦中的DDK-1活性增加,致使Wnt信號被抑制,進而會導致認知能力的下降[62]。此外,Wnt信號通路與tau蛋白磷酸化有關,研究發現GSK3β通過抑制Wnt介導tau的磷酸化[63]。
4.2.2 帕金森綜合征 PD是一種進展性的、不可治愈的和年齡相關的疾病,臨床特征主要表現為靜止性震顫、僵硬、姿勢不穩定、運動障礙并伴有認知障礙[64]。Wnt信號通路與PD發病機制相關,研究發現PD患者腦組織中的Wnt信號通路成分表達顯著下調[65]。體內研究結果證實,激活星形膠質細胞中的經典Wnt信號通路可以恢復受損中腦腹側的多巴胺神經元[66]。
4.3 心血管疾病
Wnt信號通路在心臟發育中發揮著至關重要的作用,Wnt的失調會導致一系列心臟和血管疾病,特別是心血管疾病[67]。研究發現,LRP6基因突變是高血壓患者頸動脈狹窄的危險因素[68]。LRP5/6抑制因子DKK1在冠狀動脈患者和頸動脈斑塊患者的血漿和病變組織中顯著增加[69]。另外,DKK1在血小板中高表達以抑制內皮細胞中Wnt/β-catenin信號通路活性,進而導致內皮功能障礙[69]。還有研究發現Wnt5A與晚期動脈病變相關[70]。
4.4 癌癥
Wnt信號通路在癌癥的發展中起著復雜的作用,通常該通路中的關鍵分子的突變與腫瘤的相關過程有關,包括不可控的細胞增殖、上皮間充質轉化和轉移。結直腸癌中APC多出現突變,是一個有效的治療靶點,而APC蛋白則是經典Wnt信號通路中的破壞復合物的重要組分,表明Wnt信號通路在結直腸癌的發生發展中起著重要作用[71]。此外,研究發現靶向LRP5/6在治療腫瘤中取得顯著成果,例如,在前列腺癌中,Mesd能夠結合細胞膜上的LRP5/6,從而抑制LRP5/6與配體的結合及下游Wnt/β-catenin信號通路的激活,從而抑制癌細胞的增殖[72]。Niclosamide是另外一種靶向細胞膜上LRP6的抑制劑,能夠促進癌細胞的細胞凋亡[72]。有研究發現,Wnt5A在腫瘤細胞的代謝和炎癥中發揮重要作用[73]。當Wnt與受體結合后,β-catenin從胞質破壞復合體中釋放出來,進入細胞核,隨后與TCFs結合調控下游靶基因的轉錄[74]。其中,TCF4是TCL/LEF家族中研究最多的成員,既有腫瘤促進作用[75],也有腫瘤抑制作用[76],后來證實TCF4的矛盾作用是由其可變剪接造成的[77]。另外一個與癌癥相關的Wnt信號通路分子是PTK7,它是一種孤兒受體(Orphan receptor),研究證實它與多種癌癥相關,并且可以作為癌癥中顯著上調的分子標記物[78]。
5 結語
Wnt信號通路在衰老及相關疾病中發揮著重要作用。衰老的過程非常復雜,Wnt信號通路并非是左右細胞衰老和衰老相關疾病的唯一信號通路。但對于某些衰老相關疾病來說,干預Wnt信號通路可能是比較新穎且有效的策略。研究已證實,激活經典的Wnt通路對2型糖尿病、阿爾茨海默病和帕金森綜合征的病理生理過程均有積極影響,這為針對Wnt信號通路開發抗衰老及治療衰老相關疾病的藥物或提供新的治療方案具有重要意義。此外,利用衰老模型能夠更好地模擬人類衰老的生理過程以及衰老相關病變,并為開發和篩選靶向藥物治療衰老及相關疾病提供理論支撐。水生動物作為最大且最多樣化的脊椎動物群,已經成為人類發育、行為、遺傳學等領域理想的研究模型。因此,水生動物作為衰老模型所表現出的巨大潛力,勢必將會成為該領域研究的熱點。

