基于區塊鏈的臨床試驗研究
鹿 達 陳福興 蘇文山
(第二軍醫大學 上海 200433)
1 引言
臨床試驗是藥物研發的重要環節,是保障藥物療效和安全性的重要手段。臨床試驗數據再現、數據共享、隱私保護以及受試者管理是當前臨床試驗研究過程中面臨的重要問題[1-2]。近年來國內外發生多起臨床試驗造假事件,其中包括人為數據操控、選擇性發表、設計和操作缺陷等,不僅誤導相關學術研究工作,還會造成公眾對醫學科研有效性的質疑。區塊鏈是一種新興技術,2014年卡萊爾首次提出在臨床試驗方案中使用區塊鏈來提高透明度和可信度的方法,為區塊鏈技術在臨床試驗領域的應用提供重要思路[3]。區塊鏈技術能夠改進臨床試驗研究的基礎技術,研究人員之間、研究人員和受試者之間更加透明,從而提高臨床試驗的可信度。在臨床試驗中通過區塊鏈技術形成一個點對點(Peer-to-Peer, P2P)的網絡,安全記錄臨床試驗中發生的數據交互,實現數據共享,試驗數據透明且不可更改。本文將闡述以私有鏈為基礎的區塊鏈技術在臨床試驗數據公開、知情同意簽署、隱私保護、試驗過程監管等方面的應用模式,旨在提高臨床試驗的規范性和可信性[4-7]。
2 目前臨床試驗存在的主要問題
2.1 數據缺乏可信性
近年來國內外多起以數據造假和選擇性發表為主的臨床試驗造假事件引發公眾對臨床試驗的偏見[8-11]。2014年7月《科學》(Science)雜志報道日本學者在抗高血壓藥物Diovan臨床試驗中的數據造假[12]。數據的完整性、規范性、真實性是臨床試驗的基本要求,完整性和規范性方面的問題主要是部分臨床數據缺失,不足以做出有效性和安全性的判斷,而真實性問題則涉及造假,包括編造、篡改、瞞報數據及原始數據無法溯源等。2018年7月我國市場監督管理總局頒布《藥物臨床試驗質量管理規范》,進一步規范臨床試驗過程,細化申辦者、試驗機構、藥監部門在臨床試驗質量監管中的任務和責任,但是人為管理手段并未消除數據造假隱患。
2.2 知情同意過程不規范
臨床試驗和醫學科學進步離不開患者參與,然而在以往的臨床試驗中知情同意過程并不嚴謹,部分參與臨床試驗患者對試驗過程、內容并不清楚[13-15]。美國食品藥品管理局(Food and Drug Administration, FDA)在研究報告中指出有近10%的試驗在執行知情同意過程中存在隨意擴大信息獲取范圍、私自修改知情同意書等缺陷[16]。2016年1月法國一項新藥物(BIA 10-247)臨床試驗在部分受試者出現神經并發癥后并沒有征求再次同意就進行接下來的試驗,造成1名受試者死亡、5名受試者出現神經并發癥[17]。赫爾辛基宣言第25條至32條規定參與臨床試驗必須獲得受試者同意,研究人員要將臨床試驗目的、方法、風險等內容告知。在實際操作中受試患者群體龐大,IV期臨床試驗對象要大于2 000例,獲取知情同意工作量較大,并且知情同意工作不是一次性而是反復的循環過程。因此亟需通過一種新的方法來提高臨床試驗知情同意工作效率。
2.3 試驗方案執行不嚴格
臨床試驗應當嚴格遵照前期制定的方案和計劃,然而在實際中許多臨床試驗開展未能滿足方案要求。有學者回顧分析北京大學人民醫院藥物臨床試驗數據核查情況,在17個現場核驗項目中違背臨床試驗方案的有8項。對北京市2008-2012年36家臨床試驗機構的243次臨床試驗的核查中發現31.7%違背試驗方案,占問題總數的35.5%,包括受試者不符合準入標準、試驗操作遺漏或不符合要求[18-19]。
3 區塊鏈技術在臨床試驗中的應用探討
3.1 概述
區塊鏈依據去中心化的程度不同分為公有鏈、私有鏈和聯盟鏈,私有鏈相比公共鏈更易于管理用戶和數據。對于臨床試驗數據,僅對授權用戶可見是最理想的,每個臨床試驗可以根據其協議制定不同規定,每家醫院也可以根據政策制定不同規定。因此在臨床試驗中更適合使用私有鏈系統來提高安全性和提供更便捷的監管。
3.2 提高試驗數據可信度
區塊鏈技術確保臨床試驗過程按照正確時間順序進行,每個區塊鏈交易都被蓋上時間戳。每次信息產生和交互都進行加密,確保數據完整性,限制數據偽造、美化等行為發生。在臨床試驗開始前,研究組織方需要將臨床試驗方案,包括研究類型、期望得到的主要和次要結果以及納入和排除標準等記錄在區塊鏈上,臨床試驗的時間計劃和數據集也應當公開。整個臨床試驗過程的每次信息產生與接收都記錄在區塊鏈上并加蓋時間戳,有助于避免與數據不可監控相關的臨床試驗典型問題,如選擇性報告結果、漏報(隱瞞)不顯著結果等,見表1。

表1 區塊鏈技術用于提高數據可信性
3.3 規范知情同意流程
3.3.1 基于區塊鏈技術的知情同意過程 知情同意收集是一項動態、多次的持續性工作。為保護患者權益,每次試驗方案修改或發生特殊情況,如發現新的風險等,都應再次征求受試者同意。知情同意書需要患者親自簽署并注明日期,重復征求患者同意較為繁瑣,應以一種安全、不可偽造、可驗證的方式儲存知情同意書并實時共享知情同意信息,同時要跟蹤患者以便于及時聯系,利用區塊鏈技術能夠較好地解決該問題。在基于區塊鏈技術的知情同意過程中,每名受試者具有一個私鑰以實現類似紙質同意書簽名的功能,簽署日期會自動記錄在區塊中。研究人員向受試者發送電子郵件,其中包含一個Web超鏈接,將受試者鏈接到知情同意書的界面。受試者只需點擊同意按鈕就可在區塊鏈上完成簽名并蓋上時間戳。每次協議更新時,調查人員都會發送電子郵件,解釋發生的變化并征求患者意見,簽署修改后的同意書。該過程每一步都會同步到研究人員,只有顯示同意狀態的患者才能繼續進行下一階段的臨床試驗,見圖1。
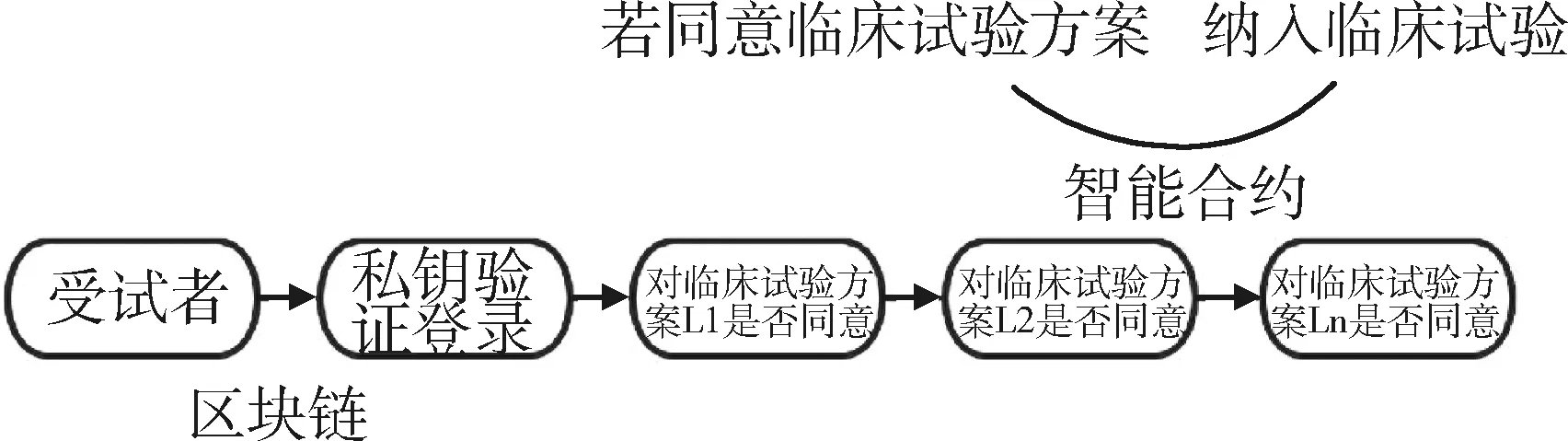
圖1 知情同意過程區塊鏈工作流程
3.3.2 患者端強身份認證功能 在實際應用中郵件驗證雖然便捷但安全性和可靠性不足,確認身份在這一過程中尤為關鍵。可以借鑒金融行業引入類似于“了解客戶”(Know Your Customer,KYC)規則,充分了解受試患者信息以提高驗證的安全性和可靠性,或使用如USB密鑰之類的實體對象實現安全認證接入。面部和指紋識別也是可選擇的安全認證方式[16]。
3.4 開展差異化隱私管理
臨床試驗應做好患者隱私保護工作,然而中心化的數據庫一直存在患者隱私安全隱患。區塊鏈技術從技術層面提高患者隱私保護力度,區塊鏈數據庫中臨床試驗數據的調用需要驗證,驗證過程使用密鑰,每個用戶都有一個由公鑰和私鑰組成的唯一密鑰對。公鑰類似于區塊鏈系統中的用戶ID,因此沒有區塊鏈節點(臨床站點)能夠識別患者身份。私鑰類似于用戶簽名。每個操作被發送到受試患者的公鑰并由發送方的私鑰進行數字簽名。接收方需要通過檢查公鑰是否與發送方的數字簽名匹配來驗證發送方身份。當臨床試驗發起者希望獲取受試者數據進行持續監測時,臨床試驗管理部門需要驗證試驗發起者身份,區塊鏈可以幫助試驗管理部門驗證其公鑰和私鑰是否匹配,從而避免受試者信息外泄。
3.5 加強試驗過程管控
3.5.1 提高試驗數據來源和過程可信性 在區塊鏈系統上有一個編碼自動執行的計算機協議,即為智能合約。智能合約允許在沒有第3方的情況下進行可信交易,可利用智能合約來提高臨床試驗的規范性和可信性。由于每次臨床試驗數據的產生都記錄在區塊內部,智能合約只接受直接從臨床試驗站點發送的數據,其他數據來源將被拒絕,確保數據的準確性。如果數據是偽造的,區塊鏈中每個后續用戶都可以檢測到數據不是直接從臨床試驗站點發送的,該信息將不被接受。除在區塊鏈上歸檔臨床試驗階段產生的數據外,還可將不同的臨床試驗步驟鏈接在一起,使每一步都依賴于前一步。區塊鏈技術具有實現這些片段和鏈接過程的工具,進一步減少人為誤差的發生。
3.5.2 提高大批量受試者數據收集準確性區塊鏈技術 用于臨床試驗的最大優勢在于試驗發起者和監管部門可實時接收來自不同受試者的原始數據。鑒于區塊鏈技術不能與區塊鏈系統以外的數據庫通信,可依托遠程過程調用(Remote Procedure Call, RPC)服務器連接到不同臨床站點和受試者。RPC服務器上的程序能夠使用智能合約,收到來自智能合約的請求后,收集受試者醫療信息并將所需數據推送回智能合約。這一功能對于 IV期臨床試驗尤為重要。IV期臨床試驗受試者數量大,該階段不需要招募新的受試者,但需要從已經服用新藥或治療的患者了解不良事件的最新情況。試驗發起者和監管部門能夠通過該技術持續監測受試者并及時通知需要召回的受試者[20]。
4 結語
區塊鏈技術是臨床試驗的一個重要突破,可以幫助構建更透明、可驗證的方法驗證臨床試驗的完整性、透明性和準確性。未來通過將數據分析軟件與智能合約集成起來分析分布式數據,能夠提高臨床試驗和決策支持的效率。此外整合患者生成的物聯網數據,如智能穿戴設備、家庭護理設備數據,添加人工智能組件,實時監測受試患者身體指標,有利于準確完成臨床試驗。

