舒洛地特對2型糖尿病伴慢性阻塞性肺疾病患者血液高凝狀態和血管內皮功能的影響
李紅梅,曹向輝,鞠 陽,郭同蘭
2型糖尿病(T2DM)、慢性阻塞性肺疾病(COPD)均為老年人群常發疾病,其發病率隨著我國環境改變、飲食結構變化、社會節奏加快不斷增多,且近年來T2DM伴COPD比例變大,兩者相互影響,病情復雜,增加了治療難度,預后差[1-2]。COPD以氣體受限為典型特征,易引發缺氧、電解質失衡等現象,造成機體血液高凝。T2DM患者也存在血液高凝、血管內皮損傷情況,隨病情加重可能造凝血-纖溶系統失衡,引發血栓[3]。T2DM被發現能導致肺臟微血管病變[4],可見加強T2DM伴COPD患者凝血功能檢測至關重要。舒洛地特為新型低分子肝素類藥物,用于糖尿病腎病(DN)治療相關報道較多[5-6],但國內關于其對T2DM伴COPD患者的報道較少。本研究回顧性分析了135例T2DM伴COPD患者的相關資料,探討了舒洛地特對T2DM伴COPD血液高凝狀態及血管內皮功能的影響,旨在為臨床治療提供參考。現報告如下。
1 資料與方法
1.1一般資料 選擇本院2017年1月—2019年12月就診的T2DM伴COPD患者135例。①納入標準:均符合T2DM、COPD相關診斷標準[7-8];年齡40~80歲;均配合完成用藥方案;臨床資料完整;對本研究知情并簽署同意書。②排除標準:肝腎功能不全、心力衰竭、惡性腫瘤者,合并其他器官相關感染者,肺栓塞、肺膿腫、肺結核者;近半個月內有抗凝藥物干預者;對舒洛地特過敏者。本研究經醫院倫理委員會批準。男78例,女57例;年齡(67.14±6.30)歲;T2DM病程6~23(12.64±4.02)年;有吸煙史63例。根據治療方法分為觀察組68例與對照組67例。2組性別、年齡、病程比較差異無統計學意義(P>0.05),具有可比性。
1.2治療方法 對照組入院后接受病史詢問及相關醫技檢查(如血常規、肺部X線、胸部CT等),行痰液的病原體培養、藥敏試驗,根據結果選擇合適的抗感染藥物,同時給予降血糖、糖皮質激素、電解質紊亂糾正等綜合治療。觀察組在對照組基礎上加用舒洛地特軟膠囊(意大利阿爾法韋士曼制藥公司,注冊證號H20140119)1粒,早、晚口服。連續用藥2個月。
1.3觀察指標及方法
1.3.1血液相關指標:2組分別于治療前、治療2個月后抽取空腹外周肘靜脈血送檢。①血糖相關指標:空腹血糖(FBG)、餐后2 h血糖(2 h PG)、糖化血紅蛋白(HbA1c),其中FBG、2 h PG采取己糖激酶法測定,HbA1c采用高效液相層析法測定。②凝血功能指標:部分凝血活酶時間(APTT)、纖維蛋白原(FIB)、D-二聚體(D-D),經由美國ACLTOP 300全自動血凝分析儀測定。③炎性因子指標:以酶聯免疫吸附法測定超敏C反應蛋白(hs-CRP)、白介素-6(IL-6)、腫瘤壞死因子-α(TNF-α)水平,試劑盒購自上海賽默科技生物發展有限公司。
1.3.2非內皮依賴性血管舒張功能(NMD)、肱動脈血流介導內皮依賴性血管舒張功能(FMD)測定:2組分別于治療前、治療2個月后通過二維超聲對2組NMD、FMD測定。操作步驟:邁瑞DC-N2S彩色超聲多普勒診斷儀超聲探頭放在患者肘窩上方5 cm左右處,對肱動脈長軸二維圖像獲取,截取最大肱動脈內徑與最佳直線狀動脈壁血液界面,之后檢查中保留儀器條件不改變。基礎肱動脈內徑測定后將血壓計綁在患者肘下,加壓到200 mmHg,240 s后快速放壓,放氣60~90 s內對肱動脈內徑檢測。休息10~20 min,等內徑恢復到基礎值后讓患者舌下含服硝酸甘油0.5 mg,對180~300 s內肱動脈最大內徑測定。經硝酸甘油介導/反應充血后肱動脈內徑比基礎肱動脈內徑變化百分比用NMD、FMD表示。
1.3.3不良反應:統計2組用藥期間有無低血糖、胃腸道不適等。
1.4療效判定標準 顯效:治療后咳嗽、喘息等癥狀及體征基本消失,X線片顯示肺部炎癥大多數被吸收,痰細菌培養為陰性。好轉:治療后咳嗽等癥狀及體征明顯緩解,X線片顯示肺部炎癥部分吸收,細菌培養為陰性。無效:治療后咳嗽等癥狀及體征不變或加重,X線片顯示肺部炎癥變化不大或加重。總有效率=(顯效+好轉)/總例數×100%。
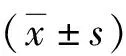
2 結果
2.1療效比較 2組治療總有效率比較差異無統計學意義(P>0.05)。見表1。

表1 2組T2DM伴COPD患者治療效果比較[例(%)]
2.2血糖相關指標比較 2組治療前的FBG、2 h PG、HbA1c比較差異均無統計學意義(P>0.05);2組治療后FBG、2 h PG、HbA1c水平均較治療前顯著下降,且觀察組低于對照組(P<0.05)。見表2。
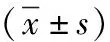
表2 2組T2DM伴COPD患者治療前后血糖相關指標比較
2.3凝血功能比較 2組治療前APTT、FIB、D-D水平比較差異無統計學意義(P>0.05)。與治療前比較,2組治療后APTT明顯延長,FIB、D-D水平明顯降低,且觀察組上述指標變化更顯著(P<0.05)。見表3。
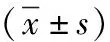
表3 2組T2DM伴COPD患者治療前后凝血功能相關指標比較
2.4炎性因子比較 2組治療前hs-CRP、IL-6、TNF-α水平比較差異無統計學意義(P>0.05)。與治療前相比,2治療后hs-CRP、IL-6、TNF-α水平均降低,且觀察組低于對照組(P<0.05)。見表4。
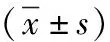
表4 2組T2DM伴COPD患者治療前后炎性因子比較
2.5血管內皮功能比較 2組治療前NMD、FMD比較差異均無統計學意義(P>0.05)。與治療前相比,2組治療后NMD、FMD均顯著上升,且觀察組高于對照組(P<0.05)。見表5。

表5 2組T2DM伴COPD患者治療前后血管內皮功能指標比較
2.6不良反應比較 2組用藥期間均未發生低血糖、胃腸道不適等癥狀。
3 討論
T2DM伴COPD患者機體免疫功能明顯降低,血管內皮功能異常、血小板聚集等致使機體血液顯著高凝,易形成血栓,增加器官功能衰竭風險,嚴重威脅了患者的生命[9]。臨床常見凝血功能指標包括APTT、FIB、D-D等,其中APTT對內源性凝血系統反映,主要與凝血因子Ⅷ、Ⅸ、Ⅻ等有關;FIB在凝血過程中發揮重要作用,其水平高低可對血栓前狀態有效反映,FIB高水平被認為是血栓形成的危險因子之一;D-D為纖溶系統激活、降解纖維蛋白后最小片段,正常情況下機體凝血-纖溶系統動態平衡,保持機體D-D處于相對穩定狀態,一旦該平衡被打破,D-D水平則會上升。本研究結果顯示,與治療前比較,2組治療后APTT顯著延長,FIB、D-D水平顯著降低,且觀察組變化更顯著。提示舒洛地特能明顯改善患者血液高凝狀態;其對相關凝血因子有一定的抑制作用,尤其是X因子,通過抗凝血酶、肝素因子雙重作用抗血栓;舒洛地特還能有效抑制血小板聚集,可激活纖溶系統抗凝。動物實驗發現,舒洛地特對糖尿病大血管病變有一定保護作用,其可能機制為藥物促使血管內皮生長因子下降[10]。
段宇芬[11]研究發現DN患者采取利格列汀聯合舒洛地特治療能顯著降低血糖,提高FMD,但難以分辨是哪種藥物發揮作用。本研究結果顯示,與治療前比較,2組治療后NMD、FMD均顯著上升,且觀察組高于對照組。NMD、FMD分別對應肱動脈血流介導內皮依賴性血管舒張功能、硝酸甘油介導非內皮依賴性血管舒張功能。提示舒洛地特能夠顯著改善T2DM伴COPD患者血管內皮功能,這可能與舒洛地特具有抗炎免疫、降低血脂、抗凝、抗氧化等作用有關[12-15]。
文獻報道,炎癥反應參與了COPD血液高凝狀態形成過程[16-18]。T2DM屬于慢性炎性疾病,其發病與炎癥密切相關,T2DM伴COPD患者炎癥反應明顯增強[19]。hs-CRP為急性非特異性炎癥指標,正常生理條件下其血清水平較低,創傷、炎癥等發生時其水平顯著上升。IL-6通過對抗原誘導促進T淋巴細胞增殖,對局部免疫調節,同時能促進全身炎性因子釋放[20]。TNF-α對炎癥反應有一定的誘導作用,能促組織纖維化[21-22]。本研究結果顯示,與治療前相比,2組治療后hs-CRP、IL-6、TNF-α水平均顯著下降,且觀察組均低于對照組。提示舒洛地特能有效減輕炎癥反應。文哲瑤等[19]研究表明,舒洛地特可能通過對高糖誘導人視網膜微血管內皮細胞轉錄因子p-NF-κB p65、TNF-α、單核細胞趨化因子-1水平抑制達到治療目的。舒洛地特抗炎機制可能與其對補體活性抑制,降低CRP水平、保護細胞有關[23-24]。
本研究結果顯示,2組治療后FBG、2 h PG、HbA1c水平均較治療前顯著降低,且觀察組低于對照組;提示舒洛地特能進一步降低T2DM伴COPD患者的血糖水平,這可能與其抗凝、改善血管內皮功能、抑炎等作用有關。本研究結果同時顯示,2組COPD治療總有效率比較差異無統計學意義,這可能與COPD病情復雜、處于病程不同時期等有關,也可能與本研究樣本量小有關。薛寒[25]研究發現,常規基礎治療加以低分子肝素注射能明顯改善COPD急性發作合并T2DM患者的高凝狀態及肺部氧合功能,減輕其炎癥反應。舒洛地特含有低分子肝素、硫酸皮膚素等成分,可以通過不同的機制,協同增強抗凝作用;同時舒洛地特生物利用度高,耐受性強,值得臨床深入研究其作用,為臨床T2DM伴COPD治療提供方便。
綜上所述,舒洛地特能有效提高T2DM伴COPD的治療效果,有利于降低炎性因子、改善血液高凝狀態及血管內皮功能。

