咸蛋清蛋白酶解液美拉德反應條件優化及揮發性風味物質分析
羅章 辜雪冬 張玉鳳 黃群


[摘要]本研究以咸蛋清蛋白酶解液為原料,將其與葡萄糖進行美拉德反應,通過單因素試驗和正交試驗,對美拉德反應條件進行優化,并采用固相微萃取-氣相色譜-質譜聯用(SPME-GC-MS)分析美拉德反應進程中揮發性風味物質的變化。結果表明,美拉德反應最佳條件為葡萄糖添加量3.5%(w/v)、初始pH9.5、反應溫度110℃、反應時間60min。產物共檢測出61種揮發性成分,主要包括酚、羰基、酯、醇、烷烴及雜環化合物。當反應進行到60min時,產物中揮發性組分種類最多,風味濃郁純正。羰基、芳香族及烯類化合物可能與美拉德反應產物的香氣形成有密切關聯,酸類物質對美拉德產物香氣形成貢獻較小或參與不良風味形成。
[關鍵詞]咸蛋清蛋白;美拉德反應;固相微萃取-氣相色譜-質譜聯用(SPME-GC-MS);揮發性風味物質
中圖分類號:TS201.2 文獻標識碼:A DOI:10.16465/j.gste.cn431252ts.202009
咸蛋作為中國傳統美食,備受消費者喜愛,但人們對咸蛋的利用往往集中在蛋黃部分,咸蛋的蛋黃因其特殊的風味和口感,常被用來制作粽子、月餅等糕點[1],而咸蛋清的價值并沒有得到充分的挖掘和利用。咸蛋清中含有卵白蛋白、伴白蛋白、卵球蛋白、卵黏蛋白、卵類黏蛋白和溶菌酶6種主要蛋白質,其生物價值高,極易被機體吸收利用[2]。目前的加工利用方式使得咸蛋清被作為廢物扔棄,既造成了蛋白質資源的極大浪費,又對環境造成嚴重污染[3]。采用生物酶解技術對動、植物蛋白進行酶解,以此來制備活性肽及游離氨基酸已成為綜合利用蛋白資源的重要手段[4]。
美拉德反應又稱為非酶促褐變反應、羰氨反應,是指羰基化合物與氨基化合物之間經過縮合、聚合最終生成類黑精的反應[5],廣泛存在于食品熱加工和貯藏過程中,可顯著影響食品的香氣、滋味、色澤、穩定性及營養價值[6]。蛋白質酶解產物(肽、游離氨基酸)是美拉德反應的重要前體物,通過肽糖交聯等方式參與反應[7]。目前主要以海鮮類(牡蠣,淡水魚,螃蟹等)、花生粕、大豆、小麥等[8-13]為蛋白質原料進行美拉德反應,而用咸蛋清蛋白酶解液進行美拉德反應的相關報道極少。
本研究以咸蛋清蛋白酶解液為原料與葡萄糖進行美拉德反應,通過單因素和正交試驗,以感官評分和褐變程度為指標,對美拉德反應條件進行優化,采用固相微萃取-氣相色譜-質譜聯用(SPME-GC-MS)分析美拉德反應過程中揮發性物質的變化,以此來研究反應產物中香味的成分,并為咸蛋清的高效利用提供相應的試驗參考和理論依據。
1 材料與方法
1.1 試驗材料
咸蛋:光陽蛋業;風味蛋白酶:江蘇銳陽生物科技有限公司;NaOH、HCl、葡萄糖等均為國產分析純。
1.2 試驗儀器
7890A-5975C型氣相色譜-質譜聯用儀:美國安捷倫公司;SPME手動進樣裝置:美國Supelco公司;HH-S2型恒溫水浴鍋:金壇區成輝儀器廠;pHS-25型pH計:上海精密科學儀器有限公司;FA2004型電子天平:上海舜宇恒平科學儀器有限公司;LXJ-IIB型離心機:上海安亭科學儀器廠;101-2AB型電熱鼓風干燥箱:天津市泰斯特儀器有限公司;722E型可見分光光度計:上海光譜儀器有限公司。
1.3 試驗方法
1.3.1 咸蛋清酶解液的制備工藝流程
取咸蛋清→過濾→稀釋(咸蛋清與去離子水的體積比為1∶5)→調節pH(1mol/L NaOH、HCl)→加熱預處理→加酶(風味蛋白酶)[14]恒溫水浴酶解(7h,55℃)→滅酶(沸水浴,15min)→冷卻后離心 (4 500r/min,10min)→取上清液→制得咸蛋清蛋白酶解液。
1.3.2 咸蛋清酶解液美拉德反應及其產物測定
取20mL上述制得的咸蛋清蛋白酶解液,調節pH(1mol/L NaOH、HCl),加入葡萄糖,使其發生美拉德反應,并對其產物進行測定。
由經過培訓后具有感官評價基礎的10名(5女,5男)食品專業學生組建感官評價小組,分別從氣味、滋味、外觀三個方面對美拉德反應的產物逐一評價打分,取其平均值作為最后評分結果。將美拉德反應液稀釋50倍,以蒸餾水為參照,使用可見分光光度計在420nm波長下測其吸光值,以此測定美拉德反應的褐變程度[15]。參照孫紅梅等[16]對美拉德反應產物的感官要求,并做適當的修改,制作出美拉德反應產物的感官評分標準,見表1。
1.3.3 美拉德反應條件優化
分別研究美拉德反應時間、反應溫度、葡萄糖添加量和酶解液初始pH這四個單因素對美拉德反應的影響。反應時間分別取20min、40min、60min、80min、100min、120min;反應溫度分別取90℃、100℃、110℃、120℃、130℃、140℃;葡萄糖添加量分別取0.5%(w/v)、1.5%(w/v)、2.5%(w/v)、3.5%(w/v)、4.5%(w/v)、5.5%(w/v);酶解液初始pH分別取5.0、6.0、7.0、8.0、9.0、10.0、11.0。
利用單因素試驗的最佳值,在此基礎上進行四因素三水平L9(34)正交試驗,確定美拉德反應的最優工藝參數,并對最優工藝參數進行重復試驗,以確保結果的準確性。
1.3.4 SPME-GC-MS對美拉德反應產物分析
固相微萃取條件:萃取纖維在GC進樣口250℃老化20min,將5mL美拉德反應產物裝入15mL萃取瓶,于80℃恒溫水浴鍋中平衡10min,然后將SPME進樣器通過瓶蓋橡皮墊插入瓶中,推出纖維頭,吸附1h,隨即插入GC-MS進樣口250℃解析5min,進行GC-MS分析。
GC條件:色譜柱為HP-5MS毛細管柱,30m×0.25um×0.25mm,325℃;以高純He為載氣,流速為1.0mL/min。升溫程序:初始柱溫35℃,保持5min;以4℃/min升溫至210℃,保持5min;再以5℃/min升溫至220℃(不保持);進樣口溫度250℃。
MS條件:離子源溫度230℃,電離方式EI,電子能量70EV,掃描質量范圍35~400amu。
利用計算機檢索NIST 11譜庫,比較樣品與標準質譜庫的質譜數據,匹配樣品中各未知揮發性成分,選擇與色譜峰匹配度較高(≥80)的化合物,加以人工解析譜圖,采用峰面積歸一化法來確定美拉德反應物的相對含量。
2 結果與分析
2.1 單因素試驗分析
2.1.1 反應時間對美拉德反應的影響
控制反應溫度為110℃,酶解液初始pH為9.0,葡萄糖添加量為3.5%(w/v),考查反應時間對美拉德反應的影響,結果見圖1。
由圖1可知,隨著反應時間的延長,A420呈現先急劇后變緩的增長趨勢。反應時間為100min時,A420基本趨于平穩狀態,其原因可能是美拉德反應進行到100min,此時該反應已處于終止階段,褐變程度也達到最大值[17];隨著反應時間的不斷延長,體系中水分大量損失,導致產物的濃度不斷增高[18]。反應時間為60min時,感官評分最高,而反應時間達到100min后,則會呈現出令人不悅的深褐色及焦苦味,感官評分值明顯降低。綜合考慮,美拉德反應時間為60min較合適。
2.1.2 反應溫度對美拉德反應的影響
控制反應時間為60min,酶解液初始pH為9.0,葡萄糖添加量為3.5%(w/v),考查反應溫度對美拉德反應的影響,結果見圖2。
溫度是影響美拉德反應的重要因素之一,溫度升高會加速美拉德反應,但當溫度過高時,會產生較強的異味;溫度過低,則會導致反應程度不夠,香氣不夠濃郁[19-20]。因此合適的溫度對于美拉德反應尤為重要。由圖2可知,隨著反應溫度的升高,其褐變程度逐漸增加。反應溫度較低時,產物中蛋腥味較濃;溫度過高時,焦苦味較明顯;當反應溫度為110℃時,產物中香味最濃郁,感官評分最高。此結論與韓科研等[21]所報道的美拉德反應的最佳溫度為115℃相接近。因此,綜合褐變程度及感官評分結果,將110℃設為美拉德反應的適宜溫度。
2.1.3 葡萄糖添加量對美拉德反應的影響
控制反應溫度為110℃,反應時間為60min,酶解液初始pH為9.0,考查葡萄糖添加量對美拉德反應的影響,結果見圖3。
葡萄糖是參與美拉德反應最常見的還原糖之一,當氨基酸添加量一定時,增加還原糖的用量有助于促進美拉德反應。由圖3可知,在低濃度范圍內,隨著葡萄糖添加量的增加,反應逐漸劇烈,其褐變程度增長較快;但當葡萄糖的添加量高于4.5%時,A420幾乎不變,其原因可能是反應體系中氨基酸態氮消耗殆盡,美拉德反應達到平衡[22]。隨著美拉德反應的持續進行,具有香味的小分子物質不斷形成,與此同時,這些小分子物質又隨反應程度的不斷加深環化成大分子物質,使得香味維持動態平衡甚至減弱[23]。因此,當葡萄糖添加量超過3.5%后,反應產物中的大分子物質遮蓋了部分揮發性香味物質,使得產物帶有焦糊苦味,感官評分值下降。綜上,選擇3.5%的葡萄糖添加量進行后續優化試驗。
2.1.4 酶解液初始pH對美拉德反應的影響
控制反應溫度為110℃,反應時間為60min,葡萄糖添加量為3.5%(w/v),考查酶解液初始pH對美拉德反應的影響,結果見圖4。
從圖4可知,隨著酶解液初始pH的增加,美拉德反應的褐變程度先緩慢增長;當pH>10.0時,其褐變程度急劇上升。其原因可能是,氨基在酸性條件下以-NH3+存在阻礙羰氨縮合,導致褐變程度不明顯;而在堿性條件下,氨基酸態氮被游離出來參與反應,堿性越高,反應越強烈[24]。當pH>9.0時,隨著反應的進行,其產物的顏色及香味物質會受到不同程度的影響,感官評分逐漸降低。因此,綜合考慮,美拉德反應的最適宜的酶解液初始pH為9.0。
2.2 美拉德反應正交試驗分析
以上述四個單因素試驗結果為基礎,可得到正交因素水平(見表2),利用L9(34)正交表進行正交試驗,結果見表3。
由表3的正交試驗結果可知,影響美拉德反應的因素有B(初始pH)>C(反應時間)>A(葡萄糖添加量)>D(反應溫度),并得到美拉德反應的最佳反應條件為B3C2A2D2,即酶解液初始pH 9.5、反應時間60min、葡萄糖添加量3.5%(w/v)、反應溫度110℃。在該條件下進行美拉德反應,感官評分值達到85,該分值是所有組合中最高的,此時測得A420為1.11,美拉德反應產物香味濃郁,色澤誘人,說明正交試驗優化所得結論較為合理。
2.3 美拉德反應產物揮發性物質分析
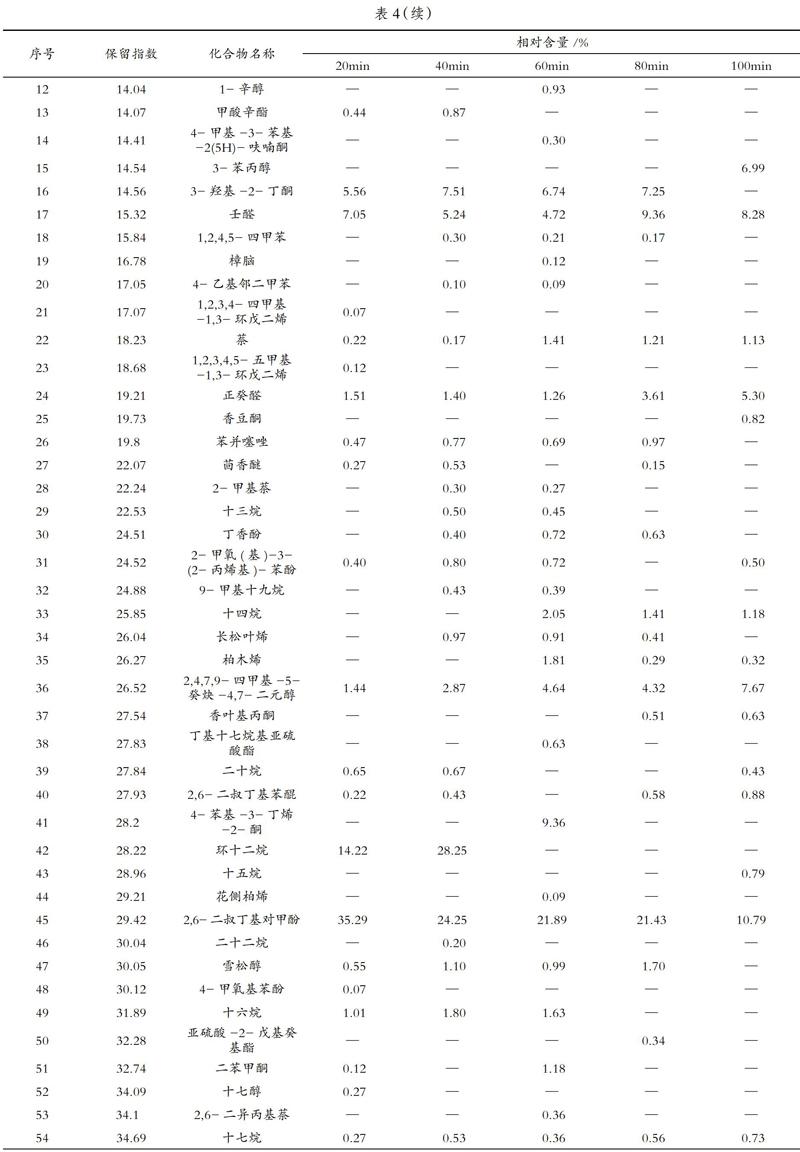
美拉德反應進行到不同時間,其揮發性產物通過固相微萃取并經GC-MS分析后,得到總離子流色譜圖見5~圖9,揮發性產物的種類及相對含量見表4。
由圖5~圖9及表4可知,在咸蛋清蛋白酶解液與葡萄糖進行美拉德反應的產物中共檢測出61種揮發性物質,主要有酚、羰基、酯、醇、烷烴及其他雜環化合物,還包括少量的烯、酸、醚類化合物。
反應進行到不同時間(20min、40min、60min、80min、100min),鑒定出的揮發性組分分別為30種、34種、41種、31種、26種,在60min時檢測到的揮發性物質種類最多,產物風味協調。因此,從揮發性成分的種類和相對含量來考慮,可以得出美拉德反應適宜的時間為60min,此結果與感官評定的結論一致。
2.4 美拉德反應過程中揮發性組分種類和含量分析
美拉德反應產物產香機理極為復雜,其產物特征香味的形成可能與閾值較低的醇、醛、酮和酯等簡單化合物及含硫、氧、氮原子等雜環化合物共同作用有關。美拉德反應在不同時間段中揮發性產物的比較見圖10。由圖10可知,在整個反應過程中,羰基、酯類和酚類化合物的含量較高,烯類、醚類及酸類等含量較低,醇類和雜環類化合物的相對含量變化不大;羰基、芳香族及烯類化合物的相對含量呈現出先上升后下降的趨勢,在60min時其含量達到最高,此結果與感官評定香氣的變化趨勢一致,由此可以推測,羰基、芳香族及烯類化合物可能對美拉德反應產物香氣的形成貢獻較大或與香氣的形成有密切關系。
在5個不同的時間段中均檢測出1,3-二甲基苯、甲氧基苯基肟、苯乙醛、苯乙酮、壬醛、正癸醛;反應進行到60min時,僅檢測到1-辛醇、4-甲基- 3-苯基-2(5H)-呋喃酮、4-苯基-3-丁烯-2-酮、樟腦。因此,上述所提及的揮發性物質極有可能共同參與了咸蛋清蛋白酶解液美拉德反應產物的特征香氣的形成。而僅在100min時檢測出了酸類化合物,說明十四酸或棕櫚油酸對美拉德反應產物香氣的形成貢獻較小,或極可能參與了異味的形成。
3 結 論
將咸蛋清蛋白酶解液與葡萄糖進行美拉德反應,并對反應條件行進優化,最終得到影響美拉德反應的主要因素有B(初始pH)>C(反應時間)>A(葡萄糖添加量)>D(反應溫度),由此可以確定美拉德反應最佳條件如下:初始pH 9.5、反應時間60min、葡萄糖添加量3.5%(w/v)、反應溫度110℃。在該條件下進行美拉德反應,感官評分值達到85,該分值是所有組合中最高的,即優化較為合理。
采用SPME-GC-MS分析美拉德反應進程中揮發性風味物質的變化,在其產物中共檢測出61種香氣組分,主要包括酚、羰基、酯、醇、烷烴及雜環化合物。反應60min時揮發性組分種類最多,產物的風味濃郁純正,此結果與感官評定香氣的變化趨勢一致。由此推測出,羰基、芳香族及烯類化合物可能與美拉德反應產物的香氣形成有密切關聯,酸類物質對美拉德產物香氣的形成貢獻較小或參與不良風味的形成。
參考文獻
[1]孔玲,張憨,劉亞萍,等.響應面優化咸蛋清酶解液工藝的研究[J].食品與生物技術學報,2017,36(11):1189-1196.
[2]李逢振.咸蛋清資源化綜合利用的研究[J].農產品加工,2020, 5(12):85-86.
[3]譚蘆蘭.蛋清凝膠性能改善及高纖維蛋片的制備研究[D].杭州:浙江工業大學,2020.
[4]王曉玲.咸蛋清蛋白酶解制備活性肽及其抗氧化、抗菌活性研究[D].武漢:華中農業大學,2010.
[5]王植,劉昊天,劉騫,等.美拉德反應及其產物在遞送生物活性物質方面的應用[J].食品科學.2020,7(22):95-100.
[6]李菁,劉騫,孔保華,等.L-賴氨酸與3種還原糖美拉德反應產物的理化特性及抗氧化活性[J].食品科學,2013,34(3): 80-85.
[7]劉平,張曉鳴.大豆肽-木糖美拉德反應體系中肽的降解與交聯規律研究[J].食品工業科技,2011,32(4):91-94.
[8]張滿,周亞軍,溫丑玉,等.不同因素對牡蠣酶解液美拉德反應產物的影響[J].食品與發酵工業,2019,45(22):190-195.
[9]余自琳,郭榮燦,姜毅,等.pH對墨魚酶解物美拉德反應產物風味的影響[J].食品工業科技,2018,39(15):274-280.
[10]劉佳夢,白苗,張邵鴻,等.細點圓趾蟹蟹肉酶解液制備美拉德型蟹風味料工藝優化[J].食品工藝科技,2019,40(10): 206-213.
[11]崔燕玲.花生粕深度降解及其降解產物的美拉德反應研究[D].廣州:廣州大學,2018.
[12]趙謀明,張佳男,吳長平,等.大豆肽的制備及其美拉德反應產物特性研究[J].現代食品科技,2015,31(2):138-144.
[13]劉麗婭,孫夢穎,王延州,等.小麥蛋白酶解物制備熱反應型肉香調味基料的研究[J].中國糧油學報,2013,5(6):63-68.
[14]萬麗娜,熊星星,羅巖,等.風味蛋白酶修飾蛋清酶解液的研究[J].食品工業,2013,34(6):105-108.
[15]王嬙.褐色風味發酵乳的研制及主要風味分析[D].沈陽:沈陽農業大學,2019.
[16]孫紅梅,王金枝,張春暉,等.應用模糊數學優化雞骨素美拉德反應工藝[J].中國食品學報,2014,14(6):74-80.
[17]Zora M C,Snezana B J.Sensory Evaluation and Microbiological Characterization of Autochthonous Sombor Cheese[J].Acta Veterinaria (Beograd),2008,58 (5-6):531-541.
[18]Mowlaeifarr M H,Aminlari M,Niakosari M,et al.Effect of Microwave Treatment on Glycation Extent of Lysozyme-Maltdextrin Maillard Conjugates[J].Journal of Food Science&Technology,2017,13(60):105-113.
[19]黃珊,王修俊,劉佳慧,等.貴州三穗鴨鴨骨酶解液美拉德反應條件優化及揮發性風味物質分析[J].中國釀造,2019, 38(9):117-123.
[20]Tan Z W,Yu A N.Volatiles from the Maillard Reaction of L-ascorbic Acid with L-glutamic Acid/L-Aspartic Acid at Different Reaction Times and Temperatures[J].Asia-Pacific Journal of Chemical Engineering,2012,7(4):563-571.
[21]韓科研,黃繼超,劉冬梅,等.鴨骨湯酶解液的美拉德反應條件優化[J].食品科學,2018,39(4):261-267.
[22]羅偉,段振華,劉小兵.貽貝煮汁酶解液美拉德反應條件優化及其產物氨基酸組成分析[J].食品科學,2014,35(24):40-44.
[23]童彥,雒莎莎,應鐵進.魚蛋白水解液美拉德反應條件優化及反應前后氨基酸組成變化[J].中國食品學報,2011,11(8): 101-106.
[24]Hwang I G,Kim H Y,Woo K S,et al.Biological Activities of Maillard Reaction Products (MRPs) in a Sugar-amino Acid Model System[J].Food Chemistry,2011,126(1):221-227.

