非水燃料電池例析
◇ 江蘇 邵曉華
燃料電池是一種通過電極反應直接將燃料的化學能轉化為電能的電化學裝置:燃料電池技術是繼水力、火力和核能之后的新一代發電技術.如將燃料和空氣分別送進燃料電池,中間不經過燃燒過程,燃料中化學能轉化為電能,就產生了電流.燃料電池中通入空氣的是正極,氧氣發生還原反應;通入燃料的是負極,發生氧化反應.非水燃料電池是以熔融金屬氧化物或碳酸鹽為電解質的燃料電池.
1 固態金屬氧化物燃料電池
固態金屬氧化物燃料電池以金屬氧化物為電解質,金屬氧化物中只能通過氧離子(O2-),O2在正極得到電子生成O2-,燃料在負極失去電子,結合O2-生成CO2和H2O.
例1直接煤—空氣燃料電池原理如圖1所示,下列說法錯誤的是( ).

圖1
A.隨著反應的進行,氧化物電解質的質量不斷減少
B.負極的電極反應式為
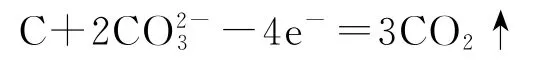
C.電極X為負極,O2-向X極遷移
D.直接煤—空氣燃料電池的能量效率比煤燃燒發電的能量效率高
分析燃料電池中O2是正極,得到電子生成O2-通過金屬氧化物電解質移向負極,燃料在負極失去電子結合O2-生成CO2和H2O.氧化物電解質的質量不會減少,在電極Y上O2得到電子生成O2-不斷再補充,選項A錯誤;由原理圖分析可知,其負極反應式為,選項B正確;原電池內部的陰離子向負極移動,選項C正確;直接煤—空氣燃料電池是把化學能直接轉化為電能,而煤燃燒發電是把化學能轉化為熱能,再轉化為電能,其中能量損耗較大,選項D正確.
2 熔融碳酸鹽燃料電池
熔融碳酸鹽燃料電池是一種以熔融碳酸鹽為電解質的燃料電池,電解質中可以通過,O2在正極得到電子生成O2-,再結合CO2生成,燃料在負極失去電子,生成CO2.
例2科學家設計的以熔融碳酸鹽為電解質,C4H10為燃料的電池工作原理如圖2,下列說法正確的是( ).

圖2
A.a為C4H10,b為CO2
C.此電池在常溫下也能工作
D.通入丁烷的一極是負極,電極反應式為
C4H10-26e-+13=17CO2↑+5 H2O
分析熔融碳酸鹽電解質中只允許通過,因此正極通入O2的同時還要通入CO2,使O2得到電子生成O2-,再結合CO2生成.燃料電池中通入燃料的電極是負極,通入氧化劑的電極是正極,根據電子流向,左邊電極是負極,右邊是正極,所以a為C4H10,b為O2,選項A錯誤;原電池放電時,陰離子移向負極,即向負極移動,選項B錯誤;碳酸鹽需要在高溫條件下才能熔化,選項C錯誤;通入丁烷的一極是負極,發生失電子的氧化反應,電極反應式為C4H10-26e-+13=17CO2↑+5 H2O,選項D正確.答案為D.
總之,非水燃料電池中一定要明確電解質中能通過什么離子,再確定正極O2得電子生成什么粒子,負極燃料失去電子生成什么粒子,同時要結合示意圖中物質轉化進行回答.

