對苯二胺縮對苯二甲醛席夫堿及其配合物的制備和電化學性能
李 倩 馬雪冬 王 偉,,2 張存社
(1長安大學,水利與環境學院化工系,西安 710054)
(2旱區地下水文與生態效應,教育部重點實驗室,西安 710054)
(3陜西省石油化工研究設計院,陜西省石油精細化學品重點實驗室,西安 710054)
能源問題是人類能否可持續發展的關鍵,隨著化石燃料的日益枯竭和全球變暖的日益加劇,發展可再生能源和能源儲存技術受到人們的關注。超級電容器也稱電化學電容器,是一種介于二次電池和物理電容器之間的儲能器件,具有充電/放電過程快、循環壽命長、功率密度高、環境友好、工作溫度范圍廣等特點而被廣泛地應用在電動汽車、太陽能發電、儲能電站、航空航天和軍事等諸多領域[1-4]。用作超級電容器的電極材料主要有多孔碳材料[5]、金屬氧化物[6]和導電聚合物3種類型[7]。導電聚合物主要有聚苯胺(PANI)、聚噻吩(PTh)以及聚吡咯(PPy),其中PANI的研究最為廣泛,主要采用化學氧化聚合法或電化學法合成。PTh[8]和PPy[9]通過摻雜或與其他無機材料雜化來獲得更好的導電性。但由于這類聚合物的循環性能較差,且制備時易受到制備方法、摻雜物質和模板等因素的影響,限制了這類導電聚合物的應用,因此探索新型穩定性高的導電聚合物目前是聚合物研究的熱點領域。
席夫堿是指含有亞胺或甲亞胺特性基團(-RC=N-)的一類有機化合物,由于席夫堿-C=N-基團的特性,席夫堿類材料具有光、電、磁、抗菌、抗癌、除草等性能[10-13]。其結構中N原子有孤對電子,能與金屬離子結合形成配位化合物,使其在醫學[14]、催化[15]、分析化學[16]、腐蝕[17]以及光致變色[18]等領域成為一類備選材料。近年來人們對席夫堿及席夫堿鹽的導電性能做了一些研究,已有多種類型的席夫堿高聚物相繼被報道。李春生[19]以對苯二胺為原料與4種不同的酮類縮聚合成了4種主鏈結構相同而取代基不同的共軛性聚席夫堿,并對本征態的共軛聚席夫堿進行碘摻雜,發現碘摻雜后電導率顯著提高。毛薇莉[20]采用縮合反應合成了共軛二茂鐵席夫堿配合物,用循環伏安法測試到一對氧化還原峰。宣芳[21]以2-氨基-8-羥基喹啉和二茂鐵甲醛為原料,合成了一種新型的二茂鐵席夫堿化合物,該化合物在半峰電位E1/2=0.245 V處出現了一對可逆的氧化還原峰,表明該氧化還原反應是可逆的。現有的研究著重于配位化合物的電催化性能,而作為導電聚合物的一類,席夫堿聚合物及其金屬配合物用作超級電容器電極材料的研究鮮有報道。Bhanja[22]和Li[23]合成了基于三嗪結構的席夫堿聚合物作為超級電容器的電極材料。這2種材料的電化學性能較為優異,但是合成過程復雜、參與反應的單體成本高都成為商業化生產的重要限制因素。目前,有關席夫堿配位聚合物的研究大都集中在聚Salphen型鎳席夫堿(Ni-Salphen)上,但是大多研究報道的聚Ni-Salphen材料電化學性能較差,很難滿足實際應用的需求[24-25]。其它金屬離子(Al3+、Co2+、Zn2+、Cr3+等)的席夫堿配位聚合物用作超級電容器電極材料的報道幾乎沒有。
利用對苯二胺與對苯二甲醛縮合制備出對苯二胺縮對苯二甲醛導電聚合物(PT),合成過程中加入水合金屬硝酸鹽的醇溶液獲得金屬離子(Al3+、Co2+、Zn2+、Cr3+)配位摻雜的席夫堿配位聚合體(PTM)。電化學性能測定表明該類聚合物及其金屬配合物具有良好的電化學性能,有望用于電化學電容器領域。
1 實驗部分
1.1 試劑與儀器
對苯二胺(分析純,麥克林);對苯二甲醛(分析純,麥克林);無水乙醇(分析純,天津市天大化學試劑廠);九水合硝酸鋁(分析純,天津市大茂化學試劑廠);六水合硝酸鈷(分析純,天津市大茂化學試劑廠);六水合硝酸鋅(分析純,天津市大茂化學試劑廠);九水合硝酸鉻(分析純,羅恩試劑)。
利用X射線粉末衍射儀(XRD,D/MAX-RA,日本Rigaku公司)研究制備材料的物相組成,銅靶Kα輻射(λ=0.154 18 nm),操作電壓和工作電流分別為40 kV和30 mA,掃描范圍為10°~50°;用掃描電子顯微鏡(SEM,S-4800,日本Hitachi公司)及EDS能譜(INCA-350,英國Oxford公司)研究材料的表面結構和相關元素組成,工作電壓和電流分別為20 kV和20 mA;用傅里葉紅外吸收光譜(FT-IR,Nexus 870,美國Thermo公司)研究聚合物官能團情況,測試波長范圍4 000~500 cm-1;用熱分析儀(德國耐馳儀器公司)研究材料的熱穩定性,N2氣氛,10℃·min-1的升溫速率,測試溫度范圍是從室溫到1 000℃;用電化學工作站測試所制備材料的電化學性能(CS310,武漢科斯特儀器有限公司)。
1.2 實驗過程
1.2.1制備對苯二胺縮對苯二甲醛聚合物
室溫下,分別稱取0.01 mol對苯二胺(1.081 4 g)與0.01 mol對苯二甲醛(1.341 3 g)溶于40 mL無水乙醇中。待完全溶解后,將醛的醇溶液緩慢滴加到胺的醇溶液中,滴加完畢后磁力攪拌3 h,有黃色沉淀析出,抽濾后用無水乙醇、去離子水洗滌多次,60℃真空干燥12 h,得到產物對苯二胺縮對苯二甲醛席夫堿聚合物(PT)。按照上述實驗步驟分別制備出對苯二胺與對苯二甲醛物質的量之比為2∶1和1∶2的聚合物,分別命名為PT(2∶1)、PT(1∶2)。
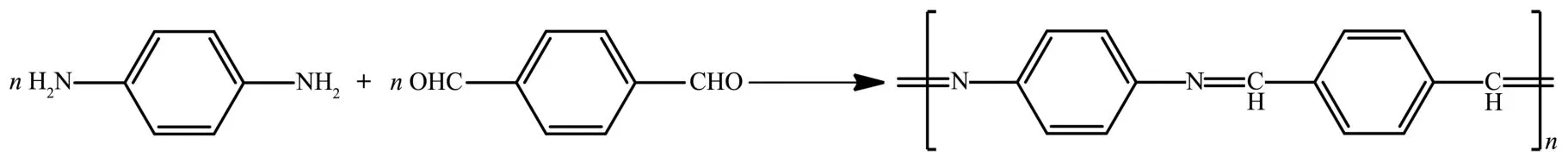
方案1 PT的合成路線Scheme 1 Synthetic route of PT
1.2.2制備對苯二胺縮對苯二甲醛金屬配合物
分別稱取0.01 mol對苯二胺、0.01 mol對苯二甲醛及相應的水合硝酸鹽(3.751 3 g九水合硝酸鋁、2.910 0 g六水合硝酸鈷、2.974 5 g六水合硝酸鋅、4.001 5 g九水合硝酸鉻),將以上藥品分別溶于40 mL無水乙醇中。首先在磁力攪拌條件下將對苯二甲醛的醇溶液緩慢滴加至對苯二胺的醇溶液中形成混合溶液。接下來,在未出現沉淀之前緩慢地將水合金屬硝酸鹽的醇溶液加入到上述混合溶液,磁力攪拌3 h,抽濾,無水乙醇、去離子水多次洗滌,60℃真空干燥12 h得到產物對苯二胺縮對苯二甲醛金屬配合物PT-M(M=Al、Co、Zn、Cr)。
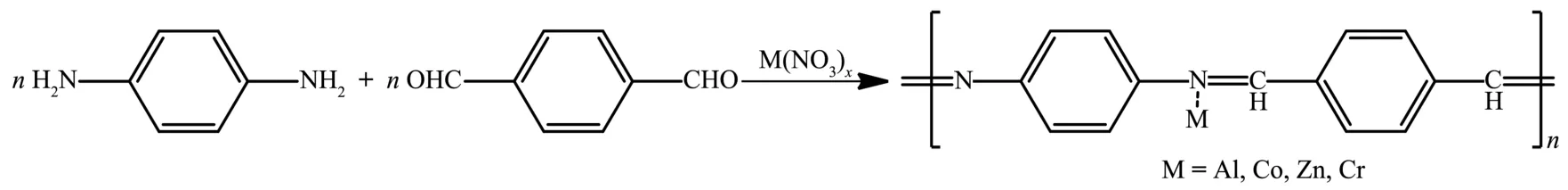
方案2 PT-M的合成路線Scheme 2 Synthetic route of PT-M
1.2.3電化學性能測試
將制得的PT-M分別與聚偏氟乙烯(PVDF)、乙炔黑按照質量比8∶1∶1混合并在瑪瑙研缽中進行研磨使其混合均勻,再滴入一定量的N-甲基吡咯烷酮(NMP)調成糊狀,將糊狀混合物均勻地涂于泡沫鎳(1 cm×1 cm)上。將上述所制備的電極放入60℃烘箱中干燥6 h,用10 MPa壓力壓制成型。
采用三電極體系測試電極材料的電化學性能,以所制備的泡沫鎳電極為工作電極、Pt電極為輔助電極、Hg/HgO電極為參比電極、6 mol·L-1的KOH溶液為電解液,分別進行循環伏安(CV)、恒電流充放電(GCD)和電化學阻抗譜(EIS)測試。
2 結果與討論
2.1 PT、PT(2∶1)及PT(1∶2)的電化學性能分析
為了測試PT、PT(2∶1)及PT(1∶2)電極材料的電化學性能,對其在0~0.6 V的電位范圍內、100 mV·s-1的掃速下進行CV測試。圖1為3個樣品的CV曲線,由圖可知3條曲線上均有一對明顯的氧化還原峰,表明不同物質的量之比下制備的電極材料均為贗電容型電極材料。比較3條曲線所圍成的面積,可以看到當對苯二胺與對苯二甲醛物質的量之比為1∶1時具有最大的封閉面積,而CV曲線所圍成的面積大小與材料的比電容成正比,表明對苯二胺與對苯二甲醛物質的量之比1:1是制備高比電容電極材料的最佳物質的量之比。
2.2 PT及PT-M的XRD分析
圖2為PT與PT-M的XRD圖。從圖中可以看出,PT樣品在14.2°、20.3°、23.6°和29.1°處有尖銳的衍射峰,表明合成的席夫堿聚合物具有較高的結晶度。這可歸因于主鏈中有序的芳香環結構和強烈的分子間π-π堆積相互作用[26-27]。隨著金屬離子進入分子鏈,位于14.2°處的衍射峰幾乎消失,20.3°、23.6°和29.1°處的衍射峰強度明顯減弱,表明由于金屬離子的摻雜導致PT-M的結晶度降低。分子間ππ堆積減弱,分子框架中無序堆積趨勢增加,從而導致結晶度降低。
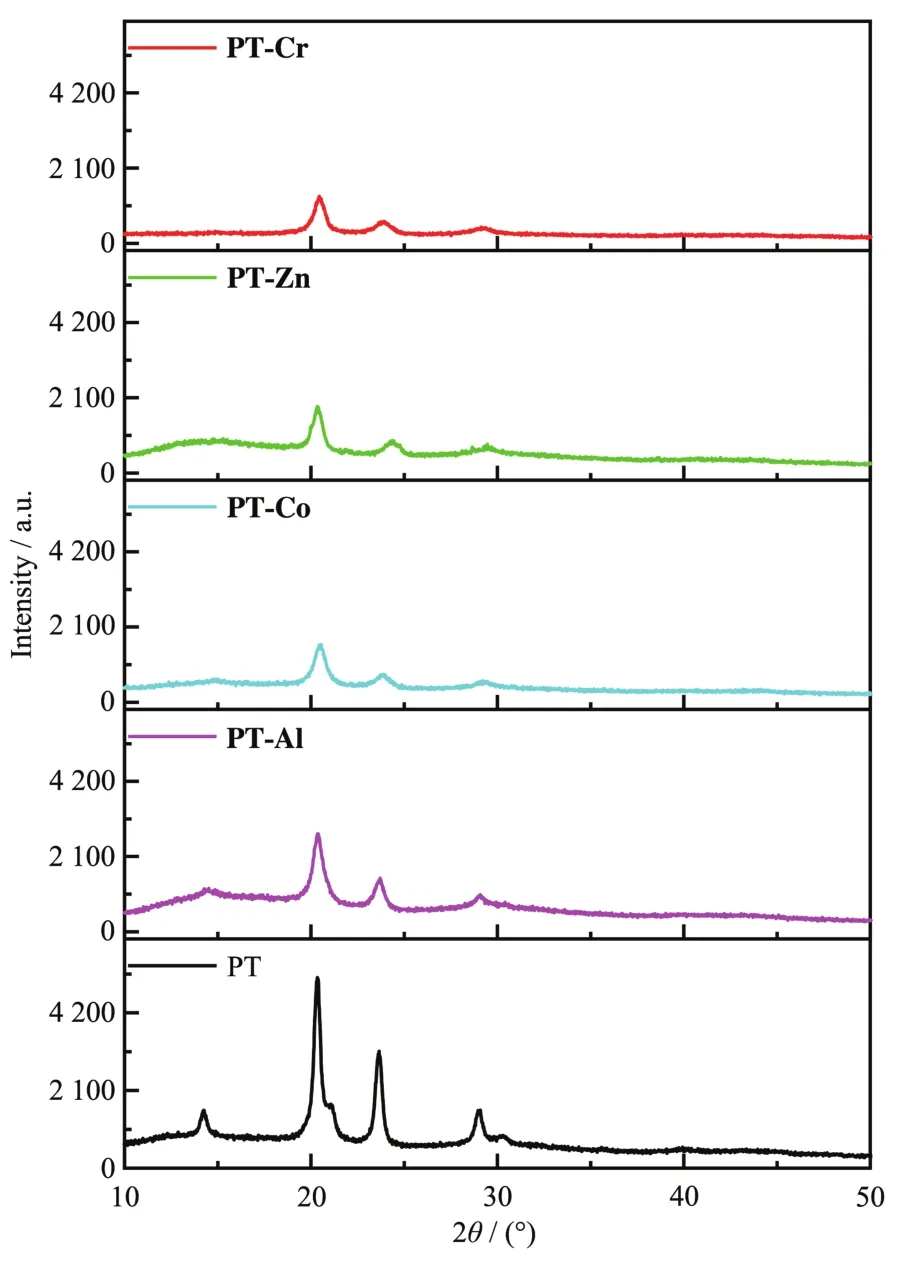
圖2 PT和PT-M的XRD圖Fig.2 XRD patterns of PT and PT-M
2.3 PT及PT-M的FT-IR分析
PT和PT-M的FT-IR如圖3所示,二者在不同波長處顯示出相似的吸收峰,證明聚合物和其配合物結構相似。PT大約在1 620 cm-1處的強吸收是席夫堿結構中-C=N-鍵的特征吸收[28]。且從圖3可以看出形成金屬配合物后-C=N-鍵仍有較強的吸收,但-C=N-鍵的吸收峰發生了移動,這是因為金屬離子與聚合物分子鏈上的N原子發生了配位作用,能夠證明金屬離子與席夫堿聚合物是以配位鍵連接的。1 499 cm-1處的吸附峰歸屬于席夫堿中苯環的吸收,表明縮合反應生成席夫堿聚合物并未破壞苯環的結構。860 cm-1處的吸收峰是苯環對位取代基引起的。
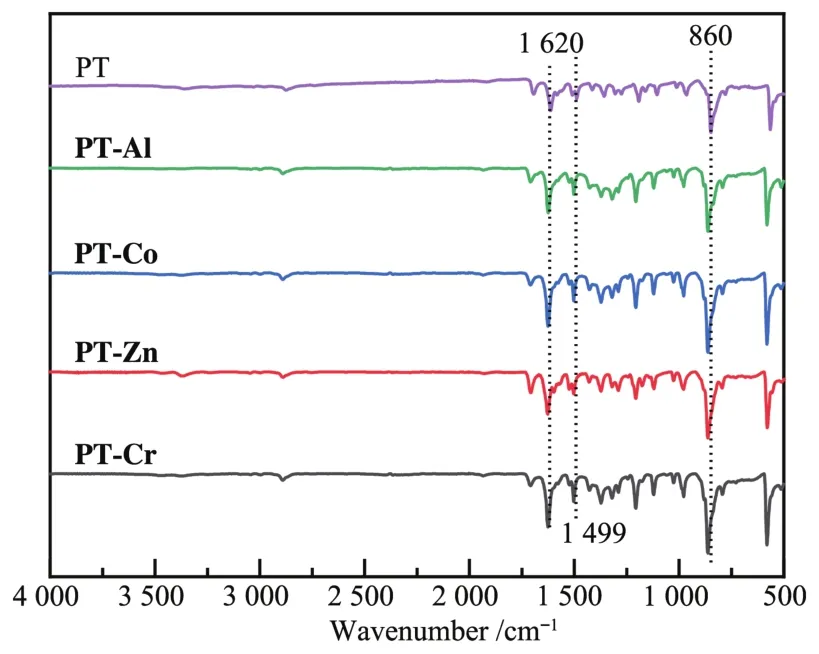
圖3 PT和PT-M的FT-IR譜圖Fig.3 FT-IR spectra of PT and PT-M
2.4 TG-DSC分析
為了評估席夫堿聚合物及其配合物的熱穩定性,對其進行了熱重-差示掃描量熱法(TG-DSC)分析,結果如圖4所示。可以看出PT和PT-M的TG曲線包含3個失重段。第1個失重段在100~400℃溫度范圍,歸因于物理吸附水和席夫堿聚合物中的一些小分子的揮發。第2個失重段發生在400~600℃范圍并產生了較大的質量損失,這是由席夫堿共軛主鏈結構的熱裂解產生。第3個失重段大概位于600~1 000℃且失重趨勢較為平緩,這主要是席夫堿苯環中碳碳鍵斷裂形成的[29]。在DSC曲線上,每個吸熱峰都與相應的熱分解過程相對應。對比PT與PT-M的熱重曲線可以看出,PT和PT-M的TG曲線非常相似,值得注意的是相比于PT-M,PT具有較好的熱穩定性,當溫度達到500℃時聚合物才開始分解,對應的DSC曲線在517℃有個明顯的吸熱峰。而PT-M的熱分解溫度向低溫區間移動,這是由于摻雜的金屬離子與N原子的配位削弱了聚席夫堿分子鏈的穩定性,且金屬離子可以作為催化劑促進有機分子鏈的熱分解,與上述XRD和FT-IR的測試結果相一致。
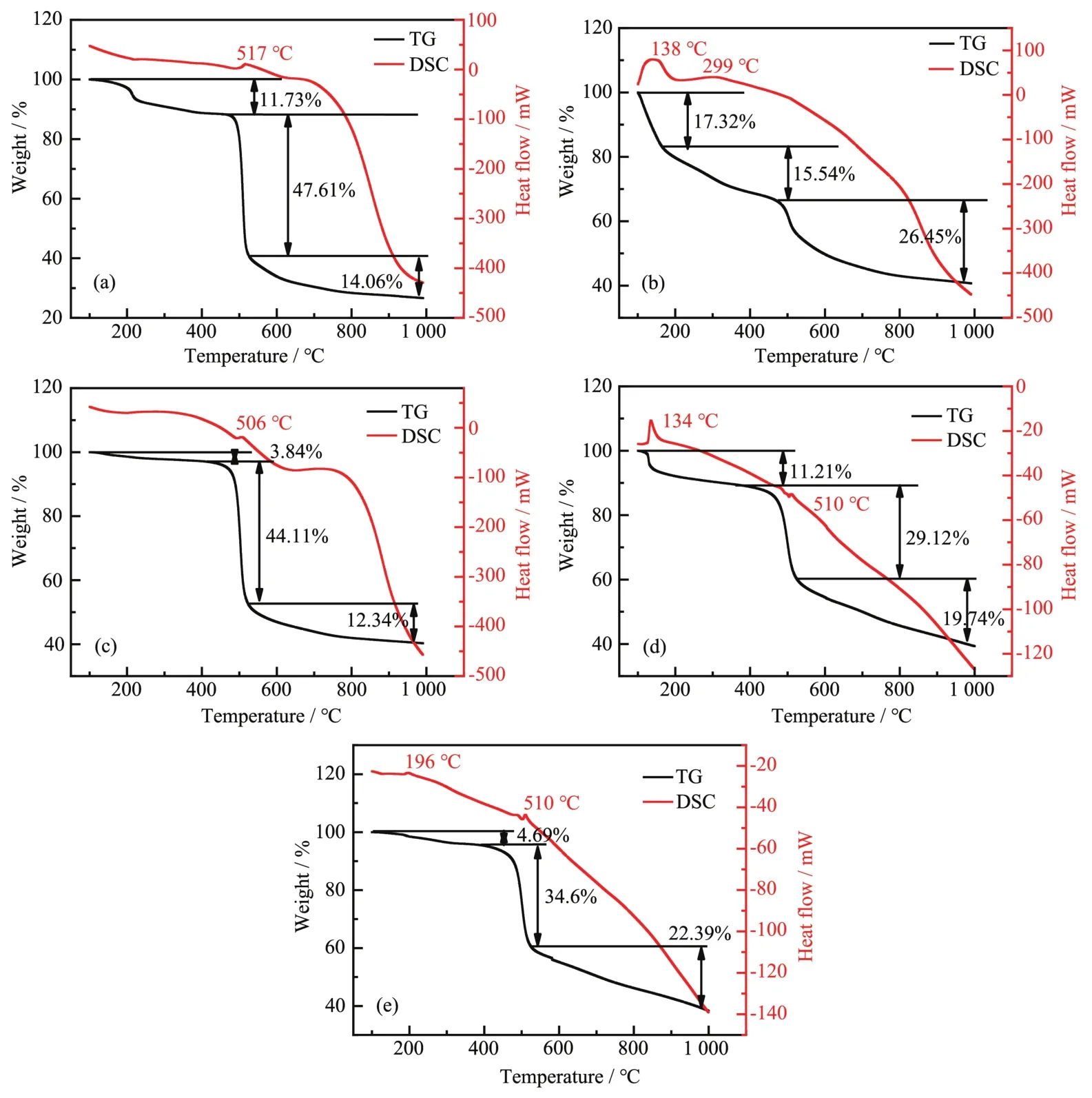
圖4 PT和PT-M的TG-DSC曲線Fig.4 TG-DSC curves of PT and PT-M
2.5 PT及PT-M的SEM分析
圖5是PT和PT-M的SEM圖。從圖中可以觀察到PT樣品表面光滑,這是由于聚合物PT的長鏈具有很強的分子間π-π堆積作用,分子鏈堆積緊密導致表面致密化。然而,隨著金屬離子的摻雜,席夫堿聚合物的結構因金屬離子摻入而降低了結晶度,導致表面形貌粗糙,這與之前的XRD結果相一致。另外不同金屬離子(Al3+、Co2+、Zn2+、Cr3+)的離子半徑、電負性和外層電子構型有明顯的差別,其配位進入席夫堿分子鏈的情況也會有差異,導致配合物在形貌在微觀上存在一定差異,這將導致電化學性能的不同。
采用能量色散光譜法(EDS)確定樣品的元素組成(圖6),在PT中檢測到元素C和O,PT-Al中測量到元素C、O和Al,PT-Co中測量到元素C、O和Co,PT-Zn中測量到元素C、O和Zn,PT-Cr中測量到元素C、O和Cr。結合XRD以及FT-IR表征,再次證明了配合物的成功合成。但是N元素的能譜峰沒有被檢測到,這可能是由于N的含量較低且容易被C元素所掩蓋而引起的。
2.6 電化學性能分析

圖5 PT和PT-M的SEM圖Fig.5 SEM images of PT and PT-M
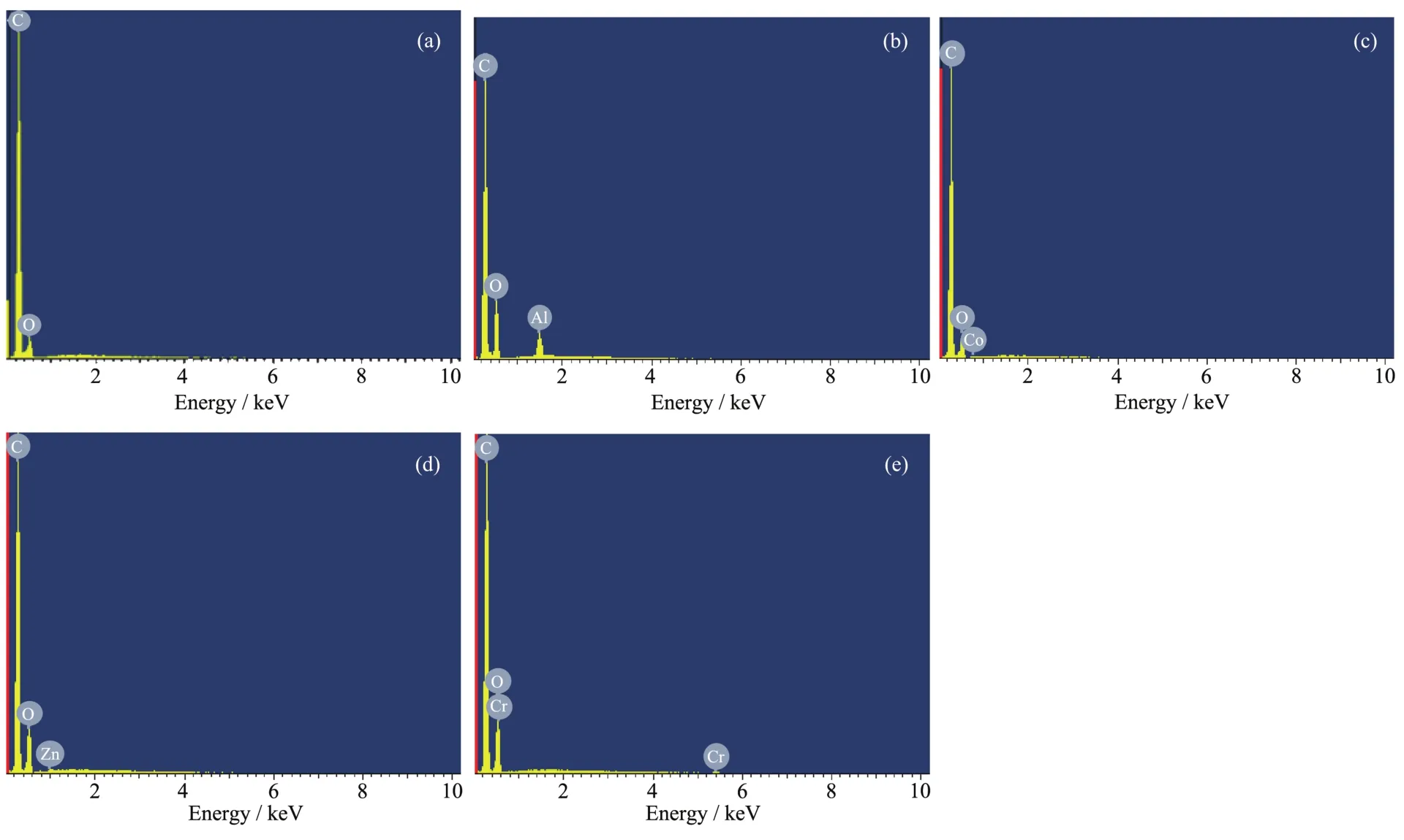
圖6 PT和PT-M的EDS圖Fig.6 EDS spectra of PT and PT-M
PT和PT-M的CV曲線如圖7a所示,二者的CV曲線形狀相似,但峰值電流存在較大的差異。PTM電極的峰值電流比PT電極的峰值電流高,表明PT-M電極具有更大的比電容[30]。這主要是因為席夫堿聚合物本體(PT)進行氧化還原反應,金屬離子與N配位進入分子鏈中,提供了電子轉移的最小電阻路徑,使得活性物質與電解液之間的電荷轉移較快。伴隨聚合物的氧化還原過程,金屬離子不進行價態轉化,電解質周圍的離子進入聚合物進行電荷補償,以保持電中性。SEM形貌分析也發現摻入金屬離子后,材料表面變得疏松,這一變化證實了摻入金屬離子有利于電解液中離子的遷入。圖7a還顯示PT-M的CV曲線面積比PT大得多,特別是PTAl,這意味著PT-Al比PT的比電容大得多。這是由于盡管引入的金屬離子不參與電極表面上快速的氧化還原反應,但金屬離子的引入將引起原始的PT框架紊亂,從而為活性電極材料的電荷轉移和離子擴散提供更多的活性位點和更短的通道。在摻入的不同金屬離子中,Al3+對比電容的提高起到了最大的協同作用,這可能與其自身電子云密度、離子半徑等有關。由CV曲線所圍成的圖形面積對比可知(PT-Al>PT-Co>PT-Zn>PT-Cr),摻入Al3+具有最好的效果。
圖7b是在0.5 A·g-1電流密度下,樣品PT和PTM的GCD曲線。GCD曲線的充放電平臺對應于CV曲線的氧化還原峰,其中充電過程分為0~0.33和0.33~0.50 V兩個區間。可以看出在低電位段,電位隨充電時間線性增加,電極的電容主要由雙電層電容提供。而在0.33~0.50 V的電位區間內發生了法拉第氧化還原反應,說明PT和PT-M的電容主要來自于法拉第贗電容[31-33]。
圖8顯示了在不同掃速下樣品PT和PT-M的CV曲線。可以看出,在每條CV曲線中都存在一對氧化還原峰,表明PT和PT-M的比電容是由氧化態和還原態之間可逆的氧化還原反應產生,證實了PT和PT-M材料具有典型的贗電容特性[34]。此外,隨著掃速從10 mV·s-1增加到100 mV·s-1,陽極峰移動到較高的電勢,而陰極峰移動到較低的電勢,造成這一現象主要是由于掃速的增加導致極化現象的發生[35]。值得注意的是在掃描速率增加至100 mV·s-1時,CV曲線的形狀依然未發生改變,說明PT和PT-M材料可在較快掃速下保持良好的充放電性能。
PT和PT-M在不同電流密度下的GCD曲線如圖9所示,工作電壓為0~0.5 V。由圖可知,PT和PT-M電極即使在6.0 A·g-1的電流密度下仍保持良好的對稱性,表明電極材料具有優異的可逆充放電能力,電解質離子在電極-電解質溶液系統中的擴散是可逆的,盡管進行了快速的充電/放電操作,電解質離子仍可以擴散到材料內部通道中。不同電流密度下的比電容可根據以下公式計算得出[36]:C=IΔt/(mΔV),其中C是比電容(F·g-1),I是充放電電流(A),Δt是放電時間(s),ΔV是電勢窗口(V),m是活性物質質量(g)。在電流密度為0.5 A·g-1時,計算得到PT的電容僅為150 F·g-1。而與金屬離子配位形成的配合物的電容量有明顯的提高,樣品PT-Al、PTCo、PT-Zn、PT-Cr的比電容分別為649.6、493.4、248.8、223.4 F·g-1,其中PT-Al具有最佳的比電容。
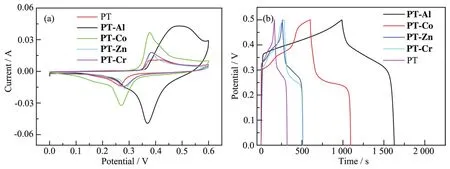
圖7 PT和PT-M:(a)在20 mV·s-1下的CV曲線;(b)在0.5 A·g-1電流密度下的GCD曲線Fig.7 PT and PT-M:(a)CV curves at 20 mV·s-1;(b)GCD curves at 0.5 A·g-1
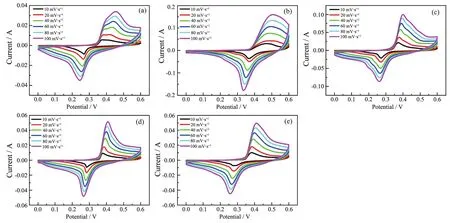
圖8 PT和PT-M在不同掃速下的CV曲線Fig.8 CV curves of PT and PT-M at different scan rates
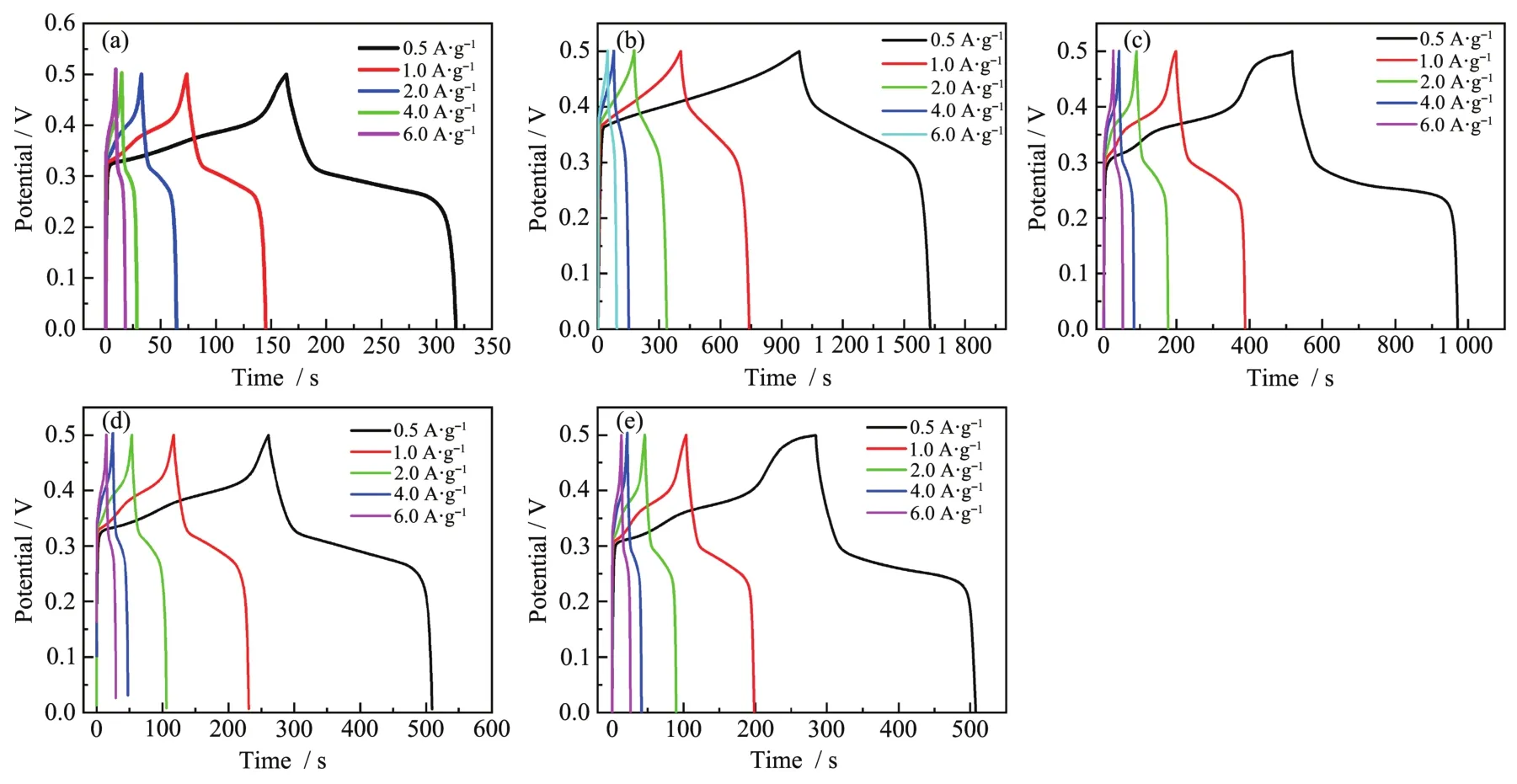
圖9 PT和PT-M在不同電流密度下的GCD曲線Fig.9 GCD curves of PT and PT-M at different current densities
圖10是PT和PT-M在0~0.5 V的電位窗口、不同電流密度下的倍率性能曲線。當電流密度從0.5 A·g-1增加至6.0 A·g-1時,PT、PT-Al、PT-Co、PTZn、PT-Cr電極容量保持率分別為70.4%、75.1%、63.2%、69.4%、68.8%。比電容隨著電流密度增加而降低是因為在較低的掃速下,離子可以達到所有活性材料內部,使得電極活性材料具有較大的利用率。在高電流密度下,進入電活性位點并參與氧化還原反應的電解質離子的擴散時間縮短,導致電極活性材料的利用率較低[37]。因此PT-Al不僅具有較高的比電容而且具有較好的倍率性能。
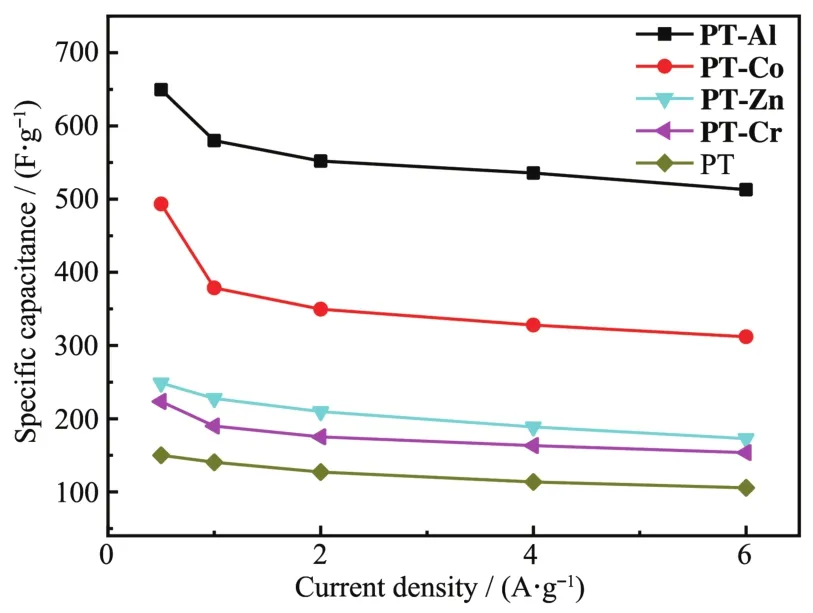
圖10 PT和PT-M在不同電流密度下的倍率性能曲線Fig.10 Specific capacitance of PT and PT-M at various current densities
循環壽命是評估材料用作超級電容器電極材料的關鍵參數。為了評估PT和PT-M的循環穩定性,我們在8 A·g-1比電容的電流密度下、0~0.5 V的電位范圍內進行了1 000次的GCD循環。圖11是5種材料進行1 000次GCD循環得到的循環穩定性圖,其中PT、PT-Al、PT-Co、PT-Zn、PT-Cr電容保持率分別為83.8%、80.9%、65.3%、63.6%、74.3%。PT及PT-M的電容量保持率隨循環次數的增加呈現出不斷下降的趨勢,這是由于在高電流密度下,聚合物中的結構單元快速可逆的氧化還原反應導致其結構單元膨脹和收縮,破壞了其結構和導電性。其中PT-Al的穩定性高于其他金屬配合物的穩定性,表明PT-Al是性能優異的電化學用電極材料,而PT-Al的循環穩定性低于PT,是由于金屬離子進入聚合物分子鏈中減小了π-π鏈堆積,這也和熱重測試結果一致。
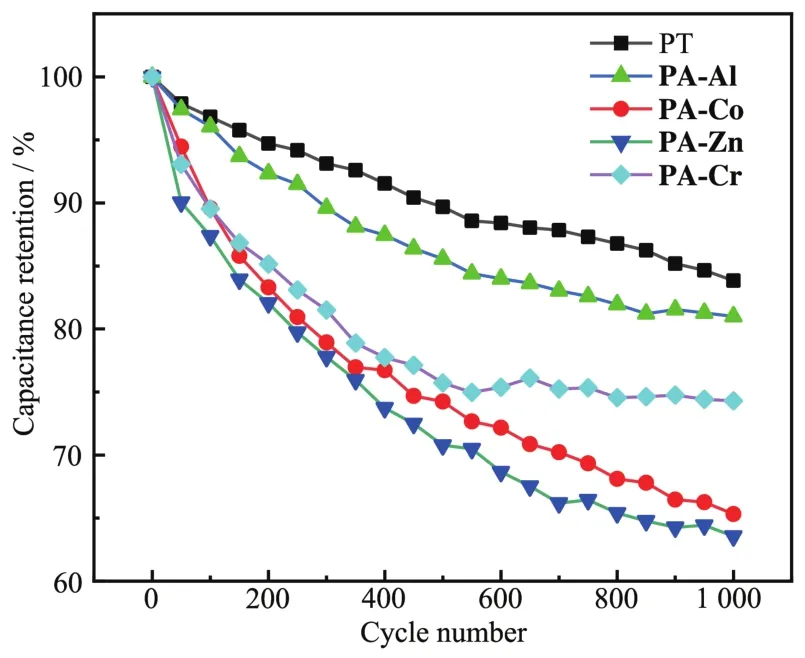
圖11 PT和PT-M的循環穩定性Fig.11 Cycling performance of PT and PT-M
EIS用于研究復合材料的電阻行為和電荷轉移動力學。Nyquist圖由高頻范圍內的半圓弧和低頻范圍內的直線組成。半圓弧形的直徑大小代表電荷轉移電阻(Rct)。半圓弧形與坐標軸的交點代表溶液電阻(Rs),主要包括電解液的離子阻抗、電極材料自身的電阻、電解液與電極材料之間的接觸電阻和電極材料上涂布的活性物質與集流體之間的接觸電阻[38]。低頻處的傾斜直線通常表示為Warburg阻抗(ZW),它與離子在電極活性物質和電解質之間的界面上的擴散有關。等效電路圖中CPE和Cf分別代表恒相位元件和法拉第電容。PT和PT-M的EIS譜圖如圖12所示,PT的溶液電阻為0.517 Ω,PTAl、PT-Co、PT-Zn、PT-Cr的Rs分別為0.511、0.582、0.535、0.528 Ω,可以看出PT和PT-M均具有較小的Rs。在低頻區域PT-M的斜率明顯大于PT的斜率,表明PT-M作為電極材料時具有較小的離子擴散阻力[39-41],進一步說明了PT-M具有優異的導電性以及有效的電解質擴散能力,這與CV和GCD測試結論相一致。在PT-M中PT-Al具有最小的溶液電阻及最小的離子擴散阻力,再次證實PT-Al具有優異的電化學特性。
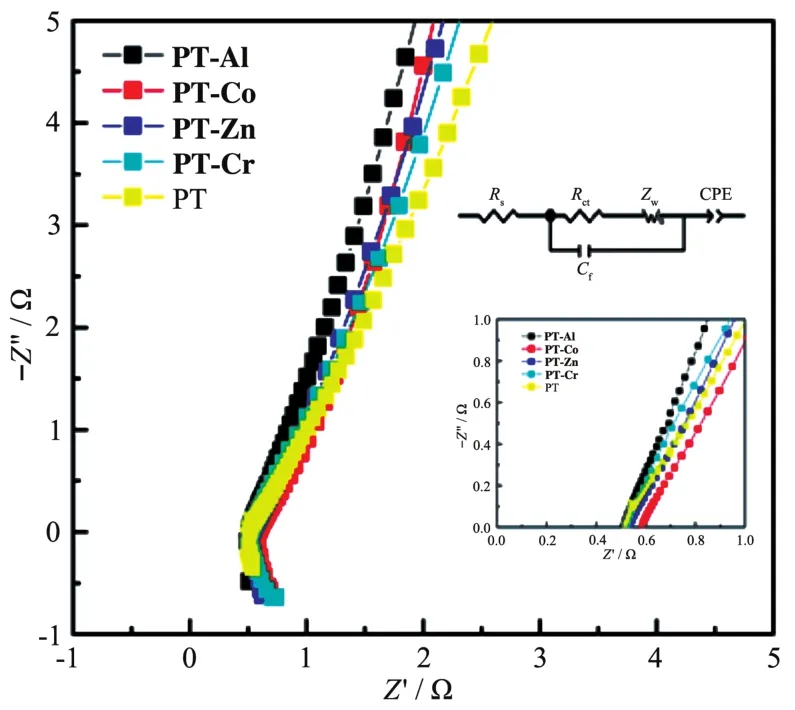
圖12 PT和PT-M的Nyquist圖Fig.12 Nyquist plots of PT and PT-M
2.7 聚合物導電機理
對苯二胺縮對苯二甲醛席夫堿聚合物通過-C=N-鍵連接形成大的π-π共軛體系。其本體(PT)自身發生氧化還原產生贗電容來存儲電荷,但聚合物內部大量的π-π鍵堆積使對苯二胺縮對苯二甲醛席夫堿聚合物比電容較小。通過對聚合物進行金屬離子摻雜來提高比電容,紅外測試證實金屬離子的進入是與N原子進行配位而未破壞席夫堿聚合物本身的π-π鏈;XRD測試發現摻雜有金屬離子的聚合物結晶度降低,證實了金屬離子使對苯二胺縮對苯二甲醛席夫堿聚合物的π-π堆積減弱;SEM掃描觀察到摻雜有金屬離子的聚合物表面較為粗糙,證實了金屬離子對聚合物的結構產生了影響。對PT和PT-M進行電化學性能測試,發現金屬離子的摻入顯著提高了對苯二胺縮對苯二甲醛席夫堿聚合物的比電容。因此我們推測這些出色的電容特性是通過擴大的層間距的協同效應產生的,而層與層之間的協同作用有助于快速離子擴散和贗電容氧化還原發生。
3 結 論
通過對苯二胺、對苯二甲醛和水合金屬硝酸鹽一步法制備了對苯二胺縮對苯二甲醛席夫堿聚合物(PT)及其配位化合物(PT-M)。采用XRD、FT-IR、TG-DSC、SEM及EDS技術對所制備材料的結晶度、官能團分布、熱穩定性、微觀形貌和元素分布進行了表征。結果表明金屬離子通過配位進入席夫堿分子鏈的骨架結構,從而降低分子鏈間的π-π堆積作用。電化學性能測試表明,0.5 A·g-1的電流密度下,對苯二胺縮對苯二甲醛席夫堿聚合物(PT)的比電容僅有150 F·g-1,經過金屬離子配位形成的對苯二胺縮對苯二甲醛席夫堿配合物(PT-M)的比電容明顯提高,其中PT-Al的比電容高達649.6 F·g-1,并且在1 000次GCD循環后仍有80.9%的電容保持率。研究表明,對苯二胺縮對苯二甲醛席夫堿金屬鋁配合物(PT-Al)具有優異的電化學性能,有望應用于超級電容器領域。
- 無機化學學報的其它文章
- Synthesis of Zn-Doped BiOBr with Enhanced Photoreduction CO2Activity under Visible Light Irradiation
- Promotional Effects of Silanization on the Hydrothermal Stability of CuCe/BEA Catalyst for Selective Catalytic Reduction of NOxwith NH3
- Disulfide-Bridged Dimeric Cobalt Porphyrin:Synthesis and Electroreduction of Dioxygen
- Syntheses,Crystal Structures and Photoluminescent Properties of Three Zinc(Ⅱ)Coordination Polymers Constructed from 9,10-Di(1H-imidazol-1-yl)anthracene
- Synthesis and Fluorescent Sensing Properties of Two Metal-Organic Coordination Polymers Based on 6-(3,5-Dicarboxylphenyl)nicotinic Acid
- Four Rare Earth Complexes with Chlorinated Carboxylic Acids and Bipyridine Ligands:Crystal Structures,Thermal Analysis and Luminescence Properties

