基于2′,4′-二氟聯苯基的新型1,2,4-三氮唑類化合物的合成及其抗真菌活性
陳 勇,魏文博,段坤坤,方家寶,張尹超,楊占濤
(安陽師范學院化學化工學院, 河南 安陽 455000)
真菌感染是十分常見的疾病,它能夠造成皮膚、粘膜等淺表皮處的感染,這類真菌感染中最常見的是皮膚癬菌病.真菌也可以造成皮下組織等深部感染,可侵犯內臟及腦膜等處,甚至引起全身播散性感染,既侵襲性真菌感染.引起的疾病如真菌性腸炎,腦膜炎等,嚴重的狀況下,會造成人的死亡.近年來,隨著高效廣譜抗生素、免疫抑制劑、抗惡性腫瘤藥物的廣泛應用,器官移植、體內置管以及久駐ICU病人的增加,侵襲性真菌感染引起的發病率和致死率逐年上升,已成為危害人類健康的嚴重威脅之一[1-6].當前,2019新型冠狀病毒(Severe Acute Respiratory Syndrome Coronavirus 2,簡稱SARS-CoV-2)引起的新型冠狀病毒肺炎(Corona Virus Disease 2019,簡稱COVID-19) 仍在全球肆虐并引起了全球性關注,新型冠狀病毒肺炎傳染性強,發病率高,重癥患者病死率高.重癥新冠肺炎患者具備侵襲性真菌感染發生的高危因素,且已有重癥病例出現繼發或合并真菌感染報告[7].藥物治療是應對侵襲性真菌感染的主要方法,然而已有的抗真菌藥物種類有限,致病性真菌對這些藥物產生耐藥性,大部分藥物還具有毒副作用等問題,使得研發新的抗真菌藥物成為必要.
氮唑類抗真菌藥物是目前常用的一類抗真菌藥物,按照藥物的分子結構可分為咪唑類和三氮唑類.氮唑類藥物的作用機制:通過抑制ERGl1基因編碼的14α-羊毛甾醇脫甲基酶(CYP51),抑制真菌細胞膜中的羊毛甾醇轉化為麥角甾醇,并使毒性的甾醇產物在真菌細胞中積累,從而抑制真菌的生長與復制[8-9].咪唑類抗真菌藥物(咪康唑,酮康唑等)是一類開發較早,抗真菌活性較高,但毒副作用較大,主要用于淺表真菌感染的治療.后來科研工作者研制出了三氮唑類抗真菌藥,相對于咪唑類抗真菌藥,三氮唑類抗真菌藥具有毒性較低,抗菌譜較廣,可用于治療深部真菌感染引起的疾病.但是三氮唑類抗真菌藥久用易使真菌產生耐藥性,藥效漸弱.為此研究者通過不斷的改進藥物分子的結構,來應對致病性真菌的耐藥性,進而提高三氮唑類抗真菌藥的療效.研究者先后研制出了第一代三氮唑類抗真菌藥氟康唑、伊曲康唑等;第二代三氮唑類抗真菌藥伏立康唑、沙伯康唑等;最新上市的三氮唑類抗真菌藥艾沙康唑[9-11].
目前臨床上可用于治療深部真菌感染的藥物除三唑類抗真菌藥物外,還有多烯類抗真菌抗生素兩性霉素B(Amphotericin B)、制霉菌素A1(Nystatin A1);棘白菌素類抗真菌藥卡泊芬凈(Caspofungin)、米卡芬凈(Micafungin)[12-14].三唑類抗真菌藥物作為一類全合成化學藥,可利用有機合成的多樣性,用有機合成的方法,合成種類繁多,結構新穎的具有潛在抗真菌活性的化合物,進而可在此基礎上開發出高效、低毒、廣譜的抗真菌藥物.因此,三唑類抗真菌藥仍是目前臨床上用于治療深部真菌感染的主要藥物.
盡管科研工作者已經開發了多個分子結構不同的三唑類抗真菌藥物,但由于多種原因導致的真菌感染的疾病也在增多,而現有的抗真菌藥物也存在一定的毒副作用,尤其是真菌耐藥性的增加,所有這些均給真菌感染疾病的治療帶來困難.因此開發新型高效、低毒的抗真菌藥物仍有必要[15-18].
為了應對致病性真菌對現有藥物產生的耐藥性,并提高藥物的藥效性,一個有效的方法是對原有藥物的分子結構進行化學修飾[19-21].已用于臨床的三唑類抗真菌藥多以2,4-二氟苯基為分子骨架,通過不斷地化學修飾,分別開發出了一、二、三代三唑類抗真菌藥[8-9].從藥物開發的實踐看,聯苯基是構成藥物分子的理想結構片段,根據藥物分子設計原理中的結構骨架變換原則[22],新藥的創制是在發現活性分子基礎上的骨架變換.因此,本研究以已有的唑類抗真菌藥物的構效關系為基礎,依據藥物分子設計原理,設計并合成以 2,4-二氟代聯苯基為分子骨架的新型三氮唑化合物.合成路線如Scheme 1所示.
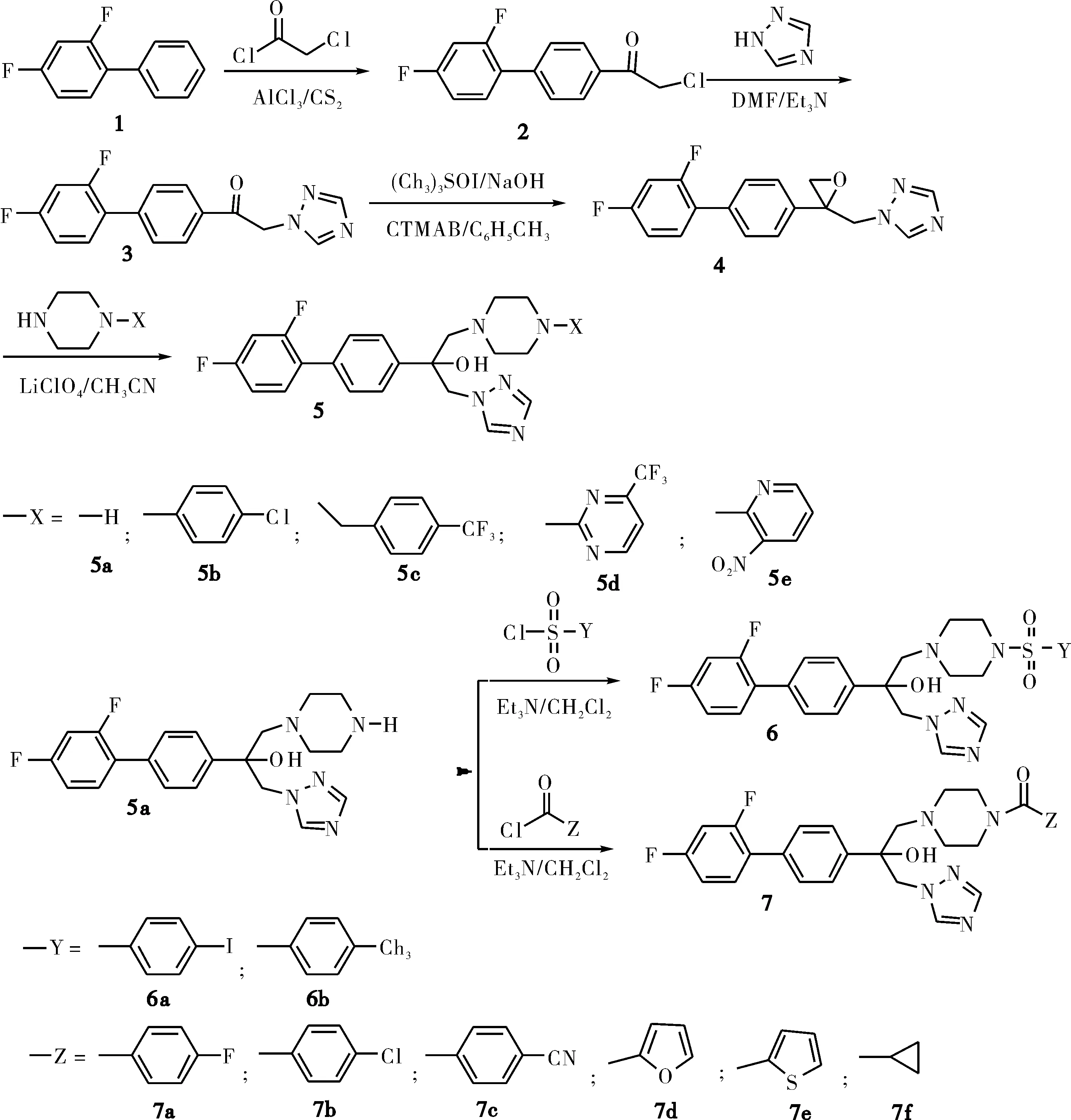
Scheme 1 目標化合物的合成路線 Scheme 1 The synthetic route of the title compounds
1 實驗部分
1.1 儀器和試劑
ACQUITYTMUPLC/LCT Premier XE型高分辨液相質譜儀(美國Waters公司);Am-400型核磁共振儀(德國Bruker公司).
試劑:2,4-二氟聯苯、 三甲基碘化亞砜、十六烷基三甲基溴化銨、CDCl3、d6-DMSO(分析純,阿拉丁)、1-(4-三氟甲基苯甲基)哌嗪、高氯酸鋰、1-(4-三氟甲基嘧啶-2-基)-哌嗪,1-(3-硝基吡啶-2-基)-哌嗪、4-碘苯磺酰氯、4-甲基苯磺酰氯、對氟苯甲酰氯、對苯甲酰氯、對氰基苯甲酰氯、2-呋喃甲酰氯、2-噻吩甲酰氯、環丙基(哌嗪-1-基)甲酮、三乙胺(分析純,阿拉丁);四氫呋喃、乙酸乙酯、石油醚、乙腈、二氯甲烷(分析純,科密歐);柱層析硅膠(青島海洋化工廠)54~57 μm.
1.2 實驗方法
1.2.1 目標化合物的合成
1) 1-[2′,4′-二氟-(1,1′-聯苯基)-4-基]-2-氯乙酮 (2) 和1-(2′,4′-二氟聯苯-4基)-2-(1H-1,2,4-三氮唑-1-基)-乙酮(3)的合成同文獻[23].
2) 1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-2,3-環氧丙烷(4)的合成向反應瓶中加入1.55 g (5.19 mmol) 化合物3、1.26 g (5.72 mmol) 三甲基碘化亞砜、0.19 g十六烷基三甲基溴化銨、13 mL的甲苯和2 mL NaOH(aq. 20 %),控溫60 ℃,攪拌反應1.5 h.向反應后的混合溶液加入25 mL乙酸乙酯,轉入分液漏斗,混合液用水洗滌,洗滌后的有機層用無水硫酸鎂干燥.減壓蒸去溶劑,余物用石油醚:乙酸乙酯(V∶V=1∶1)的展開劑過硅膠色譜柱,得到0.89 g棕紅色粘稠狀化合物4,產率54.9 %.
HMRS-ESI:m/z[M+H] calcd. for C17H14F2N3O: 314.1105; found: 314.1112.
3) {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯基-4-基)-3-(-1-哌嗪基)}-2-丙醇(5a)的合成
把11.25 mL的乙醇和11.25 mL的THF加入反應瓶中,搖勻,配成混合溶劑;再向反應瓶中加入0.48 g (5.6 mmol)哌嗪、1.17 g (3.75 mmol)化合物4和1.25 ml的三乙胺,在65 ℃下攪拌反應 7 h.反應結束后,向反應瓶中加入25 mL蒸餾水,把反應瓶中的混合液轉入分液漏斗,混合液用25 mL×2乙酸乙酯萃取,萃取液用無水硫酸鎂干燥,旋蒸除去溶劑,余物過硅膠色譜柱,先用乙酸乙酯作洗脫劑,把少量雜質先行洗脫除去,待產物流出后,改用甲醇作洗脫劑,得1.11 g白色固體產物化合物5a,產率 88.5%.
HMRS-ESI:m/z[M+H] calcd. for C21H24F2N5O: 400.1949; found: 400.1942.
4) {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-氯苯基)-1-哌嗪基]}-2-丙醇(5b)的合成
稱取0.106 7 g (0.34 mmol )化合物4,0.098 3 g(0.5 mmol )1-[(4-氯苯基)]-哌嗪,0.106 g (1 mmol)LiClO4及4 mL乙腈加入 到反應瓶中,在85 ℃下,攪拌18 h.然后,向反應混合物中加入10 mL蒸餾水并用乙酸乙酯(15 mL×2)萃取,合并有機相,無水硫酸鎂干燥,旋蒸除去有機溶劑,余物進行硅膠色譜分離,洗脫劑為石油醚:乙酸乙酯(V∶V)=1∶1,得0.116 g橙紅色蠟狀物化合物5b,產率為67.1%.
1H NMR (400 MHz,CDCl3) δ 8.14 (s,1H),7.90 (s,1H),7.49 (d,J=29.6 Hz,4H),7.42 (dd,J=15.2,8.6 Hz,1H),7.17 (d,J=8.9 Hz,2H),6.95 (dt,J=19.2,8.6 Hz,2H),6.75 (d,J=8.9 Hz,2H),4.84 (s,1H),4.48 (d,J=14.3 Hz,1H),4.37 (d,J=14.3 Hz,1H),3.06 (s,1H),3.01 (t,J=4.8 Hz,4H),2.77 (d,J=13.4 Hz,1H),2.52 (dd,J=10.4,5.3 Hz,2H),2.44 (dd,J=10.5,5.2 Hz,2H).
13C NMR (101 MHz,CDCl3) δ 163.64,161.09,158.54,151.17,149.56,144.88,143.07,134.33,131.33,129.08,128.94 (2C),125.35 (2C),124.77,117.20 (2C),111.75,111.55,104.45,73.02,63.66,58.07,54.21 (2C),49.21 (2C).
HMRS-ESI:m/z[M+H] calcd. for C27H27ClF2N5O: 510.1872; found: 510.1883.
5) 化合物5c~5e的合成方法和化合物5b的合成方法相同.
① {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-三氟甲基苯甲基)-1-哌嗪基]}-2-丙醇(5c)的合成
橙色蠟狀產物,產率 45.0%.
1H NMR (400 MHz,CDCl3) δ 8.13 (s,1H),7.88 (s,1H),7.61~7.46 (m,6H),7.43~7.35 (m,3H),7.00~6.86 (m,2H),4.43 (d,J=14.3 Hz,1H),4.33 (d,J=14.3 Hz,1H),3.85 (s,1H),3.52 (d,J=13.5 Hz,1H),3.44 (d,J=13.5 Hz,1H),2.99 (d,J=13.3 Hz,1H),2.72 (d,J=13.3 Hz,1H),2.38 (s,2H),2.32 (s,6H).
13C NMR (101 MHz,CDCl3) δ 163.65,161.15,158.35,151.21,149.66,144. 81,143.05,134.23,131.38,129.12,128.97 (2C),125.29 (2C),124.81,123.78,117.23 (2C),111.63,111.56,104.48,73.24,65.39,64.59,58.12,54.37 (2C),48.22 (2C).
HMRS-ESI:m/z[M+H] calcd. for C29H29F5N5O: 558.2292; found: 558.2285.
② {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-三氟甲基嘧啶-2-基)-1-哌嗪基]}-2-丙醇(5d)的合成
黃色蠟狀物,產率56.4%.
1H NMR (400 MHz,CDCl3) δ 8.43 (d,J=4.7 Hz,1H),8.14 (s,1H),7.89 (s,1H),7.52 (s,4H),7.41 (dd,J=15.2,8.5 Hz,1H),6.94 (dt,J=19.2,8.6 Hz,2H),6.72 (d,J=4.8 Hz,1H),4.91 (s,1H),4.48 (d,J=14.3 Hz,1H),4.38 (d,J=14.3 Hz,1H),3.73 (s,4H),3.03 (d,J=13.4 Hz,1H),2.77 (d,J=13.4 Hz,1H),2.42 (dd,J=10.7,5.4 Hz,2H),2.34 (dd,J=10.6,5.3 Hz,2H).
13C NMR (101 MHz,CDCl3) δ 163.63,161.13,160.02,158.53,156.20,151.17,144.89,142.98,134.38,131.34,129.09,128.89,125.32(2C),121.87,119.13,111.73,111.52,104.87,73.13,63.90,58.01,54.13 (2C),43.65 (2C).
HMRS-ESI:m/z[M+H] calcd. for C26H25F5N7O: 546.2041; found: 546.2035.
③ {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(3-硝基吡啶-2-基)-1-哌嗪基]}-2-丙醇(5e)的合成
橙紅色蠟狀物,產率為61.0%.
1H NMR (400 MHz,CDCl3) δ 8.31~8.24 (m,1H),8.13 (s,1H),8.08 (dd,J=8.0,1.5 Hz,1H),7.89 (s,1H),7.51 (s,4H),7.47~7.36 (m,1H),7.03~6.88 (m,2H),6.73 (dd,J=8.0,4.5 Hz,1H),4.84 (s,1H),4.47 (d,J=14.3 Hz,1H),4.37 (d,J=14.3 Hz,1H),3.45~3.32 (m,2H),3.33~3.22 (m,2H),3.05 (d,J=13.4 Hz,1H),2.76 (d,J=13.4 Hz,1H),2.52~2.43 (m,2H),2.43~2.32 (m,2H).
13C NMR (101 MHz,CDCl3) δ 163.63,161.09,158.53,152.54,151.69,151.19,144.89,142.90,135.51,134.40,133.16,131.36,129.12,129.10,125.30 (2C),113.68,111.62,104.43,73.13,63.80,58.00,54.04 (2C),47.93 (2C).
HMRS-ESI:m/z[M+H] calcd. for C26H26F2N7O3: 522.2065; found: 522.2071.
6) {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-碘苯磺酰基)-1-哌嗪基]}-2-丙醇(6a)的合成
把399 mg(1 mmol)化合物5a、303 mg(1 mmol)4-碘苯磺酰氯、15 mL新蒸的二氯甲烷和320 μL三乙胺加入到反應瓶中.室溫條件下磁力攪拌9 h.反應結束后,將反應混合物旋蒸除去溶劑,余物過硅膠色譜柱,洗脫劑為乙酸乙酯,濃縮后得到245 mg黃色固體化合物6a,產率為36.8%.
1H NMR (400 MHz,CDCl3) δ 8.05 (s,1H),7.90 (d,J=8.4 Hz,2H),7.86 (s,1H),7.51~7.35 (m,7H),7.01~6.87 (m,2H),4.50 (s,1H),4.41 (d,J=14.4 Hz,1H),4.30 (d,J=14.4 Hz,1H),2.99 (d,J=13.5 Hz,1H),2.88 (s,4H),2.69 (d,J=13.6 Hz,1H),2.50~2.42 (m,2H),2.42~2.30 (m,2H).
13C NMR (101 MHz,CDCl3) δ 163.65,161.07,158.52,151.25,149.56,144.85,142.52,138.43(2C),134.47,131.3(2C),129.04(2C),125.23 (2C),124.36,111.78,104.48,100.60,74.58,63.42,57.74,53.44 (2C),45.90 (2C).
HMRS-ESI:m/z[M+H] calcd. for C27H27IF2N5O3S: 666.0847; found: 666.0853.
7) {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-甲基苯磺酰基)-1-哌嗪基]}-2-丙醇(6b)的合成方法和化合物(6a)相同.
黃色蠟狀固體0.209 6 g,產率47.4%.
1H NMR (400 MHz,CDCl3) δ 8.05 (s,1H),7.87 (s,1H),7.59 (d,J=8.2 Hz,2H),7.44 (dt,J=14.1,7.4 Hz,5H),7.34 (d,J=8.0 Hz,2H),6.95 (ddd,J=19.3,9.3,7.2 Hz,2H),4.56 (s,1H),4.40 (d,J=14.4 Hz,1H),4.29 (d,J=14.4 Hz,1H),3.00 (d,J=13.5 Hz,1H),2.87 (s,4H),2.69 (d,J=13.5 Hz,1H),2.46 (s,3H,—CH3),2.45~2.32 (m,4H).
13C NMR (101 MHz,CDCl3) δ 163.64,161.11,158.48,151.28,149.51,144.75,142.62,139.54,134.47,132.38(2C),131.34(2C),129.04(2C),125.23 (2C),124.36,111.78,104.48,74.58,63.42,57.74,53.44 (2C),45.90 (2C),24.58 (—CH3).
HMRS-ESI:m/z[M+H] calcd. for C28H30F2N5O3S: 554.2037; found: 554.2044.
8) {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-氟苯甲酰基)-1-哌嗪基]}-2-丙醇(7a)的合成
稱取100 mg (0.25 mmol) 化合物5a、39.6 mg(0.25 mmol) 對氟苯甲酰氯、3 mL新蒸的二氯甲烷和50.6 mg (0.5 mmol) 三乙胺加入到反應瓶中,在磁力攪拌下,室溫反應8 h.待反應結束后,反應混合液旋蒸除去溶劑,余物過硅膠色譜柱,洗脫劑為純乙酸乙酯,得到72 mg灰白色固體化合物7a,產率為55.3%.
1H NMR (400 MHz,CDCl3) δ 8.17 (s,1H),8.08 (s,1H),7.91 (s,1H),7.43~7.28 (m,4H),7.11 (t,J=8.6 Hz,1H),7.05 (t,J=8.5 Hz,2H),6.92 (m,3H),5.51 (s,1H),4.48 (d,J=14.4 Hz,1H) 4.37 (d,J=14.4 Hz,1H),3.76~3.27 (m,4H),3.04 (d,J=13.4 Hz,1H),2.76 (d,J=13.4 Hz,1H),2.49~2.28 (m,4H).
13C NMR (101 MHz,CDCl3) δ 169.52,164.78,163.74,161.01,158.64,151.11,142.71,134.58,132.62,132.53,131.42(2C),129.13(2C),125.35 (2C),124.45,115.63(2C),111.87,104.56,77.36,73.31,63.82,58.03 (2C),53.99 (2C).
HMRS-ESI:m/z[M+H] calcd. for C28H27F3N5O2: 522.2117; found: 522.2109.
9) 化合物7b~7f的合成方法和化合物7a的合成方法相同.
① {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-氯苯甲酰基)-1-哌嗪基]}-2-丙醇(7b)的合成
棕色蠟狀固體,產率為41.6%.
1H NMR (400 MHz,CDCl3) δ 8.13 (s,1H),7.89 (s,1H),7.48 (s,4H),7.42~7.32 (m,3H),7.28 (d,J=2.1 Hz,2H),6.97~6.86 (m,2H),4.47 (d,J=14.4 Hz,1H),4.36 (d,J=14.4 Hz,1H),3.73 (s,1H),3.40 (d,J=105.0 Hz,4H),3.02 (d,J=13.4 Hz,1H),2.75 (d,J=13.5 Hz,1H),2.47 ~2.17 (m,4H).
13C NMR (101 MHz,CDCl3) δ 169.20 (C=O),163.62,161.05,158.48,151.12,144.89,142.64,135.93,134.46,133.67,131.27,129.13(2C),128.77(2C),128.54(2C),125.25 (2C),124.35,111.67,104.46,73.25,63.74,57.87 (2C),54.31 (2C).
HMRS-ESI:m/z[M+H] calcd. for C28H27ClF2N5O2: 538.1821; found: 538.1827.
②{1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(4-氰基苯甲酰基)-1-哌嗪基]}-2-丙醇(7c) 的合成
棕色蠟狀物固體產物,產率50.8%.
1H NMR (400 MHz,CDCl3) δ 8.13 (s,1H),7.89 (s,1H),7.72 (d,J=8.3 Hz,1H),7.65 (d,J=8.2 Hz,1H),7.47 (s,3H),7.42 (d,J=8.2 Hz,1H),7.39~7.32 (m,1H),6.99~6.84 (m,1H),5.12 (s,1H),4.42 (dd,J=47.0,14.4 Hz,2H),3.65 (d,J=71.0 Hz,2H),3.21 (s,1H),3.02 (d,J=13.5 Hz,1H),2.75 (d,J=13.5 Hz,1H),2.35 (dd,J=81.2,31.8 Hz,3H).
13C NMR (101 MHz,CDCl3) δ 168.16 (C=O),163.61,161.04,158.45,150.96,144.90,142.50,139.69,134.48,132.26(2C),129.13(2C),127.69(2C),125.25(2C),124.30,117.94,115.99,113.61,111.70,104.46,73.37,63.74,57.81(2C),54.24(2C).
HMRS-ESI:m/z[M+H] calcd. for C29H27F2N6O: 529.2164; found: 529.2158.
③ {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(呋喃甲酰-2-基)-1-哌嗪基]}-2-丙醇(7d)的合成
紫色蠟狀固體化合物,產率為48.5%.
1H NMR (400 MHz,CDCl3) δ 8.18 (s,1H),7.93 (s,1H),7.60 (s,1H),7.51 (s,4H),7.45~7.42 (m,1H),7.03~6.87 (m,3H),6.45 (dd,J=3.4,1.7 Hz,1H),4.65 (s,1H),4.49 (d,J=14.4 Hz,2H),4.40 (d,J=14.4 Hz,2H),3.71 (s,4H),3.08 (d,J=13.4 Hz,1H),2.83 (d,J=13.4 Hz,1H),2.48 (d,J=5.5 Hz,2H),2.40 (s,2H).
13C NMR (101 MHz,CDCl3) δ 165.87(C=O),163.70,161.44,158.97,150.92,147.60,144.88,143.77,142.57,134.50,131.32,129.16(2C),125.26 (2C),124.48,118.14,111.88,111.34,104.46,73.13,63.67,58.09 (2C),54.44 (2C).
HMRS-ESI:m/z[M+H] calcd. for C26H26F2N5O3: 494.2004; found: 494.2009.
④ {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(噻吩甲酰-2-基)-1-哌嗪基]}-2-丙醇(7e)的合成
紫紅色蠟狀固體化合物,產率為46.5%.
1H NMR (400 MHz,CDCl3) δ 8.13 (s,1H),7.90 (s,1H),7.51 (s,4H),7.41 (td,J=8.8,5.7 Hz,2H),7.24~7.18 (m,1H),7.00 (dd,J=4.9,3.7 Hz,1H),6.94 (dd,J=9.3,6.7 Hz,2H),4.64 (s,1H),4.48 (d,J=14.4 Hz,1H),4.37 (d,J=14.4 Hz,1H),3.62 (s,4H),3.17 (s,1H),3.05 (d,J=13.4 Hz,1H),2.78 (d,J=13.4 Hz,1H),2.47 - 2.39 (m,2H),2.34 (d,J=4.5 Hz,2H).
13C NMR (101 MHz,CDCl3) δ 166.78( C=O ),163.89,161.26,158.47,150.68,144.85,143.87,142.67,134.52,131.35,130.82,130.65,130.18,129.18(2C),128.12,125.26 (2C),124.48,111.76,104.64,73.21,63.69,58.12 (2C),54.35 (2C).
HMRS-ESI:m/z[M+H] calcd. for C26H26F2N5O2S: 510.5787; found: 510.5794.
⑤ {1-(1H-1,2,4-三氮唑-1-基)-2-(2′,4′-二氟聯苯-4-基)-3-[4-(環丙甲酰基)-1-哌嗪基]}-2-丙醇(7f)的合成
黃色蠟狀化合物,產率為62.9%.
1H NMR (400 MHz,CDCl3) δ 8.11 (s,1H),7.88 (s,1H),7.50 (s,4H),7.40 (td,J=8.6,6.6 Hz,1H),7.04 - 6.80 (m,2H),4.47 (d,J=14.3 Hz,1H),4.37 (d,J=14.3 Hz,1H),3.79 (s,1H),3.53 (s,4H),3.00 (d,J=13.4 Hz,1H),2.75 (d,J=13.4 Hz,1H),2.37 (s,2H),2.34~2.22 (m,2H),1.68~1.58 (m,1H),0.92 (dt,J=6.4,3.2 Hz,2H),0.71 (dd,J=7.8,3.0 Hz,2H).
13C NMR (101 MHz,CDCl3) δ 171.88 (C=O),163.64,161.08,158.52,151.20,144.86,142.87,134.40,131.32,129.09(2C),125.29 (2C),124.45,111.74,111.53,104.44,73.21,63.82 (2C),57.95 (2C),10.84,7.31 (2C).
HMRS-ESI:m/z[M+H] calcd. for C25H28F2N5O2: 468.2211; found: 468.2218.
1.2.2 目標化合物的體外抑菌試驗 以氟康唑和酮康唑為陽性對照藥物,以白色念珠菌(Candidaalbicans);新型隱球菌(Crytococcusneoformans);紅色毛癬菌(Trichophytonrubrum)三種常見的人體治病真菌作為實驗真菌菌株,參照美國國家臨床試驗室標準委員會推薦的標準化抗真菌敏感性實驗方法[24],采用96孔微量稀釋法測定目標化合物對各實驗真菌的最低抑菌濃度(MIC80),既對實驗真菌生長抑制率為80%時的最低抑菌濃度,實驗結果見表 1.
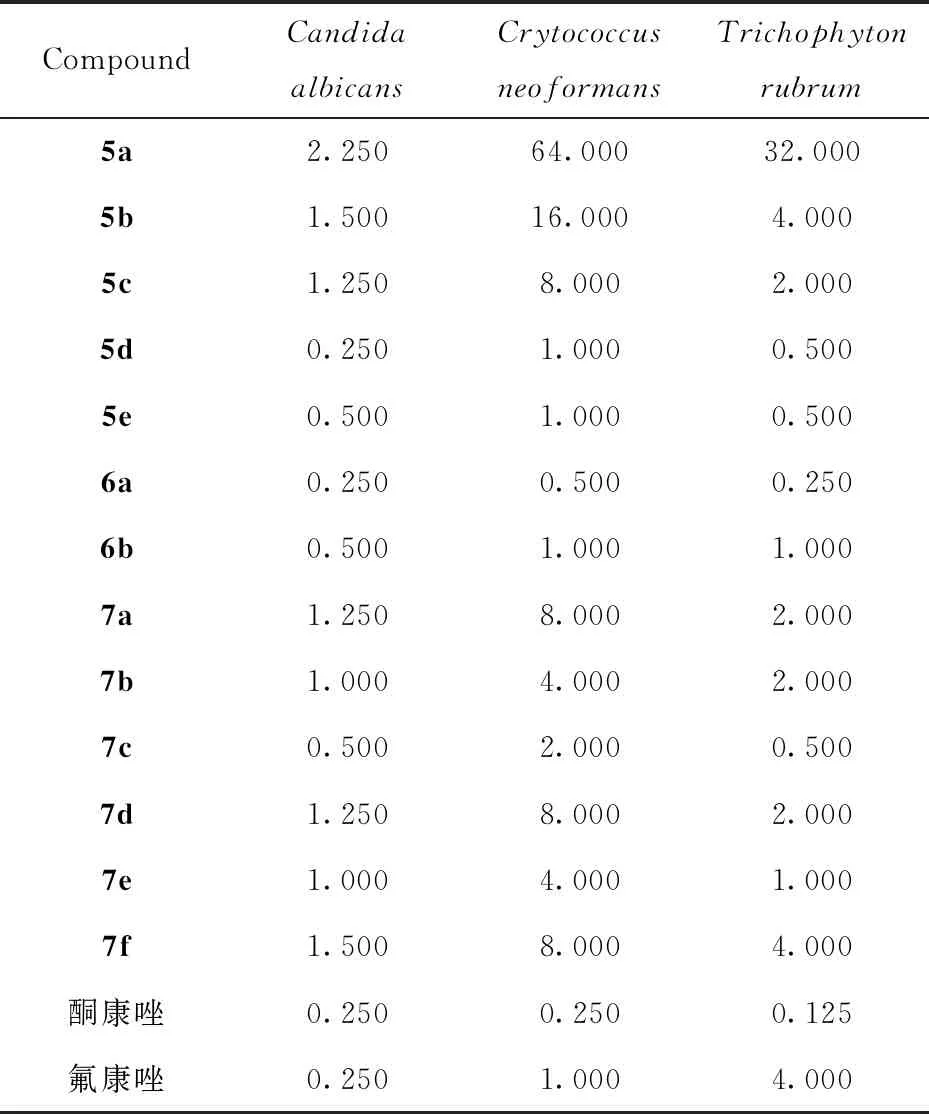
表1 目標化合物的體外抑菌活性Tab.1 In vitro antifungal activity (MIC80 ) of the target compounds /(μg·mL-1)
2 結果與討論
2.1 標化合物合成條件優化
在目標化合物的合成中,中間體化合物4的合成是關鍵步驟,嘗試了不同的反應條件對化合物4收率的影響,由表2可以看出,采用十六烷基三甲基溴化銨為相轉移催化劑,甲苯為反應溶劑,經多次實驗發現用20%NaOH溶液,反應溫度60 ℃,反應時間1.5 h得到的反應結果最佳.
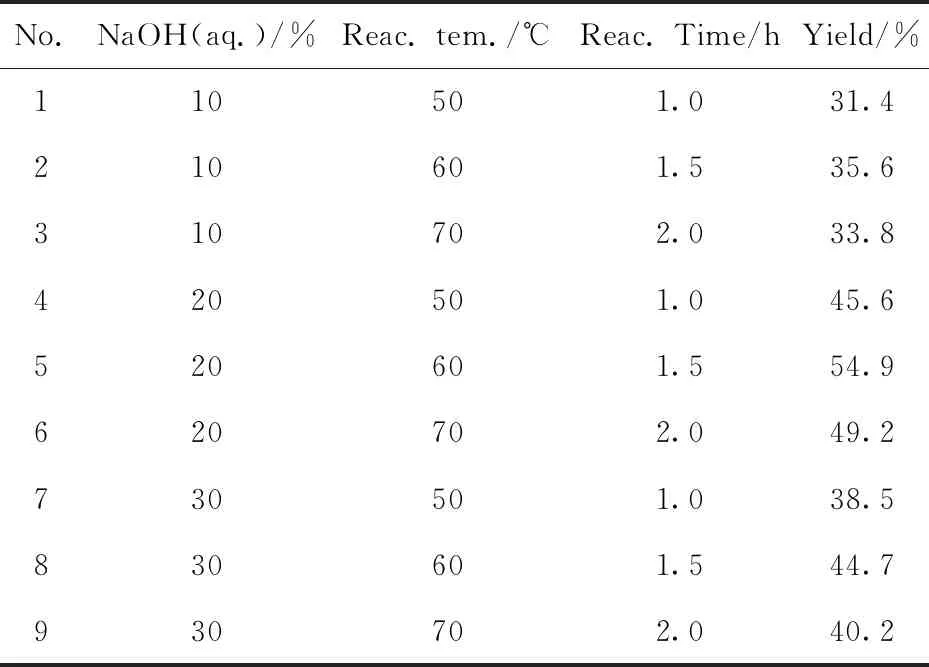
表2 不同反應條件對化合物4合成收率的影響Tab.2 Effect of reaction condition on the yield of the synthesis of compound 4
氫氧化鈉溶液濃度過大、反應溫度過高、反應時間過長將導致反應物中的—OH和生成的化合物4中的環氧乙烷基進一步反應,導致環氧乙烷開環,副產物增多,產物減少.化合物4和哌嗪反應可高產率得到化合物5a.化合物5a在多種溶劑中的溶解性較差,但作為中間體,在較多的二氯甲烷溶劑中和反應物酰氯經較長時間反應可得到目標產物6a,6b,7a~7f,目標產物在溶劑中溶解度較大,三乙胺在酰化反應中起到縛酸劑的作用,有利于產率的提高.
2.2 圖譜分析
化合物4通過硅膠柱層析分離提純后,得到的為棕紅色粘稠狀物質,所含溶劑很難出去,雜質峰較多,核磁圖譜不能正確歸屬,但作為中間體不影響下一步反應.化合物5a經分離純化后得到是白色固體產物,在CDCl3、d6-DMSO、D2O、CD3OD等溶劑中的溶解性極差,由于溶液濃度過低,核磁圖譜測試沒能成功.
目標化合物分子結構的相同之處是都含2,4-二氟聯苯基、1,2,4-三氮唑環、哌嗪環、羥基以及和1,2,4-三氮唑環、哌嗪環直接相連的兩個亞甲基,不同之處在于不同化合物分子分別接入了含有不同取代基的苯環或芳香雜環. 因此目標化合物的1H NMR和13C NMR圖譜在相應的位置有相似或接近的化學位移值,但不同的化合物之間仍稍有差異.1H NMR圖譜中,化學位移δ 8左右的兩個單峰,分別為1,2,4-三氮唑環上的兩個氫吸收峰;化學位移δ 7.5~6.5范圍的多個吸收峰為2,4-二氟聯苯基苯環上及分別接入目標化合物分子中含不同取代基的苯環或芳香雜環上的氫吸收峰,此處氫由于個數較多,且相互之間耦合,不同的氫吸收峰重合,峰形復雜,較難歸屬.—OH上氫的吸收峰為寬展的單峰,由于分子結構的差異,化學位移值有一定的差異,如:δ 4.84(5b,5c),δ 4.50(6a),δ 4.65(7d).和1,2,4-三氮唑環直接相連的亞甲基(—CH2—)上的氫吸收峰,化學位移值在δ 4.4左右,不同化合物之間稍有差異.和哌嗪環上的氮直接相連的亞甲基以及哌嗪環上的四個亞甲基上的氫吸收峰,化學位移值在大多在δ 3.45~2.32范圍內,不同化合物之間稍有差異,吸收峰多有耦合分裂現象.化合物7f中在化學位移值δ 1.68~1.58 (m,1H),0.92 (dt,J=6.4,3.2 Hz,2H),0.71 (dd,J=7.8,3.0 Hz,2H) 處的吸收峰是環丙基上氫原子吸收峰.
13C NMR圖譜中,和氟原子直接相連的苯環上的碳吸收峰,化學位移在δ 163,161.分子中其余芳香環上碳的吸收峰,化學位移在 δ 158~δ104范圍內,不同芳香環上不同碳原子吸收峰,化學位移值 δ 有些相差很大,有些非常接近,有些不同碳原子化學位移值δ完全相同,吸收峰重合,如2,4-二氟聯苯基不含氟原子的苯環上其中四個碳原子化學位移值 δ 129(2C),125 (2C).分子中亞甲基(—CH2—)上碳原子吸收峰,化學位移值在 δ 63~δ 45范圍內,其中哌嗪環上四個碳的吸收峰,化學位移值 δ 54 (2C),48 (2C).和羥基直接相連的季碳吸收峰,化學位移值δ 75.化合物7f中在化學位移值δ 10.84,7.31 (2C) 處的吸收峰是環丙基上碳原子吸收峰.
2.3 目標化合物的抗真菌活性
體外抗真菌活性測試結果表明,大部分目標化合物對參與本實驗的真菌生長有一定的抑制作用,其中目標化合物5d,5e,6a,6b,7c的抗真菌活性較好,化合物5d,6a對白色念珠菌的抑菌活性和酮康唑、氟康唑的抑菌活性相當,化合物5d,5e,6a,7c對紅色毛癬菌的抑菌活性接近酮康唑,優于氟康唑.從構效關系看,化合物5b~5e抗真菌活性比較,和哌嗪環相連的嘧啶(5d)、吡啶(5e)雜環化合物的抗真菌活性優于相連基團為苯環的化合物(5b,5c).和哌嗪環相連的磺酰基類化合物(6a,6b)其抗真菌活性優于和哌嗪環相連的酰基類化合物(7a~7f).
3 結論
依據藥物分子設計原理,設計合成了以 2,4-二氟代聯苯基為分子骨架的新型三氮唑化合物.研究了各步合成反應的最佳反應條件.分析了目標化合物的核磁圖譜,其分子結構經核磁共振氫譜、碳譜、高分辨質譜進行確證.測試了目標化合物的體外抗真菌活性,測試結果表明,大部分目標化合物對參與本研究的真菌生長有抑制一定的作用,其中目標化合物5d,5e,6a,6b,7c的抗真菌活性較好,化合物5d,6a對白色念珠菌的抑菌活性和酮康唑、氟康唑的抑菌活性相當,化合物5d,5e,6a,7c對紅色毛癬菌的抑菌活性接近酮康唑,優于氟康唑.

