全腦全脊髓放療中靜態調強和容積調強的劑量學對比
朱俐穎,胡小洋,孫磊,汪洋,
(1.復旦大學附屬華山醫院放射治療中心,上海,200235;2.上海伽瑪醫院放療科,上海,200235)
全腦全脊髓照射(craniospinal irradiation, CSI)是一種常用的中樞神經系統腫瘤放療技術,主要應用于容易沿腦脊液播散的惡性腫瘤,如髓母細胞瘤、生殖細胞腫瘤和播散性的室管膜瘤等。CSI靶區包括全腦和整個脊髓腔,照射范圍大,患者容易出現如惡性、嘔吐、和骨髓抑制等不良反應。特別是接受CSI的患者大多是青少年和兒童。因而如何在靶區獲得足夠劑量的前提下,降低CSI帶來的的毒副反應,成為臨床上關注的熱點[1-6]。
近幾年隨著放射治療設備和技術的不斷進步,調強放射治療(intensity modulated radiation therapy,IMRT),容積旋轉調強放射治療(volumetric modulated arc therapy,VAMT)等先進技術在臨床上廣泛應用,成為目前放射治療的主流技術。IMRT技術要求照射野內的射線強度按照一定要求進行調節,以達到更好的靶區適形度。VMAT是通過在機架旋轉的同時改變劑量率和多葉準直器(multi-leaf collimator,MLC)的射野形狀來實現靶區劑量覆蓋的一種動態調強技術。VMAT技術可以通過增加受照正常組織的分散度來減少正常組織的受照量,以期減少放療后不良反應;并通過多中心計劃優化的方式實現對較長靶區進行高度適形照射。本研究通過比較兩種技術在CSI的劑量學差異,為臨床合理選擇照射技術提供依據。
1 資料和方法
1.1 研究對象
回顧性分析2019年在上海伽瑪醫院放療中心接受CSI的連續病例20例,其中男性14例,女性6例。病理分類:髓母細胞瘤4例,生殖細胞瘤13例,松果體中間分化型腫瘤3例。其中14歲以下兒童8例:生殖細胞瘤6例,松果體中間分化型腫瘤2例。所有患者均行全腦全脊髓定位掃描,完成臨床靶體積(clinical target volume,CTV)和危及器官(organ at risk,OAR)勾畫。
1.2 儀器設備
定位采用GE 公司的CT Optima 660定位系統,放療計劃系統是Oncentra治療計劃系統(Elekta,Version 4.1),治療機是Elekta公司的Synergy醫用電子直線加速器,配置Agility 機頭,機頭葉片等中心處寬度為5 mm,最大治療野40 cm×40 cm。加速器的輸出劑量每周由物理師進行校準。
1.3 定位方式和靶區勾畫
患者采取仰臥位,雙手平放于身體兩側,使用熱塑料頭頸肩膜體位固定,頭部使用B號枕。使用CT進行模擬定位,模擬定位時采取頭先進,掃描層厚為5 mm。掃描范圍為頭頂空白處至坐骨結節處下2 cm。由醫生在Oncentra 醫生工作站上勾畫CTV和OAR,CTV外放5 mm定義為計劃靶區(planning target volume,PTV),并將Body體積減去PTV定義為正常組織(normal tissue,NT)。然后由物理師在治療計劃系統上分別設計用于臨床治療的ss-IMRT(step and shoot IMRT)和 VAMT 計劃。
1.4 治療計劃的設計
PTV的處方劑量為36 Gy/20次,單次劑量1.8 Gy。由于目前加速器等中心處的最大射野為40 cm×40 cm,根據患者靶區的長度,設置三個治療中心,對應三個計劃。ss-IMRT計劃治療每個中心均采取5野分布方式,照射野角度分別為180°、310°、50°、130°、230°。VAMT計劃每個中心采用2個全弧照射(順時針182°~178°,逆時針178°~182°),因Onentra治療計劃系統不支持三個中心的計劃同時進行優化,為避免射野銜接處出現劑量冷點和熱點,相鄰中心射野使用Oncentra中的Pre-treated plan功能,此功能是在計劃優化時,加入上一個治療中心已優化完成的計劃劑量分布,可以使相鄰中心計劃的射野銜接處的劑量分布更為理想。
ss-IMRT與VMAT設計時使用相同的三個治療中心,第一段是全腦照射野,下界設置在頸4錐體水平;第二段照射野的上界銜接全腦照射野的下界,下界設在胸10錐體,第三段照射野上界到胸10錐體,下界包含完整的PTV。三段計劃按次序優化,在二、三段計劃優化前,分別使用Pre-treated Plan功能,即加入上一段計劃的劑量分布,使接野處得到較均勻的劑量分布。ss-IMRT設置每個射野的子野控制點上限為20個,VMAT設置每4°為一個子野控制點,兩種計劃優化時計算網格大小為2.5 mm×5 mm×2.5 mm,對PTV和OAR使用相同的限制函數和劑量參數進行優化。
1.5 劑量學評估
在2 組計劃都能滿足臨床要求(95%處方劑量線覆蓋至少95%的靶區體積)的前提下,利用劑量體積直方圖、劑量分布圖得出的兩種放射治療計劃的靶區適形指數(CI)、劑量均勻指數(HI)、107%處方劑量線所包含的靶區體積(V107)和靶區內最大劑量點劑量值(Dmax),并進行劑量學差異分析,其中,CI=VP-t2/(VP×Vt),VP-t代表95%處方劑量線所包繞的靶區體積,VP為靶區體積,Vt是95%處方劑量包含的體積8。CI值越接近1,說明靶區適形性越好。HI=D5/D95,即5% 及95% 靶區體積所接受的照射劑量之比;HI值越大表示靶區劑量的均勻性越差9。各OAR的評估通過劑量-體積直方圖(dose-volumne histogram,DVH)讀取劑量學參數,比較OAR最大劑量點Dmax值、5Gy所包含的OAR體積(V5)、10 Gy所包含的0AR體積(V10)和20 Gy所包含的0AR體積(V20)。主要正常組織包括晶體、肺、心臟、肝臟和腎臟等。最后通過對比機器跳數及計劃實施時間來評估兩種計劃的實施效率。
1.6 統計學方法
所有數據均采用SPSS 19.0分析軟件進行統計學分析,計量資料采用均數±標準差表示,兩組數據分析方法使用單因素方差分析,p<0.05為差異具有統計學意義。
2 結果
2.1 靶區比較
兩種計劃的靶區劑量對比列于表1。由表1可見,兩種照射技術均能得到較好的靶區劑量分布,包括靶區劑量覆蓋度和靶區均勻性。靶區均勻指數比較,VMAT技術優于ss-IMRT技術,差別有統計學意義(p<0.05)。靶區適形指數比較,VMAT高于ss-IMRT,但差別未達到顯著性水平(p=0.067)。
2.2 正常器官、組織比較
表2為兩種計劃危及器官劑量學對比。通過對兩種計劃產生的各OAR劑量學參數進行比較發現,兩種計劃均達到了OAR的臨床劑量限制要求。其中,晶體、心臟、肝臟、腎臟及雙肺的V5、V10和V20,VAMT組與ss-IMRT組各有優勢。而在比較中發現,VAMT組比ss-IMRT組差,V5、V10差別有統計學意義,V20,ss-IMRT也要好于VMAT,但差別未達到顯著性水平。
2.3 治療效率比較
表3列出了兩種計劃治療效率的對比。通過對機器出束跳數和治療時間的比較,VAMT組比ss-IMRT組具有出束調數少和治療時間短的優勢,差別有統計學意義。
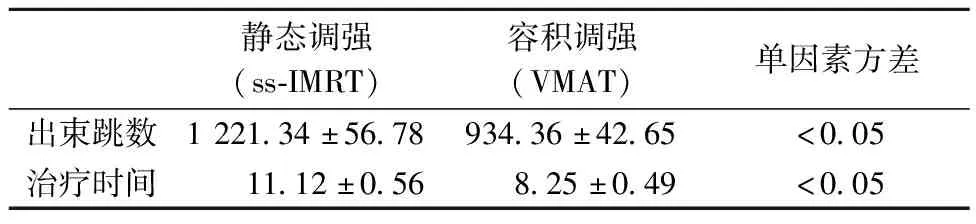
表3 治療效率對比
3 討論
近幾年來,顱內腫瘤出現CNS播散發生率有上升趨勢比[7],播散型腦腫瘤往往需要CSI。CSI技術復雜,尤其是涉及到多個射野銜接等技術難點[8-9]。,另外,相比于其它中樞神經系統惡性腫瘤的放射治療,CSI每次照射時間較長,患者依從性較差。本研究顯示:與ss-IMRT相比,VAMT技術適形性和均勻性更好,照射效率更高,減少了每次照射時間,提高了患者接受CSI的依從性,也減少患者因治療時間過長產生的位移增加所引起的劑量不確定性[10-15]。但是本研究也發現由于VAMT的低劑量學輻射區域明顯大于ss-IMRT,而兒童患者對于低劑量的放療引起的不良反應包括胃腸帶反應和骨髓抑制等可能要高于成人[16],而且低劑量的輻射范圍的增加是否會增加放射致癌的風險也需進一步的研究。所以筆者認為在進行CSI時,要根據患者的年齡、體質狀況、體位配合等多種因素綜合考慮,選取合適的CSI照射技術。

