氯胺酮聯合異丙酚麻醉對無抽搐電休克治療難治性抑郁癥的療效及認知功能的影響
古智文,黃雄,張春平,王志杰,張敏玲
難治性抑郁癥(treatment-resistant depression,TRD)是指既往采用至少2種抗抑郁劑按照標準劑量及療程治療后并無明顯效果的疾病,患者主要臨床癥狀為思維動作減慢、常出現軀體不適感及極度負面情緒,甚者具有明顯的自殺意圖,使其正常生活受到嚴重困擾,危及生命[1]。因此,如何治療TRD以減輕患者臨床癥狀是近年來臨床研究的重點課題之一。目前,臨床常采用無抽搐電休克(MECT)治療TRD,其有效率約60%,但大部分患者MECT治療后存在暫時性意識模糊和順行性遺忘,其中少部分患者的逆行性遺忘可持續6個月以上,這種對于認知功能損害的擔憂阻礙了MECT在臨床的更廣泛應用。故臨床急需采取一種有效的治療措施,在提高該類患者治療效果的同時減少認知不良反應,對MECT的治療有著重要的臨床意義。
現臨床常采用的MECT麻醉劑有依托咪酯、美索比妥鈉、丙泊酚及硫噴妥鈉等,上述藥物對電流誘發的癲癇可產生不同程度的拮抗,對MECT療效造成影響[2]。近年來,氯胺酮(ketamine)的快速抗抑郁效果得到該領域的高度重視,已有國外學者證實,采用氯胺酮作為MECT的麻醉劑治療TRD,可有效提高治療效果。異丙酚(propofol)是臨床常用的一種全身麻醉劑,在臨床應用廣泛。ketamine與propofol混合劑被簡稱為ketafol麻醉[3]。但臨床關于氯胺酮如何在MECT治療中發揮抗抑郁機制的報道甚少。基于此,現探討ketafol麻醉提高MECT治療難治性抑郁癥的療效同時減少認知功能損害的機制,以期為臨床提供借鑒,報道如下。
1 資料與方法
1.1 臨床資料 選取2012年2月—2018年2月廣州醫科大學附屬腦科醫院收治難治性抑郁癥患者120例作為研究對象,按隨機數字表法分為異丙酚MECT組、氯胺酮MECT組、 聯合MECT組,每組40例。異丙酚MECT組男21例,女19例,年齡21~44(30.83±3.21)歲;病程1.8~13.9(7.8±1.2)年;莫茲利分級(MSM):中度29例,重度11例;誘因:身體疾病17例,社會心理因素14例,無誘因9例;臨床表現:睡眠障礙17例,食欲下降31例,軀體不適36例,頭痛32例,頭暈21例;并發癥:神經衰弱38例,失眠17例,高血壓7例,低血壓6例;既往治療史:6個月前曾治療過1次,家族遺傳史7例。氯胺酮MECT組男22例,女18例,年齡22~45(30.91±3.52)歲;病程1.9~14.0(7.9±1.3)年;MSM分級:中度30例,重度10例;誘因:身體疾病16例,社會心理因素16例,無誘因8例;臨床表現:睡眠障礙16例,食欲下降30例,軀體不適37例,頭痛33例,頭暈22例;并發癥:神經衰弱37例,失眠16例,高血壓6例,低血壓7例;既往治療史:8個月前曾治療過1次,家族遺傳史7例。聯合MECT組男20例,女20例,年齡21~45(30.93±3.31)歲;病程1.8~13.92(7.9±1.3)年;MSM分級:中度31例,重度9例;誘因:身體疾病18例,社會心理因素15例,無誘因7例;臨床表現:睡眠障礙17例,食欲下降32例,軀體不適35例,頭痛33例,頭暈22例;并發癥:神經衰弱36例,失眠17例,高血壓5例,低血壓8例;既往治療史7個月前曾治療過1次,家族遺傳史6例。3組患者一般資料比較差異無統計學意義(P>0.05),具有可比性。本研究方案的制定符合《世界醫學協會赫爾辛基宣言》的相關要求,經醫院倫理委員會審核批準,患者及家屬知情同意并簽署知情同意書。
1.2 病例選擇標準 (1)納入標準:①年齡18~45歲;②符合《中國精神障礙分類與診斷標準》第3版CCMD-3中關于抑郁癥的診斷標準;③采用≥2種抗抑郁藥物按規范化治療后無效;④漢密爾頓抑郁量表(HAMD-17項)評分≥20分。(2)排除標準:①不適合進行MECT治療者;②同時合并其他精神障礙,如癡呆、精神分裂癥;③高血壓、青光眼、動脈瘤,或腦血管畸形;④既往麻醉劑過敏史;⑤存在對酒精濫用等依賴病史;⑥體內存在起搏器或腦內電極等金屬異物。
1.3 治療方法 治療前患者均禁食8 h,麻醉過程:患者均給予阿托品1 mg, 異丙酚MECT組給予異丙酚1.0 mg/kg,氯胺酮MECT組給予氯胺酮1.0 mg/kg,聯合MECT組給予氯胺酮0.5 mg/kg、異丙酚1.0 mg/kg;麻醉后面罩給氧手控呼吸。待患者腱反射消失且全身肌肉松弛后,將患者貼電極處的皮膚進行清潔,測電阻(正常電流量>500 Ω,<2 500 Ω),等待醒脈通電抽搐治療儀(美國)顯示準備狀態,將電極片放置于患者顳部兩側,若患者年齡<20歲,電阻則選擇年齡值的50%;若患者年齡20~25歲,電阻則選擇年齡值的60%;若患者年齡>25歲~<45歲,電阻則選擇年齡值的70%~80%;若患者年齡45~50歲,電阻則選擇年齡值的100%或120%。選擇DGX模式3 min,2XDOS模式4 min,治療結束后待患者恢復自主呼吸后安全離開治療室。每周治療3次,每次間隔1~2 d,總療程為8次, 在3周內完成。治療過程均由同一組治療醫師及麻醉醫師共同完成。為確保患者的治療安全性,進行MECT時必須監護呼吸、血氧飽和度、腦電圖(EEG)、促性腺激素(ECG)及排空大小便,且在治療過程中禁用其他抗癲癇藥、抗焦慮藥及精神病藥。
1.4 臨床療效評價 治療8次后采用漢密爾頓抑郁量表(HAMD)[4],蒙哥馬利抑郁量表(MARDS)[5],臨床總體印象量表(CGI)[6],簡明精神病量表(BPRS)[7]對患者進行評價。其中HAMD包括精神和軀體2個維度,共14個項目,評分采用5級評分法,0分為無癥狀,4分為極重,得分越高表示患者癥狀越嚴重。MARDS包括內心緊張、睡眠減少等共10個條目,評分0~6分,0分為無癥狀,6分為極度嚴重,得分越高表示患者癥狀越明顯。CGI可分為病情嚴重程度、療效總評及療效指數3個維度,評分為0~7分,0分為無病,7為極重,得分越高表示患者癥狀越明顯。BPRS共18個項目,評分為1~7分,1分為無病,7分為極度嚴重,得分越高表示患者癥狀越明顯。痊愈:各項總評分減分率≥75%;顯效:各項總評分減分率50%~74%;好轉:各項總評分減分率30%~49%;無效:各項總評分減分率<30%。總有效率=(痊愈+顯效+好轉)/總例數×100%。
1.5 觀察指標與方法
1.5.1 認知功能評估: 在治療前和末次治療結束1周時,采用神經認知功能測驗(MCCB)量表[8]評估認知功能,該量表包括7個心理維度和10項分測驗,總分越高表示患者恢復越好。
1.5.2 血清腦源性神經營養因子(BDNF)及BDNF/BDNF前體(pro-BDNF)比值: 觀察治療前和末次治療結束1周后翌日清晨抽取空腹肘靜脈血3~5 ml,離心取上清保存于-80℃ 冰箱待測。采用雙抗體夾心ELISA法檢測血清BDNF水平,并計算血清BDNF/pro-BDNF比值,其比值越高表示抗抑郁效果越好,反之則效果差。
1.5.3 腦電慢波發生率檢測:患者腦電圖慢波特征均采用美國Cadwell公司生產的Easy Ambulatory 腦電圖儀及上海諾誠電氣有限公司生產的NATION7128W視頻腦電圖儀進行觀察,統計屏幕上出現腦電慢波的例數,基線腦電慢波水平可預測患者對氯胺酮治療的療效。腦電慢波發生率=出現腦電慢波的例數÷總例數×100%。
1.5.4 不良反應(TESS)評定[9]:根據患者出現行為毒性可分為中毒性意識模糊、興奮或激越、情感憂郁及活動增加,根據嚴重程度評分:無為0分,較輕為1分,輕度為2分,中度為3分,重度為4分。
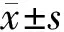
2 結 果
2.1 3組治療效果比較 治療后,聯合MECT組總有效率(95.0%)優于異丙酚MECT組(50.0%)(χ2=62.297,P<0.001),而與氯胺酮MECT組(92.5%)比較,差異無統計學意義(χ2=0.213,P=0.644),見表1。
2.2 3組治療前后MCCB總分比較 治療前,3組MCCB總分比較,差異無統計學意義(P>0.05);治療后,3組MCCB總分均提高,且聯合MECT組>氯胺酮MECT組>異丙酚MECT組(P均<0.01),見表2。
2.3 3組治療前后血清BDNF及BDNF/pro-BDNF比值比較 治療前,3組患者血清BDNF水平及血清BDNF/pro-BDNF比值比較,差異無統計學意義(P>0.05);與治療前比較,治療后異丙酚MECT組上述指標變化不明顯(P>0.05),而氯胺酮MECT組及聯合MECT組均增高,且聯合MECT組高于氯胺酮MECT組(P均<0.01),見表3。
表1 3組患者治療8次后效果比較 [例(%)]
表2 3組患者治療前后MCCB總分比較分)
表3 3組患者治療前后血清BDNF及BDNF/pro-BDNF比較
2.4 3組腦電慢波發生率比較 治療后,聯合MECT組腦電慢波的發生率5.0%(2例)低于氯胺酮MECT組25.0%(10例)低于異丙酚MECT組72.5%(29例)(χ2=38.393,P<0.01)。
2.5 3組不良反應評分比較 治療后,不良反應評分異丙酚MECT組為(9.67±2.38)分,氯胺酮MECT組為(9.92±3.01)分,聯合MECT組為(9.41±2.17)分,3組比較,差異均無統計學意義(F=0.402,P=0.670)。
3 討 論
抑郁癥是全球重大的慢性、致殘性精神疾病之一,預計到2030年抑郁癥的發病率將位居所有疾病負擔的首位[10]。該病的主要特點為高患病率、高致殘率、高自殺率及高復發率,其中最為嚴重的后果為自殺死亡。相關研究提示[11],近50%的抑郁癥患者采用一線抗抑郁藥物治療無效,近33%的抑郁癥患者對2種或2種以上的藥物及心理干預并無效果,該類抑郁癥被稱為TRD。目前公認TRD最為有效的治療方法為MECT,其緩解率為50%~70%。大部分TRD患者經MECT治療后,會伴隨不同程度的認知功能損害,影響MECT在臨床的推廣。故如何提高MECT治療TRD的臨床療效,同時減少認知不良反應具有重要臨床意義。
氯胺酮是苯環己哌啶的衍生物,是一種麻醉劑,該藥具有潛在的快速抗抑郁效果,已成為精神醫學領域研究的重點及熱點[12]。有臨床研究提示[13],采用氯胺酮治療單相和雙相抑郁,能迅速緩解患者的自殺觀念。故相關研究推測,氯胺酮可作為MECT麻醉劑以提高其治療效果。異丙酚又稱丙泊酚,是臨床常用的一種快速強效的全身麻醉劑,具有起效快、持續時間短、蘇醒快而平穩,且安全性高,該藥已在臨床廣泛應用。MECT是將處于麻醉狀態的TRD患者通過短暫、適量的電流對大腦造成刺激,在其腦內誘發一次癲癇發作,從而達到控制精神癥狀的一種物理療法。已有相關小樣本研究對不同麻醉劑在治療MECT時的療效進行對比,如Wang等[14]通過研究發現,治療后,混合組(氯胺酮合并異丙酚)與氯胺酮組的臨床療效明顯優于異丙酚組,且混合組不良反應明顯低于氯胺酮組與異丙酚組,由此可推斷將ketafol麻醉作為首選的MECT麻醉劑。Amini等[15]研究提示,氯胺酮是一種安全有效的麻醉藥物,且起效快。本研究結果與以往研究相似,提示ketafol麻醉MECT治療TRD起效更快,HAMD、MARDS、CGI、BPRS量表評分均明顯改善。
研究提示[16],MECT會對患者的記憶及認知功能造成不同程度的影響,特別是對近記憶的影響更為明顯,損傷程度有限且具有可逆性,停止用藥后過段時間可恢復正常。Chen等[17]將氯胺酮作為麻醉劑,結果顯示,氯胺酮對患者的認知功能損傷更少。本研究結果與之相似,聯合MECT組MCCB總分增加,提示ketafol麻醉MECT可減少對TRD患者認知功能的損害,使TRD患者定向力恢復更佳,對其短期記憶功能損害較少。
BDNF主要在中樞神經系統內表達,集中分布在皮質、杏仁核及海馬,其主要作用為刺激和促進神經細胞生長分化、對神經細胞存活和正常功能起到維持作用,可調控活性依賴的突觸修飾、效能和聯系。已有相關研究證實[18],BDNF可參與神經元的生存,是神經可塑性的分子標志物,參與中樞神經系統中5-HT神經元的可塑性,對神經系統的發育和成熟具有重要作用,參與抑郁障礙的生理病理過程。大腦和外周中存在豐富的BDNF,且在人類血漿及血清中均存在,血清BDNF水平明顯高于血漿100倍,上述差異主要是由于凝血過程中血小板脫落顆粒造成的。故血漿BDNF水平可充分反映循環血液的水平,且BDNF可透過血腦屏障循環,從而可能促進產生大腦神經元和基底節細胞,因此,可通過測量人體血漿BDNF水平反映大腦BDNF水平。諸多研究證實[19],BDNF表達參與了抑郁癥的病理過程。抑郁癥與BDNF水平下降有關,抑郁癥患者大腦BDNF水平降低會影響血循環BDNF水平。文獻研究提示,抑郁癥的發病與大腦神經網絡可塑性受損呈正相關,BDNF水平降低反映了神經網絡和可塑性受損,且BDNF水平降低會造成邊緣結構的縮小,引發情緒障礙[20]。相關研究提示,TRD患者血清BDNF水平降低,經有效治療后BDNF水平上升,提示BDNF水平為反映抗抑郁療效的生物學指標,且BDNF在抑郁癥的病理生理機制和恢復過程中起到重要的作用[21]。Vasic等[22]研究提示,抑郁癥患者的腦組織形態學改變為海馬狀突起明顯較正常人的腦組織小,其細胞數目減少或神經膠質細胞及神經元縮小,給予有效治療后可逆轉或阻止神經元縮小及神經細胞數目減少,提示抑郁癥發病與腦損傷相關。Su等[23]研究提示,抑郁癥患者BDNF水平降低可能與萎縮的海馬體積、神經細胞凋亡及某些神經元攝取神經營養因子能力降低相關。最新研究提示[24],MECT治療和亞麻醉劑量的氯胺酮治療TRD有可能促使血清BDNF水平升高。最新報道指出[25],pro-BDNF是BDNF釋放進入循環系統的初始形式,pro-BDNF與胰島素類似,在機體內循環系統經酶切后轉化為活性更高的BDNF,由此可推斷反映抗抑郁療效的有效指標可能是BDNF/pro-BDNF的比值。喬卉等[26]研究證實,BDNF及pro-BDNF均參與了應激性抑郁的發生,其在神經元可塑性變化中發揮了重要作用。 陳英等[27]研究提示,將氯胺酮作為麻醉劑可有效提高TRD患者血清BDNF濃度水平;黃雄等[28]研究也證實,以氯胺酮作為麻醉劑可有效提高MECT治療難治性抑郁癥患者BDNF濃度水平。本研究結果與上述研究相符,這與ketafol麻醉MECT治療可刺激TRD患者血清BDNF水平、BDNF/pro-BDNF比值有關,可減少神經細胞凋亡、預防海馬體積縮小及發揮維護神經元正常狀態的作用,確保神經突觸的可塑性,從而作用于丘腦與垂體釋放促腎上腺皮質激素,改善腦損傷。
在抑郁癥患者中慢波睡眠明顯降低,特別是睡眠早期階段。有效地抗抑郁治療可增加慢波睡眠比例。反映大腦皮質神經元突觸可塑性的有效指標是睡眠腦電圖活動。且已有相關研究提示,對抑郁癥患者采用亞麻醉劑量的氯胺酮注射治療后,可明顯增加抑郁癥患者睡眠早期階段的睡眠腦電圖慢波活動,而基線睡眠腦電圖慢波水平可預測抑郁癥患者對氯胺酮治療的療效。且MECT治療的主要作用機制是誘導大腦皮質增加睡眠腦電圖慢波水平。氯胺酮是一種精神活性物質,若劑量過高會誘發精神病性癥狀,且其可興奮交感神經;另外可大量激活兒茶酚胺,故氯胺酮在MECT治療時是否會誘發清醒恢復期的興奮激越行為,是否會成癮,是否會導致患者血壓升高而引發意外需進一步研究。本研究結果顯示,ketafol麻醉MECT并不會對腦電慢波的發生率造成不良影響,且不會增加不良反應,其原因如下:(1)氯胺酮具有抗抑郁作用,主要表現為通過升高BDNF水平和增加腦電慢波,從而改變中樞神經系統的突觸可塑性,而誘導大腦皮質增加腦電慢波水平一直被認為是MECT治療的作用機制之一。(2)由于ketafol麻醉MECT需要的電流量較小,且具有較高的抽搐指數及長時間抽搐,與治療的最終療效和認知不良反應程度密切相關。由此可推斷,ketafol麻醉MECT能夠提高TRD患者的療效,同時減少認知不良反應,中樞突觸可塑性的改變是重要的作用機制。但由于本研究所納入樣本量較少,且未對BDNF基因Val66Met位點基因分型進行分析,尚需擴大樣本量進行更深一步研究,應同時對TRD患者的BDNF基因Val66Met位點基因分型展開分析。
總之,在TRD患者中采用ketafol麻醉MECT治療,效果明顯優于氯胺酮MECT和異丙酚MECT,且可減少對TRD患者認知功能的損傷,提高血清BDNF水平及血清BDNF/pro-BDNF比值,減少腦電慢波的發生率,且安全性較高。ketafol麻醉MECT治療TRD患者的主要機制為其可減少認知不良反應,改變中樞突觸的可塑性。
利益沖突:所有作者聲明無利益沖突
作者貢獻聲明
古智文、黃雄:提出研究方向、思路、選題,制定方案、流程,撰寫論文;張春平:進行文獻整理;王志杰、張敏玲:實施研究過程,數據收集,分析整理

