不同eGFR公式與ACR聯合應用在腎功能損傷高危人群中的臨床價值
徐文俊,李甲勇,李會丹
(上海交通大學附屬第一人民醫院檢驗醫學中心,上海 200080)
慢性腎病(chronic kidney disease,CKD)是各種原因引起腎臟結構和功能異常的一類疾病,以出現腎臟損傷標志物或腎小球濾過率(glomerular filtration rate,GFR)<60 mL/(min·1.73 m2)且持續時間超過3個月為診斷標準。根據GFR分期標準,G2期屬于腎功能下降早期、腎功能輕度受損,G3~G5期為腎功能中度受損至腎功能衰竭[1]。高血壓、糖尿病、心血管疾病等慢性疾病患者是腎功能損傷的危險人群,常會繼發CKD。全世界CKD患病率為14.3%,我國18歲以上人群的患病率為10.8%[2],若能早期診斷,盡早干預,即可顯著改善患者腎功能。長久以來,臨床將估算腎小球濾過率(estimated glomerular filtration rate,eGFR)作為診斷、監測腎功能的首選指標,但各估算公式由于標志物的不同,導致計算結果與實際GFR出現不同程度的偏差,在不同種族、人群和性別中的適用性也不同。另外,尿白蛋白/肌酐比值(albumin to creatinine ratio,ACR)是判斷腎小球濾過膜電荷、機械屏障受損的敏感指標,其價值越來越為被臨床認可[3]。為此,本研究擬探討基于胱抑素C(cystatin C,Cys C)的eGFR對基于血清肌酐(serum creatinine,SCr)的eGFR的彌補作用以及聯合ACR后對提高高危人群中腎功能損傷和早期腎功能下降檢出率的價值。
1 材料和方法
1.1 研究對象
選取2016年1月—2017年12月上海市第一人民醫院內分泌科和腎內科的住院患者1 253例,通過查閱患者病史,收集性別、年齡、身高、體重、SCr、血清Cys C、ACR、血清尿素、血清尿酸(uric acid,UA)、基于99m锝-二乙烯三胺五乙酸(99mtechnetium-diethylene triamine pentaacetic acid,99mTC-DTPA)腎動態顯像法的測量腎小球濾過率(measuring glomerular filtration rate,mGFR)及基礎病史等資料。計算體質量指數(body mass index,BMI)及體表指數(body surface area,BSA),BMI(kg/m2)=體質量(kg)/身高(m)2,BSA=0.007 184×體質量(kg)0.425×身高(cm)0.725。排除標準:(1)患急性腎臟病或急性腎功能不全;(2)既往做過一側或雙側腎臟手術,如腎移植、腎切除等;(3)合并腎臟其他疾病,如腎臟占位、嚴重腎積水等;(4)腎動態顯像前1周內做過透析治療;(5)合并水腫、胸腔積液、腹腔積液或甲狀腺疾病、病毒性肝炎(不含肝炎病毒攜帶者);(6)肢體、五官及體表不全;(7)正在服用藥物,尤其是苯羥磺酸鈣、甲氧芐啶和西米替丁;(8)前3個月應用過激素;(9)患白血病或惡性腫瘤。根據以上排除標準,共入選符合CKD診斷標準的患者850例,男511例,年齡59(51~67)歲,女性339例,年齡62(55~71)歲。850例患者中患糖尿病559例(65.8%)、高血壓540例(63.5%)、冠心病165例(19.4%)、動脈粥樣硬化599例(70.5%)。參照mGFR結果并依照腎臟病預后質量倡議(the Kidney Disease Out-comes Quality Initiative,K/DOQI)指南的分期標準,將850例患者分為6期,具體結果見表1。以G2期為早期腎功能下降,以G3~G5期為腎功能受損。

表1 腎功能分期標準及患者分期結果
1.2 樣本采集及測定
采用干燥真空無菌管采集所有對象入院后第2天清晨空腹靜脈血,1 000×g離心10 min,分離血清;同時留取10 mL晨尿(中段),1 000×g離心5 min,取上清。
SCr、血清尿素、血清UA、血清Cys C及尿Cr采用cobas 8000全自動生化分析儀(瑞士羅氏公司)及配套試劑檢測。尿微量白蛋白(microalbumin,mAlb)采用BNⅡ特定蛋白分析儀及配套試劑(德國西門子公司)檢測。嚴格按標準操作規程進行操作,所有儀器質控均在控。
1.3 mGFR
mGFR采用核素腎動態顯像Gate'S法[4]測定,檢測儀器為EXCEL EVO型單光子發射計算機斷層掃描系統(德國西門子公司),配低能高分辨率平行孔準直器(能峰140 keV,窗寬±20%)。99mTC-DTPA由上海原子科興藥業有限公司提供。顯像前20~30 min使患者充分水化(常規飲水300~500 mL),于前臂肘靜脈彈丸式注射99mTC-DTPA 0.5 mL(185 MBq/mL)后立即進行雙探頭前后位動態采集圖像。前1 min采集血流灌注相,2 s/幀,共30幀;后20 min采集皮質功能相,1 min/幀,共20幀。在后期處理軟件中輸入患者的身高、體質量信息,勾畫腎臟及本底的感興趣區(region of interest,ROI)并采用Gate'S法測定雙側腎臟的GFR。本研究中mGFR為雙側腎臟mGFR之和。
1.4 eGFR公式[5]
分別采用3種基于SCr的eGFR公式(CKDEPI 2009SCr公式、簡化MDRD方程和改良MDRD方程)、6種基于Cys C的eGFR公式(CKD-EPI 2012Cys C公式、Grubb公式、Arnal-Dade公式、Rule公式、Macisaac公式、Tan公式)和1種基于Cys C、SCr聯合檢測的eGFR公式(CKD-EPI 2012SCr-Cys C公式)計算eGFR。見表2。

表2 各種eGFR公式
1.5 統計學方法
采用SPSS 19.0軟件進行統計分析。采用K-S檢驗進行正態性檢驗。呈正態分布的數據以±s表示,組間比較采用t檢驗。呈非正態分布的數據以中位數(M)[四分位數(P25~P75)]表示,2個組之間比較采用Mann-WhitneyU檢驗,多組間比較采用Kruskal-Wallis檢驗。計數資料以率表示,組間比較采用χ2檢驗。各項目之間的相關性采用Spearman相關分析。eGFR與mGFR的一致性采用Bland-Altman一致性分析進行評價。以P<0.05為差異有統計學意義。
2 結果
2.1 不同性別的CKD患者之間一般資料及eGFR、mGFR的比較
男、女性CKD患者基于SCr的eGFR水平均高于mGFR(P<0.01),基于血清Cys C的eGFR水平均低于mGFR(P<0.01)。見表3。
2.2 不同公式計算的eGFR之間及與mGFR的相關性
2.2.1 基于SCr的3種eGFR公式之間及與mGFR的相關性 eGFR簡化MDRD、eGFR改良MDRD、eGFRCKD-EPI2009SCr與mGFR均呈正相關(r值分別為0.800、0.799、0.812,P<0.01);eGFR簡化MDRD、eGFR改良MDRD和eGFRCKD-EPI2009SCr之間均呈正相關(P<0.01)。見表4。

表3 CKD患者不同性別之間一般資料及eGFR、mGFR的比較

表4 基于SCr的eGFR之間及與mGFR的相關性 r值
2.2.2 基于Cys C的6種eGFR公式之間及與mGFR的相關性 eGFRMacisaac、eGFRRule、eGFRTan、eGFRGrubb、eGFRCKD-EPI2012CysC、eGFRArnal-Dade均與mGFR呈正相關(r值分別為0.793、0.793、0.793、0.793、0.809、0.793,P<0.01);eGFRMacisaac、eGFRRule、eGFRTan、eGFRGrubb、eGFRCKD-EPI2012CysC和eGFRArnal-Dade之間均呈正相關(P<0.01)。見表5。

表5 基于Cys C的eGFR之間及與mGFR的相關性 r值
2.2.3 基于SCr和Cys C聯合檢測的eGFR公式與mGFR的相關性 eGFRCKD-EPI2012SCr-CysC與mGFR呈正相關(r=0.838,P<0.01)。
2.3 eGFR與mGFR的一致性
Bland-Altman一致性分析結果顯示,基于SCr的3種eGFR公式計算出的eGFR與mGFR的平均偏差為-4.2~-20.8 mL/(min·1.73 m2),高估了患者的GFR,落在界限外的百分比為2.71%~3.18%。基于Cys C的6種eGFR公式計算出的eGFR與mGFR的平均偏差為3.7~16.9 mL/(min·1.73 m2),低估了患者的GFR,落在界限外的百分比為2.94%~3.76%。基于SCr與Cys C聯合檢測的eGFR公式計算出的eGFR與mGFR的平均偏差為9.6 mL/(min·1.73 m2),低估了患者的GFR,落在界限外百分比為3.53%。
基于SCr的3種eGFR公式中以eGFRCKD-EPI2009Scr與mGFR的一致性最好,基于Cys C的6種eGFR公式中以eGFRMacisaac與mGFR的一致性最好,基于SCr與Cys C聯合檢測的eGFRCKD-EPI2012SCr-CysC與mGFR的一致性結果不理想。見表6、圖1、圖2。

表6 不同eGFR公式得出的eGFR與mGFR的Bland-Altman一致性分析

圖1 eGFRCKD-EPI 2009SCr與mGFR的Bland-Altman圖

圖2 eGFRMacisaac與mGFR的Bland-Altman圖
2.4 基于SCr的eGFR公式聯合eGFR-sCys C和/或ACR對腎功能異常檢出率的分析
以eGFRCDK-EPI2009SCr為基于SCr的eGFR公式的代表,以eGFRMacisaac為基于Cys C的eGFR公式的代表,聯合ACR進行腎功能異常檢出率的分析。將因eGFRCDK-EPI2009SCr>mGFR導致G2期誤分為G1期或G3~G5期誤分為G2期作為eGFRCDK-EPI2009SCr漏檢。
在G2期患者中,依據eGFRCDK-EPI2009SCr結果漏檢患者為154例(45.4%),其中分別有122例(79.2%)和86例(55.8%)可依據eGFRMacisaac60~<90 mL/(min·1.73 m2)和ACR>30 μg/mg被檢出,eGFRMacisaac與ACR聯合可檢出135例(87.7%)。
在G3~G5期患者中,依據eGFRCDK-EPI2009SCr結果漏檢患者為90例(31.1%),其中分別有39例(43.3%)和55例(61.1%)可依據eGFRMacisaac<60 mL/(min·1.73 m2)和ACR>30 μg/mg被檢出。eGFRMacisaac與ACR聯合可檢出66例(73.3%)。
分別用eGFRCKD-EPI2009SCr、eGFRCKD-EPI2009SCr+eGFRMacisaac、eGFRCKD-EPI2009SCr+ACR、eGFRCKD-EPI2009Scr+eGFRMacisaac+ACR 4種模式對G2期、G3期~G5期患者進行篩查,G2期以滿足eGFRCKD-EPI2009SCr或eGFRMacisaac<90 mL/(min·1.73 m2)、ACR>30 μg/mg中任意一項為陽性檢出,G3~G5期滿足以eGFRCKD-EPI2009SCr或eGFRMacisaac<60 mL/(min·1.73 m2)、ACR>30 μg/mg中任意一項為陽性檢出。在G2期和G3~G5期的篩查中,eGFRCKD-EPI2009SCr+eGFRMacisaac+ACR模式可將陽性檢出率分別提高至94.4%、91.7%。見表7。
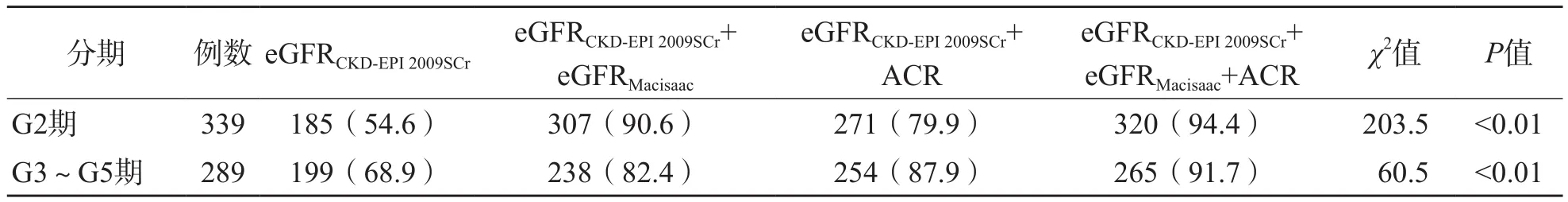
表7 4種檢測模式對G2期和G3~G5期患者檢出率的比較
2.5 eGFRCKD-EPI 2009SCr+eGFRMacisaac+ACR聯合應用漏檢患者血清尿素、UA水平分析
G2期患者采用eGFRCKD-EPI2009SCr+eGFRMacisaac+ACR模式判別后仍有19例患者被漏檢,漏檢患者的血清尿素水平明顯高于G1期患者(P<0.05),而血清UA水平差異無統計學意義(P>0.05)。見表8。
G3~G5期患者采用eGFRCKD-EPI2009Scr+eGFRMacisaac+ACR判別后仍有24例患者被漏檢,漏檢患者的血清尿素、UA水平與G1期+G2期患者比較,差異均無統計學意義(P>0.05)。見表9。

表8 eGFRCKD-EPI 2009SCr+eGFRMacisaac+ACR模式判別G2期漏檢患者的血清尿素、UA水平分析M(P25~P75)

表9 eGFRCKD-EPI 2009SCr+eGFRMacisaac+ACR模式判別G3~G5期漏檢患者的血清尿素、UA水平分析M(P25~P75)
3 討論
流行病學統計結果顯示,我國CKD患者數在2012年就已達到了1.2億,且呈逐年上升趨勢[2]。高血壓、糖尿病和心血管疾病等高發慢性病大大增加了腎臟損傷的風險[1]。腎臟一旦形成器質性損傷,病情就不可逆轉,前驅病因的持續存在或加劇促進了腎功能衰竭的發生。本研究患者中有65.8%患糖尿病、63.5%患高血壓、19.4%患冠心病、70.5%患動脈粥樣硬化。在這些基礎疾病的持續負作用下,本研究1 253例患者中僅有26.1%的患者腎功能正常(G1期),39.9%的患者出現早期腎功能下降(G2期),剩余44.0%的患者腎功能受損(G3~G5期)。處于G2期的患者通過早期干預、慎用藥物、著重監測,發展為G3期以上的風險將大大降低。處于G3~G5期的患者的生存時間和生存質量將受到影響,除了要更加謹慎地對待腎臟功能下降的趨勢外,更要面臨考慮最終措施——透析或移植。因此,對于腎臟功能的正確評估是臨床關注的焦點及患者預后的重點[6]。
目前,國內、外均以mGFR作為臨床評估腎臟功能的金標準,但由于準備和操作過程繁瑣,且為有創檢查,需要使用同位素制劑,因此其在臨床上的應用受到了一定的限制[4]。與mGFR結果有較好一致性的eGFR,僅需采集患者血液檢測SCr、Cys C就可計算GFR,現已作為腎功能篩查的有效方法。目前臨床上已有多個eGFR公式,但對于各種公式的適用人群范圍、適用腎功能階段及與mGFR的一致性等問題始終存在不同的觀點[7-10]。因此,為了更準確地反映腎功能改變,需要選出最適合本地區人群的代表公式。本研究結果顯示,基于SCr的3種eGFR公式之間和基于Cys C的6種eGFR公式之間均呈正相關(P<0.01),說明基于同一標志物計算出的eGFR結果具有同一趨勢。Bland-Athman一致性分析結果顯示,eGFRCKD-EPI2009SCr與mGFR呈正相關(r=0.812,P<0.01),平均偏差為-4.2 mL/(min·1.73 m2),高估了患者的GFR;eGFRMacisaac與mGFR呈正相關(r=0.793,P<0.01),平均偏差為3.7 mL/(min·1.73 m2),低估了患者的GFR。依據一致性分析結果,以eGFRCKD-EPI2009SCr為基于SCr的eGFR公式的代表,以eGFRMacisaac為基于Cys C的eGFR公式的代表。
除了GFR,ACR也是診斷腎功能損傷的常用指標之一。在相關共識中,均以GFR<60 mL/(min·1.73 m2)或ACR≥30 μg/mg持續3個月及以上作為診斷CKD的重要標準[1,11]。美國腎臟病協會(the National Kidney Foundition,NKF)也明確將ACR列入CKD診斷標準,并且要求在3~6個月內至少檢測3次ACR,有2次異常方可診斷為CKD[12]。但在實際工作中,以SCr及基于SCr的eGFR為主的臨床篩查、診斷過程較為常見,ACR的使用遠不及eGFR。
由于eGFR是通過血流灌注、腎臟濾過水平來反映腎臟功能,因此也有局限性,且受諸多因素影響。在有些情況下是血流灌注降低而非腎實質受損,如突發的心力低下造成大循環血流不足,從而降低腎臟灌注;肝硬化患者大量腹水時由于醛固酮水平異常而并發“肝性腎病”,表面上出現SCr、UA水平升高及尿量減少,提示腎臟灌注不足,其實腎實質并未受到損傷,腹水消除后,腎功能恢復正常;還有些情況是腎實質已經受損但血流灌注仍未降低,如自身免疫性腎病,沉積的自身抗體激活補體損傷腎小球基底膜,早期因屏障效應降低導致尿微量白蛋白出現,后期演變成腎小球硬化時GFR才開始出現明顯下降。所以對于腎功能的全面評價,有必要將GFR與ACR聯合應用。本研究結果顯示,在G2期和G3~G5期使用eGFRCKD-EPI2009SCr判斷后漏檢的患者中分別有55.8%和61.0%的患者ACR異常。
由于SCr和血清Cys C在反映腎功能上有一定的差異,所以基于SCr或Cys C的eGFR也會出現一定的差異[13]。如單一使用基于SCr的eGFR,會造成一部分患者漏檢。本研究結果顯示,在G3~G5期患者中,有31.1%的患者eGFRCKD-EPI2009SCr>60 mL/(min·1.73 m2),出現高估患者GFR而漏檢的情況,通過eGFRMacisaac或ACR可以檢出其中43.3%或61.1%的患者,二者聯合可以檢出其中的73.3%;在G2期患者中,有45.4%的患者GFRCKD-EPI2009SCr>90 mL/(min·1.73 m2),出現高估患者GFR而漏檢的情況,通過eGFRMacisaac或ACR可以檢出其中79.2%或55.8%的患者,二者聯合應用可檢出其中87.7%的患者。在G2期患者中,eGFRCKD-EPI2009Scr、eGFRMacisaac和ACR聯合應用可將檢出率提高至94.4%;在G3~G5期患者中,可提高至91.7%。由此可見,基于SCr的eGFR、基于Cys C的eGFR和ACR聯合應用可顯著提高高危人群中腎功能損傷與早期腎功能下降者的檢出率。但三者聯合應用后仍存在一定的漏檢情況,分析這些漏檢患者的情況,僅G2期中漏檢患者的血清尿素水平高于G1期患者(P<0.05),其他項目差異均無統計學意義(P>0.05)。提示由此入手尋找相關切點來完善腎功能改變的檢出是有可能的。然而由于樣本量的限制,本研究未能給出相關結論,這也是本研究的不足之處。另一個不足就是所有患者的ACR僅檢測了1次,且無24 h尿蛋白結果,這也可能是本研究使用ACR判斷G2期漏檢患者腎功能損傷的敏感性不及eGFRMacisaac的原因。
綜上所述,基于SCr的eGFR存在高估患者GFR的情況,將eGFRCKD-EPI2009SCr、eGFRMacisaac和ACR聯合應用可以有效解決這一問題。雖然Cys C是一個較敏感的腎功能標志物,但基于Cys C的eGFR會出現低估腎功能的情況。然而,該低估情況恰是一個腎功能損傷的風險提示,反而高估腎功能極易導致臨床忽視,進而產生不良后果。目前,對于eGFR公式的選擇和聯合ACR的使用尚無統一標準,實際工作中如何進行取舍需要通過循證及大數據的驗證,期望本研究結果能為臨床相關工作提供借鑒。

