早產兒李斯特菌敗血癥臨床特征及治療分析
余 劍,潘 濤,徐利曉,馮 星,孫 斌
(蘇州大學附屬兒童醫院,江蘇 蘇州 215000)
單核細胞增生性李斯特菌(listeria monocytogenes,LM)是一種胞內寄生的革蘭陽性無芽孢短小桿菌,屬于食物致病菌,其死亡率是食源性疾病中最高的[1]。人類食用了被LM污染的食物后通常會出現發熱、流感樣癥狀及腹痛嘔吐腹瀉等癥狀,嚴重時可出現敗血癥、腦膜炎和自發性流產等。受影響的主要是老人、孕婦及免疫功能低下的患者,新生兒感染的主要方式是母親垂直傳播。南非的一項流行病學調查發現,在實驗室確診的病例中41%是≤28天的新生兒,其中96%在生后一周發病,死亡率28%[2-3]。2004—2009年在美國報告的760例李斯特菌病病例中,17%與懷孕有關,圍產期死亡率(胎兒死亡和新生兒死亡)總體率為29%[4]。由于早產兒李斯特菌感染病例數報道較少,本文對14例早產兒李斯特菌敗血癥的臨床資料進行回顧性分析,進一步豐富早產兒李斯特菌敗血癥的診治經驗。
1資料與方法
1.1臨床資料收集
采用回顧性研究的方法,收集2011年1月至2020年10月蘇州大學附屬兒童醫院新生兒科血培養為LM的14例早產兒的臨床資料,回顧性分析患兒母親孕期病史、圍產期高危因素、臨床特點、實驗室檢查、抗生素治療及轉歸。該研究通過蘇州大學附屬兒童醫院倫理委員會批準并豁免知情同意,倫理號(2020CS090號)。
1.2血培養標本采集及細菌培養
患兒均在入院時嚴格消毒后經外周靜脈采集≥1.0mL血液標本,注入血培養瓶中,于60min內將標本送檢。血液標本采用專用微生物培養儀進行培養,在12~48h內有菌株生長則會收到報警,如無菌株生長則培養延長至5~7天。分離菌株采用專用微生物鑒定系統進行菌株鑒定。
1.3統計學方法
采用SPSS 18.0軟件進行數據處理。計數資料采用例數(n)和百分數(%)表示,不符合正態分布的計量資料以中位數(P25~P75)表示。以P<0.05為差異有統計學意義。
2結果
2.1母孕期情況
14例產婦的中位年齡為29.5歲(26.75~32.75歲),初產婦3例(21.42%),經產婦11例(78.57%)。13例(92.86%)產婦有臨床表現,其中7例(50%)出現產前發熱,3例(21.42%)出現流感樣癥狀,6例(42.85%)伴有不規則腹痛,4例(28.57%)陰道出血或流液,3例(21.42%)胎膜早破,4例(28.57%)出現胎心異常。
2.2發病季節分布
相關的LM敗血癥病例如圖1所示,發生在春季和夏季(即3—8月)較多,占總發病例數的92.86%(13/14)。

注:春季(3—5月)、夏季(6—8月)、秋季(9—11月)、冬季(12月至次年2月)。圖1 14例早產兒LM敗血癥病例數的季節分布Fig.1 Seasonal distribution of 14 premature infants with LM septicemia
2.3一般情況及圍產期高危因素
14例確診LM敗血癥的早產兒中,男性9例,女性5例,男女比為1.8∶1。胎齡中位數為32.4周(30.4~34.1周),入院年齡中位數為5h(2~14.5h),出生體質量中位數為1 885g(1 513~2 188g)。剖宮產7例(50%),自然分娩7例(50%);有宮內窘迫12例(85.71%),發生窒息12例(85.71%),胎膜早破2例(14.29%),羊水污染11例(78.57%),見表1。
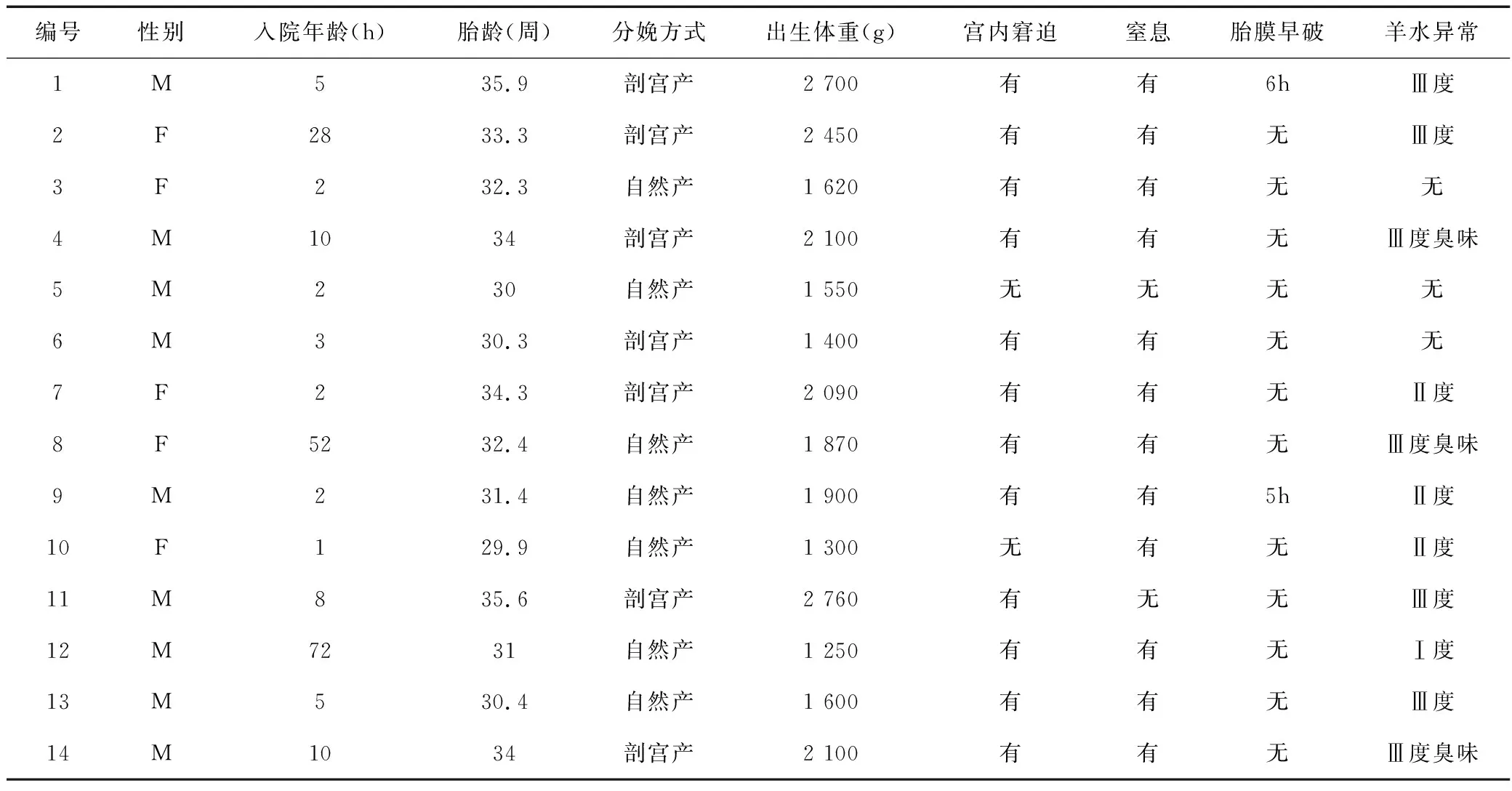
表1 14例早產兒LM敗血癥患兒的一般情況及圍產期高危因素Table 1 General information and perinatal risk factors of 14 premature infants with LM septicemia
2.4臨床表現及并發癥
14例確診LM敗血癥早產兒中,13例(92.86%)出現氣促呻吟,11例(78.57%)出現發熱或體溫不升,2例(14.29%)出現抽搐,2例(14.29%)出現腹脹,6例(42.86%)出現黃疸,8例(57.14%)出現出血點或紅色斑丘疹。14例患兒血培養均提示LM生長,血培養報警時間中位數16.5h(12.42~18.32h),9例進行了腦脊液檢查,6例(42.86%)腦脊液符合細菌性腦膜炎改變,1例腦脊液培養提示LM生長,5例因病情危重未行腦脊液檢查。13例(92.86%)患兒的胸片均有不同程度的肺部炎癥表現,其中6例(42.86%)出現呼吸窘迫綜合癥、7例(50%)感染性休克、3例(21.43%)出現肺出血、2例(14.29%)新生兒硬腫癥;6例(42.86%)顱內出血,其中4例頭顱磁共振發現存在顱內出血,2例行頭顱B超檢查發現腦室內大量出血;肝功能谷丙轉氨酶升高2例(14.29%);缺血缺氧性腦病2例(14.29%),見圖2。

圖2 14例早產兒李斯特敗血癥的并發癥情況Fig.2 Complications of 14 premature infants with LM septicemia
2.5輔助檢查
14例早產患兒中血常規白細胞計數(2.12~126)×109/L,7例(50%)明顯升高>25×109/L,2例(14.29%)明顯降低<5×109/L,8例(57.14%)血小板減少,最低為14×109/L。13例患兒行C反應蛋白(C-reactive protein,CRP)檢測,其中12例(92.31%)CRP≥8mg/L,最高為231mg/L。9例患兒行降鈣素原(procalcitonin,PCT)檢測,均>2ng/mL,最高者>62.35ng/mL。9例行腦脊液檢查,其中5例(55.56%)腦脊液白細胞升高,葡萄糖降低,1例(11.11%)腦脊液常規及生化正常,但腦脊液培養為陽性。
2.6抗生素使用情況及轉歸
14例患兒標本采集后均經驗性抗感染治療,血培養結果出來后更換抗生素,救治成功的7例(50%)患兒,其中6例使用美羅培南聯合阿莫西林舒巴坦或美洛西林,1例美羅培南聯合萬古霉素。電話隨訪患兒,其中4例預后良好,1例存在生長發育落后的后遺癥,2例失訪。死亡的7例患兒,其中3例單用頭孢菌素類藥物治療,1例用美羅培南聯合阿莫西林舒巴坦,1例用美羅培南聯合頭孢哌酮舒巴坦,1例單用美羅培南,1例用萬古霉素聯合美洛西林,見表2。
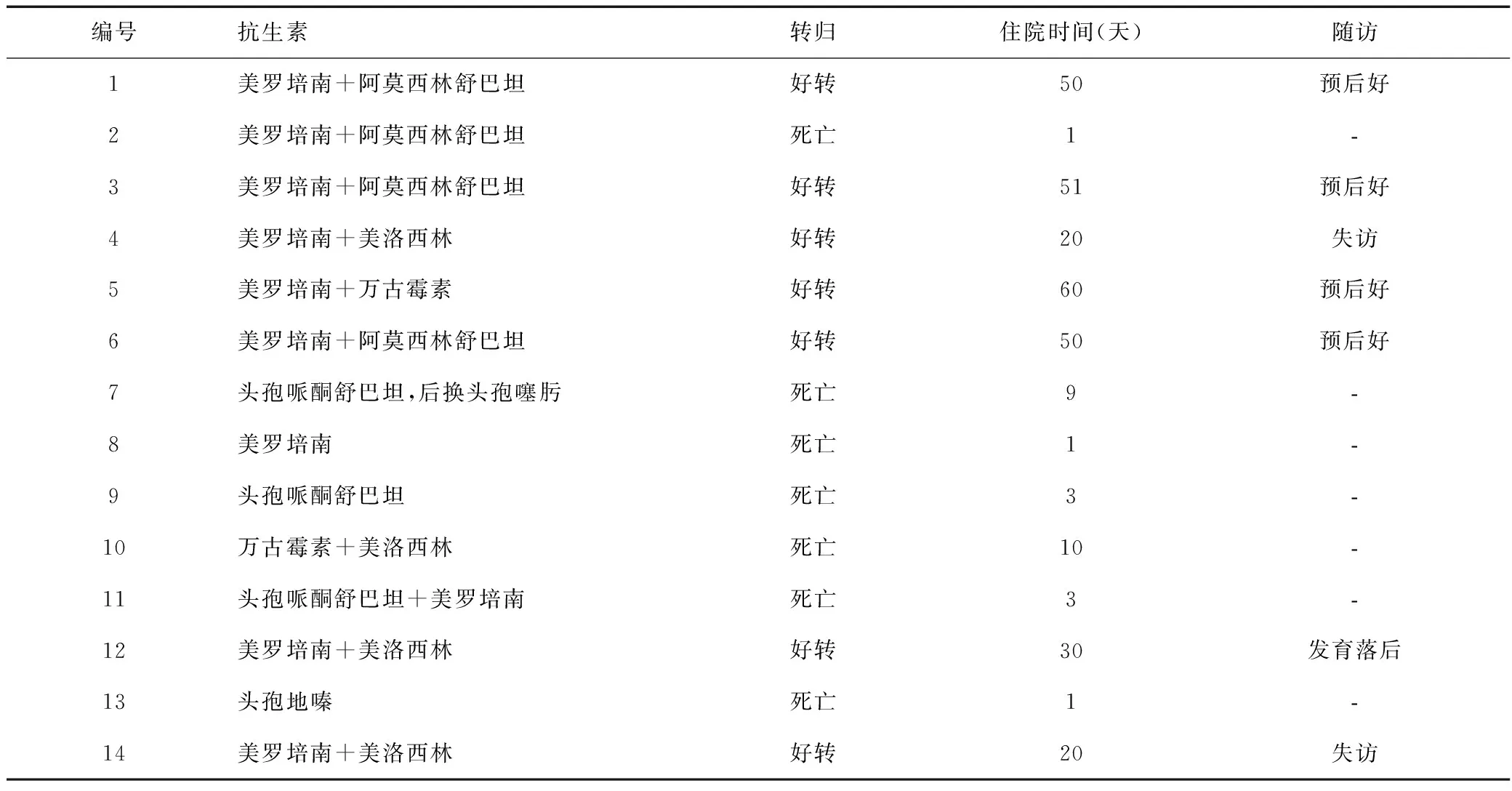
表2 14例早產兒LM敗血癥患兒的抗生素使用情況及轉歸Table 2 Antibiotic use and outcome of 14 premature infants with LM septicemia
3討論
3.1發病季節分布
李斯特菌廣泛分布于自然界中,為兼性厭氧菌,屬于革蘭陽性桿菌,該菌耐冷不耐熱,可以污染奶制品類、肉類、蔬菜水果等,在冰箱內可長期生存[5]。人類通常食用被污染的食物后而感染,與懷孕相關的李斯特菌病的發病率大約是普通人群的13倍,新生兒的感染途徑主要是感染的母親通過胎盤垂直傳播[6-7]。本研究發現LM感染發生在春季和夏季(即3—8月)較多,占總發病例數的92.86%(13/14例),分析原因可能與氣候炎熱導致孕婦食用容易被LM污染的未熟食物或冷藏食物等有關。本組病例中初產婦11例(78.57%),初產婦3例(21.42%),有2例產婦提及產前食用冷藏食品史,原因可能是大部分孕婦未意識到食用不潔或冷凍食物所帶來的風險。因此,應加強對妊娠期婦女的飲食宣教,建議孕婦避免食用李斯特菌污染風險高的食物,如水果蔬菜要在自來水中徹底的清洗,對于肉類熟食等食品需要加熱至74℃,奶制品要經過巴氏消毒等[8]。
3.2母孕期情況及圍產期高危因素
產婦感染可能是無癥狀的,當有癥狀時,感染通常表現為一種非特異性的流感樣癥狀,伴有發熱、肌肉痛、背痛和頭痛,通常在出現腹瀉或其他胃腸道癥狀之前[9]。然而,胎兒和新生兒感染可能是嚴重的,導致死胎、早產、新生兒敗血癥、腦膜炎和死亡。對11例李斯特菌病孕婦的病例和對222例文獻的回顧發現,大約1/5的孕婦并發李斯特菌病導致自然流產或死產;大約2/3存活的嬰兒發展為新生兒李斯特菌病[10-11]。早產兒LM敗血癥多為宮內感染,早發性敗血癥,發病時間早[12],本組病例早產兒胎齡中位數為32.4周(30.4~34.1周),入院年齡中位數為5h(2~14.5h),出生體重中位數為1 885g(1 513~2 188g)。有13例(92.86%)產婦有臨床表現,產婦有7例(50%)出現生產前發熱,3例(21.42%)出現流感樣癥狀,6例(42.85%)伴有腹痛。圍產期出現宮內窘迫12例(85.7%),發生窒息12例(85.71%),羊水污染11例(78.57%),與其他文獻報道一致[13]。對于產婦孕期出現發熱、流感樣癥狀、胎兒宮內窘迫、分娩時羊水有污染或者臭味等高危因素者,分娩時及時行血培養,羊水和胎盤組織培養,并盡早開始抗生素治療。
3.3患兒臨床表現、并發癥及治療效果
14例確診LM敗血癥的早產兒中,臨床表現主要為呼吸窘迫,發熱或體溫不升,皮膚出現出血點或典型紅色斑丘疹。實驗室檢查有7例白細胞明顯升高,2例明顯降低,8例血小板減少,最低為14×109/L,白細胞、血小板越低,可能提示病情越重;12例CRP≥8mg/L,最高者231mg/L,9例患兒行PCT檢測,均>2ng/mL,最高者>62.35ng/mL,CRP、PCT值的高低可反映感染的嚴重程度。白細胞、血小板、CRP、PCT的數值有助于判斷患兒感染的嚴重程度,而且監測其動態變化可評估抗感染的效果。本組病例中化膿性腦膜炎的發生率為42.86%,5例因病情嚴重未行腦脊液檢查,因此不能體現早產兒李斯特菌敗血癥中化膿性腦膜炎真實的發生率。9例行腦脊液檢查,其中5例腦脊液呈化膿性腦膜炎樣改變,1例腦脊液常規及生化檢查正常,但腦脊液培養為陽性,考慮原因是行腦脊液檢查的時機早,顱內尚未產生炎癥反應。死亡的7個病例中有5例在入院后3天內病情迅速進展,出現感染性休克、彌散性血管內凝血、肺出血導致死亡,其中病例2、病例3、病例13的入院年齡分別是出生28h、52h、5h,入院時已經出現感染性休克,并在數小時內迅速進展并死亡;病例9和病例11雖已得到血培養結果報警,由于藥敏結果未出,臨床醫生未意識到早產兒LM敗血癥的臨床特點,未及時更改有效抗生素,這兩例患兒在入院3天內因治療效果差并發彌散性血管內凝血、肺出血導致死亡;病例7由于未更換有效抗生素,治療效果差,病例10雖然更換萬古霉素+美洛西林治療,由于其胎齡小,體重低,治療效果不佳,這兩例并發腦膜炎和嚴重的顱內出血,家屬考慮預后不良,在生后第10天左右放棄治療后死亡。病例12雖然救治成功,但因其為31周1 250g的早產兒,入院年齡已72h,并發化膿性腦膜炎,在后期的隨訪中該患兒存在生長發育及智力發育落后。本研究中的死亡率為50%,遠高于文獻報道李斯特菌感染圍產期死亡率29%[4],可能由于本研究病例數少,且僅以早產兒為研究對象,并未納入足月兒及晚發性LM敗血癥患兒。早產兒LM敗血癥臨床癥狀不典型,難以早期識別,并且容易迅速進展為感染性休克,救治存活也容易合并細菌性腦膜炎和顱內出血,可留下不同程度的后遺癥。因此對于不明原因早產、出生時窒息,生后不久即出現呼吸窘迫、發熱、全身皮疹等癥狀的早產兒,需進一步詢問產前母親發熱或上呼吸道感染病史,臨床高度懷疑LM感染,應及時行血液相關指標及病原學檢查,盡快應用能覆蓋LM的抗生素。
本研究中,14例早產兒血培養均為陽性,血培養報警時間中位數16.5h(12.42~18.32h),其中9例根據血培養危急值回報,及時調整抗生素為美羅培南聯合青霉素類或者萬古霉素聯合青霉素類,救治成功7例,3例單用頭孢菌素類藥物感染均未得到有效控制。目前LM感染抗生素首選青霉素或氨芐西林[14],而我們臨床上對于早產兒感染非特異性臨床癥狀經常經驗性選用頭孢菌素類抗生素,但LM對此天然耐藥[15]。因此,對于高度懷疑LM感染的早產兒應盡早使用青霉素或氨芐西林,嚴重病例應早期使用碳青霉烯類及萬古霉素,并考慮聯合用藥。2016年歐洲臨床微生物和感染病學會在指南[16]中提出美羅培南可作為LM腦膜炎的替代治療。一些研究也嘗試抗菌藥物的聯合應用,特別是針對LM腦膜炎的重癥患者,可以使用氨芐西林聯合美羅培南治療[17]。
綜上所述,早產兒LM敗血癥多為早發性敗血癥,發病時間早,病情進展快,并發癥多,合并細菌性腦膜炎的發生率高,致死致殘率高。早產兒LM敗血癥的治療效果取決于醫務人員是否能早期識別并選用合適的抗菌藥物、有效抗生素治療是否及時、患兒胎齡、出生體質量等。治療上首選青霉素或氨芐西林,對于嚴重病例或合并化膿性腦膜炎時,可考慮聯合美羅培南治療。總之,產科、兒科醫師應了解LM感染的特點,早診斷并盡早給予有效抗生素治療,降低LM感染患兒的并發癥及死亡率。

