漆黃素脂質(zhì)體的制備及其質(zhì)量評價
王蓓蓓,姜亞莉,林郁,許穎
(1. 江蘇大學(xué)藥學(xué)院,江蘇 鎮(zhèn)江 212013; 2. 揚(yáng)州大學(xué)附屬醫(yī)院藥劑科,江蘇 揚(yáng)州 225001)
漆黃素是一種天然黃酮類化合物,又名非瑟酮。作為一種天然的黃酮類抗氧化劑,漆黃素廣泛存在于漆木科植物木蠟樹(Rhussuccedanea.L)、鹽膚木(RhuschinensisMill.)等植物以及蔬菜、水果中。研究表明,漆黃素具有廣泛的藥理活性,包括抗炎抗氧化、抗抑郁[1]、降低膽固醇,對老年小鼠腦出血誘導(dǎo)的神經(jīng)炎癥[2]、對心肌缺血再灌注損傷[3]均具有一定的保護(hù)作用。此外,研究表明,漆黃素可能通過抑制由糖尿病誘導(dǎo)的p300表達(dá)以及促進(jìn)MMP2的表達(dá),從而發(fā)揮顯著改善糖尿病大鼠腎臟病變的功效[4]。更重要的是,漆黃素還具有抑制多種癌細(xì)胞如HepG2 和Hela的增殖,誘導(dǎo)癌細(xì)胞凋亡的作用[5]。然而,漆黃素具有水溶性較差,不易被胃腸等生物膜吸收,半衰期較短,口服生物利用度低等缺點,其臨床應(yīng)用受到一定的限制。因此漆黃素新劑型的開發(fā)已經(jīng)成為研究熱點。
漆黃素作為一種天然產(chǎn)物,相關(guān)研究主要集中于藥理活性方面,制劑的相關(guān)報道較少。目前,已報道的漆黃素制劑僅有環(huán)糊精包合物[6],殼聚糖修飾的漆黃素聚乳酸納米粒。脂質(zhì)體是一種優(yōu)良的藥物載體,具有毒性低和生物相容性高等優(yōu)點。此外,脂質(zhì)體具有親水性內(nèi)核和疏水性磷脂雙分子層,能夠有效包載親水和親脂性藥物,是最具前景的納米給藥系統(tǒng)之一。目前已有多種脂質(zhì)體制劑用于臨床。
為解決漆黃素溶解度低、口服吸收差的問題,本實驗設(shè)計開發(fā)漆黃素脂質(zhì)體,并對其理化性質(zhì)進(jìn)行評價,以期提高漆黃素的溶解度和生物利用度。
1 材料與方法
1.1 主要材料與儀器
漆黃素(98.58%)購自成都瑞芬思生物科技有限公司;膽固醇(98%)、膽酸鈉(98%)購自上海阿拉丁試劑公司;肉豆蔻酸異丙酯(IPM)、大豆卵磷脂(98%)購自上海麥克林試劑公司;甲醇、乙腈(國藥集團(tuán)化學(xué)試劑有限公司)為色譜純;無水乙醇(國藥集團(tuán)化學(xué)試劑有限公司)為分析純。
旋轉(zhuǎn)蒸發(fā)儀(上海亞榮儀器廠);恒溫振蕩器(太倉華利達(dá)有限公司);高效液相色譜儀(Agilent 1260 系列,美國安捷倫科技公司);電子天平FA2004N(上海精密儀器有限公司);Nano Brook 90 plus PALS分析儀(美國布魯克海文儀器公司);TecnaiG2 F30 S-TWIN場發(fā)射透射電子顯微鏡(美國FEI公司)。
1.2 實驗動物
清潔級SD大鼠12只,雄性,標(biāo)準(zhǔn)體重(200± 20)g,由江蘇大學(xué)實驗動物中心提供。實驗方案經(jīng)過江蘇大學(xué)實驗動物倫理委員會審查。
1.3 漆黃素的定量分析方法的建立
1.3.1 漆黃素標(biāo)準(zhǔn)溶液的制備(建立體外標(biāo)準(zhǔn)曲線) 精密稱取漆黃素對照品25 mg,加少量甲醇溶解,超聲30 min后,移至250 mL的容量瓶,并用甲醇定容至刻度,得100 μg/mL 漆黃素儲備液。精密量取漆黃素母液0.01、0.05、0.1、0.5、1、2、5 mL置10 mL容量瓶中,用甲醇稀釋至刻度,得濃度分別為0.1、0.5、1、5 、10、20和50 μg/mL的漆黃素標(biāo)準(zhǔn)溶液。
1.3.2 色譜條件 色譜柱:Agilent C18反相色譜柱(250 mm×4.6 mm,5 μm),流動相:甲醇 ∶水=60 ∶40,流速:1 mL/min,檢測波長:364 nm,柱溫:25 ℃,進(jìn)樣量:20 μL。內(nèi)標(biāo):異甘草素。
1.3.3 血漿樣品的處理 取血漿樣品 200 μL置于1.5 mL 的離心管中,加入內(nèi)標(biāo)溶液異甘草素 20 μL(50 μg/mL),渦旋30 s混勻。加入乙酸乙酯 600 μL,漩渦 2 min,萃取2次,10 000 r/min離心10 min,合并萃取液,氮?dú)獯蹈桑?100 μL流動相復(fù)溶,取20 μL進(jìn)樣檢測。
1.4 脂質(zhì)體的制備
采用薄膜分散法制備漆黃素脂質(zhì)體。稱取處方量的大豆卵磷脂、膽固醇、膽酸鈉和肉豆蔻酸異丙酯,加入無水乙醇溶解,超聲使其充分溶解,再加入處方量的漆黃素,超聲溶解后置于旋轉(zhuǎn)蒸發(fā)儀上(50 r/min, 40 ℃),減壓除去無水乙醇,并獲得均勻的脂質(zhì)體薄膜。向其中加入適量雙蒸水,置恒溫振蕩器中水化30 min,超聲一定時間使脂質(zhì)體分子分散后備用。
1.5 單因素考察
以粒徑為指標(biāo),按照“1.4”項下方法,制備不同磷脂與膽固醇總量(100、150、200 mg),不同磷脂膽固醇比例(5 ∶1、8 ∶1、11 ∶1)及不同藥脂比(1 ∶5、1 ∶6、1 ∶7)的漆黃素脂質(zhì)體,以粒徑為指標(biāo),對脂質(zhì)體進(jìn)行處方優(yōu)化。
1.6 粒徑、電位測定及形態(tài)觀察
脂質(zhì)體用雙蒸水稀釋10倍,采用激光散射粒徑儀測定脂質(zhì)體的粒徑、多分散系數(shù)以及Zeta電位。對漆黃素脂質(zhì)體進(jìn)行負(fù)染,采用場發(fā)射透射電子顯微鏡觀察漆黃素脂質(zhì)體的形態(tài)。
1.7 包封率與載藥量的測定
采用超濾離心法測定漆黃素脂質(zhì)體的包封率。精密移取0.5 mL漆黃素脂質(zhì)體,置于超濾離心管(截留分子量8 000)中,12 000 r/min離心20 min。取超濾膜上的樣品及濾膜下的濾液分別置于2個容量瓶中,用色譜甲醇破乳定容后,HPLC法測定濃度,分別記為C1,C2,按如下公式計算漆黃素脂質(zhì)體的包封率:包封率=C1/(C1+C2)×100%。處方中加入的藥物量記為W1,加入的總的輔料的量記為W2,如下公式計算漆黃素脂質(zhì)體的載藥量:載藥量=(包封率×W1)/(W1+W2)×100%。
1.8 漆黃素脂質(zhì)體初步穩(wěn)定性試驗
精密稱取一定量漆黃素脂質(zhì)體,密封于棕色玻璃瓶中,分別置于4 ℃, 25 ℃, 60 ℃恒溫干燥器中放置30 d,于第 0、15、30天取出,測定粒徑變化。
1.9 體外釋放考察
采用透析法考察漆黃素脂質(zhì)體在pH 1.2 鹽酸、雙蒸水和pH 7.4 磷酸鹽緩沖液3種釋放介質(zhì)中的體外釋放情況。分別取漆黃素溶液、漆黃素脂質(zhì)體1 mL(含漆黃素1 mg)置于透析袋中,兩端扎緊,放入100 mL 不同的釋放介質(zhì)中,(37.0±0.5) ℃,轉(zhuǎn)速為 100 r/min,分別在0.25、0.5、0.75、1、2、4、6、8、10、12、24 h取樣 1 mL,并及時補(bǔ)充同等體積同溫度的釋放介質(zhì)。取出的樣品10 000 r/min離心后,取上清液,采用HPLC法測定釋放液中游離漆黃素的濃度,計算出漆黃素的累積百分釋放率,繪制累積釋放曲線。
1.10 藥物動力學(xué)實驗
健康雄性SD大鼠10只隨機(jī)分為兩組,每組5只,分別以50 mg/kg的劑量灌胃給予漆黃素混懸液和漆黃素脂質(zhì)體。給藥前12 h禁食不禁水,分別在給藥后 0.083、0.25、0.5、0.75、1、1.5、2、3、4、6、8、10、12 h于大鼠眼眶靜脈叢取血,3 700 r/min離心10 min,吸取上清液,置于-20 ℃冰箱中保存?zhèn)溆谩Q獦犹幚矸椒▍⒄铡?.3.3”方法。
漆黃素和漆黃素脂質(zhì)體的血藥濃度-時間曲線采用BAPP 2.3軟件進(jìn)行擬合,得到相關(guān)藥代動力學(xué)參數(shù)。Cmax為給藥后的最大血藥濃度,Tmax為給藥后血藥濃度達(dá)峰時間,t1/2為末端消除半衰期,T1/2為藥物在大鼠體內(nèi)的半衰期,AUC(0-24 h)為血藥濃度-時間曲線下面積。
1.11 漆黃素體外抗腫瘤實驗
將HepG2細(xì)胞接種于96孔板中,每孔1×105個細(xì)胞,每孔100 μL培養(yǎng)基(含有10%胎牛血清的DMEM高糖培養(yǎng)基)于37 ℃培養(yǎng)箱5% CO2下培養(yǎng)細(xì)胞貼壁生長24 h后,用不同濃度(0.5、1、2、5、10、25、50、100 μg/mL)的漆黃素原料藥,漆黃素脂質(zhì)體,空白脂質(zhì)體(陰性對照)和5-Fu(陽性對照)處理72 h。每孔加入20 μL MTT(5 mg/mL),37 ℃孵育4 h,加入100 μL DMSO,于490 nm采用酶標(biāo)儀測定光密度。
1.12 統(tǒng)計學(xué)方法
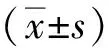
2 結(jié)果
2.1 方法學(xué)考察
按照“1.3.2”及“1.3.3”項下色譜條件和樣品處理方法,漆黃素、空白血漿+漆黃素+內(nèi)標(biāo)的HPLC色譜圖如圖1所示,表明分析方法具有良好的專屬性。

A:漆黃素;B:空白血漿+漆黃素+內(nèi)標(biāo)
標(biāo)準(zhǔn)曲線結(jié)果:以濃度(C)對峰面積(Y)進(jìn)行回歸,得體外樣品測定標(biāo)準(zhǔn)曲線Y=19.211 3C+2.083 1,R2=0.9991,體內(nèi)樣品測定的標(biāo)準(zhǔn)曲線為Y=0.3612C-0.1026,R2=0.9978。漆黃素體內(nèi)外樣品測定的線性范圍均為0.1~100 μg/mL, 相對標(biāo)準(zhǔn)偏差(RSD)<2%(n=6),日內(nèi)、日間精密度,方法回收率和重復(fù)性均符合方法學(xué)要求。
2.2 單因素考察
磷脂與膽固醇的總量為150 mg時,脂質(zhì)體的粒徑最小,因此選擇150 mg為磷脂與膽固醇的總量。當(dāng)磷脂與膽固醇的比例為8 ∶1時,脂質(zhì)體粒徑最小,因此磷脂與膽固醇的比例確定為8 ∶1。藥物與磷脂比為1 ∶6及1 ∶7時,漆黃素脂質(zhì)體的粒徑差別不大,因此選擇藥脂比為1 ∶6。膽酸鈉用量與脂質(zhì)體粒徑成負(fù)相關(guān),膽酸鈉用量為110 mg時,漆黃素脂質(zhì)體的粒徑最小,因此,選擇膽酸鈉用量為110 mg。見圖2。由此,通過單因素實驗得到最優(yōu)處方為漆黃素22.2 mg、磷脂133.3 mg、膽固醇16.7 mg、膽酸鈉110 mg、肉豆蔻酸異丙酯60 mg。

圖2 漆黃素脂質(zhì)體單因素處方篩選實驗
2.3 體外表征
粒子粒徑分布圖及形貌觀察結(jié)果如圖3所示。粒徑、電位測定結(jié)果顯示,漆黃素脂質(zhì)體的粒徑為(60.32±1.08) nm,多分散系數(shù)為0.198±0.011,電位為(-31.34±1.45) mV。由透射電鏡圖可知,漆黃素脂質(zhì)體粒子外形圓整,呈現(xiàn)為類球形,與粒徑分布儀所測結(jié)果一致。漆黃素脂質(zhì)體包封率為(94.37±0.62)%,載藥量為(4.500±0.021) %。

A:漆黃素脂質(zhì)體粒徑分布圖;B:漆黃素脂質(zhì)體透射電鏡圖
2.4 穩(wěn)定性考察
不同溫度條件下漆黃素脂質(zhì)體粒徑30 d內(nèi)變化較小(表1),表明所制備的漆黃素脂質(zhì)體30 d內(nèi)穩(wěn)定性良好。

表1 漆黃素脂質(zhì)體在4 ℃、25 ℃、60 ℃下的初步穩(wěn)定性考察
2.5 體外釋放
在3種介質(zhì)(pH1.2 鹽酸、雙蒸水、pH7.4 磷酸鹽緩沖液)中,漆黃素的累積釋放率均低于50 %,而漆黃素脂質(zhì)體的累積釋放率均高于70 %,漆黃素脂質(zhì)體的累積釋放率均高于游離漆黃素。此外可以觀察到,漆黃素脂質(zhì)體在pH1.2鹽酸水溶液中的累積釋放率均高于其在pH 7.4磷酸鹽緩沖液和雙蒸水中的累積釋放率。見圖4。

圖4 漆黃素原料藥及漆黃素脂質(zhì)體在不同介質(zhì)中的體外釋放
2.6 藥物動力學(xué)結(jié)果
漆黃素脂質(zhì)體在大鼠體內(nèi)各時間點的血藥濃度均高于漆黃素原料藥(圖5)。漆黃素原料藥的AUC(0-12 h)為(6.29±0.35) μg/(mL·h),而漆黃素脂質(zhì)體為(20.28±0.66) μg/(mL·h),是漆黃素原料藥的3.22倍,具有顯著性差異(P<0.01),見表2。同時,漆黃素脂質(zhì)體的T1/2為(3.79±0.12) h,相比于漆黃素原料藥的(1.91±0.09) h,半衰期延長了1.88 h(約1倍),具有顯著性差異(P<0.01)。因此,將漆黃素包裹于脂質(zhì)體中,能有效延長漆黃素的半衰期,增加其生物利用度。

圖5 漆黃素和漆黃素脂質(zhì)體的血藥濃度-時間曲線

表2 SD大鼠尾靜脈注射漆黃素和漆黃素脂質(zhì)體的主要藥動學(xué)參數(shù)
2.7 抗腫瘤活性評價
MTT實驗結(jié)果顯示,陽性對照和漆黃素脂質(zhì)體組的抑制率在各濃度水平均顯著高于漆黃素原料藥組。漆黃素原料藥和漆黃素脂質(zhì)體對HepG2細(xì)胞均有抑制作用,且呈現(xiàn)為劑量依賴關(guān)系,隨著給藥濃度增加,HepG2細(xì)胞的抑制率增加。見圖6。

*:P<0.05,與漆黃素原料藥組比較
3 討論
漆黃素具有多種藥理活性,但因高親脂性和低水溶性致使口服生物利用度低,限制了其在臨床上的應(yīng)用和發(fā)展[7]。為了克服這些問題,基于脂質(zhì)體的藥物傳遞系統(tǒng)具有良好的市場前景。作為一種性質(zhì)優(yōu)良的藥物遞送系統(tǒng),包括氯膦酸二鈉等在內(nèi)的多種藥物均被制備成脂質(zhì)體[8-9]。此外,脂質(zhì)體已被證明可以使藥物具有很高的腫瘤蓄積性,這種腫瘤保留作用是由于脂質(zhì)體藥物可以通過腫瘤的多孔毛細(xì)血管內(nèi)皮滲透[10]。目前在臨床上已經(jīng)有幾種脂質(zhì)體形式的蒽環(huán)類藥物,這些制劑有助于降低毒性,同時又保持它們在乳腺癌和軟組織癌中的抗癌活性[10-11]。
本實驗制備的漆黃素脂質(zhì)體具有合適的粒徑(60.32±1.08)nm,較窄的粒徑分布0.198±0.011和高達(dá)94.37 %的包封率。較小的粒徑有助于提高脂質(zhì)體粒子穿透血管膜,進(jìn)入組織臟器從而發(fā)揮作用[12]。本實驗制備的漆黃素脂質(zhì)體Zeta電位為(-31.34±1.45) mV,較高的電位意味著脂質(zhì)體具備更好的穩(wěn)定性,原因在于脂質(zhì)體粒子之間的斥力較強(qiáng),不易沉積。
本實驗中,漆黃素脂質(zhì)體能夠提高漆黃素的溶解度,改善漆黃素的體外釋放行為。在pH 1.2鹽酸條件下的累積釋放率均高于其在pH 7.4磷酸鹽緩沖液和雙蒸水中的累積釋放率。這與Pawar等[7]的研究結(jié)果類似。這是由于漆黃素在酸性pH下的溶解度更高,這會增加其在癌細(xì)胞中的選擇性吸收以及靶向吸收的優(yōu)勢。因為在癌細(xì)胞中,pH值比正常生理pH值略偏酸性。
藥動學(xué)擬合結(jié)果表明漆黃素脂質(zhì)體能延長漆黃素在體內(nèi)的滯留時間,可能是由于更快的吸收以及逃避了巨噬細(xì)胞的吞噬從而延長了在體內(nèi)的停留時間。脂質(zhì)體可以通過以下幾種方式來影響藥物吸收:① 通過增強(qiáng)藥物在腸道環(huán)境中的溶解性;② 基于腸細(xì)胞的運(yùn)輸和代謝過程相互作用,從而可能改變藥物的吸收、外排、轉(zhuǎn)運(yùn)和腸細(xì)胞內(nèi)代謝產(chǎn)物的形成;③ 通過改變藥物轉(zhuǎn)運(yùn)到體循環(huán)的途徑(門靜脈和腸淋巴系統(tǒng)),這反過來可以減少藥物代謝的首過效應(yīng),因為腸淋巴系統(tǒng)不經(jīng)過肝臟而直接進(jìn)入體循環(huán),從而可以達(dá)到降低給藥劑量以及毒副作用的效果。脂質(zhì)體是一種良好的提高生物利用度的藥物遞送系統(tǒng)[13],粒子的大小會直接影響其穩(wěn)定性、藥物釋放、生物分布和細(xì)胞攝取。因為大于10 nm的納米顆粒可以逃避腎臟的清除,而小于200 nm的納米顆粒可以逃避巨噬細(xì)胞的吞噬,延長了其循環(huán)半衰期,也更有利于通過EPR效應(yīng)被動靶向?qū)嶓w腫瘤。此外,在脂質(zhì)體的脂質(zhì)雙膜中添加膽酸鈉可使其與腸上皮接觸時發(fā)揮膜破壞作用,從而促進(jìn)藥物從脂質(zhì)體中釋放,潛在地提高了藥物的口服生物利用度[14]。
本研究結(jié)果表明,漆黃素原料藥和漆黃素脂質(zhì)體對于HepG2細(xì)胞均有抑制作用,且呈現(xiàn)為劑量依賴關(guān)系,隨著給藥濃度增加,HepG2細(xì)胞的抑制率增加。相關(guān)研究表明,漆黃素通過調(diào)控多種信號通路實現(xiàn)抗HepG2 細(xì)胞的增殖作用[15],其通過降低Bcl2的表達(dá),并降低Bax、caspase-3和多聚ADP-核糖聚合酶(PARP)的水平,從而誘導(dǎo)HepG2細(xì)胞凋亡和細(xì)胞壞死。且經(jīng)過脂質(zhì)體的有效包封,漆黃素對HepG2的抑制效果得到顯著增強(qiáng)。其抑制作用的增強(qiáng)可能是由于腫瘤細(xì)胞內(nèi)皮屏障的異常有利于脂質(zhì)體在腫瘤組織中內(nèi)滲,在脂質(zhì)體膜與細(xì)胞膜相互作用中,漆黃素迅速釋放、進(jìn)入細(xì)胞,導(dǎo)致漆黃素在腫瘤細(xì)胞內(nèi)的濃度增加[16]。此外,在酸性環(huán)境中,漆黃素具有較好的溶解度,能增加藥物的釋放,有助于提高漆黃素脂質(zhì)體作為高效藥物遞送系統(tǒng)的效率。因此,腫瘤細(xì)胞所處的弱酸性環(huán)境可以觸發(fā)漆黃素從漆黃素脂質(zhì)體中快速釋放,從而大大增強(qiáng)其細(xì)胞毒性,并降低其對正常細(xì)胞的影響。
綜上所述,本實驗通過優(yōu)化制備的漆黃素脂質(zhì)體具有較好的理化性質(zhì),可有效提高難溶性藥物漆黃素的溶解度及生物利用度,且體外實驗證實其對HepG2細(xì)胞具有明顯的抑制作用。本研究結(jié)果為漆黃素的臨床應(yīng)用提供了參考,并為難溶性藥物的增溶提供借鑒。

