馬鈴薯A病毒不同分離物的侵染鑒定及致病力分析
張 威,魏旭言,高艷玲,范國權,邱彩玲,孫旭紅,武新娟,張俐俐,白艷菊*
(1.黑龍江省農業科學院,黑龍江 哈爾濱 150086;2.昭通學院農學與生命科學學院,云南 昭通 657000)
病毒病一直以來都是危害馬鈴薯生產,導致塊莖減產并影響品質的主要因素。目前,侵染馬鈴薯的病毒約有50 余種[1,2],其中馬鈴薯A 病毒(Potato virus A,PVA)是馬鈴薯Y病毒屬(Potyvirus)成員[3],也是常見的侵染馬鈴薯主要病毒之一。一般情況下,PVA 單獨侵染馬鈴薯嚴重時減產可達40%左右[4],而當PVA 與其他病毒復合侵染,可導致更嚴重的產量損失[5-7]。所以PVA 的危害性已經受到世界各國的重視,多個國家將其列為檢疫性有害生物,中國2007 年也將PVA 列入《中華人民共和國進境植物檢疫性有害生物名錄》[8]。國內馬鈴薯PVA 的相關研究多集中在病毒檢測和分離鑒定方法上,且已初步取得成果[9-11],但對于PVA 不同分離物在馬鈴薯生長發育過程中引起的致病性研究較少。PVA 不同分離物因其核酸或所編碼蛋白的差別,在馬鈴薯上引起的致病癥狀有所不同。明確PVA 分離物的致病力表現,從傳統生物學癥狀著手,結合分子生物學方法,深入研究其致病性,可為PVA 病毒的鑒定與防治提供理論依據。
早在1990 年,Jones[12]對PVA 侵染馬鈴薯后引起癥狀與品種的關系就有報道,將PVA 接種到12 個馬鈴薯品種上,各品種敏感度不同,出現不被侵染、無癥狀感染、輕癥狀和重癥狀表現,而不同株系的PVA 在同一品種上的致病癥狀也有差異。本研究選擇PVA 3 個遺傳背景不同的分離物,分別接種在指示植物‘黃花煙’和較敏感馬鈴薯品種‘克新13號’上,觀察其致病性差異,比較馬鈴薯植株體內病毒含量、葉片及塊莖癥狀的表現,以明確3 個分離物對馬鈴薯生長發育的影響,對PVA 的鑒定及防治具有重要意義。
1 材料與方法
1.1 試驗材料
馬鈴薯原原種‘克新13 號’和指示植物‘黃花煙’(Nicotiana rustica),由原黑龍江省農業科學院馬鈴薯研究所提供。
PVA 3 個遺傳背景不同的分離物2017-171、KB117 和2017-176,由原黑龍江省農業科學院馬鈴薯研究所測序并保存。
1.2 試驗試劑
M-MLV 反轉錄酶試劑購自Promega 公司;RNA 酶抑制劑、dNTP、Taq DNA 聚合酶、DNA Marker 均購自于Takara 公司;Trizol 提取液購自Invitrogen 公司;75%乙醇、異丙醇、氯仿、NaH2PO4·2H2O、Na2HPO4·12H2O 等試劑為分析純。
1.3 試驗方法
1.3.1 植物種植
在智能溫室中,按照珍珠巖∶爐灰∶草炭= 1∶1∶3的比例配制基質,混勻后121℃濕熱滅菌30 min,冷卻后裝在口徑為25 cm 的花盆中。澆透水后將‘黃花煙’的種子均勻撒播,覆土1.0 cm 左右,待苗長至2~3 cm 時分苗、移栽[13]。馬鈴薯塊莖芽眼朝上栽到盆中再覆土。
1.3.2 摩擦接種
待植株4~6 葉期,選擇在陰天或晚上,采用摩擦方式接種。在植株中上部兩片對稱葉上均勻噴灑適量碳化硅細粉,然后用棉簽沾PVA 病毒汁液摩擦接種[毒源∶接種緩沖液(含32 mmol/L Na2SO3和 10 mmol/L 磷酸鈉緩沖液,pH 7.5)=1 g∶3.3 mL],30~60 min后清水沖洗掉殘余病毒汁液[14]。
對照(Mock)植株用接種緩沖液摩擦接種葉片,方法同上。每個處理5 次重復。接種后避光過夜。取新生的系統葉片進行qRT-PCR 檢測,確認是否已成功接種PVA,并系統侵染。
1.3.3 總 RNA 提取及 cDNA 合成
試驗采用Trizol 法提取植物總RNA,操作步驟參考Trizol 使用說明書。提取后的RNA 采用紫外分光光度計測RNA 的OD260/OD280比值,當比值在1.8~2.0 說明RNA 的純度較好,可以進行后續試驗。先將其保存于-70℃備用。
取1 μg總RNA,使用Takara公司的M-MLV反轉錄試劑盒,參照說明書進行cDNA 合成,于-20℃保存備用。
1.3.4 TaqMan 熒光定量PCR 探針和引物的選擇與合成
參考 Bright 等[15]PVA 的檢測方法。PVA 的特異性探針和引物均由生工生物工程(上海)股份有限公司合成。探針PVA 102-probe 序列為:5′ -Texas-CACTACCAATGCTCAAAGGTAGAGTGTCG-BHQ-3′; 上 游 引 物 PVA102-F: 5′-TGTCGATTTAGGTACTGCTGGGAC-3′; 下 游 引物PVA102-R:5′- TGCTTTGGTTTGTAAGATAGCAAGTG-3′,擴增片段長度為132 bp。
1.3.5 TaqMan 熒光定量 PCR 擴增
反應體系為,模板cDNA 2 μL,上、下游引物各 0.5 μL(10 μmol/L),探針 0.5 μL,10 ×PCR Buffer 2.5 μL,Taq DNA 聚合酶 0.20 μL,dNTPs(2.5 mmol/L)0.25 μL,補水至25 μL。用水作為陰性對照,取濃度為 2.72 × 106copies/μL 的質粒作為陽性對照,每個樣品3 次重復。反應程序:95℃ 30 s,58℃ 30 s,72℃ 30 s,40 個循環。將樣品放入LightCycler?480 熒光定量儀進行TaqMan RT-qPCR 擴增。
2 結果與分析
2.1 PVA 不同分離物對指示植物‘黃花煙’的致病性差異
當接種‘黃花煙’第7 d 時,分別取新生葉進行PVA 的qRT-PCR 檢測,檢測結果均為陽性,表明PVA 3 個分離物可以成功侵染‘黃花煙’。隨著時間的推移,其系統發病癥狀逐漸表現出來,圖1 為接種15 d 后的癥狀表現。
不同分離物在‘黃花煙’上的癥狀表現各有不同(圖1)。與對照相比,分離物2017-171 侵染‘黃花煙’后表現出葉片皺縮、泡斑和葉緣變形等癥狀;分離物KB117 侵染后,除了葉緣微皺縮外,還伴有明脈癥狀;分離物2017-176 侵染后葉片癥狀比較輕,僅表現微皺縮和點狀輕花葉現象。通過3個分離物侵染‘黃花煙’后葉片的癥狀差異,可以初步推斷他們的致病性具有一定差異。

圖1 PVA 不同分離物接種‘黃花煙’的癥狀Figure 1 Symptoms of 'Rustica Tobacco' inoculated with different PVA isolates
2.2 PVA不同分離物對馬鈴薯品種‘克新13號’的致病性差異
2.2.1 PVA 不同分離物在‘克新13 號’植株體內病毒含量差異
分別在接種后的第2、5、10、15、20 和25 d取新生葉片,進行PVA的qRT-PCR檢測。檢測結果顯示,3個分離物均可以成功侵染‘克新13號’。
每個分離物在6 個時間點病毒在植株體內變化趨勢相似,即病毒進入植株體內,隨著時間的推移病毒含量逐漸增加,達到發病高峰期,隨后病毒含量開始降低。但3 個分離物在侵入植株體內的初始時間、發病速度、發病高峰期的病毒含量方面具有一定的差異(表1)。
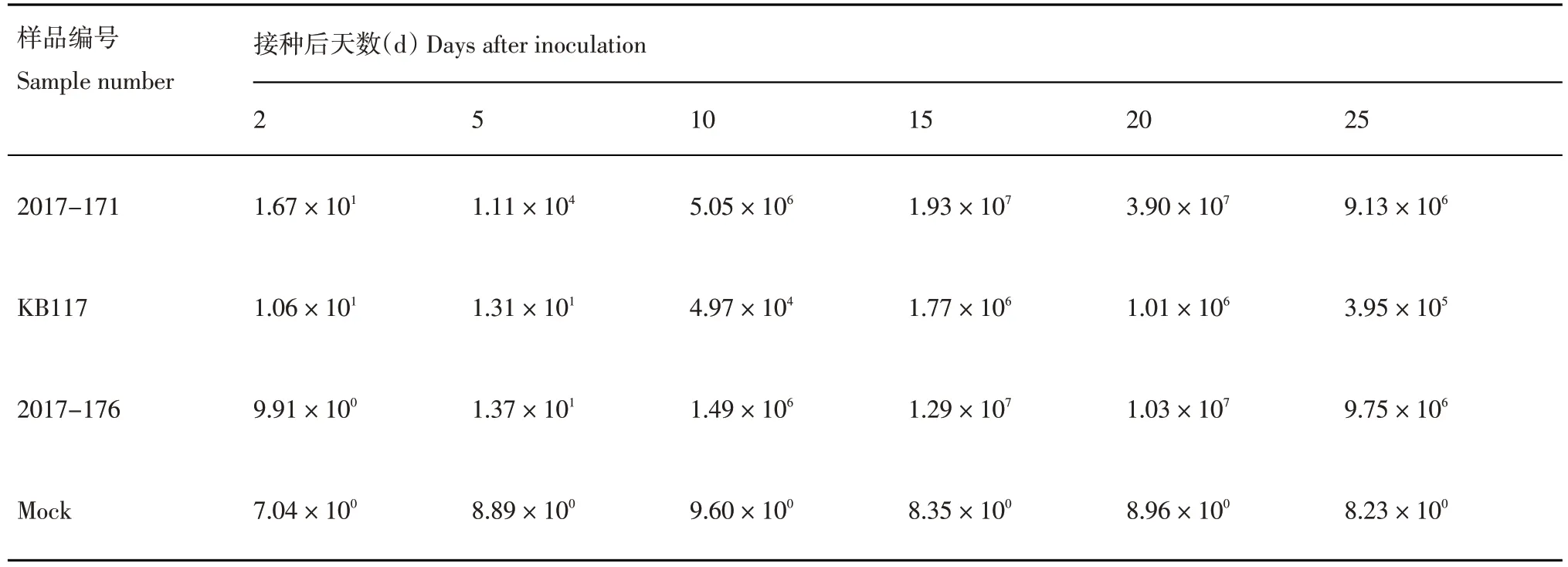
表1 不同PVA 分離物植株體內病毒含量的變化(copies/μL)Table 1 Changes of virus contents in plants inoculated with different PVA isolates
分離物2017-171 接種后的第2 d qRT-PCR 檢測結果為陽性,表明該分離物可以在接種后第2 d成功侵染‘克新13號’,其病毒在體內含量為1.67×101copies/μL,隨著時間的推移,植株體內病毒含量逐漸升高,第20 d 時達到最高值3.90 × 107copies/μL,隨后病毒含量又呈降低趨勢;分離物KB117接種后的第2 d開始侵染‘克新13號’,在第2~5 d 病毒含量累積緩慢,隨后病毒含量大幅度升高,第15 d 時達到發病高峰期,植株體內病毒含量達最高值1.77 × 106copies/μL,隨后呈降低趨勢;分離物2017-176 接種后的第2 d 未能侵染‘克新13 號’,在第5 d 時才呈現病毒含量有所升高趨勢,隨后病毒含量大幅度升高,第15 d 時達到發病高峰期,植株體內病毒含量達最高值1.29×107copies/μL,隨后病毒含量呈降低趨勢,表明此分離物侵染植株相對較慢。
由以上分析可知,分離物2017-171 和KB117均在接種后第2 d 開始侵入植株體內,而2017-176 侵染速度相對較慢;2017-171 在接種后第20 d 病毒含量達到高峰,而2017-176 和KB117 在第5~10 d 病毒含量大幅度升高,都在15 d 時植株體內病毒含量達到高峰,但KB117 的高峰含量低于2017-171 及2017-176。
2.2.2 PVA 不同分離物侵染‘克新13 號’植株癥狀差異
分別在接種后達到發病高峰期時觀察植株發病癥狀。與對照相比,分離物2017-171 接種‘克新13 號’后呈現輕花葉、葉緣微皺縮等癥狀;分離物KB117 接種‘克新13 號’后會出現葉緣變尖、波浪狀皺縮等癥狀;分離物2017-176 接種后,癥狀不明顯,僅個別葉片呈現輕微葉緣皺縮等癥狀(圖2)。不同分離物接種‘克新13 號’的植株癥狀表現存在差異,說明3 個分離物致病力有一定差別,但對植株整體長勢影響不大。

圖2 不同PVA 分離物接種‘克新13 號’植株癥狀Figure 2 Symptoms of 'Kexin 13' inoculated with different PVA isolates
2.2.3 PVA 不同分離物侵染‘克新13 號’塊莖癥狀差異
從各分離物接種后的單株塊莖個數和塊莖癥狀可以看出(圖3),與對照相比,整體趨勢為,單株塊莖數減少、塊莖變小、芽眼變深,個別塊莖出現變形等癥狀。其中典型的塊莖癥狀與對照相比較,分離物2017-171 接種后塊莖出現裂口、芽眼變深癥狀;分離物KB117 接種后塊莖出現畸形癥狀、芽眼變深癥狀;分離物2017-176接種后塊莖僅出現芽眼變深癥狀。
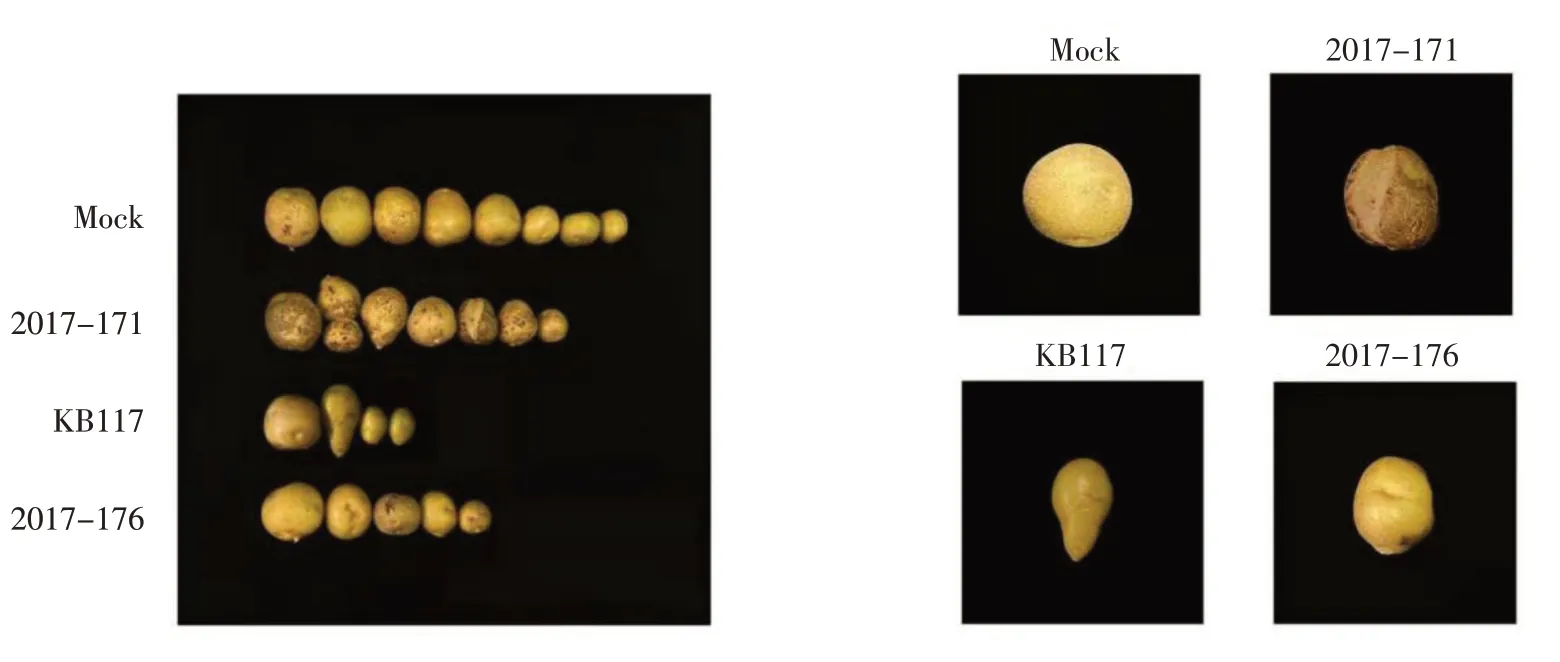
圖3 不同PVA 分離物接種‘克新13 號’塊莖癥狀Figure 3 Symptoms of tubers of 'Kexin 13' inoculated with different PVA isolates
3 討 論
PVA 的寄主范圍相對較窄,主要以侵染茄科等植物為主,如馬鈴薯、番茄、洋酸漿、假酸漿、煙草等[16]。其侵染癥狀于1914年首次被報道[17],并于1932 年正式命名[18]。PVA 主要通過種薯傳播和摩擦接觸傳播,還可以通過蚜蟲以非持久性方式傳播。隨著馬鈴薯種植面積的不斷擴大以及各地種薯調運而在世界范圍內傳播。在中國,于1975年首次在黑龍江省克山縣發現此病毒[19],而后幾乎遍布于馬鈴薯的各主要產區[20]。
PVA 侵染馬鈴薯時,其癥狀類型,與馬鈴薯品種、病毒株系、環境條件等具有一定相關性[21-23],抗性較強品種,一般不表現癥狀,而致病性相對較強株系可以導致馬鈴薯敏感品種產生花葉、斑駁、皺縮等較嚴重癥狀。
范國權等[24]將馬鈴薯9 種病毒接種在黑龍江省10 個馬鈴薯主栽品種上,當PVA 和PVY 復合侵染品種‘克新13 號’時,植株癥狀較其他品種明顯,且產量影響顯著。魏旭言[25]將具有較強致病性的PVA 分離物接種在10 個馬鈴薯主栽品種上,有5 個品種接種成功,其中‘克新13 號’和‘麗薯6 號’接種后植株及塊莖致病癥狀較明顯,測定發病高峰期PVA 病毒含量,結果為‘克新13 號’表現最高,說明PVA 對此品種危害性最強。
不同PVA 分離物在同一馬鈴薯品種上引起的致病癥狀也不相同。Valkonen 等[26]將PVA 接種到馬鈴薯品種‘King Edward’上,根據侵染癥狀不同將PVA 分離物分成了3 組,分別為植株上部葉片典型性壞死、葉片斑駁和無感染癥狀3 種類型,之后Rajam?ki 等[22]研究又增加了一組,該株系可引起‘King Edward’全株葉片發黃、植株矮化。同時Rajam?ki 等[22]將來源于不同國家的18 個PVA分離物CP 序列進行系統發育分析,發現其序列差異顯著,存在明顯多樣性。
本研究將3 種PVA 分離物分別接種在指示植物‘黃花煙’和馬鈴薯品種‘克新13 號’上,通過qRT-PCR 檢測,結果均為陽性,其中分離物2017-171 癥狀最明顯,導致‘黃花煙’葉片皺縮、泡斑和葉緣變形等癥狀,馬鈴薯植株葉片出現葉緣皺縮并伴有輕花葉癥狀,塊莖出現嚴重裂口、芽眼變深癥狀;KB117 次之,可使‘黃花煙’葉緣微皺縮并伴有明脈癥狀,馬鈴薯植株葉緣變尖、波浪狀皺縮,塊莖發生畸形且芽眼變深;2017-176 癥狀相對不明顯,‘黃花煙’僅葉片微皺縮、點狀輕花葉,馬鈴薯植株僅個別葉片呈現輕微葉緣皺縮,塊莖未出現畸形只存在芽眼變深癥狀。同時進行qRT-PCR 表達模式分析,發現2017-171 在馬鈴薯體內病毒含量最高,其次為2017-176 和 KB117。綜上分析看出,3 種 PVA 分離物均可以成功侵染指示植物‘黃花煙’和馬鈴薯植株,且分離物2017-171 致病力最強,不僅在植株體內含量最高,還能導致馬鈴薯塊莖畸形并產生裂口現象。PVA 不同株系的致病性分析為其有效防治提供了有價值的理論依據。

