IABP輔助經皮冠狀動脈介入治療高危冠心病患者的危險因素
李丹 胡昊 吳佳緯 馬禮坤
(中國科學技術大學附屬第一醫院心血管內科,安徽 合肥 230036)
《中國心血管病報告2018》中顯示我國心血管死亡率仍居首位,介入治療總數上升的同時,冠心病的死亡率仍持續上升〔1〕。主動脈內球囊反搏(IABP)是全世界廣泛應用的循環輔助裝置,在1968年首次被應用于心源性休克(CS)患者的治療管理〔2〕,隨著介入治療的發展,在高危冠心病患者的圍術期治療中被更多應用。研究顯示,IABP在高危冠狀動脈介入(PCI)中的保護性應用有極高比例〔3〕。臨床研究發現,IABP有助于降低高危冠心病患者心肌梗死的發生率,但并不降低死亡率〔4〕。如何早期綜合這些患者的臨床高危特點,以影響臨床決策,顯得尤為重要。本研究收集IABP輔助介入治療高危冠心病患者的臨床資料,擬觀察其臨床高危因素,對提前干預、優化治療有更好的指導價值。
1 資料和方法
1.1一般資料 回顧性分析中國科學技術大學附屬第一醫院2015年1月至2018年7月所有植入IABP輔助PCI治療的高危冠心病患者172例的臨床資料,隨訪中失聯36例,最終入組136例,其中男102例,女34例。高危冠心病的定義:(1)急性心肌梗死合并心功能不全、射血分數≤40%和(或)CS;(2)不穩定型心絞痛,Q波或非Q波的心肌梗死及機械并發癥;(3)冠脈嚴重病變,包括冠脈多支或彌漫性病變,無保護左主干、左主干末端分叉;(4)冠狀動脈旁路移植術(CABG)或經皮冠狀動脈血管成形術(PTCA)失敗后轉行CABG;(5)合并腦梗死、腎功能不全等多種合并疾病。心源性休克的定義:(1)末梢循環明顯供血不足;(2)顯著的血流動力學障礙,收縮壓<90 mmHg,和(或)舒張壓<60 mmHg,或平均動脈壓下降超過30 mmHg;(3)尿量低于0.5 ml/(kg·h);(4)升壓和(或)補充血容量等治療后無改善。
1.2治療方案 所有患者予以雙聯抗血小板、調脂、抗凝等治療。血流動力學不穩定者給予血管活性藥物治療,嚴重緩慢心律失常植入臨時起搏器,快速惡性心律失常給予藥物復律或電復律;酌情利尿、抗感染、支持等治療;必要時采用機械通氣。
1.3IABP置入及撤離情況 IABP由經驗豐富的心內科介入醫生置入,其適應證和置入時間由兩位及以上有經驗的副主任或主任醫師共同決定,IABP儀型號Datescope100。排除IABP禁忌證,經一側股動脈,根據患者的身高體重,選擇30 ml或40 ml球囊反搏導管,置于降主動脈起始部和腎動脈開口之間,心電模式1∶1觸發,術中給予普通肝素或比伐盧定抗凝,術后給予低分子量肝素3 200~4 000 U每12 h皮下注射,持續心電血壓監護。
IABP禁忌證:(1)主動脈夾層、主動脈竇瘤破裂;(2)中重度主動脈瓣關閉不全;(3)嚴重的周圍血管疾病;(4)凝血功能障礙;(5)活動性出血、大面積腦梗死、腦出血急性期。IABP使用時間由主治醫生決定,取決于患者的血流動力學狀態或不能耐受的并發癥。撤機指征:患者血流動力學穩定1 d以上,已停用血管活性藥物,尿量>30 ml/h,無惡性心律失常發生,心率低于110次/min。拔除前器調整IABP球囊反搏比為1∶2,觀察2 h無異常,即可拔管。
1.4方法 回顧病歷資料,收集患者的一般臨床資料、既往史、合并疾病、并發癥、實驗室檢查、手術資料,術后平均隨訪1年。實驗室測試血標本為患者入院后即刻(急救室或心內科病房)采集。心臟彩超為此次入院期間完成。術前血壓、心率為入導管室即刻記錄;術后血壓、心率均為PCI結束患者返回病房記錄。根據患者生存情況,分為存活組102例和死亡組34例。
1.5觀察指標 比較兩組一般臨床資料、手術資料、圍術期的生命體征變化等相關指標。術后隨訪及臨床終點事件:隨訪患者圍術期至術后1年的出血事件和主要不良心腦血管事件(MACCE):包括支架內血栓形成、支架內再狹窄、再發心肌梗死、腦卒中及全因死亡(包括心血管死亡)的發生情況。
1.6統計學方法 采用SPSS19.0軟件進行t檢驗、χ2檢驗及非條件Logistic回歸分析。
2 結 果
2.1兩組基線資料比較 兩組性別、入科血糖、血鉀、血紅蛋白、左室內徑、左室收縮功能、是否為急性心肌梗死等差異無統計學意義(P>0.05),既往病史中高血壓、糖尿病、缺血性心肌病、慢性腎功能不全、吸煙史等差異無統計學意義(P>0.05)。存活組合并心力衰竭(Killip Ⅲ~Ⅳ級)比例顯著高于死亡組(P=0.048),而死亡組較存活組更高齡(P=0.002),更多合并CS(P=0.017),既往腦卒中史更多(P=0.009),見表1。
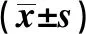
表1 兩組基線資料對比
2.2兩組圍術期臨床資料比較 兩組術前、術后收縮壓、舒張壓及術前心率、肌酐水平差異無統計學意義(P>0.05),術后死亡組肌酐水平、心率明顯高于存活組(P<0.01),見表2。術中植入臨時起搏器比例〔2例(5.8%)〕顯著高于存活組(0例;χ2=6.090,P=0.014)。
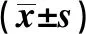
表2 兩組圍術期臨床資料比較
2.3兩組圍術期出血事件和MACCE發生情況比較 兩組術后發生小出血事件、腦卒中、支架內血栓形成差異均無統計學意義(均P>0.05)。死亡組心律失常、大出血事件發生比率顯著高于存活組(P<0.005)。見表3。

表3 兩組住院期間不良事件的發生情況比較〔n(%)〕
2.4兩組手術相關臨床資料比較 多數患者罪犯血管為前降支(LAD)和左主干(LM)。兩組LM比率差異有統計學意義(P=0.009),兩組LAD病變、右回旋支(LCX)病變、右冠狀動脈(RCA)病變、多支病變、分叉病變差異均無統計學意義(P>0.05)。見表4。

表4 兩組手術相關臨床資料比較〔n(%)〕
2.5Logistic回歸分析 將單因素分析結果中有統計學意義的相關因素,采用逐步向前(LR)法進行模型擬合,多因素回歸分析結果顯示,年齡、圍術期最高肌酐、CS、LM病變為患者死亡的獨立危險因素。見表5。

表5 多因素Logistic回歸分析
3 討 論
IABP是目前常用的安全性較高的簡單循環支持輔助裝置,可以降低心臟后負荷和心肌耗氧量,改善冠狀動脈的血流量〔2〕,一直被認為是CS管理的基石。但在IABP-SHOCK-Ⅱ的研究中,因為沒有表現出明顯臨床獲益,在國內外指南中,證據級別被降低,IABP-SHOCK-Ⅱ的研究結果表明〔5〕置入IABP未能降低心肌梗死合并CS患者30 d內的死亡率,并對再發心肌梗死、再次血運重建及腦卒中等MACCE發生率也無優勢,甚至IABP組缺血性及出血性腦卒中發生率更高。但這個結論與IABP的病理生理機制不符,考慮使用IABP的患者本身合并更多的高危因素,故臨床有較多爭議。
在隨機試驗中發現,高危PCI治療前置入IABP與長期死亡率顯著降低相關〔6〕。在我國的臨床工作中,高危冠心病的介入治療中同樣有較多選擇。研究表明,IABP在急性心肌梗死合并CS的患者無獲益,故2016年ESC指南中推薦等級為ⅢB級,這類患者的預后不良,與其伴隨嚴重的全身炎癥反應綜合征(SIRS)、多器官功能障礙綜合征(MODS)等后果相關〔7〕。本研究結果與之相符。
有研究報道年齡是心臟病患者最常見的死亡預測因子〔8〕。國外研究表明,行開放性心臟手術的老年患者院內死亡率為75.0%〔9〕。國內有研究表明,年齡增長是急性冠狀動脈綜合征死亡的危險因素之一〔10〕。本研究也表現為死亡組的年齡更大,這可能與高齡患者免疫力低下,炎癥因子水平更高相關。但高齡不是PCI術的禁忌,國內研究顯示,高齡急性冠狀動脈綜合征患者行PCI術操作成功率高,住院期間病死率和隨訪期間不良心血管事件發生率較低〔11〕。故高齡患者需動態監測生命體征,對于病程中可能的并發癥早期干預,促進患者恢復并改善預后〔12〕。本研究發現死亡組術后的肌酐水平與死亡率及 MACE事件的發生率相關,此前國內也有臨床研究報道急性心肌梗死患者并發急性腎衰竭患者死亡率達100%〔13〕。這可能與危重患者左室功能顯著下降,導致酸性代謝產物增多,腎臟灌注不足等多因素相關。
此前有研究發現罪犯血管為LAD的患者使用IABP輔助治療可降低住院期間死亡率,而LM及RCA病變則無差異〔14〕。本研究也顯示LM病變為置入IABP的高危冠心病人群的獨立危險因素,有更高的死亡率。此外,死亡組術后心率更快,考慮一方面有患者腎素-血管緊張素-醛固酮系統(RASS)激活的原因,導致心肌耗氧增加,負荷加重;另一方面,心動過速會減少IABP作用下舒張壓的增加〔15〕,削弱其支持作用。同時本研究結果提示心臟功能及傳導系統嚴重受損,故圍術期的心率管理需早期重視干預。
IABP-SHOCK-Ⅱ研究認為入院時血糖濃度升高是30 d和1年死亡率的獨立預測因子,與既往糖尿病史無關〔16〕。本研究結果與之不符。本研究還發現,既往腦卒中病史人群在死亡組更多,可能與該類患者相對病情更重有關。術后并發大出血的患者也更多,這一結果可能與手術時間更長,使用肝素量更大有關。
本研究為回顧性研究,且樣本量較小,隨訪時間不夠長,有待進一步的大樣本長期隨訪研究。本研究結果表明,年齡、圍術期最高肌酐、CS、LM病變為患者死亡的獨立危險因素。圍術期需加強監測,早期識別這些特點,估計患者預后,干預高危因素,優化治療,或可以早期選擇其他循環輔助器械等臨床決策,達到更佳的救治目的。

