非洲豬瘟病毒熒光定量PCR的建立及4種檢測試劑盒的比較
肖琦 蔣彩霞 史慧 趙霞玲 錢雯嫻 朱家平 張馮禧 溫立斌 汪偉 何孔旺

摘要:為評估目前常用商品化非洲豬瘟熒光定量PCR檢測試劑盒,參考OIE推薦的非洲豬瘟病毒(ASFV)熒光定量PCR方法合成引物和探針,建立非洲豬瘟病毒qPCR檢測方法(OIE-qPCR);并與市面4種ASFV檢測試劑盒進行了比較。以人工合成的ASFV p72基因TA克隆重組質粒為陽性標準品,OIE-qPCR可以檢測到10~102 copies;而4種ASFV熒光定量PCR檢測試劑盒中,進口試劑盒TF-qPCR能檢測到10 copies,進口試劑盒ID-qPCR和國產試劑盒QD-qPCR能檢測到10~102 copies,而國產試劑盒LY-qPCR能檢測到102 copies。對健康豬組織樣及臨床模擬樣品的檢測結果顯示:OIE-qPCR與4種檢測試劑盒之間的符合率為92.60%~99.03%。其中,陽性樣品CT值的相關系數為0.988~0.997(Perason法),表明各試劑盒之間相關性良好;但在檢測病毒核酸含量較低的樣品時,各試劑盒結果之間存在一定差異,其中,TF-qPCR試劑盒顯示更高的陽性檢出率,ID-qPCR試劑盒和LY-qPCR試劑盒次之。本研究為臨床選用非洲豬瘟病毒快速檢測試劑盒提供了依據。
關鍵詞:非洲豬瘟病毒;檢測;熒光定量PCR;靈敏性;穩定性;敏感性
中圖分類號:S852.65+1 文獻標志碼: A文章編號:1002-1302(2021)02-0119-06
收稿日期:2020-11-13
基金項目:江蘇省現代農業(生豬)產業技術體系生物安全創新團隊項目(編號:JATS[2019]403)。
作者簡介:肖琦(1980—),女,遼寧丹東人,博士,助理研究員,主要從事豬病及人獸共患病防控研究。E-mail:xiaoqi_2122@163.com。
通信作者:何孔旺,研究員,主要從事豬病及人獸共患病防控研究。E-mail:kwh2003@263.net。
非洲豬瘟自從2018年8月在我國首次報道[1]以來,對我國養豬業造成了巨大的經濟損失[2]。病原的快速檢測在防控非洲豬瘟上發揮著十分重要的作用。實時熒光PCR因其特異性高、敏感性好,是目前應用最為廣泛的非洲豬瘟檢測技術[3]。市場上主流使用的試劑盒的品牌較多,既有國產品牌,也有進口品牌。在實際使用過程中,各種品牌非洲豬瘟病毒熒光定量PCR檢測試劑盒的效果是否存在差異,相關報道較少。為了建立統一的參比方法,本研究參考OIE推薦的非洲豬瘟病毒熒光PCR方法[4]合成引物和探針,建立非洲豬瘟病毒qPCR(簡稱OIE-qPCR)檢測方法,以人工合成的非洲豬瘟病毒p72蛋白基因TA克隆為陽性質粒標準品,以健康豬組織樣及臨床模擬樣品作為檢測對象,比較OIE-qPCR和4種臨床常用的非洲豬瘟病毒熒光定量PCR檢測試劑盒的靈敏性、穩定性、特異性,為臨床檢測非洲豬瘟病毒時的試劑盒選用提供參考依據。
1材料與方法
1.1儀器與試劑
QuantStudio 6 Flex實時熒光定量PCR系統,購自美國應用生物系統(ABI)公司;美國MP*FastPrep-24樣品均質儀,購自美國MP公司。TIANDZ柱式動物DNAout試劑盒、柱式病毒DNAout試劑盒,購自北京天恩澤公司;TaKaRa Premix Ex TaqTM(Probe qPCR)、pMD19-T,購自寶生物工程(大連)有限公司。
1.2病毒株
豬圓環病毒2型p58株、豬偽狂犬病病毒Bartha-K61株、豬細小病毒NADL-2株、豬瘟病毒HCLV株、豬繁殖與呼吸綜合征病毒NJGC、豬流行性腹瀉病毒AH2012株,均由江蘇省農業科學院獸醫研究所保存。
1.3商品化非洲豬瘟病毒檢測試劑盒
國產和進口的商品化非洲豬瘟病毒檢測試劑盒各2種,共4種。國產試劑盒包括A公司非洲豬瘟病毒熒光PCR檢測試劑盒(簡稱QD-qPCR試劑盒)、B公司非洲豬瘟病毒實時熒光PCR檢測試劑盒(簡稱LY-qPCR試劑盒),進口試劑盒有C公司非洲豬瘟(ASF)qPCR檢測試劑盒(TF-qPCR試劑盒)和D公司非洲豬瘟病毒DNA實時定量PCR檢測試劑盒(ID-qPCR試劑盒)。所有試劑盒均在其有效期內使用。
1.4臨床健康豬樣品
1.4.1樣品來源共33份樣品。其中,豬脾臟、肝臟、腎臟、淋巴結等組織樣品均來自江蘇某菜市場,血清和唾液樣品來自江蘇某豬場。
1.4.2樣品處理
1.4.2.1組織樣品取100 mg組織樣品(脾臟、肝臟、腎臟、淋巴結)置于無菌破碎管中,加入1 mL無菌PBS(pH值7.2)和3顆鋼珠,在樣品均質儀上勻漿處理,然后以12 000 r/min離心3 min,吸取上清200 μL,置于1.5 mL無菌離心管中,用于DNA提取。
1.4.2.2血清、唾液樣品血清、唾液樣品直接取上清200 μL,置于1.5 mL無菌離心管中,用于DNA提取。
1.4.3DNA提取組織樣品用TIANDZ柱式動物DNAout試劑盒,按其說明書提取DNA;血清、唾液樣品用TIANDZ柱式病毒DNAout試劑盒,按其說明書提取DNA。
1.5非洲豬瘟病毒p72陽性質粒標準品的制備
1.5.1非洲豬瘟病毒p72全長基因合成根據GenBank中已登錄的非洲豬瘟病毒安徽株XCGQ(MK128995.1)序列,合成p72蛋白基因全長序列,長度1 941 bp,委托寶生物工程(大連)有限公司合成。置于-20 ℃保存。
1.5.2非洲豬瘟病毒p72全長基因質粒構建將人工合成的p72全長基因克隆至pMD19-T載體中,篩選獲得陽性重組質粒,作為非洲豬瘟病毒p72基因核酸檢測的陽性標準品。
1.6非洲豬瘟病毒qPCR(OIE-qPCR)檢測方法的建立
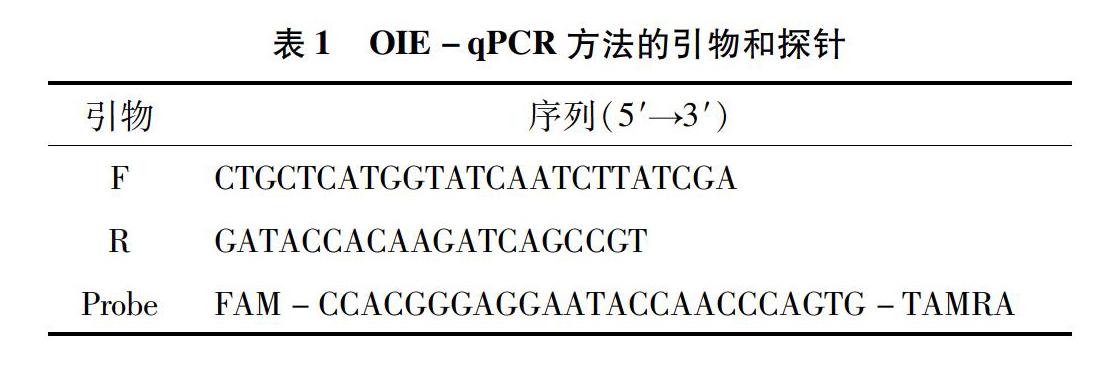
1.6.1引物和探針參照OIE推薦的非洲豬瘟病毒熒光定量PCR方法[4],合成引物和探針。引物和探針序列見表1,由寶生物工程(大連)有限公司合成。
1.6.2反應體系與反應條件參照OIE推薦的方法,OIE-qPCR反應體系為20 μL,其中水5.1 μL、Mix 10 μL、ROXⅡ 0.4 μL、上游引物(10 μmol/L)1 μL、下游引物(10 μmol/L)1 μL、探針(10 μmol/L)0.5 μL、DNA模板2 μL;qPCR反應程序為50 ℃ 120 s;95 ℃ 10 min;95 ℃ 15 s,58 ℃ 60 s,40個循環。
1.6.3結果判定標準陰性對照無CT值或無擴增曲線;陽性對照CT值≤35,并出現典型的擴增曲線,判為試驗成立。檢測樣品CT值≤40,并出現典型的擴增曲線,判為陽性;檢測樣品無CT值或CT值>40,判為陰性。
1.6.4特異性試驗按照“1.4.3”節的方法提取豬圓環病毒2型、豬偽狂犬病病毒、豬細小病毒、豬瘟病毒、豬繁殖與呼吸綜合征病毒、豬流行性腹瀉病毒核酸進行OIE-qPCR特異性試驗。
1.7商品化非洲豬瘟病毒檢測試劑盒檢測方法
4種商品化非洲豬瘟病毒檢測試劑盒均為熒光定量PCR方法,按照各試劑盒說明書的要求進行非洲豬瘟病毒核酸檢測。各試劑盒的反應條件、結果判定標準等見表2。
1.8OIE-qPCR與4種商品化檢測試劑盒的比較
1.8.1靈敏性試驗將“1.5”節獲得的非洲豬瘟病毒核酸陽性標準品p72全長基因重組質粒,用無菌ddH2O稀釋至103、102、101、100 copies/μL,用于 OIE-qPCR 及各商品化檢測試劑盒的靈敏度檢驗。
1.8.2重復性試驗用OIE-qPCR及各商品化檢測試劑盒分別檢測稀釋到103、102、101、100 copies/μL 的p72全長基因重組質粒樣品,每個樣品設3個重復。
1.8.3組織樣品及模擬臨床樣品的檢測比較用OIE-qPCR及4種商品化檢測試劑盒檢測33份正常豬組織樣品和33份模擬臨床樣品(在陰性組織樣品中加入不同濃度的p72全長基因重組質粒),比較各試驗盒的檢測符合率和相關系數。
2結果與分析
2.1OIE-qPCR檢測方法的建立
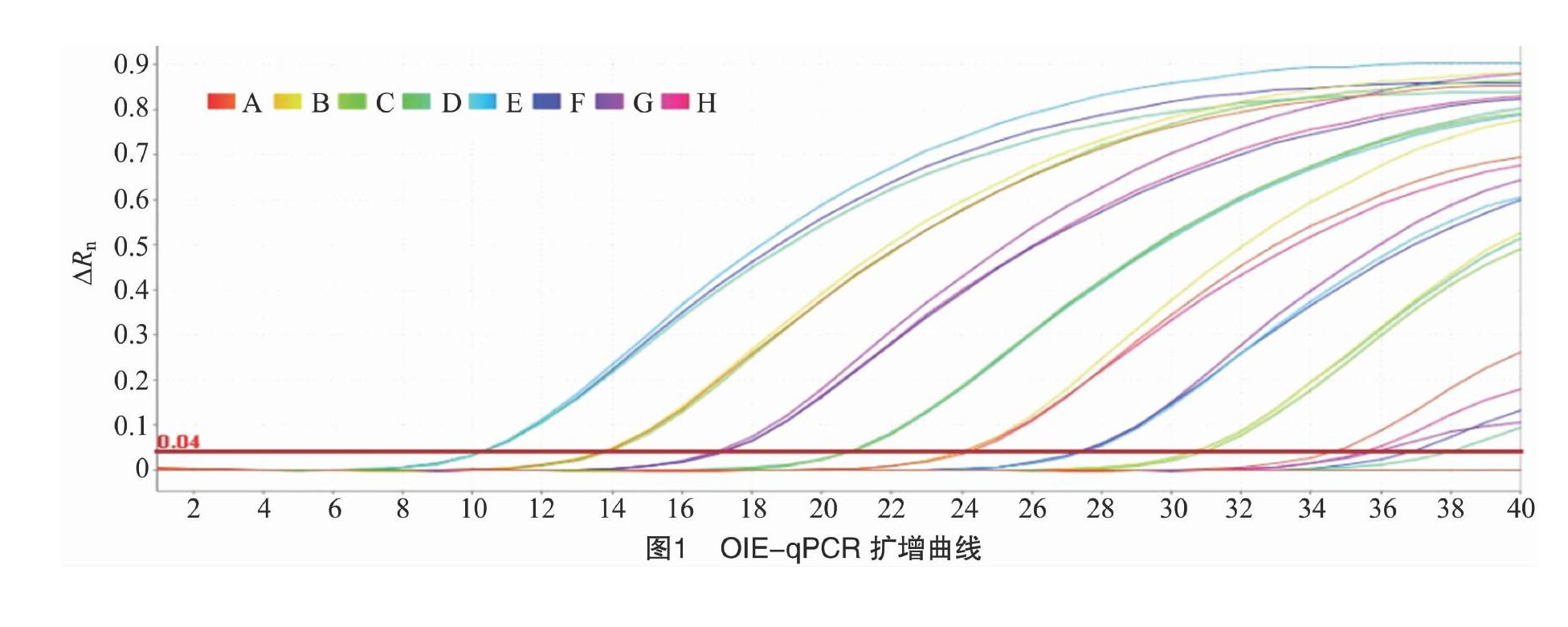
用建立的OIE-qPCR檢測方法,檢測不同稀釋度的非洲豬瘟病毒p72全長基因重組質粒,能出現典型的擴增曲線(圖1);而檢測豬圓環病毒2型、豬偽狂犬病病毒、豬細小病毒、豬瘟病毒、豬繁殖與呼吸綜合征病毒、豬流行性腹瀉病毒等,均沒有出現擴增曲線。
2.2OIE-qPCR與4種商品化檢測試劑盒靈敏性與穩定性試驗
靈敏性試驗結果表明:OIE-qPCR的靈敏度可以檢測到101~102 copies;4種商品化非洲豬瘟病毒熒光定量PCR檢測試劑盒中,有1種試劑盒(TF-qPCR)能檢測到101 copies,有2種試劑盒(QD-qPCR和ID-qPCR)能檢測到101~102 copies,有1種試劑盒(LY-qPCR)能檢測到102 copies。
穩定性試驗結果顯示:OIE-qPCR與4種商品化檢測試驗盒,在檢測103 copies和102 copies濃度的陽性標準質粒時均能100%檢出;在檢測 100 copies 時,所有檢測結果均為陰性;檢測濃度為101 copies的陽性質粒時,TF-qPCR的陽性檢出率為100%,OIE-qPCR與QD-qPCR、ID-qPCR的陽性檢出率均只有33.3%,而LY-qPCR的陽性檢出率為0%(表3)。
2.3OIE-qPCR與4種商品化檢測試劑盒檢測組織樣品及臨床模擬樣品
用OIE-qPCR方法及4種商品化檢測試劑盒檢測33份臨床健康豬組織樣品及血清、唾液樣品,結果均為陰性;檢測33份臨床模擬樣品,結果出現一定差異(表4)。檢測結果顯示,OIE-qPCR方法檢測為陽性的22份樣品,4種商品化檢測試劑盒的檢測結果也均為陽性,且CT值之間均有良好的相關性,相關系數為0.988~0.997(PERASON法)。但用OIE-qPCR方法檢測為陰性的樣品中,有6份樣品用4種商品化檢測試劑盒分別檢測出1份(QD-qPCR試劑)、3份(LY-qPCR試劑盒)、4份(TF-qPCR試劑盒)和3份(ID-qPCR試劑盒)陽性,提示在檢測核酸含量處于臨界值的臨床樣品時,TF-qPCR試劑盒的陽性檢出率最高;在這6份檢測結果有差異的樣品中,僅1份樣品被3種試劑盒同時檢測為陽性,另有3份樣品被2種試劑盒檢測為陽性,其他2份樣品均只有1種試劑盒檢測為陽性,表明當樣品中的非洲豬瘟病毒核酸含量較低時,各試劑盒的檢測結果存在一定的差異。此外,將用OIE-qPCR方法及4種商品化試劑盒檢測的CT值在30以上的14份樣品進行相關性比對時,相關系數為0.503~0.952,進一步表明當樣品中的非洲豬瘟病毒核酸含量較低時,各試劑盒的檢測結果存在一定的差異。統計結果顯示,OIE-qPCR方法與4種商品化檢測試劑盒之間檢測結果的符合率為92.60%~99.03%(表5)。
3討論
非洲豬瘟最早于1921年在非洲肯尼亞被報告[5-6],屬于重大動物疫病,豬一旦發病,死亡率可高達100%,給世界養豬業造成了巨大的經濟損失。但迄今為止,全球還沒有安全、有效的非洲豬瘟商品化疫苗和藥物,非洲豬瘟的防控主要依賴于嚴格的生物安全措施。
2018年8月我國首次報道非洲豬瘟疫情以來,經過2年多的艱苦努力,我國非洲豬瘟防控工作取得了積極的成效,但是非洲豬瘟病毒已在我國定植,污染面較大,疫情點狀發生的態勢將在較長時期內存在[7]。因此,迫切需要能夠在感染早期快速檢測出非洲豬瘟病毒的技術,及時發現非洲豬瘟病毒感染豬,及時撲滅疫情。我國農業農村部在2020年5月印發的2020年第二版《非洲豬瘟疫情應急實施方案》中明確規定:具備良好生物安全防護水平的規模豬場,在出現非洲豬瘟疫情時,可以僅將發病豬舍作為疫點進行處理;豬場在自檢時發現非洲豬瘟陽性豬,也只需要撲殺陽性豬及其同群豬,而對其余豬群在隔離觀察21 d無異常且檢測為陰性的情況下,可以就近屠宰或繼續飼養。這一政策的出臺和調整,為規模豬場及時篩查和發現非洲豬瘟陽性豬,精準清除非洲豬瘟感染豬,保障豬群安全提供了政策保障,同時也對非洲豬瘟病毒檢測及篩查技術提出了更高的要求。
非洲豬瘟病毒常見的檢測技術包括檢測抗原的ELISA方法[8]、熒光抗體試驗[9]和試紙條檢測法[10],以及檢測非洲豬瘟病毒核酸的PCR方法[11]、實時熒光PCR法[12-16]和等溫擴增技術[17]等。2019年6月11日,中國動物疾病預防控制中心公布了通過專家評審的第二批非洲豬瘟現場快速檢測試劑名單,其中一共有34種試劑,全部為核酸檢測類,包括熒光定量PCR類28種和等溫擴增類6種。但從實際應用情況來看,熒光定量PCR檢測試劑盒應用最為廣泛,但目前,對多種非洲豬瘟病毒熒光定量PCR檢測試劑盒的敏感性、特異性及穩定性等尚缺乏較為系統的比較。
由于現有的非洲豬瘟病毒熒光定量PCR檢測試劑盒多數參照OIE推薦的以p72基因為靶標的熒光定量PCR(OIE-qPCR)方法研制,所以我們以OIE-qPCR方法為參照,對臨床常用的4種商品化非洲豬瘟病毒核酸qPCR檢測試劑盒進行評估。結果表明,OIE-qPCR方法與市面上使用較多的4種商品化非洲豬瘟病毒qPCR檢測試劑盒的符合率為92.60%~99.03%,在檢測臨床模擬強陽性樣品時,各試劑盒的檢測結果之間均具有良好的相關性;因此,在臨床檢測和診斷中,尤其是在檢測已明顯表現出非洲豬瘟臨床癥狀的病死豬樣品時,由于樣品中非洲豬瘟病毒核酸含量較高,所以幾種試劑盒均可以達到檢測要求。但是,在檢測非洲豬瘟病毒核酸含量較低的樣品(10~100 copies)時,OIE-qPCR方法與4種商品化試劑盒的檢測結果之間存在一定差異,僅進口的TF-qPCR試劑盒能穩定檢測到10 copies,進口的ID-qPCR和國產的QD-qPCR以及OIE-qPCR的檢出范圍為10~102 copies,而另一種國產試劑盒LY-qPCR僅能檢測到102 copies。在6份檢測結果不一致的臨床模擬樣品中,進口的TF-qPCR檢測出4份陽性樣品,ID-qPCR和LY-qPCR各檢測出3份陽性樣品,而QD-qPCR只檢測出1份陽性樣品;而且,各試劑盒檢出的陽性樣品之間,重合率非常低,僅有1份樣品同時被3種試劑盒檢測為陽性,另有2份樣品同時被2種試劑盒檢測為陽性,其他3份樣品均只有1種試劑盒檢測為陽性,表明在非洲豬瘟病毒核酸含量較低時,各試劑盒檢測的結果會出現較為明顯的差異。提示在臨床篩查時,一是盡量選擇敏感度高的試劑盒,二是當樣品CT值在35或35以上時,以及在沒有CT值時,需要慎重判定結果,必要時可用不同的試劑盒重復檢測,或對豬群連續采樣監測。
上述結果也提示,目前的非洲豬瘟病毒熒光定量PCR方法雖然敏感度較高、特異性強,但用于檢測拷貝量低的核酸樣品時(如未出現臨床癥狀的豬,或病毒感染早期的豬),還存在一定的局限。由于非洲豬瘟病毒在自然感染后的潛伏期為4~9 d,這也是早期診斷、早期精準清除的關鍵時期,但由于在潛伏期內,感染豬的排毒量通常比較低,因此,需要進一步提高非洲豬瘟檢測試劑盒的敏感度,以便能夠盡早篩查出可能感染的豬,實現早期精準清除。
參考文獻:
[1]Zhou X,Li N,Luo Y,et al. Emergence of African swine fever in China,2018[J/OL]. Transboundary and Emerging Diseases,2018 Aug 13.doi:10.1111/tbed.12989.[Epub ahead of print]
[2]Woonwong Y,do Tien D,Thanawongnuwech R. The Future Of The Pig Industry After The Introduction of African swine fever into Asia[J]. Animal Frontier,2020,10(4):30-37.
[3]張麗,羅玉子,王濤,等. 非洲豬瘟診斷技術發展現狀與需求分析[J]. 中國農業科技導報,2019,21(9):1-11.
[4]于康震,張仲秋,馮忠武,等. OIE陸生動物診斷試驗與疫苗手冊(哺乳動物、禽類與蜜蜂)下卷[M]. 7版.世界動物衛生組織(OIE),2012:1198.
[5]Beltran A D,Aris M,Gallardo C,et al. 非洲豬瘟:發現與診斷-獸醫指導手冊[M]. 羅馬:聯合國糧食及農業組織(FAO),2018:7.
[6]Montgomery R E. On a form of swine fever occurring in British East Africa(Kenya Colony)[J]. Journal of Comparative Pathology and Therapeutics,1921,34:159-191.
[7]農業農村部. 農業農村部回應非洲豬瘟疫情防控情況[J]. 北方牧業,2020(21):16.
[8]Wardley R C,Hamilton F,Wilkinson P J. The replication of virulent and attenuated strains of African swine fever virus in porcine macrophages[J]. Archives of Virology,1979,61(3):217-225.
[9]Bool P,Ordas A,Sachez-Botija C. El diagnostico de la peste porcina African por immunofluorescencia[J]. Bullutin of International Epizoot,1969,72:819-839.
[10]吳海濤,成大榮,吳萌,等. 非洲豬瘟病毒膠體金免疫層析試紙條的研制[J]. 黑龍江畜牧獸醫,2018(17):126-128,238.
[11]Agüero M,Fernández J,Romero L,et al. Highly sensitive PCR assay for routine diagnosis of African swine fever virus in clinical samples[J]. Journal of Clinial Microbiology,2003,41(9):4431-4434.
[12]King D P,Reid S M,Hutchings G H,et al.Development of a TaqMan PCR assay with internal amplification control for the detection of African swine fever virus [J]. Journal of Virological Methods,2003,107(1):53-61.
[13]李維彬,蔣正軍,王玉炯,等. 非洲豬瘟病毒TaqMan探針實時熒光定量PCR檢測方法的建立[J]. 寧夏大學學報(自然科學版),2007,28(1):56-59.
[14]張泉,朱鴻飛,孫懷昌. 非洲豬瘟病毒常規PCR及Real-time PCR檢測方法的建立[J]. 中國預防獸醫學報,2007,29(6):458-460.
[15]吳亞楠,朱瀟靜,周博倫,等.非洲豬瘟病毒TaqMan熒光定量PCR檢測方法的建立[J]. 中國獸醫學報,2020,40(5):888-891,896.
[16]杜楠楠,高飛,姜一峰,等. 非洲豬瘟TaqMan實時熒光定量PCR檢測方法的建立與應用[J]. 中國獸醫科學,2020,50(4):423-429.
[17]王建昌,王金鳳,劉立兵,等.非洲豬瘟病毒RPA等溫檢測方法的建立[J]. 中國動物檢疫,2016,33(7):78-81,94.呂孫建,袁雪梅,張海琪,等. 凡納濱對蝦養殖期間水體及腸道菌群變化研究[J]. 江蘇農業科學,2021,49(2):125-131.

