限碳背景下燃煤電廠對(duì)策分析與電化學(xué)催化還原技術(shù)進(jìn)展
馬雙忱,武 凱,劉 暢,別 璇,王 智,王雨菲,李嘉雨
(華北電力大學(xué) 環(huán)境科學(xué)與工程系 河北省電廠煙氣多污染物控制重點(diǎn)實(shí)驗(yàn)室,河北 保定 071003)
0 引 言
對(duì)于人類社會(huì)和地球,氣候變化是一項(xiàng)緊迫的威脅,且具有潛在的不可逆轉(zhuǎn)性。2018年10月,聯(lián)合國(guó)政府間氣候變化專門委員會(huì)(IPCC)審議了《關(guān)于全球升溫1.5 ℃的特別報(bào)告》(SR1.5)[1],報(bào)告指出:截至2017年,人類活動(dòng)導(dǎo)致的氣候變暖比工業(yè)化前的水平高出約1 ℃,若繼續(xù)以目前的速率升溫,全球升溫可能會(huì)在2030—2052年達(dá)到1.5 ℃,將增大健康、生計(jì)、糧食安全、水供應(yīng)、安全、經(jīng)濟(jì)增長(zhǎng)等氣候相關(guān)風(fēng)險(xiǎn)。根據(jù)美國(guó)國(guó)家航空航天局戈達(dá)德太空研究所(NASA GISS)科學(xué)家正在進(jìn)行的一項(xiàng)溫度分析[2-3],與1951—1980年的平均溫度相比,2019年全球年平均溫度增幅0.98 ℃。
Jouzel和Lüthi等[4-5]通過分析南極的冰層結(jié)構(gòu)及其成分,證實(shí)了溫度與CO2濃度關(guān)系密切。據(jù)夏威夷莫納羅亞觀測(cè)站(Mauna Loa Observatory)的監(jiān)測(cè)結(jié)果,2020年5月大氣CO2濃度達(dá)750.77 mg/m3的季節(jié)性峰值,創(chuàng)造了有監(jiān)測(cè)記錄以來(lái)CO2月平均濃度新高。同時(shí)大氣中CO2濃度的增速正穩(wěn)步加快,2000—2010、2010—2020年的年平均增長(zhǎng)分別為3.60、4.32 mg/m3,大量證據(jù)表明,大氣中CO2濃度增速加快是由排放量增加引起[6]。據(jù)《2018年國(guó)民經(jīng)濟(jì)和社會(huì)發(fā)展統(tǒng)計(jì)公報(bào)》[7]數(shù)據(jù),2018年中國(guó)能源消費(fèi)總量為46.4億t標(biāo)準(zhǔn)煤,其中煤炭消費(fèi)占比59.0%,在能源構(gòu)成中仍處于主體地位。根據(jù)全球碳計(jì)劃組織發(fā)布的報(bào)告[8],中國(guó)碳排放量在全球碳排放總量的占比由2016年的25%升至2017年的27%,是全球最大的碳排放國(guó),正面臨著嚴(yán)峻的碳減排形勢(shì)。
采用物理、化學(xué)、生物等方式對(duì)分離后的CO2加以利用或封存,以實(shí)現(xiàn)CO2減排的工業(yè)過程,是減少CO2排放、控制溫室效應(yīng)、實(shí)現(xiàn)化石能源清潔利用的重要手段。電化學(xué)催化還原(Electrochemical catalytic reduction,ECR)由于具有產(chǎn)物的選擇性可控、反應(yīng)條件溫和、反應(yīng)器形式緊湊等優(yōu)勢(shì)逐漸受到國(guó)內(nèi)外研究人員的關(guān)注,且用于驅(qū)動(dòng)反應(yīng)的電能可由太陽(yáng)能、風(fēng)能、潮汐能等非穩(wěn)定能源提供,為棄風(fēng)、棄光、棄水等低品位電能的利用提供了途徑。
本文對(duì)CO2電化學(xué)催化還原技術(shù)的過程原理進(jìn)行了闡述,圍繞電極、電解質(zhì)、CO2溶解性、反應(yīng)器形式進(jìn)行了討論,通過對(duì)比分析不同體系的特點(diǎn),提出燃煤電廠煙氣中CO2電化學(xué)催化還原對(duì)策,并指出在向?qū)嶋H應(yīng)用轉(zhuǎn)化過程中該技術(shù)面臨的障礙和研究趨勢(shì)。
1 CO2電化學(xué)催化還原
自20世紀(jì)80年代,電化學(xué)催化還原CO2逐漸成為國(guó)內(nèi)外科研界的研究熱點(diǎn)。CO2電化學(xué)催化還原是通過外加電壓、電流提供電子,在不同的催化劑、電極、電解液以及電解電勢(shì)等條件下,將CO2轉(zhuǎn)化為CO、甲酸、甲醇、草酸和甲烷等產(chǎn)物,基本化學(xué)反應(yīng)式為
(1)
CO2電化學(xué)催化還原流程通常分為:① CO2分子吸附到催化劑表面;② 催化劑催化轉(zhuǎn)化、電子轉(zhuǎn)移和質(zhì)子遷移;③ 目標(biāo)產(chǎn)物從催化劑表面脫附并擴(kuò)散到電解質(zhì)中。隨著CO2在不同電極上的還原過程得到廣泛研究,學(xué)者們普遍認(rèn)可的CO2電化學(xué)催化還原過程[9-13]為
1)電極對(duì)CO2(g)的吸附和活化
(2)


(3)

(4)
③·CO+(ads)脫除一個(gè)O原子生成 ·C(ads):

(5)
④·CO+(ads)加H+生成·COH(ads):

(6)

(7)
3)中間產(chǎn)物加H+和聚合生成最終產(chǎn)物

(8)
乙二酸:

(9)

(10)

(11)

(12)

(13)
在一定的過電位條件下,H+和·C(ads)、·COH(ads)、·COOH(ads)等中間產(chǎn)物通過聚合生成鏈狀大分子有機(jī)物CxHy、CxHyOH、CxHyCHO、CxHyCOOH等,CO2電化學(xué)催化還原過程如圖2所示。

圖1 CO2電化學(xué)催化還原路徑及中間產(chǎn)物

圖2 CO2電化學(xué)催化還原過程
1.1 電催化過程中的電極問題
CO2電化學(xué)催化還原過程的最終產(chǎn)物通常為CO、HCOOH、(COOH)2等小分子物質(zhì),難以生成更具利用價(jià)值的長(zhǎng)鏈大分子有機(jī)物。最終產(chǎn)物的影響因素復(fù)雜,除了電極材質(zhì)和電解液組成,物種在電極上的吸附能力差異也是影響反應(yīng)路徑及最終產(chǎn)物的顯著因素。在水溶液中部分金屬電極對(duì)物種的吸附能力與最終主要產(chǎn)物的關(guān)系如圖3所示。
由圖3可知,當(dāng)陰極M對(duì)CO2的吸附能力很弱時(shí)(如Ti、Mo等),通常只在陰極生成H2,只有在較高CO2濃度或壓力下,部分陰極(如Fe、Co等)才會(huì)通過路徑⑤生成HCOOH;當(dāng)中間產(chǎn)物M-CO易脫附時(shí)(如Zn、Ag等),反應(yīng)傾向于通過路徑①生成CO;當(dāng)中間產(chǎn)物M-COOH易脫附時(shí)(如In、Sn等),反應(yīng)傾向于通過路徑⑤生成HCOOH;當(dāng)陰極M對(duì)CO2具有一定的吸附能力,且各類中間產(chǎn)物脫附差異不明顯時(shí)(如Cu、Ru),反應(yīng)傾向于路徑①~⑤聯(lián)合生成種類更多、鏈?zhǔn)浇Y(jié)構(gòu)更長(zhǎng)的CxHy、CxHyOH、CxHyCOOH等大分子。因此強(qiáng)化電極對(duì)CO2及其中間產(chǎn)物的吸附能力是促使生成更具利用價(jià)值的長(zhǎng)鏈大分子有機(jī)物的有效方法。
由于Cu與Cu基材料具有產(chǎn)物種類豐富、材料廉價(jià)易得等特點(diǎn),在電化學(xué)催化還原CO2研究中受到關(guān)注。Kendra等[15]試驗(yàn)研究了在Cu電極上還原CO2,發(fā)現(xiàn)CH4、C2H4、羧酸、醛、酮等16種還原產(chǎn)物。Hansen等[16-17]結(jié)合DFT計(jì)算,發(fā)現(xiàn)Cu電極對(duì)—CO和—COOH基團(tuán)的結(jié)合能力處于最均衡的狀態(tài),電極上吸附的中間產(chǎn)物種類豐富,為還原反應(yīng)提供了更多路徑,為生成烴類、長(zhǎng)鏈終產(chǎn)物提供了更多可能。

圖3 物種在電極上的吸附能力差異與最終主要產(chǎn)物的關(guān)系
為了進(jìn)一步強(qiáng)化以Cu基材料為陰極的CO2電化學(xué)催化還原特性,對(duì)Cu基材料進(jìn)行改性和修飾,其中改進(jìn)Cu基電極的形貌結(jié)構(gòu)、制備Cu基合金和Cu基復(fù)合材料的研究最受關(guān)注。
Cu基電極的形貌結(jié)構(gòu)對(duì)產(chǎn)物具有重要影響,Pardal等[18]在研究樹狀、蜂窩狀和泡沫狀結(jié)構(gòu)的Cu電極時(shí)發(fā)現(xiàn),樹狀結(jié)構(gòu)電極上的產(chǎn)物主要為CO和CH4,而蜂窩狀和泡沫結(jié)構(gòu)電極上的主要產(chǎn)物為C2H4、C2H6。由于不同金屬電極的CO2催化還原活性不同,因此通過制備合金的方式,可在改善電化學(xué)反應(yīng)活性的同時(shí),提升電極對(duì)產(chǎn)物的選擇性。Jia等[19]以納米銅薄膜(Nano copper film,NCF)為基底,通過電化學(xué)沉積法制備納米Cu-Au合金電極,并在KHCO3水溶液中表現(xiàn)出較強(qiáng)的催化活性,研究表明在其所制Cu63.9Au36.1/NCF合金電極上,甲醇的法拉第效率達(dá)15.9%,約為純銅電極的19倍,同時(shí)乙醇的法拉第效率提升12%左右,Au的加入有效促進(jìn)了產(chǎn)物對(duì)醇的選擇性。金屬電極的功能單一、適用范圍較小,因此通過對(duì)金屬和非金屬材料的復(fù)合和修飾來(lái)顯著提升電極性能、豐富電極功能受到重視。Li等[20]通過將納米銅顆粒負(fù)載在富含吡啶-N的石墨烯(pyridinic-N Graphene,p-NG)上制備p-NG-Cu復(fù)合電極,結(jié)果表明,該電極對(duì)CO2和質(zhì)子均具有極強(qiáng)的吸附能力,可有效促進(jìn)C—C鍵的結(jié)合和加氫反應(yīng),并表現(xiàn)出對(duì)C2H4產(chǎn)物較高的選擇性。目前對(duì)Cu基材料的研究較為廣泛[21],但缺乏對(duì)確定反應(yīng)路徑的切實(shí)支撐理論和中間產(chǎn)物的形成機(jī)理,電極材料、結(jié)構(gòu)與反應(yīng)活性、產(chǎn)物選擇性間的關(guān)系有待進(jìn)一步揭示。
1.2 電催化過程中的電解質(zhì)和CO2溶解
電解質(zhì)為反應(yīng)提供了環(huán)境,其成分組成是影響反應(yīng)過程的關(guān)鍵因素,主要可分為水、有機(jī)溶劑、離子液體3類。
水體系的反應(yīng)優(yōu)勢(shì)在于有充足的質(zhì)子來(lái)源,在水溶液中進(jìn)行CO2還原更經(jīng)濟(jì),但存在析氫反應(yīng)與CO2還原反應(yīng)間的競(jìng)爭(zhēng)問題。通常CO2在有機(jī)溶劑中的溶解度比在水中大,且在有機(jī)溶劑中缺少以水為主的大量質(zhì)子來(lái)源,可削弱析氫副反應(yīng),但有機(jī)溶劑的揮發(fā)性、致毒性、解吸能耗高、設(shè)備腐濁性大等特點(diǎn)引發(fā)了諸多難以解決的問題。離子液體以其極低的揮發(fā)性、較寬的液態(tài)溫度范圍、對(duì)CO2優(yōu)良的溶解性、極高的熱和化學(xué)穩(wěn)定性、電化學(xué)窗口寬等優(yōu)點(diǎn)[22-23]引起學(xué)者關(guān)注。其中,咪唑類離子液體因其物理、化學(xué)結(jié)構(gòu)易于調(diào)整、黏度低、對(duì)CO2的吸收容量大、較好的CO2/N2、CO2/CH4分離效果等特點(diǎn),得到廣泛研究。
CO2作為所消耗的反應(yīng)物,在電解質(zhì)中的濃度直接影響反應(yīng)過程的進(jìn)行。相比于水和有機(jī)溶劑,在離子液體中主要利用其特有的氫鍵網(wǎng)絡(luò)結(jié)構(gòu)和陰離子與CO2之間的弱Lewis酸堿作用,將CO2固定于離子液體的網(wǎng)絡(luò)空隙中[24]。表1為CO2在部分溶劑中的亨利系數(shù)(25 ℃)[25-32]。
在實(shí)際應(yīng)用過程中,高品質(zhì)的CO2氣源難以獲得,以燃煤電廠尾氣中的CO2為例,其體積占尾氣總量的10%~15%,經(jīng)估算,25 ℃、101.325 kPa、15% CO2下CO2在部分溶劑中的摩爾分率分布如圖4所示。
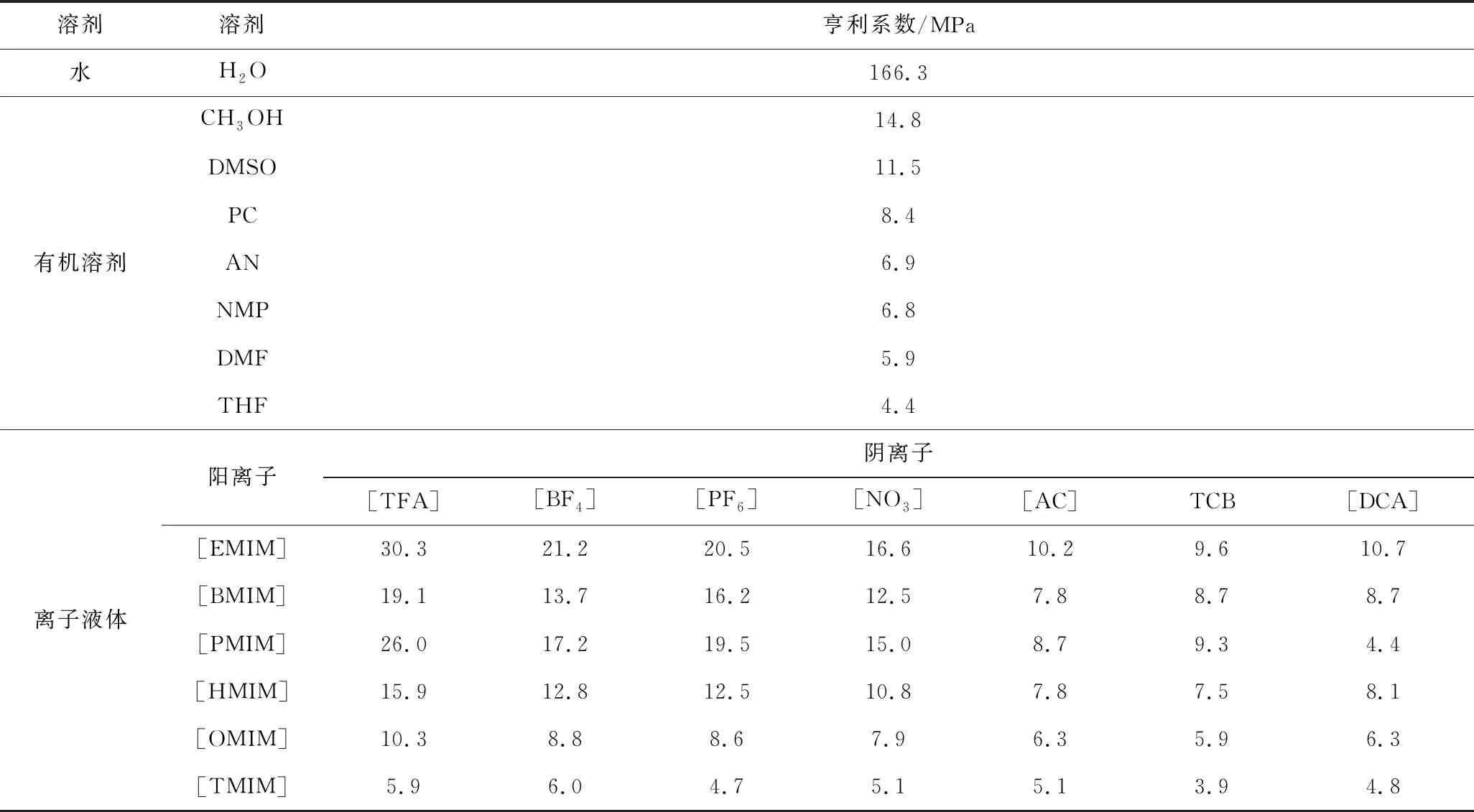
表1 CO2氣體在不同溶劑中的亨利系數(shù)(25 ℃)

圖4 15% CO2在部分溶劑中的摩爾分率(25 ℃、101.325 kPa)
離子液體的引入對(duì)CO2電化學(xué)催化還原有促進(jìn)作用,可明顯提高體系中CO2的溶解性[35],降低還原電位[36],但在離子液體中CO2電化學(xué)催化還原的電流密度仍較低[37],距實(shí)際應(yīng)用仍有一定的差距。
1.3 電催化過程中的反應(yīng)器型式問題
根據(jù)反應(yīng)連續(xù)性的不同,反應(yīng)形式可分為間歇式和連續(xù)式[38-40]。間歇式反應(yīng)受限于CO2在電解質(zhì)體系中擴(kuò)散和溶解特性,隨著反應(yīng)進(jìn)行,電解質(zhì)溶液中CO2濃度降低導(dǎo)致反應(yīng)速率下降,典型的間歇式反應(yīng)器形式如圖5所示。

圖5 間歇式反應(yīng)器
為了保證連續(xù)電化學(xué)反應(yīng)工作的進(jìn)行,在連續(xù)式反應(yīng)器上氣體擴(kuò)散電極得到了廣泛應(yīng)用,相比于需將CO2溶解在電解質(zhì)中的間歇式反應(yīng),直接將CO2氣相輸送至陰極,保持入口CO2濃度處于相對(duì)高位,保證CO2轉(zhuǎn)化效率和體量,在保證陰極上反應(yīng)物濃度穩(wěn)定的同時(shí)有效減弱了氣液傳質(zhì)的影響。典型的連續(xù)式反應(yīng)器形式如圖6所示。
向陰極持續(xù)供應(yīng)一定濃度的CO2,CO2經(jīng)氣流均布板,為氣體擴(kuò)散陰極提供穩(wěn)定的CO2氛圍,CO2在電極上被還原為產(chǎn)物并隨后從電極上脫附下來(lái),部分氣態(tài)產(chǎn)物(CO、 CH4等)隨CO2氣流排出,部分氣、液態(tài)產(chǎn)物溶解至電解質(zhì)中。同時(shí),向陽(yáng)極持續(xù)供應(yīng)H2O等質(zhì)子源,為電解液補(bǔ)充所消耗的質(zhì)子,并產(chǎn)出一定量的O2等副產(chǎn)物。

圖6 連續(xù)式反應(yīng)器
作為影響連續(xù)電化學(xué)催化還原過程的關(guān)鍵因素,氣體擴(kuò)散電極(Gas diffusion electrode,GDL)因其優(yōu)良的孔隙結(jié)構(gòu)和比表面積,極大提升了其上CO2的擴(kuò)散和傳遞,同時(shí)其微孔效應(yīng)在內(nèi)部產(chǎn)生較大壓力,從而促進(jìn)了電化學(xué)催化還原反應(yīng)的發(fā)生[41]。陳國(guó)錢等[42]基于碳?xì)种苽淞素?fù)載錫-石墨烯催化層的新型氣體擴(kuò)散電極,在含飽和CO2的KHCO3電解質(zhì)溶液中將CO2電化學(xué)催化還原為甲酸,平均電流密度達(dá)12.79 mA/cm2,甲酸的法拉第效率達(dá)41.55%,與溶解態(tài)CO2反應(yīng)條件相比,采用氣相CO2反應(yīng)條件電化學(xué)催化還原性能更好。Prakash等[43]分別制備了Sn粉修飾的氣體擴(kuò)散電極(SnGDL)和Sn粉末涂層的石墨電極(SnG),研究發(fā)現(xiàn)相對(duì)于SnG電極,SnGDL電極上CO2反應(yīng)的電流密度增加5倍左右。
盡管間歇式反應(yīng)器無(wú)法實(shí)現(xiàn)連續(xù)的電化學(xué)反應(yīng),但其具有結(jié)構(gòu)簡(jiǎn)單、維護(hù)方便、運(yùn)行穩(wěn)定、干擾因素少等特點(diǎn),為精確的電化學(xué)特性研究提供了便利,被廣泛應(yīng)用于電化學(xué)基礎(chǔ)研究中。大體量CO2氣源在實(shí)際應(yīng)用時(shí),間歇式反應(yīng)器受容積限制,需選擇連續(xù)式反應(yīng)器,但連續(xù)式反應(yīng)器存在對(duì)制造工藝要求高、投資和維護(hù)成本大、氣體擴(kuò)散電極易污堵等缺點(diǎn),未來(lái)式反應(yīng)器的劣勢(shì)有望得到改變。
2 燃煤電廠煙氣中CO2電化學(xué)催化還原對(duì)策
由于燃煤電廠煙氣成分復(fù)雜,氣體中主要包含N2、O2、CO2和少量SO2、SO3、NOx、CH化合物等有害氣體,且夾雜少量石膏、粉塵等固體顆粒,同時(shí)攜帶細(xì)小液滴,作為復(fù)雜的復(fù)合氣固液三相體系,對(duì)煙氣中的CO2進(jìn)行電化學(xué)催化還原具有一定難度。
針對(duì)燃煤電廠尾氣體量大、成分復(fù)雜、CO2含量低(10%~15%)、CO2氣源品質(zhì)低等問題,對(duì)不同體系下CO2電化學(xué)催化還原特點(diǎn),及應(yīng)用于燃煤電廠尾氣中CO2還原的可行性進(jìn)行對(duì)比分析(表2)。

表2 CO2電化學(xué)催化還原特點(diǎn)及應(yīng)用于燃煤電廠尾氣中CO2還原的可行性對(duì)比分析
大體量、低濃度CO2電化學(xué)催化還原過程應(yīng)選擇連續(xù)式反應(yīng)器,Cu基材料的產(chǎn)物種類豐富且可利用價(jià)值高、材料廉價(jià)易得等特點(diǎn)更適合作為電極,離子液體以其優(yōu)異的電化學(xué)反應(yīng)特性和能夠復(fù)合多功能的特點(diǎn)更具應(yīng)用潛力,結(jié)合電化學(xué)催化還原技術(shù)特點(diǎn)和燃煤電廠結(jié)構(gòu)特征,對(duì)大體量、低濃度CO2電化學(xué)催化還原條件進(jìn)行篩選,提出燃煤電廠尾氣中CO2連續(xù)電化學(xué)催化還原技術(shù)應(yīng)用路線(圖7)。

圖7 大體量、低濃度CO2電化學(xué)催化還原條件選擇與技術(shù)應(yīng)用路線
CO2電化學(xué)催化還原技術(shù)研究已經(jīng)初具規(guī)模,但面向?qū)嶋H工業(yè)應(yīng)用仍存在諸多技術(shù)障礙,在向?qū)嶋H應(yīng)用轉(zhuǎn)化過程中,其技術(shù)障礙和研究趨勢(shì)如圖8所示。
工業(yè)CO2點(diǎn)源排放常伴隨雜質(zhì),如NOx、SOx、O2、CO、NH3、VOCs、微量金屬、未燃盡碳、TSP、水蒸氣等,CO2氣源品質(zhì)難以保證。實(shí)際應(yīng)用中,對(duì)于大體量易脫除雜質(zhì)(如水蒸氣等),可通過現(xiàn)有預(yù)處理技術(shù)凈化脫除,但由于氣源中仍有部分雜質(zhì)體量較小,現(xiàn)有技術(shù)難以對(duì)CO2氣源進(jìn)一步提純,因此圍繞微量雜質(zhì)對(duì)CO2電化學(xué)催化還原的潛在影響研究尤為重要。
Byung等[44]證明了由于NOx優(yōu)先CO2參與電化學(xué)催化還原反應(yīng),高濃度NOx將導(dǎo)致CO2電化學(xué)催化還原過程的法拉第效率顯著降低,但NOx濃度較低時(shí)(0.083%,即1 112 mg/m3),CO2電化學(xué)催化還原的法拉第效率僅降低5%,更低濃度的NOx(0.008 3%,即111 mg/m3)對(duì)CO2電化學(xué)催化還原過程幾乎無(wú)影響。Kindle等[45]研究表明,O2的溶解性較CO2弱,O2傳質(zhì)受到較大阻礙,在高電流密度下,O2的存在對(duì)CO2電化學(xué)還原電流無(wú)顯著影響,且未對(duì)CO2電化學(xué)還原機(jī)理造成影響,但O2的存在將降低電化學(xué)過程中的有效電功率,在典型的燃?xì)怆姀S尾氣氣氛(V(CO2)∶V(O2)≈1.67∶1)中,在-1.06 V(相較于SHE)條件下反應(yīng),約12%的電能被O2的電化學(xué)還原所消耗。Zhai等[46]以Cu箔或Cu絲為工作電極,通過將一定濃度的SO2、NO2、O2通入KHCO3或KCL電解液中對(duì)雜質(zhì)氣體的影響進(jìn)行探究,表明較小濃度(0.001%~0.002%)的亞硝酸鹽和氨可產(chǎn)生顯著影響,NO2濃度為0.166 7%時(shí),催化劑中毒,低于1% 的SO2對(duì)反應(yīng)的影響輕微,但即使極低濃度(0.000 15%)的溶解性硫化物可通過與電極形成Cu2S造成電極中毒。張志盼等[47]以Ag為工作電極,通過在KHCO3電解液中加入KCl、KBr和KI發(fā)現(xiàn),鹵族元素對(duì)于CO2的還原反應(yīng)具有促進(jìn)作用,其中I-的存在加快了CO的生成,在過電勢(shì)為590 mV時(shí),CO在含I-溶液中的選擇性是無(wú)I-溶液的28倍。文獻(xiàn)[48-50]對(duì)氣體雜質(zhì)的影響行為進(jìn)行研究。此外,氣源中的微量金屬可能誘導(dǎo)電極催化劑中毒,Hori等[51]發(fā)現(xiàn),電解質(zhì)溶液中的微量Fe2+、Zn2+導(dǎo)致Cu電極中毒,降低其催化活性,失活的主要原因是微量雜質(zhì)金屬在Cu電極上沉積,且CO2還原的中間產(chǎn)物不會(huì)導(dǎo)致Cu電極失活,氣源中的細(xì)微顆粒物存在堵塞催化劑孔道的可能。關(guān)于氣源品質(zhì)對(duì)CO2電化學(xué)催化還原的影響仍需深入研究,可借鑒有選擇性催化還原脫硝(SCR)在電力行業(yè)的成功應(yīng)用的舉措。
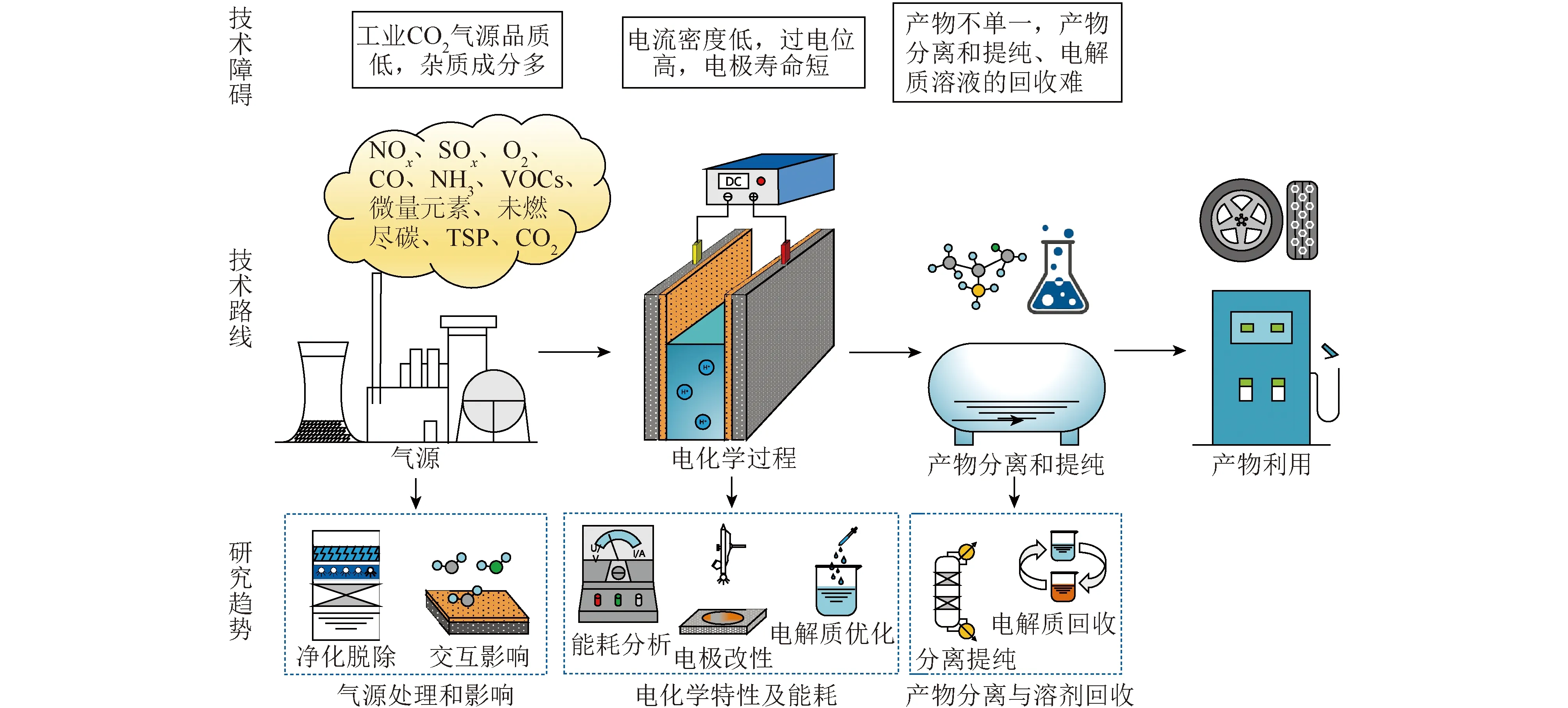
圖8 技術(shù)發(fā)展過程中存在的障礙與趨勢(shì)

延長(zhǎng)電極壽命,維持催化活性是面向?qū)嶋H應(yīng)用過程的重要問題。目前,電極及催化劑維持活性的時(shí)間普遍在幾小時(shí)內(nèi),仍無(wú)法達(dá)到工業(yè)應(yīng)用標(biāo)準(zhǔn)。Fengcai 等[57]將金屬Sn量子片嵌入石墨烯中制備出具有優(yōu)異CO2電催化活性的薄層電極,產(chǎn)物甲酸的法拉第電流效率達(dá)85%,且穩(wěn)定運(yùn)行時(shí)間50 h。Yang等[58]利用單原子Ni修飾多孔碳薄膜制備出可提供大量Ni單原子活性位點(diǎn)的氣體擴(kuò)散電極,所產(chǎn)出的CO法拉第效率達(dá)88%,電流密度達(dá)308.4 mA/cm2,且可維持120 h的催化活性。
此外,具備優(yōu)異性能的離子液體電解質(zhì)制備成本較高,面對(duì)大體量工業(yè)應(yīng)用時(shí)投資成本難以承受,開發(fā)新配方、優(yōu)化制備工藝來(lái)降低成本是工業(yè)應(yīng)用研究的熱點(diǎn);CO2電化學(xué)催化還原的產(chǎn)物多樣,其分離和提純及電解質(zhì)溶液的回收是未來(lái)考慮的重點(diǎn)。
3 結(jié)語(yǔ)與展望
我國(guó)已成為全球最大的碳排放國(guó),面臨著嚴(yán)峻的碳減排形勢(shì),化石燃料電站作為化石燃料消耗大戶,每年向大氣排放體量龐大的CO2,CO2電化學(xué)催化還原由于具有諸多優(yōu)勢(shì)有望成為大規(guī)模工業(yè)化CO2減排的核心應(yīng)用技術(shù)。
本文對(duì)CO2電化學(xué)催化還原技術(shù)的過程原理進(jìn)行了簡(jiǎn)述,圍繞電極、電解質(zhì)、CO2溶解性、反應(yīng)器形式進(jìn)行討論:Cu及Cu基材料由于對(duì)還原過程的多類中間產(chǎn)物吸附能力較為均衡,易通過更多的反應(yīng)路徑促成種類更多、鏈?zhǔn)浇Y(jié)構(gòu)更長(zhǎng)、更具利用價(jià)值的大分子產(chǎn)物生成,且材料廉價(jià)易得,適用于大規(guī)模工業(yè)化CO2還原;離子液體的引入對(duì)CO2電化學(xué)催化還原具有促進(jìn)作用,可顯著降低還原電位,提升電流密度,其對(duì)CO2優(yōu)異的吸收能力更適用于對(duì)低濃度CO2的還原工作;連續(xù)式反應(yīng)器擺脫了反應(yīng)器容積的限制,保持入口CO2濃度處于相對(duì)高位,保證CO2的轉(zhuǎn)化效率和體量,對(duì)于連續(xù)大體量、低濃度CO2氣源的實(shí)際應(yīng)用更具優(yōu)勢(shì)。
結(jié)合電化學(xué)催化還原技術(shù)特點(diǎn)和燃煤電廠結(jié)構(gòu)特征,對(duì)大體量、低濃度CO2電化學(xué)催化還原條件進(jìn)行篩選,確定了以Cu基氣體擴(kuò)散電極-離子液體-連續(xù)式反應(yīng)器為核心的基本電化學(xué)體系,并提出燃煤電廠尾氣中CO2連續(xù)電化學(xué)催化還原技術(shù)應(yīng)用路線,但實(shí)際工業(yè)應(yīng)用仍存在諸多技術(shù)障礙,建議未來(lái)的重點(diǎn)研究工作為:
1)圍繞以Cu基材料為核心的電化學(xué)過程的產(chǎn)物選擇性低、過電位較高、電流密度低,電極壽命短,造成產(chǎn)物種類復(fù)雜、反應(yīng)能耗高、產(chǎn)物產(chǎn)出速率慢、運(yùn)行穩(wěn)定性差等問題,目前仍未能工業(yè)應(yīng)用,對(duì)電極進(jìn)行結(jié)構(gòu)調(diào)控、材料復(fù)合,對(duì)電解質(zhì)進(jìn)行功能復(fù)合、配方優(yōu)化等改性路線是研究重點(diǎn)。
2)工業(yè)CO2氣源品質(zhì)低、雜質(zhì)成分多,氣源中存在的NOx等雜質(zhì)氣體可能與CO2形成競(jìng)爭(zhēng)還原,微量雜質(zhì)金屬可能誘導(dǎo)電極催化劑中毒,細(xì)微顆粒物存在堵塞催化劑孔道的可能,因此,氣源雜質(zhì)對(duì)CO2電化學(xué)催化還原的潛在影響研究將成為面向?qū)嶋H應(yīng)用的研究熱點(diǎn)。
3)CO2電化學(xué)催化還原的產(chǎn)物多樣,其分離和提純及電解質(zhì)溶液的回收是亟待解決的問題。

