黑鯛催乳素基因PRL1和PRL2在急性鹽脅迫環境下的表達分析
林李泉 韋信賢 林國榮 譚紅連 黃婷 劉明珠 楊艷 童桂香

摘要:【目的】明確催乳素基因(PRL1和PRL2)在黑鯛不同組織及不同鹽度脅迫下的表達模式,為黑鯛養殖過程中最適鹽度范圍的確定提供參考依據。【方法】通過RT-PCR擴增黑鯛PRL1和PRL2基因,以ExPASy、NetNGlyc及SWISS-MODEL等在線軟件進行生物信息學分析,并采用實時熒光定量PCR檢測PRL1和PRL2基因在黑鯛不同組織及不同鹽度脅迫下的表達情況。【結果】黑鯛PRL1基因開放閱讀框(ORF)全長639 bp,共編碼212個氨基酸殘基,其編碼蛋白分子量為23.32 kD,理論等電點(pI)為6.70;黑鯛PRL2基因ORF全長750 bp,共編碼249個氨基酸殘基,其編碼蛋白分子量為28.31 kD,pI為8.37。黑鯛PRL1和PRL2蛋白均由1個為信號肽結構域和1個為Hormone 1結構域組成;黑鯛PRL1蛋白二級結構中α-螺旋占69.34%、無規則卷曲占30.66%,包含1個糖基化位點及37個磷酸化位點;黑鯛PRL2蛋白二級結構中α-螺旋占67.07%、無規則卷曲占32.93%,包含1個糖基化位點及21個磷酸化位點。黑鯛PRL1和PRL2基因在12個待檢測組織中均有表達,且均以腦組織中的相對表達量最高,顯著高于其他組織中的相對表達量(P<0.05,下同);在鹽度5‰處理組中,黑鯛PRL1基因在脅迫4 h開始顯著上調,黑鯛PRL2基因在脅迫8 h開始極顯著上調(P<0.01),二者均在脅迫24 h時達峰值,隨后開始緩慢下降,至脅迫72 h時其相對表達量仍顯著高于對照組;在鹽度25‰和35‰處理組中,黑鯛PRL1和PRL2基因在脅迫72 h時其相對表達量均顯著低于對照組。【結論】低鹽脅迫能促進黑鯛PRL1和PRL2基因的表達,高鹽脅迫則抑制黑鯛PRL1和PRL2基因的表達,即黑鯛PRL1和PRL2基因在其適應淡水環境的過程中發揮重要調節作用。
關鍵詞: 黑鯛;催乳素(PRL);PRL1基因;PRL2基因;鹽脅迫;組織表達
中圖分類號: S917.4? ? ? ? ? ? ? ? ? ? ? ? ?文獻標志碼: A 文章編號:2095-1191(2021)12-3254-11
Expression analysis of Acanthopagrus schlegelii PRL1 and
PRL2 in response to acute salinity stress
LIN Li-quan1, WEI Xin-xian2, LIN Guo-rong1, TAN Hong-lian2, HUANG Ting2,
LIU Ming-zhu3, YANG Yan2, TONG Gui-xiang2*
(1Hengsheng Aquaculture Professional Cooperative of Yangxi, Yangjiang, Guangdong? 529500, China; 2Guangxi? Academy of Fishery Science/Guangxi Key Laboratory of Aquatic Genetic Breeding and Healthy Aquaculture, Nanning 530021, China; 3Guangxi Academy of Sciences/Guangxi Engineering Research Center for Fishery Major Diseases
Control and Efficient Healthy Breeding Industrial Technology (GERCFT), Nanning? 530007, China)
Abstract:【Objective】To understand the expression patterns of prolactin genes (PRL1 and PRL2) in different tissues and under different salinity stresses, so as to provide a reference for the determination of the optimal salinity range in the breeding process of Acanthopagrus schlegelii. 【Method】PRL1 and PRL2 genes of A. schlegelii were amplified by RT-PCR, and bioinformatics analysis was performed by ExPASy, NetNGlyc, Swiss-Model and other online softwares. The expression of PRL1 and PRL2 genes in different tissues and under different salinity stresses was detected by real-time fluorescence quantitative PCR. 【Result】The full length of PRL1 open reading frame (ORF) was 639 bp, encoding 212 amino acids with a molecular weight of 23.32 kD and an isoelectric point(pI) of 6.70; and the ORF of PRL2 gene was 750 bp, encoding 249 amino acids with a molecular weight of 28.31 kD and pI of 8.37. PRL1 and PRL2 proteins were both composed of a signal peptide domain and a Hormone 1 domain. In the secondary structure of PRL1 protein, 69.34% of α-helix and 30.66% of random curl were found, including 1 glycosylation site and 37 phosphorylation sites. In the secondary structure of PRL2 protein, α-helix accounted for 67.07% and random curl accounted for 32.93%, including 1 glycosyla-tion site and 21 phosphorylation sites. The results of tissue expression analysis showed that PRL1 and PRL2 genes were expressed in all 12 tested tissues. The highest expression levels of PRL1 and PRL2 were both detected in brain, significantly higher than the relative expression levels in other tissues (P<0.05, the same below). In the 5‰ salinity treatment group, PRL1 gene was significantly up-regulated at 4 h under salt stress, PRL2 gene was extremely significantly up-regulated at 8 h under stress (P<0.01). Both of them reached peak value at 24 h, then began to decline slowly, and their expression levels were still significantly higher than those of the control group at 72 h of stress. The expression levels of PRL1 and PRL2 genes in the 25‰ and 35‰ salinity treatment groups were significantly lower than those in the control group after 72 h stress. 【Conclusion】Low salinity stress can promote the expression of PRL1 and PRL2 genes, while high salinity stress can inhibit the expression of PRL1 and PRL2 genes. In other words, A. schlegelii PRL1 and PRL2 genes play important regulatory roles in the adaptation to fresh water.
Key words: Acanthopagrus schlegelii; prolactin(PRL); PRL1 gene; PRL2 gene; salinity stress; tissue expression
Foundation item: Regional Project of National Natural Science Foundation of China(41966004);Guangdong Science and Technology Development (Vertical Coordinated Management and Linkage Between Provinces and Cities) Special Project(2017B020246046);Guangxi Innovation Team Project of National Modern Agricultural Industrial Technology System (nycytxgxcxtd-20-02);Independent Research Project of Guangxi Key Laboratory of Aquatic Genetic Breeding and Healthy Breeding (2020-A-03-01)
0 引言
【研究意義】催乳素(Prolactin,PRL)是一種單鏈多肽類激素,由動物腦垂體合成及分泌,廣泛參與機體各種生物學功能,包括生長發育、內分泌代謝、繁殖泌乳、免疫調節及電解質平衡等(Kelly et al.,2001;劉瑞鑫等,2013)。在魚類研究中,同樣證實PRL是調節硬骨魚類滲透壓和離子平衡的主要激素(Manzon,2002),在海水魚類適應淡水的過程中PRL在腦垂體和血漿中的合成與分泌顯著增加,認為PRL是通過改變鰓、皮膚、腎臟及腸道等滲透壓調節器官的滲透性及離子運輸途徑以減少水分吸收或增加離子吸收來實現水鹽平衡(左映平和曹勁松,2007)。因此,分析魚類PRL基因在不同鹽度下的表達特征,了解其在鹽脅迫適應方面的功能作用,對揭示海水魚類滲透壓調節機制具有重要意義,同時能為海水魚類養殖最適鹽度范圍的確定提供參考依據。【前人研究進展】PRL是廣鹽性硬骨魚類適應淡水的重要調節激素,通過降低魚類鰓組織滲透率,并刺激鰓黏液細胞分泌黏液,減少Na+和Cl?的排出量,從而維持離子平衡(魏渲輝等,2001)。Yang等(1999)研究發現PRL基因在虹鱒胚胎形成和孵化過程中均有表達,即在魚體早期發育過程中發揮重要作用;左映平和曹勁松(2007)在海水羅非魚中發現PRL能引起腎臟中的Na重吸收和水排泄量增加,并證實PRL是通過作用于腎小球而發揮作用;Breves等(2011)在莫桑比克羅非魚淡水馴化中發現PRL發揮著重要的調節作用,并證實PRL信號通路與斑馬魚鰓組織中的Cl?攝取能力密切相關(Breves et al.,2013);Cunha等(2019)在藍鰓太陽魚中的研究發現PRL對魚體的養育行為和攻擊行為均有重要影響;Takashi等(2019)研究證實PRL參與日本鰻鱺洄游過程中的滲透壓調節;Hu等(2020)研究發現草魚PRL基因轉錄與表達受表皮生長因子(Epidermal growth factor,EGF)的影響;Villalba等(2020)研究表明PRL基因在虹鱒免疫反應中也參與調控作用;Si等(2021)研究表明PRL在牙鲆變態發育尤其是眼睛的不平衡遷移過程中發揮重要作用。【本研究切入點】黑鯛(Acanthopagrus schlegelii)隸屬于硬骨魚綱(Osteichthyes)鱸形目(Perciformes)鯛科(Sparidae),是一種暖溫性底層海水魚類(林李泉等,2021),廣泛分布在我國渤海、黃海、東海、南海沿海及臺灣海峽,因其具有生長速度快和抗病力強等特點,且兼具廣溫性和廣鹽性及營養價值高等優點(鄧惠文等,2019),而深受廣大養殖戶和消費者的喜愛。目前,有關鹽度對黑鯛影響的研究主要集中在生長、生理生化及營養成分分析等方面(Min et al.,2015;賈超峰,2020;王裕玉等,2020);此外,熱休克蛋白和胰島素生長因子I (鄧利等,2003)、催乳激素及其受體(Chang et al.,2007;Tomy et al.,2009)、水通道蛋白和精氨酸催產素受體(An et al.,2008)及抗氧化基因(An et al.,2010)等對黑鯛的鹽度適應機制也起到一定作用,但至今鮮見基于PRL基因表達水平探究黑鯛鹽度適應機制的研究報道。【擬解決的關鍵問題】通過RT-PCR擴增黑鯛PRL1和PRL2基因,以ExPASy、NetNGlyc及SWISS-MODEL等在線軟件進行生物信息學分析,并基于實時熒光定量PCR探討PRL基因在黑鯛不同組織及不同鹽度脅迫下的表達模式,以期為黑鯛養殖過程中最適鹽度范圍的確定提供參考依據。
1 材料與方法
1. 1 試驗材料
黑鯛幼魚(體質量約30±3 g)由陽西縣恒生水產養殖專業合作社提供,共500尾,試驗前將其置于300 L的海水循環養殖缸中暫養1周,水溫(28±1)℃,溶氧量控制在6.5~7.0 mg/L。暫養期間隨機挑選3尾黑鯛幼魚,采集其肝臟、腎臟、心臟、腦、眼、鰓、鰭條、脾臟、皮膚、腸道、性腺及白肌等12個組織,液氮保存備用。RNA提取試劑盒購自北京全式金生物技術股份有限公司,PCR產物回收試劑盒及pMD18-T載體購自寶生物工程(大連)有限公司,SYBR Green染料及RT反轉錄試劑盒購自TOYOBO公司,熒光定量檢測試劑盒SYBR Green PCR Master Mix購自TaKaRa公司,大腸桿菌DH5α感受態購自天根生化科技(北京)有限公司。
1. 2 試驗設計
鹽脅迫試驗設5‰、15‰(對照組)、25‰和35‰共4個處理組,每組50尾黑鯛幼魚。將暫養的黑鯛幼魚隨機分配到各處理組中,分別于鹽脅迫第0、4、8、12、24、48和72 h隨機挑選3尾黑鯛幼魚采集鰓組織,置于液氮中保存備用。
1. 3 總RNA提取及cDNA合成
按RNA提取試劑盒說明提取黑鯛幼魚鰓組織總RNA,以1.0%瓊脂糖凝膠電泳和NanoDrop 2000微量紫外分光光度計分別檢測總RNA的質量及其濃度。利用RT反轉錄試劑盒對總RNA進行反轉錄,反轉錄合成的cDNA樣品-80 ℃保存備用。
1. 4 黑鯛PRL1和PRL2基因克隆
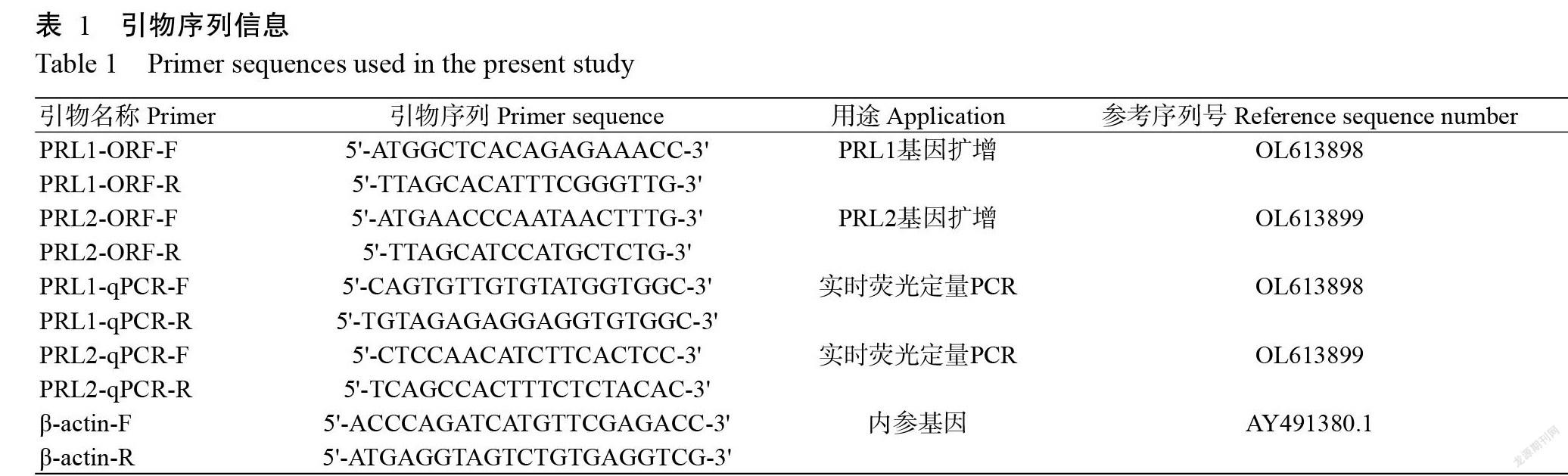
從已構建的黑鯛基因組數據庫中調取PRL基因序列作為參考,利用Primer Premier 5.0設計PRL基因擴增引物(表1),以反轉錄合成的cDNA或基因組DNA樣品為模板進行PCR擴增,反應體系25.0 μL,包括上、下游引物各1.0 μL,cDNA模板1.0 μL。擴增程序:95 ℃預變性3 min;95 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,進行35個循環;72 ℃延伸10 min。純化回收陽性PCR擴增產物,將其連接至pMD18-T載體并轉化DH5α感受態細胞,經搖床培養后接入含Amp+抗性的LB培養基上,挑取單克隆進行菌液PCR鑒定,陽性樣品送至廣州擎科生物技術有限公司進行測序驗證。
1. 5 黑鯛PRL基因生物信息學分析
在Ensembl基因組數據庫中,對比黑鯛PRL基因組序列與近緣物種的基因組序列;利用DNAMAN對測序獲得的序列進行拼接,運用ClustalX 2.1進行氨基酸序列比對分析,再以MEGA 6.0中的鄰接法(Neighbor-joining,NJ)構建系統發育進化樹,Bootstrap設為1000次;使用ExPASy(http://smart.embl-heidelberg.de/smart/set_mode)預測黑鯛PRL蛋白的結構域、分子量、理論等電點(pI)及信號肽;運用NetNGlyc(http://www.cbs.dtu.dk/services/NetNGylc/)預測黑鯛PRL蛋白的糖基化和磷酸化位點;采用PSIPRED (http://bioinf.cs.ucl.ac.uk/psipred/)和SWISS-MODEL(https://swissmodel.expasy.org/)分別預測黑鯛PRL蛋白二、三級結構。
1. 6 實時熒光定量PCR檢測
利用Primer Premier 5.0設計實時熒光定量PCR擴增特異性引物(表1),以β-actin基因為內參基因,以暫養黑鯛幼魚肝臟、腎臟、心臟、腦、眼、鰓、鰭條、脾臟、皮膚、腸道、性腺和白肌等12個組織的cDNA為模板進行PRL基因組織表達特征分析,在LightCycler 96實時熒光定量PCR儀進行檢測。在鹽脅迫試驗中,選擇鹽脅迫第0、4、8、12、24、48和72 h的鰓組織cDNA進行PRL基因表達水平分析。所有樣品cDNA稀釋至100 ng/μL作為實時熒光定量PCR的模板,實時熒光定量PCR反應體系12.5 μL:cDNA模板1.0 μL,ChamQ SYBR qPCR Master Mix 6.5 μL,上、下游引物各0.5 μL,ddH2O補足至12.5 μL。擴增程序:95 ℃預變性30 s;95 ℃ 15 s,55 ℃ 15 s,進行40個循環。每個樣品設3次生物學重復。采用2–△△CT法換算黑鯛PRL基因相對表達量(Livak and Schmittgen,2001),并以SPSS 19.0的單因素方差分析(One-way AMOVA)檢測其差異顯著性。
2 結果與分析
2. 1 黑鯛PRL基因序列特征分析結果
黑鯛PRL1基因開放閱讀框(ORF)全長639 bp,共編碼212個氨基酸殘基,編碼蛋白分子量為23.32 kD,pI為6.70;黑鯛PRL2基因ORF全長750 bp,共編碼249個氨基酸殘基,編碼蛋白分子量為28.31 kD,pI為8.37。ExPASy預測結果顯示,黑鯛PRL1和PRL2蛋白均由2個結構域(圖1)組成,即1個信號肽結構域和1個Hormone 1結構域。
黑鯛PRL1基因在基因組上的全長為2678 bp,含有5個外顯子和4個內含子。黑鯛PRL2基因在基因組上的全長為3211 bp,含有4個外顯子和3個內含子(圖2)。此外,PRL1基因中各物種的外顯子和內含子數目較保守;在PRL2基因方面,黑鯛PRL2基因和青鳉PRL2基因均包含4個外顯子和3個內含子,而大黃魚(Larimichthys crocea)、河豚(Takifugu rubripes)和斑馬魚(Danio rerio)PRL2基因包含5個外顯子和4個內含子(表2)。
2. 2 黑鯛PRL基因同源比對分析結果
利用ClustalX 2.1進行PRL1和PRL2氨基酸序列比對分析,結果表明,黑鯛PRL1氨基酸序列與黃鰭鯛(A. latus)PRL1氨基酸序列的相似性最高,達99.1%;其次是與金頭鯛(Sparus aurata),二者的PRL1氨基酸序列相似性為93.4%;與小鼠(Mus musculus)及人類(Homo sapiens)等外源物種的PRL氨基酸序列相似性較低,分別為33.2%和35.0%(表3)。同樣,黑鯛PRL2氨基酸序列與黃鰭鯛PRL2氨基酸序列的相似性也最高,為98.6%;與金頭鯛PRL2氨基酸序列的相似性為96.0%;與小鼠、雞(Gallus gallus)及人類等外源物種的PRL氨基酸序列相似性較低,分別為32.9%、31.6%和28.9%(表4)。
基于PRL氨基酸序列相似性構建的系統發育進化樹(圖3)顯示,黑鯛PRL1氨基酸序列與黃鰭鯛PRL1氨基酸序列先聚為一支,再與鄰近鱸形目的金頭鯛、平鯛(Rhabdosargus sarba)及真鯛(Pagrus major)等魚類的PRL1氨基酸序列聚在一起,最后與斜帶石斑魚(Epinephelus coioides)、大黃魚、花鱸(Lateolabrax japonicus)等硬骨魚類的PRL1氨基酸序列聚為一支;黑鯛PRL2氨基酸序列則與黃鰭鯛PRL2氨基酸序列先聚為一支,再與金頭鯛、高體鰤(Seriola dumerili)、海參斑(Cyclopterus lumpus)、蔭平鲉(Sebastes umbrosus)等魚類的PRL2氨基酸序列聚在一起,最后與龍膽石斑魚(E. lanceolatus)PRL2氨基酸序列聚為一支;人類和小鼠的PRL氨基酸序列先聚在一起,再與雞PRL氨基酸序列聚為一支。
2. 3 黑鯛PRL蛋白結構及其糖基化和磷酸化位點預測結果
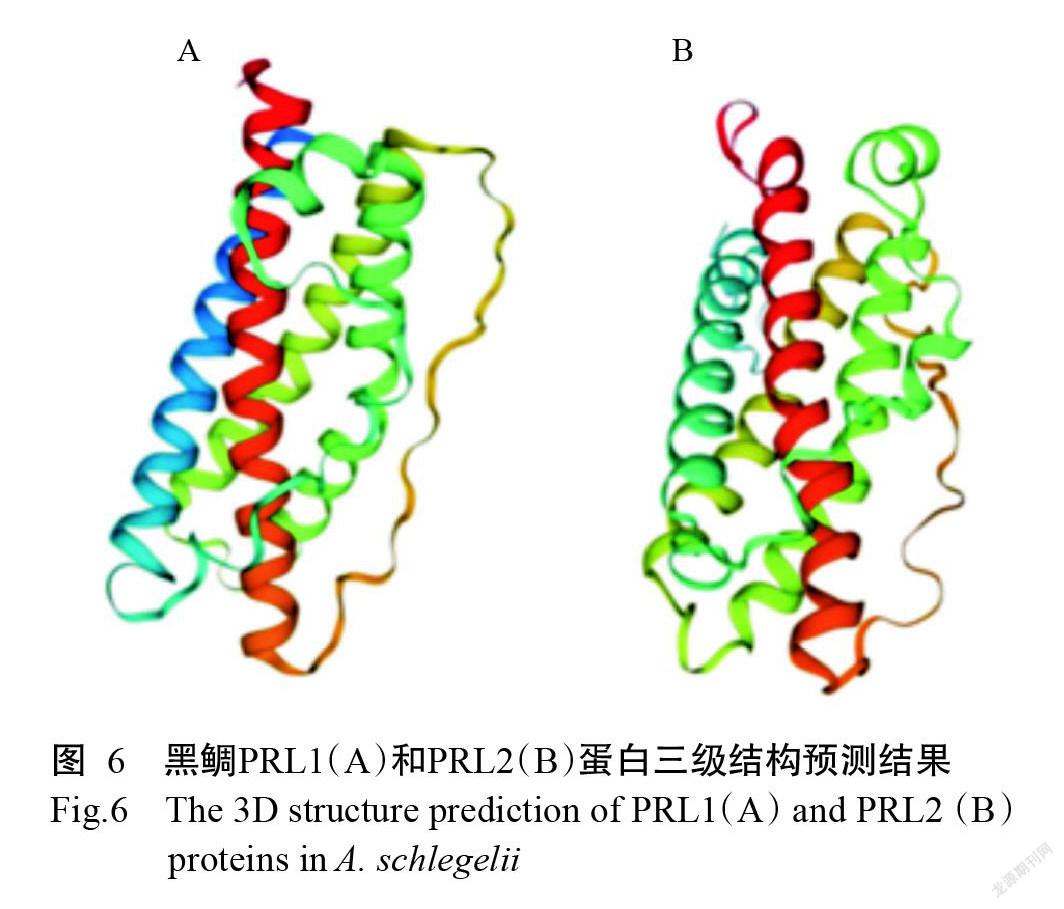
在黑鯛PRL1蛋白二級結構中α-螺旋占69.34%、無規則卷曲占30.66%;NetNGlyc預測結果(圖4)表明,黑鯛PRL1氨基酸序列中包含1個糖基化位點及37個磷酸化位點,37個磷酸化位點中包括:13個細胞周期蛋白依賴性激酶2(cdc2)位點、10個蛋白激酶C(PKC)位點、5個DNA依賴蛋白激酶(DNAPK)位點、4個蛋白激酶A(PKA)位點、1個酪蛋白激酶2(CKII)位點、1個核糖體蛋白激酶(RSK)位點、1個細胞周期依賴蛋白激酶5(cdk5)位點、1個絲氨酸/蘇氨酸激酶(ATM)位點和1個細胞分裂素活化蛋白激酶(p38MAPK)位點。在黑鯛PRL2蛋白二級結構中α-螺旋占67.07%、無規則卷曲占32.93%;NetNGlyc預測結果(圖5)表明,黑鯛PRL1氨基酸序列中包含1個糖基化位點及21個磷酸化位點,21個磷酸化位點中包括:6個蛋白激酶C(PKC)位點、6個蛋白激酶A(PKA)位點、2個酪蛋白激酶2(CKII)位點、2個核糖體蛋白激酶(RSK)位點、1個細胞周期蛋白依賴性激酶2(cdc2)位點、1個DNA依賴蛋白激酶(DNAPK)位點、1個細胞周期依賴蛋白激酶5(cdk5)位點、1個絲氨酸/蘇氨酸激酶(ATM)位點和1個細胞分裂素活化蛋白激酶(p38MAPK)位點。黑鯛PRL1和PRL2蛋白三級結構預測結果顯示,二者均具有由4個長α-螺旋組成的反式平行排列特征(圖6)。
2. 4 黑鯛PRL基因組織表達分析結果
采用實時熒光定量PCR檢測黑鯛PRL1和PRL2基因在不同組織中的表達情況,結果顯示黑鯛PRL1和PRL2基因在12個待檢測組織中均有表達。其中,黑鯛PRL1基因在腦組織中的相對表達量最高,顯著高于其他組織中的相對表達量(P<0.05,下同),其次是性腺和鰓組織,在心臟中的相對表達量最低(圖7-A);黑鯛PRL2基因在不同中組織中的表達水平與黑鯛PRL1基因基本一致,以腦組織中的相對表達量最高,其次是性腺和鰓組織,而在鰭條中的相對表達量最低(圖7-B)。
在鹽脅迫試驗中,選取不同鹽脅迫處理的黑鯛幼魚鰓組織探究PRL1和PRL2基因的表達情況。實時熒光定量PCR檢測結果(圖8)表明,在對照組中,黑鯛PRL1和PRL2基因的相對表達量不會隨著時間推移而顯著變化。在鹽度5‰處理組中,黑鯛PRL1基因在脅迫4 h開始顯著上調,至脅迫24 h是達峰值,隨后開始緩慢下降,至脅迫72 h時其相對表達量仍顯著高于對照組;黑鯛PRL2基因則在脅迫8 h開始極顯著上調(P<0.01),至脅迫24 h時達峰值,隨后開始緩慢下降,至脅迫72 h時其相對表達量仍顯著高于對照組。在鹽度25‰處理組中,黑鯛PRL1基因在脅迫72 h時的相對表達量顯著下調,黑鯛PRL2基因則在脅迫48 h時開始顯著下調,至脅迫72 h時其相對表達量仍顯著低于對照組。在鹽度35‰處理組中,黑鯛PRL1基因在脅迫72 h時其相對表達量顯著下調,黑鯛PRL2基因則在脅迫48 h時開始顯著下調,至脅迫72 h時其相對表達量仍顯著低于對照組。
綜上所述,低鹽脅迫能顯著促進黑鯛PRL1和PRL2基因的表達,且從早期脅迫即開始產生顯著影響,一直持續到脅迫結束;高鹽脅迫則抑制黑鯛PRL1和PRL2基因的表達,但其抑制效果在脅迫后期才開始體現。可見,PRL1和PRL2基因在黑鯛調節滲透壓及離子平衡過程中發揮重要作用。
3 討論
PRL是一種單鏈多肽類激素,由動物腦垂體合成及分泌,廣泛參與機體的各種生物學功能,在魚類研究中認為PRL是調節硬骨魚類滲透壓和離子平衡的主要激素(陳松林等,1996;Manzon,2002)。本研究克隆獲得黑鯛PRL1和PRL2基因,其中,黑鯛PRL1基因編碼212個氨基酸殘基,黑鯛PRL2基因編碼249個氨基酸殘基。黑鯛PRL蛋白結構域預測結果顯示,PRL1和PRL2蛋白均由1個信號肽結構域和1個Hormone 1結構域組成。目前,已知大多數物種的PRL蛋白均由200多個氨基酸組成,其信號肽約包含20個氨基酸,C端緊接鄰1個Hormone 1結構域。其中,人類PRL蛋白全長包含227個氨基酸,其信號肽由28個氨基酸組成;鼠PRL蛋白全長包含226個氨基酸,其信號肽由21個氨基酸組成;雞PRL蛋白全長包含229個氨基酸,其信號肽由23個氨基酸。可見,黑鯛PRL1和PRL2蛋白氨基酸序列長度及相關結構域長度與大多數物種相似。
黑鯛PRL1和PRL2蛋白二級結構預測結果表明,在黑鯛PRL1和PRL2蛋白二級結構約有70.00%的氨基酸序列以α-螺旋形式結構存在,剩氨基酸余序列則呈無規則卷曲。黑鯛PRL1和PRL2氨基酸序列中均只含有1個糖基化位點,但包含多個磷酸化位點,在黑鯛PRL1氨基酸序列中以cdc2位點最多(13個),而黑鯛PRL2氨基酸序列中以PKC位點最多(6個),暗示二者在翻譯后修飾過程中受到的激酶調控模式存在差異。黑鯛PRL1和PRL2蛋白三級結構均具有由4個長α-螺旋組成的反式平行排列特征,與在人類中的研究結果(Maus et al.,1999)相似,提示PRL在低等脊椎動物和高等脊椎動物中均以相似的結構域來發揮蛋白功能。
早期針對魚類PRL基因的研究主要集中在垂體和性腺等組織中,隨著生物技術的發展,利用RT-PCR在越來越多的魚類垂體和性腺以外的其他組織中陸續檢測到PRL基因表達。Santos等(1999)在海鯛的垂體、鰓、腸道、肝臟、卵巢和精巢中均檢測到PRL基因表達;Imaoka等(2000)研究發現PRL基因在金魚的腦、性腺、皮膚、肌肉、肝臟、脾臟和腎臟中均有表達;Zhang等(2004)在斜帶石斑魚中同樣發現PRL基因在腦、垂體、性腺、鰓、肝臟、脾臟和腎臟中均有表達,但在腎臟和肝臟等組織中的相對表達量較低。本研究以實時熒光定量PCR分析黑鯛PRL1和PRL2基因在不同組織中的表達情況,結果顯示,黑鯛PRL1和PRL2基因在12個待檢測的組織中均有表達。其中,黑鯛PRL1基因在腦組織中的相對表達量最高,其次是性腺和鰓組織,在心臟中的相對表達量最低;黑鯛PRL2基因在不同中組織的表達水平與黑鯛PRL1基因基本一致,同樣以腦組織中的相對表達量最高,其次是性腺和鰓組織,而在鰭條中的相對表達量最低。表明黑鯛PRL基因同其他魚類一樣,具有廣泛表達性,且以腦組織、性腺及鰓組織中的表達量較高。
在鹽脅迫試驗中,選取不同鹽脅迫處理的黑鯛幼魚鰓組織探究PRL1和PRL2基因的表達情況,結果表明,低鹽脅迫能顯著促進黑鯛PRL1和PRL2基因的表達,且從早期脅迫即開始產生顯著影響,并一直持續到脅迫結束;高鹽脅迫則抑制黑鯛PRL1和PRL2基因的表達,但其抑制效果在脅迫后期才開始體現。前人的相關研究也發現,黑鯛在適應淡水環境時其PRL基因參與調節體內Na+、Cl?及Ca+等離子的平衡,從而提高魚體適應淡水環境過程的滲透調節能力(Chang et al.,2007)。PRL基因在廣鹽性硬骨魚類適應淡水環境的過程中發揮重要作用,其表達水平在垂體和血清中均呈上調趨勢,導致鰓、腎臟、腸道、皮膚和膀胱等滲透調節器官的滲透性和離子運輸機制發生改變,從而減少魚體對水分的攝入或增加對離子的吸收,最終起到調節滲透壓平衡的效果。
4 結論
低鹽脅迫能促進黑鯛PRL1和PRL2基因的表達,高鹽脅迫則抑制黑鯛PRL1和PRL2基因的表達,即黑鯛PRL1和PRL2基因在其適應淡水環境的過程中發揮重要調節作用。
參考文獻:
陳松林,陳細華,鄧文濤,夏盛芹. 1996. 草魚催乳素抗血清的制備與鑒定[J]. 動物學雜志,31(5):35-37. [Chen S L,Chen X H,Deng W T,Xia S Q. 1996. Preparation and identification of antibody against grass carp prolactin[J]. Chinese Journal of Zoology,31(5):35-37.]
鄧惠文,劉峰,李桂豪,包衛洋,鄒松保,鄭鵬飛,龔駿,孫汝江. 2019. 黑鯛(Acanthopagrus schlegelii)腸道細菌群落對飼料中添加不同羽毛粉的響應[J]. 海洋與湖泊,50(6):1309-1317. [Deng H W,Liu F,Li G H,Bao W Y,Zou S B,Zheng P F,Gong J,Sun R J. 2019. Response of gut bacterial community in black sea bream to diffe-rent feather meal in feed[J]. Oceanologia et Limnologia Sinica,50(6):1309-1317.] doi:10.11693/hyhz2019040 0072.
鄧利,張為民,林浩然. 2003. 鹽度變化對黑鯛生長激素及其受體的影響[J]. 熱帶海洋學報,22(6):9-14. [Deng L,Zhang W M,Lin H R. 2003. Impacts of salinity on growth hormone and its receptor of blank seabream sparus macrocephalus[J]. Journal of Tropocal Oceanography,22(6):9-14.] doi:10.3969/j.issn.1009-5470.2003.06.002.
賈超峰,祝斐,孟乾,孫瑞鍵,劉海林,張志偉,陳淑吟,徐津,張志勇. 2020. 低鹽養殖對黑鯛營養成分的影響[J]. 食品工業科技,41(1):284-288. [Jia C F,Zhu F,Meng Q,Sun R J,Liu H L,Zhang Z W,Chen S Y,Xu J,Zhang Z Y. 2020. Effect of low-salinity water cultivation on nutrient components of black porgy(Acanthopagrus schle-gelii)[J]. Science and Technology of Food Industry,41(1):284-288.] doi:10.13386/j.issn1002-0306.2020.01.046.
林李泉,劉明珠,林國榮,黃帥帥,李夢夢,童桂香. 2021. 黑鯛NKCC1分子特征及其對急性鹽度脅迫的表達響應[J]. 廣西科學院學報,37(2):133-143. [Lin L Q,Liu M Z,Lin G R,Huang S S,Li M M,Tong G X. 2021. Molecular characteristics of NKCC1 in black sea bream Acanthopagrus schlegelii and its expression in response to acute salinity stress[J]. Journal of Guangxi Academy of Sciences,37(2):133-143.] doi:10.13657/j.cnki.gxkxyxb. 20210806.005.
劉瑞鑫,韋玲靜,董博,莫柳忠,蔣欽楊. 2013. 娟姍牛催乳素基因型與產奶量的關聯性分析[J]. 南方農業學報,44(11):1904-1908. [Liu R X,Wei L J,Dong B,Mo L Z,Jiang Q Y. 2013. Relation analysis of prolactin genotypes and milk yield of Jersey cow[J]. Journal of Southern Agriculture,44(11):1904-1908.] doi:10.3969/j:issn.2095-1191.2013.11.1904.
王裕玉,徐跑,張志偉,張志勇,聶志娟,吳建平,曾海峰,徐鋼春. 2020. 不同養殖模式對黑鯛生長、血清生化指標及抗氧化性能的影響[J]. 江蘇農業科學,48(23):155-160. [Wang Y Y,Xu P,Zhang Z W,Zhang Z Y,Nie Z J,Wu J P,Zeng H F,Xu G C. 2020. Effect of different culture modes on the growth,serum biochemical indexes and antioxidant performance of Acanthopagrus schlegelii[J]. Jiangsu Agricultural Sciences,48(23):155-160.] doi:10. 15889/j.issn.1002-1302.2020.23.031.
魏渲輝,汝少國,徐路,Isoda H. 2001. 海水和淡水適應過程中廣鹽性魚類鰓氯細胞的形態與功能變化及其激素調節[J]. 海洋科學,25(4):16-20. [Wei X H,Ru S G,Xu L,Isoda H. 2001. Structural and functional changes of euryhaline fish branchial chloride cell and hormonal regulation during seawater and freshwater adaptation[J]. Marine Science,25(4):16-20.] doi:10.3969/j.issn.1000-3096.2001. 04.006.
左映平,曹勁松. 2007. 魚類體內催乳素的滲透調節作用[J]. 生命的化學,27(5):455-457. [Zuo Y P,Cao J S. 2007. The role of prolactin in fish[J]. Chemistry of Life,27(5):455-457.] doi:10.3969/j.issn.1000-1336.2007.05.032.
An K W,Kim N N,Choi C Y. 2008. Cloning and expression of aquaporin 1 and arginine vasotocin receptor mRNA from the black porgy,Acanthopagrus schlegeli:Effect of freshwater acclimation[J]. Fish Physiology and Bioche-mistry,34:185-194. doi:10.1007/s10695-007-9175-0.
An K W,Kim N N,Shin H S,Kil G S,Choia C Y. 2010. Profiles of antioxidant gene expression and physiological changes by thermal and hypoosmotic stresses in black porgy(Acanthopagrus schlegeli)[J]. Comparative Biochemistry and Physiology. Part A:Molecular & Integrative Phy-siology,156(2):262-268. doi:10.1016/j.cbpa.2010.02.013.
Breves J P,Seale A P,Helms R E,Tipsmark C K,Hirano T,Grau E G. 2011. Dynamic gene expression of GH/PRL-family hormone receptors in gill and kidney during freshwater-acclimation of Mozambique tilapia[J]. Comparative Biochemistry and Physiology. Part A:Molecular & Integrative Physiology,158(2):194-200. doi:10.1016/j.cbpa. 2010.10.030.
Breves J P,Serizier S B,Goffin V,McCormick S D,Karlstrom R O. 2013. Prolactin regulates transcription of the ion uptake Na+/Cl- cotransporter(ncc) gene in zebrafish gill[J]. Molecular and Cellular Endocrinology,369(1-2):98-106. doi:10.1016/j.mce.2013.01.021.
Chang Y J,Min B H,Choi C Y. 2007. Black porgy(Acanthopagrus schlegeli) prolactin cDNA sequence:mRNA expression and blood physiological responses during freshwater acclimation[J]. Comparative Biochemistry and Physiology. Part B:Biochemistry and Molecular Biology,147(1):122-128. doi:10.1016/j.cbpb.2007.01.006.
Cunha A A P,Partridge C G,Knapp R,Neff B D. 2019. Androgen and prolactin manipulation induces changes in aggressive and nurturing behavior in a fish with male parental care[J]. Hormones and Behavior,116:104582. doi:10. 1016/j.yhbeh.2019.104582.
Hu Q Y,Qin Q B,Xu S H,Zhou L L,Xia C H,Shi X T,Zhang H Y,Jia J Y,Ye C,Yin Z,Hu G F. 2020. Pituitary actions of EGF on gonadotropins,growth hormone,prolactin and somatolactins in grass carp[J]. Biology(Basel),9(9):279. doi:10.3390/biology9090279.
Imaoka T,Matsuda M,Mori T. 2000. Extrapituitary expression of the prolactin gene in the goldfish,African clawed frog and mouse[J]. Zoological Science,17(6):791-796. doi:10.2108/zsj.17.791.
Kelly P A,Binart N,Lucas B,Bouchard B,Goffin V. 2001. Implications of multiple phenotypes observed in prolactin receptor knockout mice[J]. Frontiers in Neuroendocrinlogy,22(2):140-145. doi:10.1006/frne.2001.0212.
Livak K J,Schmittgen T D. 2001. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method[J]. Methods,25(4):402-408. doi:10.1006/meth.2001.1262.
Manzon L A. 2002. The role of prolactin in fish osmoregulation:A review[J]. General and Comparative Endocrinology,125(2):291-310. doi:10.1006/gcen.2001.7746.
Maus M V,Reilly S C,Clevenger C V. 1999. Prolactin as a chemoattractant for human breast carcinoma[J]. Endocrinology,140(11):5447-5450. doi:10.1210/endo.140.11.7245.
Min B H,Park M S,Myeong J I,Seo J S,Park J J,Noh G E,Kang D Y. 2015. Gill Na+/K+-ATPase activity and expression in black sea bream Acanthopagrus schlegelii exposed to a hyposaline environment[J]. Korean Journal of Fisheries and Aquatic Sciences,48(1):64-70. doi:10.5657/ KFAS.2015.0064.
Santos C R A,Brinca L,Lagleton P M,Power D W. 1999. Cloning,expression,and tissue localization of prolactin in adult sea bream(Spares antata)[J]. General and Comparative Endocrinology,114(1):57-66. doi:10.1006/gcen. 1998.7228.
Si Y F,Li H,Gong X L,Bao B L. 2021. Isolation of prolactin gene and its differential expression during metamorphosis involving eye migration of Japanese flounder Paralichthys olivaceus[J]. Gene,780:145522. doi:10.1016/J.GENE.2021.145522.
Takashi Y,Nobuto F,Michihisa A,Katsumi T. 2019. Changes in PRL gene expression during upstream movement of the Japanese eel,Anguilla japonica[J]. Zoological Scien-ce,36(6):521-527. doi:10.2108/zs190012.
Tomy S,Chang Y M,Chen Y H,Cao J C,Wang T P,Chang C F. 2009. Salinity effects on the expression of osmoregulatory genes in the euryhaline black porgy Acanthopagrus schlegeli[J]. General and Comparative Endocrinology,161(1):123-132. doi:10.1016/j.ygcen.2008.12.003.
Villalba M,Gómez G,Torres L,Maldonado N,Espi?eira C,Payne G,Vargas-Chacoff L,Figueroa J,Yá?ez A,Ola-varría V H. 2020. Prolactin peptide (pPRL) induces anti-prolactin antibodies,ROS and cortisol but suppresses specific immune responses in rainbow trout[J]. Molecular Immunology,127:87-94. doi:10.1016/j.molimm.2020.08.020.
Yang B Y,Greene M,Chen T T. 1999. Early embryonic expression of the growth hormone family protein genes in the developing rainbow trout,Oncorhynchus mykiss[J]. Molecular Reproduction and Development,53(2):127-134. doi:10.1002/(SICI)1098-2795(199906)53:2<127::AID-MRD1>3.0.CO;2-H.
Zhang W M,Tian J,Zhang L H,Zhang Y,Li X,Lin H R. 2004. cDNA sequence and spatio-temporal expression of prolactin in the orange-spotted grouper,Epinephelus coioi-des[J]. General and Comparative Endocrinology,136(1):134-142. doi:10.1016/j.ygcen.2003.12.001.
(責任編輯 蘭宗寶)

