肝細胞癌影像診斷的“術”與“道”
——影像技術與病理特征
魏毅,葉錚,蔣涵羽,曲亞莉,張韻,陳婕,魏鴻,姚杉,宋彬
原發性肝癌是全球第六常見惡性腫瘤和排名第三的腫瘤致死病因,其中又以肝細胞癌(hepatocelluar carcinoma,HCC)多見,約占85%~90%[1]。HCC是目前唯一無需術前病理證實、僅依靠流行病史和典型影像征象即可確診的實體腫瘤[2]。然而,對于部分極早期和早期HCC,往往因缺乏典型的影像征象而致病灶的漏診;另一方面,對于部分進展期HCC,可出現與其它肝臟腫瘤易于混淆的影像表現,而致病灶的誤診。
時空異質性是不典型HCC影像學表現的微觀病理學基礎,其主要表現為同一病灶內的不同部位往往具有不同基因組和免疫微環境改變,從而表現出不同的病理學行為特征。基于病理特征的功能影像技術為全方位評估HCC的病理特征提供了可能,不僅可反映腫瘤新生血管生成、腫瘤細胞密度和結構改變,還可反映腫瘤細胞膜的功能、組織代謝和生理狀態改變等,為聚焦微觀病理特征改變的影像診斷打下基礎。
微觀病理特征改變是HCC不同影像征象的基礎。HCC的診斷不應僅局限于典型的影像學征象,其診斷標準更應圍繞反映腫瘤發生、發展過程中不同病理特征改變的影像征象,多維度、全方位地挖掘肝細胞癌異質性的“影像-病理”特征,從而真正實現HCC的個體化精準診療。基于此,本文擬結合肝硬化結節多步癌變的多層次病理特征,復習歸納相關功能影像技術進展和HCC診斷新標準,以期加深對影像成像的“術”和所反映的病理層面的“道”的認識和理解。
影像征象的組織病理改變基礎
1.肝細胞癌的新生血管生成
肝硬化結節進展為HCC是一個多步驟癌變過程,由再生結節(regenerative nodule,RN)、低級不典型增生結節(low-grade dysplastic nodule,LGDN)、高級不典型增生結節(high-grade dysplastic nodule,HGDN)逐漸演變為HCC,在這一過程中其血供可發生顯著改變(圖1)[3]。隨著腫瘤新生血管生成、血管內皮細胞通透性增加,門靜脈供血逐漸減少,異常動脈供血逐步增加并成為主導[3]。多期動態增強掃描可反映腫瘤的新生血管生成和血供改變情況:由于病灶內新生腫瘤血管生成使得腫瘤動脈血流灌注增加,因此在增強掃描動脈期HCC相對于鄰近肝實質常表現為明顯強化;但在門脈期和延遲期,由于門靜脈供血減少,相較于強化的正常肝臟實質,HCC病灶常表現為低強化,此為HCC典型征象“快進快出”的病理基礎。
然而,在極早期及部分早期HCC病灶中,新生血管尚未完全形成;而在部分進展期HCC中,則可因無氧糖酵解致腫瘤新生血管的形成過程停止。因此,上述原因可導致部分HCC缺乏典型的強化特征。腫瘤新生血管的定量評估對此類缺乏典型征象HCC的診斷和生物學行為評估至關重要。CT和MRI多期灌注成像技術可通過血流動力學模型定量評估組織的血流灌注、血管通透性和血管外-細胞外間隙的情況,直接反映腫瘤的新生血管生成和新生腫瘤血管面積等。此外,多期灌注成像參數亦可反映如CD31、微血管密度(microvessel density,MVD)和血管包埋腫瘤簇(vessels encapsulating tumor clusters,VETC)等表達情況,有助于探明腫瘤新生血管生成的相關特征改變,并輔助HCC療效評估及預后判定[4-6]。
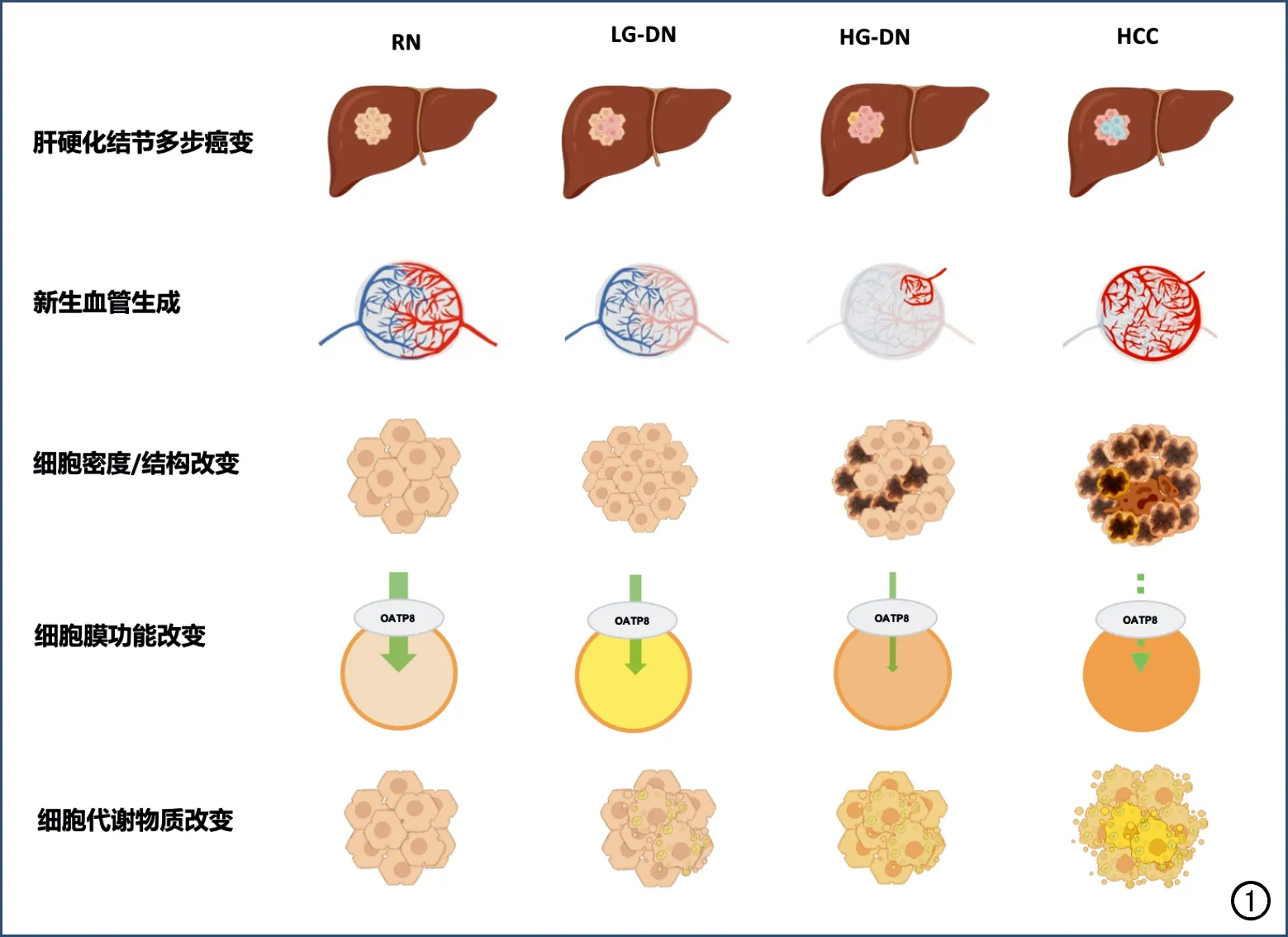
圖1 肝硬化結節多步驟癌變過程中主要病理特征改變[3]。
2.腫瘤細胞結構和細胞密度改變
在肝硬化結節多步癌變過程中,腫瘤細胞在增殖過程中逐步發生異型分化和分裂,其細胞形態、結構和密度常隨之發生顯著改變。癌前結節中腫瘤細胞核可正常或輕度異型,細胞核/細胞漿比值正常或稍高;早期HCC分化良好,癌細胞體積小,排列成細梁狀;晚期HCC分化差,細胞核濃染,細胞形狀不規則,排列松散,細胞密度可達周圍肝實質的兩倍及以上。
擴散加權成像(diffusion weighted imaging,DWI)主要反映細胞外水分子的擴散受限程度,當細胞形態(細胞異型化)、結構(細胞核腫大、深染)和細胞密度(細胞分裂加快)發生改變時,細胞外水分子表現為擴散受限,即病灶在DWI圖像上呈高信號。研究顯示,DWI受限診斷HCC的敏感度為93.07%~98.93%,特異度為43.96%~64.93%[7]。此外,基于DWI不同模型可對腫瘤的細胞密度、細胞結構和細胞外間隙進行準確評估,從而間接反映腫瘤的病理分級、微血管侵犯、腫瘤內淋巴細胞浸潤和腫瘤侵襲性等生物學行為。
3.肝臟細胞膜功能改變
肝臟細胞的種類多樣、功能復雜,細胞膜上有多種信號通路和受體,這為特異性對比劑在肝臟成像方面的應用提供了基礎。目前廣泛應用的肝臟特異性對比劑釓塞酸二鈉(gadoxetate disodium,Gd-EOB-DTPA),不僅具有如其它細胞外對比劑縮短T1弛豫時間的動態增強效果,更重要的是,對于正常功能的肝細胞,約有50%的對比劑可被細胞膜表面的有機陰離子轉運多肽(orga-nic anion transporting polypeptide,OATP)攝取而進入肝細胞內,再以多耐藥相關蛋白(multi-drug resistance protein,MRP)為載體由膽道系統排泄。但是,對于腫瘤細胞其細胞膜功能異常或缺失,無法通過細胞膜受體攝取造影劑,在肝膽期(hepatobiliary phase,HBP)相對背景肝實質而表現為低或稍低信號。有研究顯示,HBP低信號診斷HCC的敏感度達94.65%~99.64%,特異度為54.36%~74.35%[7]。對于肝臟病灶的診斷,肝膽期掃描的真正價值在于對再生結節、高度不典型增生結節和早期HCC的鑒別,對于肝膽期呈低信號的高危結節,2年內進展為HCC的概率為85%,故此征象常可用于早期高危肝結節的篩查。此外,基于肝膽特異性對比劑的對比增強掃描還可對腫瘤的生物學行為、Wnt/β-catenin 通路及HCC早期復發和預后預測等進行評估,提高對HCC全程的管理水平。
4.肝臟代謝物質的改變
肝臟是人體最重要的物質代謝器官,在HCC的發生和發展過程中常伴隨著代謝物質的改變,如脂肪代謝、鐵代謝等,故可通過定量影像手段進行精準評估。腫瘤細胞內無氧糖酵解增加、腫瘤內乏氧,可進一步導致脂代謝異常、致脂肪變性和腫瘤內脂粒沉積。故高危結節內出現脂肪相關影像征象,可提高HCC診斷的特異度。質子密度脂肪分數(proton density fat fraction,PDFF)的定量測量是基于人體組織內脂肪質子比水質子進動頻率慢3.5 ppm的化學位移現象,運用水脂分離技術,能夠定量分析肝臟的脂肪含量,且具有無創、準確和可重復性高等優勢,有望取代目前的金標準即病理活檢[8-9]。另一方面,肝臟是人體最大且最重要的貯鐵器官,多種病因可引起鐵過載,致肝細胞損害和肝功能異常,進而促使肝纖維化、肝硬化及HCC的發生、發展[10-11]。鐵具有順磁性,可增加馳豫率,縮短馳豫時間、尤其是T2弛豫時間。可以利用T2*-mapping技術、磁敏感加權成像技術或定量磁化率圖技術測得的T2*和R2*等定量參數值的變化來反映肝臟鐵代謝情況。

圖2 HCC患者,男,43歲。a)T1WI示肝右后上段內有一圓形結節呈低信號(箭);b)T2WI示結節呈高信號(箭);c)DWI示結節呈明顯高信號(箭);d)ADC圖示結節呈低信號(箭);e)增強后動脈晚期示結節無明顯強化(箭);f)門脈期示結節信號低于周圍肝實質(箭);g)延遲期示結節信號稍低于周圍肝實質(箭);h)肝膽期示病灶呈低信號(箭)。基于傳統“快進快出”的診斷標準,本例的MRI表現不足以診斷為HCC,而采用“HBP低信號+DWI高信號”的診斷標準可診斷為HCC,術后病理證實該結節為中~低分化HCC。
肝細胞癌診斷標準的探討
1.各指南中的HCC診斷標準
目前常用的肝細胞癌診斷標準主要包括我國衛生健康委員會發布的原發性肝癌診療規范(2019年版)、美國放射學院提出的肝臟影像報告及數據系統(Liver Imaging Reporting and Data System,LI-RADS)、歐洲肝病研究學會提出的肝癌診療指南,其診斷流程中均將“快進快出”的強化方式作為診斷依據。相較于LI-RADS等西方指南更注重HCC診斷的特異度,亞太地區HCC的主要危險因素為病毒性肝炎,故診斷重點為提高HCC診斷的敏感度。2017版亞太肝臟研究學會指南中推薦Gd-EOB-DTP增強掃描作為HCC的一線檢查方法,在非典型“快進快出”強化方式的病灶中,HBP低信號可作為診斷HCC的重要依據[12]。
2.HCC影像診斷新標準
現有的HCC診療指南中,推薦將“快進快出”作為HCC的診斷標準。但對于部分不具有典型征象HCC,采用基于微觀病理改變的影像征象,對腫瘤的早期檢出、診斷則至關重要。近年來,隨著功能影像的不斷發展,一些基于微觀病理改變的功能影像診斷標準相繼提出。Choi等[13]采用動脈期高強化+肝膽期低信號作為新的診斷標準,對直徑小于2 cm HCC的診斷敏感度顯著高于歐洲肝病研究學會(European Association for the Study of Liver,EASL)制訂的診斷標準(83.0% vs. 74.5%,P=0.008),特異度與之相當(76.7% vs. 81.1%,P=0.125)。Kim等[14]將“廓清”征象延長至過渡期或肝膽期來診斷HCC,獲得了較高的敏感度[移行期(transitional phase,TP):90.9%;HBP:95.2%;門脈期(portal venous phase,PVP):75.3%],且特異度并未顯著降低(TP:82%;HBP:82%;PVP:94.1%)。Joo等[15]的研究中將“廓清”征象延長至肝膽期,診斷HCC的敏感度為93.8%,顯著高于僅將“廓清”征象定義至移行期(86.6%)和門脈期(70.9%)。新的診斷標準將“廓清”征象延伸至“TP低信號”和“HBP低信號”,可提高診斷HCC的敏感度。但相較于門脈期或延遲期的“廓清”,“HBP低信號”所揭示的“放射-病理”有本質差異,前者主要基于腫瘤的異常引流血管生成,本質上仍然反映的腫瘤的血供,而后者是由于HCC細胞的細胞膜表面OATP表達下降或缺失導致對比劑攝取減少或不攝取,主要反映的是功能的改變。
僅依靠“HBP低信號”征象亦不足以實現對HCC的最優診斷,尤其是對部分早期高分化HCC,可導致假陰性結果。DWI可反映細胞密度和結構改變,HBP低信號+擴散受限兩個征象的聯合應用,在保證HCC診斷特異度的同時,顯著提高了診斷的敏感度(圖2)。Song等[7]在一項前瞻性研究中發現, 聯合應用HBP低信號+DWI高信號作為新的診斷標準,診斷HCC的敏感度為92.57%~93.71%,特異度為74.44%~82.22%。Renzulli等[16]采用肝膽期低信號+動脈期高信號+擴散受限作為診斷標準,其診斷HCC的敏感度與美國肝病研究學會(American Association for the Study of Liver Diseases,AASLD)影像學標準(動脈期高強化+門脈期廓清)比較有顯著提高(96.0% vs. 76.4%,P<0.001),特異度則與之相當(91.8% vs. 98.6%,P=0.063)。此外,該診斷標準能夠準確鑒別早期HCC與HGDN,其診斷HGDN的敏感度和特異度分別高達94.7%和99.3%。
總結和展望
“術”是方法、“道”是準則。利用功能影像學成像技術對多種微觀病理改變進行精準量化和可視化分析,此為HCC影像評價的“術”;基于肝硬化高危結節多步癌變其真實微觀病理改變特征,為HCC高危人群篩查與監測、早期診斷、嚴重程度評價和臨床決策提供準確、穩定和可靠的依據,此為HCC影像評價的 “道”。建立和健全HCC的全程管理需要“術”與“道”相結合,方法與準則的統一,才能最終推動臨床實踐,使患者獲益。
展望未來,需持續聚焦于HCC發生、發展的關鍵病理過程,探索各種成像技術,尤其是基于腫瘤功能、代謝的影像新技術,多維度、全方位監測和反映HCC腫瘤異質性中的潛能和價值,建立基于“影像-病理”的HCC診斷體系。此外,應注重高階影像學量化方法的應用和推廣,更加積極地運用影像組學和人工智能等技術手段深入挖掘影像學信息,以構建穩定、高效和可靠的HCC智能分析影像平臺,為提升對HCC診斷效能、輔助臨床治療決策、改善患者生存預后及推動腫瘤個性化精準治療提供有力支撐。

