以輝銻礦為原料放電等離子燒結快速制備黝銅礦Cu12Sb4S13 及反應機理
李良,陳玉奇,朝倉貴一,平井伸治
(1.南陽師范學院機電工程學院,河南 南陽 473061;2.上海電機學院材料學院,上海201306;3.室蘭工業大學工學院,北海道 室蘭079-1100)
黝銅礦系Cu12Sb4S13 包含資源豐富的銅和環境友好的硫元素構成[1],同時具有金屬-半導體轉變[2]和良好的熱電性能[3-4]。這種礦物近些年來已經引起研究者的關注,作為潛在的磁性材料,光電薄膜材料和熱電材料[5]。
黝 銅 礦 系 Cu12+xSb4+yS13(0 ≤x ≤1.92,-0.02 ≤y ≤0.27)具有小范圍波動的化學組成[6]。而且Cu12Sb4S13的穩定性跟Cu-Sb-S 三元相圖中相變有關[7-8]。Cu12Sb4S13常用的制備方法是以元素粉[3,5,7,9-15],CuS, Cu2S and Sb2S4[16]或者CuS,Sb2S3and Cu[17]為原料,封管后高溫熔融再長時間熱處理制備。這種方法優點是純度高,但耗時長(熔融約3 d,熱處理2 周),能耗高[5]。為了縮短時間減少能耗,熱處理時間對Cu12Sb4S13熱電性能的影響已經被研究;同時一種快速高效的制備方法已經被提出[5,18]。如果采用放電等離子燒結技術,不需要長時間的熱處理。另一方面,天然黝銅礦系列的磺酸鹽礦物由于電阻值較高不能直接作為熱電材料原材料使用[19],但是可以作為制備Cu12Sb4S13熱電的“種子”促進Cu12Sb4S13合成[1-3,20]。
輝銻礦Sb2S3是冶煉金屬銻的重要礦物原料;資源豐富,價格低廉。本研究嘗試以輝銻礦Sb2S3為原材料制備Cu12Sb4S13。研究不同燒結程序工藝,燒結溫度和保溫時間,燒結塊的粉碎球磨,再燒結條件,原料配比波動等因素對Cu12Sb4S13制備的影響。分析Cu12Sb4S13微觀組織結構和成分分布。
1 實驗材料與方法
1.1 實驗過程
實驗原料包括CuS 粉末(純度99%,平均粒度150 μm),Cu 粉(純度99.99%;平均粒度1 μm)和輝銻礦粉。為了確定輝銻礦粉末中具體元素成分和含量,采用電感耦合等離子體質譜法(ICP-MS法)對輝銻礦粉末進行化學分析見表1。
通過對比輝銻礦粉和高純度Sb2S3粉末(純度99.99%,)的化學成分,證實輝銻礦主成分是Sb2S3,且含有較高的Fe 和As 含量。因為輝銻礦粉是通過赤銅礦直接分離制備的。
為了研究燒結程序工藝,燒結溫度和時間的影響,原材料按照Sb2S3: Cu : CuS = 2 : 5 : 7 的化學計量比進行稱料混合。為了確定Cu 和CuS 成分波動的影響,Cu12+xSb4S13(-0.15 ≤ x ≤0.05)和Cu12-ySb4S13-y (0 ≤y ≤0.5)按照摩爾計量比進行稱料。混合后的粉料被添加到內徑10.5 mm的石墨模具中進行放電等離子燒結。由于CuS 在220℃以上分解為Cu2S。為了確定CuS 分解對制備Cu12Sb4S13的影響,本研究采用一步式和兩步式(220℃保溫)兩種燒結程序。根據文獻[6,16]報道Cu12Sb4S13 的穩定區域隨著燒結溫度變化而變化,同時反應和熱處理溫度至少需要400℃,因此燒結溫度選定400 ~ 460℃。為了減少雜質相,先用手工或球磨機破碎和研磨初次燒結塊。球磨時間限定1 h。同時研究在球磨過程中乙醇對二次燒結的影響。
1.2 材料表征
采用X 射線衍射(XRD)在40 kV 和20 mA的單色Cu Kα 輻射下檢測燒結產物的相組成。合成的Cu12Sb4S13的形貌用掃描電子顯微鏡(SEM)進行了表征。
2 結果與分析
2.1 燒結溫度的影響
圖1 是燒結溫度對合成Cu12Sb4S13的影響。
從圖1 中可以看出,初次燒結可以合成高純Cu12Sb4S13,但是存在第二相(Cu12Sb4S13,CuS1.95)。同時,Cu12Sb4S13 所有特征峰強度隨溫度的升高有向低角度偏移的趨勢,表明晶格常數隨燒結溫度升高而增加。整體上二次燒結夠進一步減少中間相Cu3SbS3和殘留CuS。但二次燒結溫度對合成Cu12Sb4S13的影響較小。文獻[21]采用573 K 進行二次燒結減小第二相提高Cu12Sb4S13 純度。
2.2 燒結時間的影響
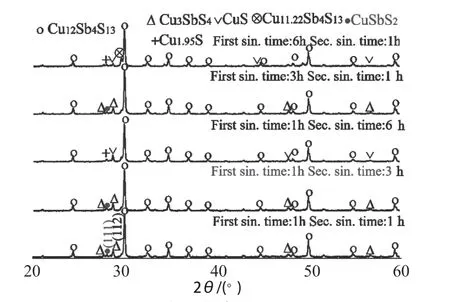
圖2 不同燒結時間合成Cu12Sb4S13 的XRDFig. 2 XRD pattern of synthesized Cu12Sb4S13 at different sintering time
圖2 是不同初次和二次燒結時間下合成Cu12Sb4S13的XRD。對于初次燒結1 ~ 6 h 的燒結產物主要是黝銅礦Cu12Sb4S13。第二相Cu3SbS4 和殘留相CuS的特征峰隨著燒結時間的延長而降低。在燒結時間延長到6 h 時出現富銅相Cu11.22Sb4S13的特征峰。與初次燒結相比,二次燒結后第二相Cu3SbS4和殘留相CuS 的特征峰明顯減弱。無論是初次燒結還是二次燒結,反應時間在小范圍內影響第二相Cu3SbS4 和殘留相CuS 的特征峰強度。本研究較短燒結時間1 h。
2.3 干磨和濕磨的差異
原料機械化球磨能夠提高分散均勻性,但是干法球磨不可避免存在團聚。初次燒結后球磨再球磨不僅能減少未反應的殘留相,還能增加晶界數量,有利于減小電阻率。
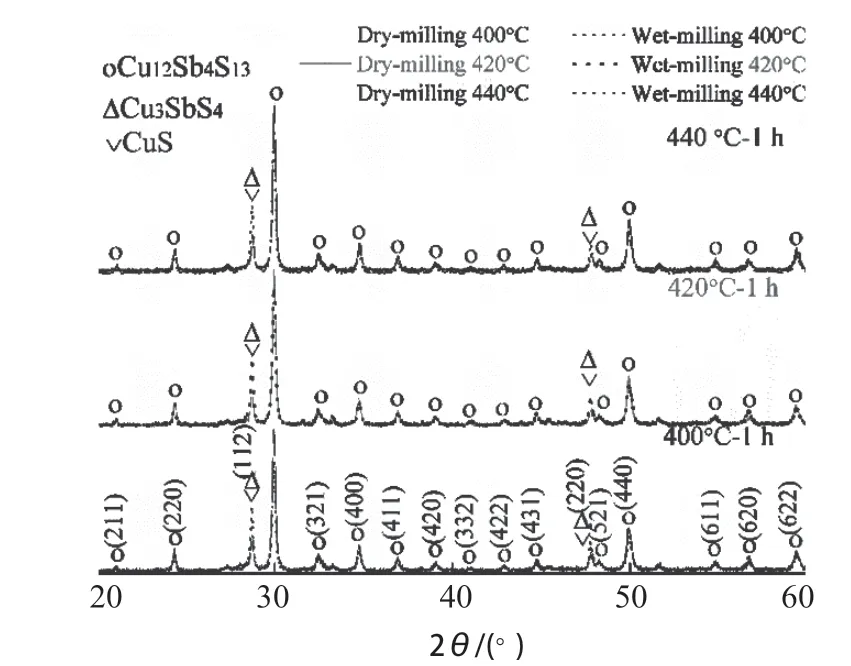
圖3 干法球磨和濕法球磨后二次燒結Cu12Sb4S13 的XRDFig. 3 XRD pattern of secondary synthesized Cu12Sb4S13 after dry milling and wet milling
圖3 是干法球磨和濕法球磨后再燒結Cu12Sb4S13的XRD 結果。濕法球磨的溶劑為無水乙醇。干磨的效果要好于濕磨。干磨碰撞更劇烈能夠將未反應的殘留相暴露出來,在二次燒結過程中參與反應。
2.4 微觀形貌分析
圖4是初次燒結Cu12Sb4S13的掃描電鏡和能譜分析(SEM-EDS)。

圖4 初次燒結的掃描電鏡和能譜分析(SEM-EDS)Fig. 4 SEM-EDS images of primary sintered
結合圖1 結果說明原料直接混合原位燒結Cu12Sb4S13是可行的,但是需要注意粉料團聚。整體上分析,初次燒結Cu12Sb4S13種存在中間相和團聚現象(約80 μm)。在團聚區域(圖4 a 中紅色圓圈),粉體在燒結過程中處于固體/半固體狀態,熱擴散速率較小,即使延長燒結時間也不能消除局部團聚。文獻[21]中初次燒結合成Cu12Sb4S13,延長燒結時間到120 h 也不能消除不純相。
另一方面,從Cu、Sb 的EDS 能譜分析結果可以看出,團聚區域的位置類似,且團聚區域的Cu 元素含量明顯偏高,同時Sb 元素含量明顯偏低。這種現象可以從兩方面解釋:(1)輝銻礦的主成分是Sb2S3,其常壓下理論熔點是550℃。在燒結壓力和微量雜質金屬元素的影響下輝銻礦的液化溫度有可能進一步降低。因此在400 ~ 460℃的燒結區間內Sb2S3的液化程度高,流動性好,不存在明顯的團聚;(2) 原料中Cu 的熔點較高(熔點1083.4±0.2℃),且粒徑較細(1 μm);CuS 的熔點220℃,但在220℃,CuS 發生分解生成高熔點Cu2S(α-Cu2S 熔點1130℃,β-Cu2S 熔點1100℃)。再結合S 元素的EDS 能譜結果,團聚區域的物相可能是未反應的Cu 或Cu2S(圖4a 中藍色圈和黃色圈)。

圖5 二次燒結的掃描電鏡Fig. 5 SEM images of secondary sintered
圖5是二次燒結Cu12Sb4S13的掃描電鏡結果。圖5a 中按照計量比稱料,Cu12Sb4S13存在明顯的顆粒和孔洞(圖5b 是局部放大結果),說明燒結反應是通過顆粒表面液化后粘結為整體,粉碎得到的顆粒形狀不規則,但是可以將未反應的團聚顆粒破碎并暴露出來。結合之前的研究,減少Cu 或CuS 含量可以促進Cu12Sb4S13 的合成。圖5c 是減少原料配比中Cu摩爾量Cu11.9Sb4S13的二次燒結結果。同時可以看出明顯的晶粒痕跡,說明二次燒結可以增加晶界數量。圖5d 是Cu11.9Sb4S13二次燒結后局部放大的結果。與圖5b 相比,孔洞含量明顯減少,致密性增加。圖5e 是減少CuS 的摩爾含量Cu11.9Sb4S12.9的微觀形貌。減少CuS 的摩爾含量同樣可以提高顆粒之間的結合。
2.5 反應機理分析
Cu-Sb-S 三元體系在300 ~ 500 ℃的相圖已經被報道[6-9,22]。CuSbS2(銅銻礦), Cu12Sb4S13(黝銅礦), Cu3SbS3(硫銻銅礦), and Cu3SbS4(法馬丁礦)四種化合物穩定存在。Cu3SbS3中硫含量最低,Cu3SbS4中硫含量最高,非計量比Cu12Sb4S13的硫含量介于二者之間[22]。可能發生的反應為:

本研究中按照最理想的反應方程式(1)進程稱量原料,但是混料不均勻和局部顆粒團聚導致原料配比的波動。反應方程式(2-4)導致雜質相(CuSbS2和Cu3SbS3/ Cu3SbS4)的生成(見圖2、3)。CuSbS3的生成和Cu 含量過高有關。四方結構的CuSbS3層狀薄膜可以通過CuS 和Sb3S3在400 ℃反應得到(如反應方程式2)[23]。
Cu3SbS3/Cu3SbS4 相的生成不僅跟燒結工藝有關還與硫磺蒸汽壓有關。因為CuS 的分解導致局部硫磺蒸汽壓較高。因此Cu3SbS4存在于燒結塊的內部。真空氣氛下燒結導致Cu3SbS3多存在于燒結塊表面。Cu3SbS4失硫后形成Cu12Sb4S13(如反應方程式9)。
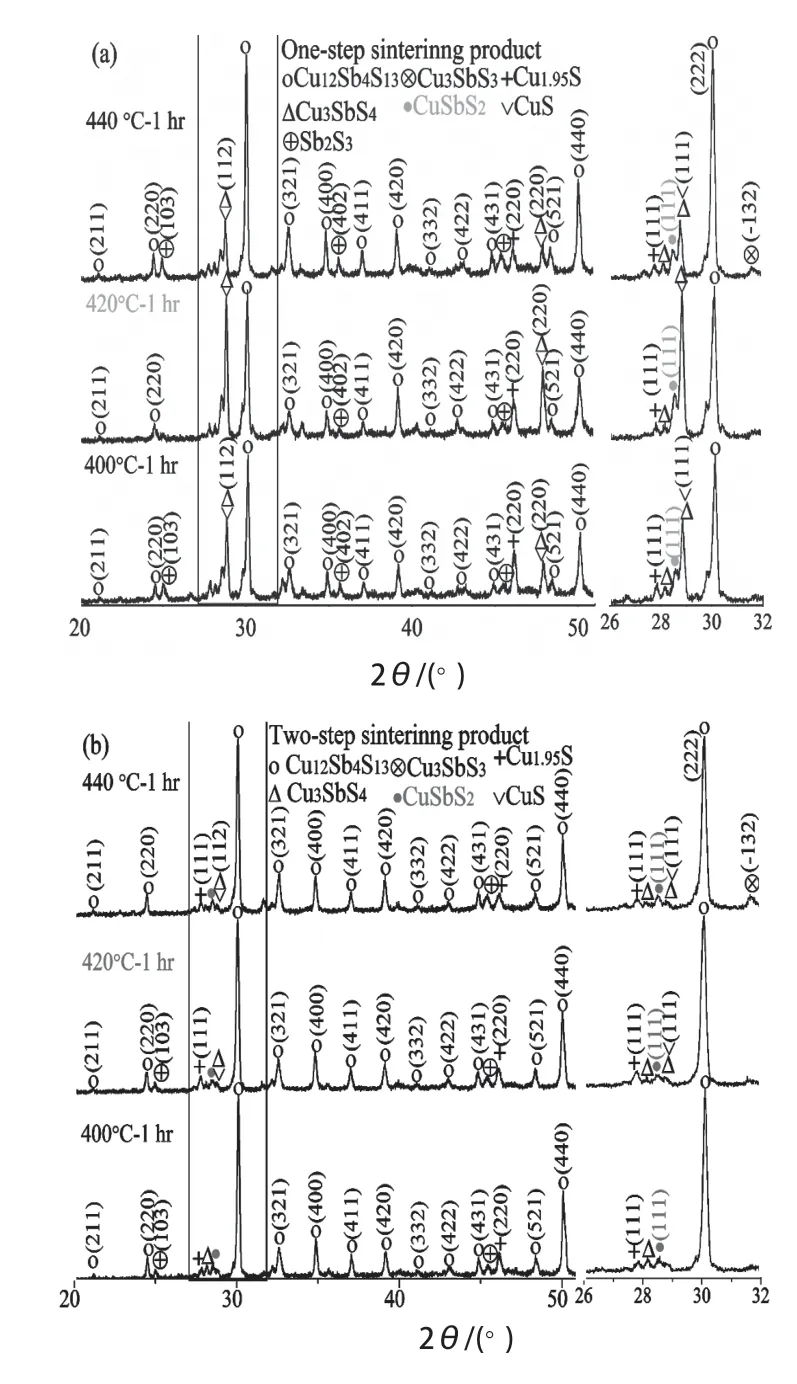
圖6 一步式(a)和分步式(b)燒結工藝下合成Cu12Sb4S13塊體表面的XRDFig. 6 XRD patterns of surface of Cu12Sb4S13 bulk by onestep sintering (a) and two-step sintering (b)
圖6是不同燒結工藝下合成Cu12Sb4S13塊體表面的XRD 結果。無論是采用一步式燒結工藝還是采用分步式燒結工藝,雜質相(CuSbS2和Cu3SbS3/Cu3SbS4)都比燒結塊破碎后粉體對應的特征峰強。另一方面,一步式燒結工藝和分步式燒結工藝對表面組成影響較大,一步式燒結CuS 分解少,表面硫磺蒸汽壓高,Cu3SbS4 的特征峰強;而分步法燒結表面CuS 在真空氣氛下分解,表層硫磺蒸汽壓相對降低,Cu3SbS4的特征峰減弱。
根據文獻[22]的Cu-Sb-S 三元相圖和本實驗研究的變化參數,Cu12Sb4S13的反應機理見圖7。
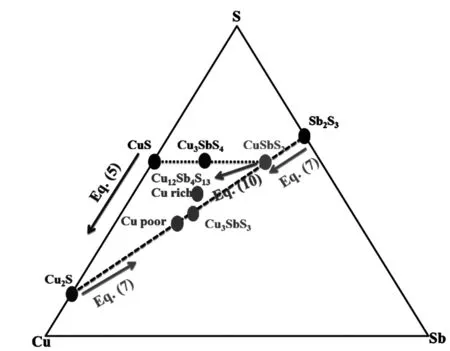
圖7 合成Cu12Sb4S13的反應機理Fig. 7 Reaction mechanism of synthesis Cu12Sb4S13
在加熱過程中,CuS 在220 ℃發生分解生成Cu2S(圖7 中表示方程式5 的箭頭方向)。Cu2S 與Sb2S3在400 ℃反應生成CuSbS2(圖7 中表示方程式7 的箭頭方向)。CuSbS2分解為Cu12Sb4S13和易氣化的Sb2S3或易升華的Sb4類結構[22]。減少Cu或CuS 的摩爾配比能夠減緩反應方程式(3)和(4)的進行,因此Cu3SbS4的相對含量減少。
3 結 論
本文研究以輝銻礦Sb2S3為原料制備高純Cu12Sb4S13的合成工藝。在400℃保溫1 h 可以快速合成主成分為Cu12Sb4S13 塊體。通過粉碎機械化球磨和二次燒結可以進一步消除初次反應殘留Cu2S 同時減少第二相CuSbS2和Cu3SbS3。結合XRD 結果和可能存在的化學反應,提出一種合成Cu12Sb4S13的反應機理。原料CuS 分解為Cu2S 同時提供富硫環境。Cu2S 和Sb2S3通過固相反應先生成CuSbS2 后轉化為Cu12Sb4S13。硫化蒸汽壓和Cu含量將會影響中間相的成分(CuSbS2,Cu3SbS3,Cu3SbS4)和相對含量。

