KIF4A在卵巢癌中的預(yù)后、生物學(xué)功能及富集分析*
馮嵩崴,羅山暉,王露玉,季晨晨,朱維培
215000 江蘇 蘇州,蘇州大學(xué)附屬第二醫(yī)院 婦產(chǎn)科(馮嵩崴、羅山暉、王露玉、朱維培);215000 江蘇 蘇州,蘇州大學(xué) 骨科研究所(季晨晨)
在女性生殖器惡性腫瘤當(dāng)中,卵巢癌的總死亡率排在首位,并且5年生存率僅為25%~30%[1]。絕大多數(shù)患者在早期沒(méi)有癥狀,在確診時(shí)已經(jīng)處于晚期并伴轉(zhuǎn)移。因此,探索卵巢癌新的診斷和治療方法,對(duì)卵巢癌的治療具有重大意義。
KIF4A為驅(qū)動(dòng)蛋白超家族成員之一,這些蛋白在細(xì)胞內(nèi)微管轉(zhuǎn)運(yùn)和細(xì)胞分裂中起關(guān)鍵作用[2]。KIF4A位于細(xì)胞質(zhì)和細(xì)胞核中,被認(rèn)為是腫瘤發(fā)生發(fā)展的重要因素[3]。KIF4A基因在腫瘤中有著不同的作用,它在大多數(shù)腫瘤中作為原癌基因,如膠質(zhì)母細(xì)胞瘤[4]、肝癌[5]和胰腺癌[6]。有趣的是,KIF4A在胃癌中起著抑癌基因的作用[7]。近來(lái)的生物信息學(xué)研究表明,KIF4A的表達(dá)在正常卵巢和腫瘤樣本中存在顯著差異,提示KIF4A可能與卵巢癌的發(fā)生發(fā)展有關(guān)[8]。然而,KIF4A在卵巢癌中的潛在分子機(jī)制及基因功能研究尚未見(jiàn)相關(guān)報(bào)道。
本研究通過(guò)生物信息學(xué)方法對(duì)KIF4A在卵巢癌中進(jìn)行基因其富集分析,并進(jìn)一步在高表達(dá)KIF4A的卵巢癌細(xì)胞系中沉默KIF4A基因,觀察其對(duì)于腫瘤細(xì)胞的增殖、遷移、凋亡、周期分布等生物學(xué)功能的影響。
1 材料與方法
1.1 主要材料
細(xì)胞系A(chǔ)2780、HO-8910PM、COC1、SKOV3和IOSE80購(gòu)自中國(guó)科學(xué)院上海細(xì)胞生物所細(xì)胞庫(kù);培養(yǎng)基RPMI 1640、胎牛血清、PBS、胰酶購(gòu)自Hyclone公司;慢病毒干擾載體sh-NC、sh-KIF4A-1、sh-KIF4A-2、sh-KIF4A-3購(gòu)自GenePharma公司;實(shí)時(shí)熒光定量PCR相關(guān)試劑盒購(gòu)自TaKaRa公司;lipofectamineTM2000、TRIzol及相關(guān)引物購(gòu)自Invitrogen公司;兔抗人KIF4 (ab122227)及鼠抗人GAPDH (ab8245)均購(gòu)自Abcam公司;Transwell小室購(gòu)自Corining公司;MTT試劑盒,BCA試劑盒,二甲基亞砜(dimethyl sulfoxide,DMSO)購(gòu)自Sigma公司;凋亡試劑及細(xì)胞周期試劑盒購(gòu)自杭州聯(lián)科。
1.2 生物信息學(xué)分析
下載TCGA數(shù)據(jù)庫(kù)(http://portal.gdc.cancer.gov)中327例卵巢癌患者的轉(zhuǎn)錄組數(shù)據(jù),以中KIF4A表達(dá)量的中位值,將樣本分為KIF4A高表達(dá)和低表達(dá)兩個(gè)亞組,設(shè)置篩選條件為logFC>0.5,P<0.05,篩選出高低亞組中上調(diào)及下調(diào)最明顯的前20個(gè)基因進(jìn)行基因表達(dá)熱圖和基因相關(guān)性分析熱圖的繪制,然后將這些相關(guān)基因進(jìn)行GO功能富集分析和KEGG通路富集分析。使用GEPIA數(shù)據(jù)庫(kù)(http://gepia.cancer-pku.cn)檢測(cè)卵巢癌及正常卵巢上皮組織中KIF4A的表達(dá)水平及FIGO分期情況。使用KM-plotter數(shù)據(jù)庫(kù)(http://www.kmplot.com/)檢測(cè)KIF4A表達(dá)量與卵巢癌患者總生存期(overall survival, OS)的關(guān)系,并顯示P值,HR(95%CI)和生存曲線。以上數(shù)據(jù)庫(kù)所有臨床數(shù)據(jù)及轉(zhuǎn)錄組數(shù)據(jù)均基于TCGA數(shù)據(jù)庫(kù)中的卵巢癌數(shù)據(jù)。使用人類蛋白質(zhì)圖譜數(shù)據(jù)庫(kù)(HPA, http://www.proteinatlas.org)檢測(cè)KIF4A基因在正常卵巢上皮及卵巢癌上皮組織的免疫組化染色情況。
1.3 細(xì)胞培養(yǎng)及轉(zhuǎn)染
將細(xì)胞株接種于含有FBS(10%)和青霉素(100 U/mL)和鏈霉素(100 μg/mL)的RPMI-1640培養(yǎng)基中,均在37℃,5%CO2條件下培養(yǎng),當(dāng)匯合度達(dá)90%時(shí)進(jìn)行傳代培養(yǎng)。轉(zhuǎn)染前,用磷酸鹽緩沖鹽水沖洗,采用攜帶sh-NC、sh-KIF4A-1、sh-KIF4A-2、sh-KIF4A-3的慢病毒對(duì)KIF4A相對(duì)表達(dá)量最多的細(xì)胞株進(jìn)行轉(zhuǎn)染。
1.4 RT-qPCR及Western Blot
在RT-qPCR實(shí)驗(yàn)中,應(yīng)用Trizol試劑從細(xì)胞中提取總RNA,應(yīng)用PrimeScript RT試劑盒進(jìn)行逆轉(zhuǎn)錄,SYBR Prime Script RT-PCR試劑盒用于RT-qPCR,采用熒光定量PCR儀進(jìn)行擴(kuò)增,反應(yīng)條件為95 ℃ 30 s;60 ℃ 30 s,72 ℃ 60 s反復(fù)40個(gè)循環(huán)。以GADP為內(nèi)參基因,通過(guò)2-ΔΔCt方法計(jì)算結(jié)果并繪制直方圖。使用的引物序列是:KIF4A-F: 5’-TGAACTCCCAGTCGTCC-3’;KIF4A-R: 5’-GCACTGATTACATTTCCC-3’;GAPDH-F: 5’-GGAGCGAG-ATCCCTCCAAAT-3’; GADPH-R: 5’-GGCTGTTGTCATACTTCTCATGG-3’。在Western Blot實(shí)驗(yàn)中,使用BCA試劑盒測(cè)定蛋白濃度,在SDS-PAGE膠的孔空中上樣,電泳后轉(zhuǎn)移至PVDF膜上,用5%脫脂奶粉封閉2小時(shí)。然后將兔抗人KIF4A抗體(稀釋1∶1 000)和GAPDH鼠抗人抗體(1∶2 500)加入,并在4℃下孵育過(guò)夜。使用PBST緩沖液洗膜,隨后將二抗加入并在室溫下孵育1小時(shí),用PBST緩沖液洗滌后曝光顯影。
1.5 細(xì)胞增殖實(shí)驗(yàn)(MTT法)和克隆形成實(shí)驗(yàn)
在MTT實(shí)驗(yàn)中,細(xì)胞培養(yǎng)24 h、48 h、72 h后加入10 μL MTT(5 mg/mL)試劑,在37℃下孵育4小時(shí),加入150 μL DMSO后震蕩10 min,用酶標(biāo)儀在490 nm的吸光度下進(jìn)行測(cè)量,用于分析細(xì)胞增殖情況。在克隆形成實(shí)驗(yàn)中,胰蛋白酶消化細(xì)胞后接種于6孔板中培養(yǎng)3周,PBS 洗滌,4%多聚甲醛室溫下固定細(xì)胞0.5 h。棄去固定液后結(jié)晶紫染色液染色10 min,最后得到集落數(shù)。
1.6 細(xì)胞遷移實(shí)驗(yàn)(Transwell及劃痕實(shí)驗(yàn))
在Transwell小室遷移實(shí)驗(yàn)中,下室加600 μL含10%FBS的培養(yǎng)基。取對(duì)數(shù)生長(zhǎng)期得細(xì)胞,用無(wú)血清的培養(yǎng)基進(jìn)行重懸后取3×105/mL的懸液加入上室。培養(yǎng)48 h,用棉簽擦去上室中的細(xì)胞后,使用4%的多聚甲醛將小室底部細(xì)胞固定15 min,結(jié)晶紫避光染色15 min,最后在光學(xué)顯微鏡下觀察計(jì)數(shù),隨機(jī)選取五個(gè)視野進(jìn)行細(xì)胞計(jì)數(shù)。在劃痕實(shí)驗(yàn)中,PBS沖洗懸浮細(xì)胞并將細(xì)胞以2×105個(gè)/孔接種于6孔板中,用200 μL無(wú)菌移液槍頭筆直的產(chǎn)生劃痕傷口。劃痕后0小時(shí)和24小時(shí)使用顯微鏡拍攝匯合情況。
1.7 細(xì)胞凋亡及細(xì)胞周期檢測(cè)
將轉(zhuǎn)染后的卵巢癌細(xì)胞1×105個(gè)/孔接種于6孔板,37℃培養(yǎng)3天進(jìn)行PBS洗滌,洗滌后用不含乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)的胰蛋白酶進(jìn)行消化,重懸于PBS然后離心收集,重復(fù)3次。凋亡:每管細(xì)胞加入5 μL FITC annexin V和Propidium Iodide Staining Solution避光孵育30分鐘,至流式細(xì)胞儀中檢測(cè)。周期:酒精固定后,10 μL破膜劑及1 mL PI(50 μL/mL)加入每管細(xì)胞后混勻,避光孵育60分鐘,至流式細(xì)胞儀中檢測(cè)。
1.8 統(tǒng)計(jì)學(xué)分析
所有數(shù)據(jù)用均數(shù)±標(biāo)準(zhǔn)差表示。兩組間數(shù)據(jù)比較采用t檢驗(yàn);多組間計(jì)量比較采用單因素方差分析。使用Graphpad Prism 5.0繪制所有直方圖和線圖。實(shí)驗(yàn)部分統(tǒng)計(jì)均在Graphpad Prism 5.0及SPSS 16.0軟件中進(jìn)行,轉(zhuǎn)錄組數(shù)據(jù)在R 3.6.1中進(jìn)行統(tǒng)計(jì)分析及繪圖。P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié) 果
2.1 KIF4A在卵巢癌中的基因富集分析
為了解KIF4A在卵巢癌中的調(diào)控機(jī)制及相關(guān)基因,基于TCGA數(shù)據(jù)庫(kù)中轉(zhuǎn)錄組數(shù)據(jù),篩選出高低亞組中上調(diào)及下調(diào)最明顯的前20個(gè)基因進(jìn)行表達(dá)熱圖和相關(guān)性分析熱圖的繪制(圖1A)。其中基因富集分析顯示KIF4A與MYH11、ACTG2、HSPB6等基因成負(fù)相關(guān),與BUB1、CCNA2、MELK等基因呈正相關(guān)(圖1B)。接下來(lái)將這些共表達(dá)基因進(jìn)行GO功能富集分析和KEGG通路富集分析。結(jié)果表明,KIF4A在卵巢癌中具有有絲細(xì)胞核分裂,有絲分裂姐妹染色單體分離,細(xì)胞器裂變的功能。KEGG通路富集結(jié)果顯示,KIF4A可能影響細(xì)胞周期,細(xì)胞黏附分子,血管平滑肌收縮等通路(圖1C、D)。
2.2 KIF4A在卵巢癌中的表達(dá)情況
在不同細(xì)胞系中分別檢測(cè)KIF4A的表達(dá)。RT-qPCR的結(jié)果表明,與正常卵巢上皮細(xì)胞IOSE80相比,卵巢癌細(xì)胞株A2780(5.532±0.263),SKOV3(6.565±0.224),HO-8910PM(4.868±0.311),COC1(5.486±0.458)中KIF4A的表達(dá)量差異具有統(tǒng)計(jì)學(xué)意義(P<0.01)(圖2A);western blot結(jié)果顯示,卵巢癌細(xì)胞與正常卵巢上皮細(xì)胞相比,KIF4A的蛋白表達(dá)水平顯著增加,其差異均具有統(tǒng)計(jì)學(xué)意義(P<0.01)(圖2B);因此,本研究選取KIF4A表達(dá)相對(duì)最高的SKOV3細(xì)胞進(jìn)行后續(xù)試驗(yàn)。與此同時(shí),GEPIA數(shù)據(jù)庫(kù)中分析KIF4A在卵巢癌患者中的表達(dá)情況,KIF4A基因在腫瘤組中同樣高表達(dá)(P<0.01);HPA數(shù)據(jù)庫(kù)中檢索KIF4A基因在卵巢癌上皮細(xì)胞及正常卵巢上皮細(xì)胞的免疫組織化學(xué)法染色情況,結(jié)果顯示卵巢癌上皮細(xì)胞中染色程度更強(qiáng)。
研究結(jié)果表明,KIF4A在卵巢癌細(xì)胞系及臨床樣本中較正常組織相比,mRNA及蛋白質(zhì)表達(dá)水平均明顯升高。

圖1 KIF4A在卵巢癌中的基因富集分析
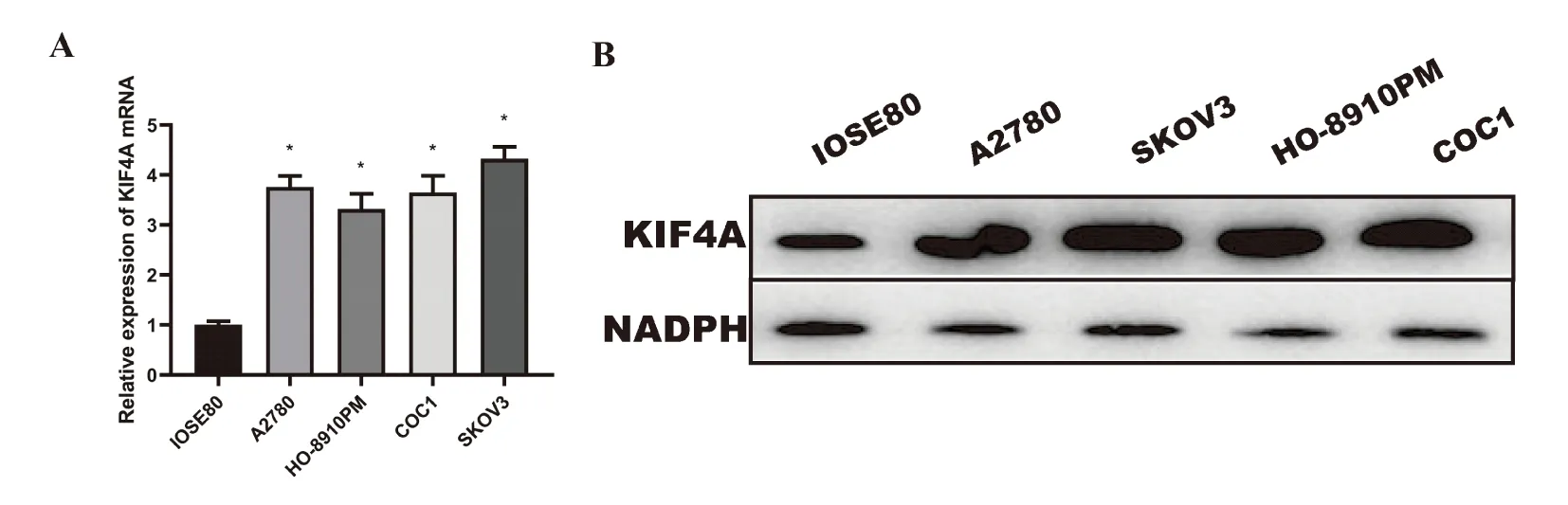
圖2 KIF4A在卵巢癌中的表達(dá)情況
2.3 KIF4A與卵巢癌患者預(yù)后的關(guān)系
在Kaplan-Meier Plotter數(shù)據(jù)庫(kù)中查詢KIF4A基因表達(dá)情況與卵巢癌患者生存時(shí)間的關(guān)系,發(fā)現(xiàn)KIF4A高表達(dá)組具有較短的總生存期(HR=1.570,P<0.01),見(jiàn)圖3A。在GEPIA數(shù)據(jù)庫(kù)中查詢KIF4A
基因表達(dá)量與FIGO分期的關(guān)系,結(jié)果顯示KIF4A表達(dá)量在不同分期之間具有統(tǒng)計(jì)學(xué)差異(F=3.860,P<0.05),見(jiàn)圖3B。
研究結(jié)果表明,卵巢癌KIF4A高表達(dá)患者中與低表達(dá)患者相比,具有更差的預(yù)后,但卵巢癌患者中KIF4A的表達(dá)量隨著臨床分期的增高而減少。
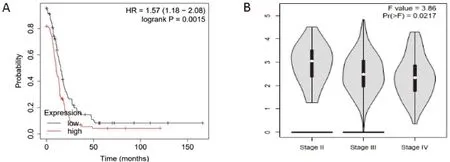
圖3 KIF4A與卵巢癌患者預(yù)后的關(guān)系
2.4 KIF4A對(duì)卵巢癌細(xì)胞生長(zhǎng)的影響
三組sh-KIF4A分別轉(zhuǎn)染SKOV3細(xì)胞系,結(jié)果顯示KIF4A的mRNA和蛋白均表達(dá)明顯下降(P<0.05),選擇其中沉默效率最佳的sh-KIF4A-3進(jìn)行后續(xù)實(shí)驗(yàn),見(jiàn)圖4。MTT法測(cè)定結(jié)果顯示,轉(zhuǎn)染24 h、48 h和72 h后,sh-KIF4A組OD值(0.239±0.020、0.735±0.056、1.611±0.001)顯著低于sh-NC組(0.602±0.023、1.632±0.025、2.718±0.048),差異具有統(tǒng)計(jì)學(xué)意義(P<0.05)(圖5A)。克隆形成實(shí)驗(yàn)檢測(cè)結(jié)果顯示,sh-NC 組和 sh-KIF4A組細(xì)胞克隆形成數(shù)分別為(305±27)個(gè)和(142±12)個(gè),差異有統(tǒng)計(jì)學(xué)意義(圖5B)。
研究結(jié)果表明,sh-KIF4A-3的沉默效果最好,且沉默KIF4A可明顯抑制卵巢癌細(xì)胞的生長(zhǎng)。
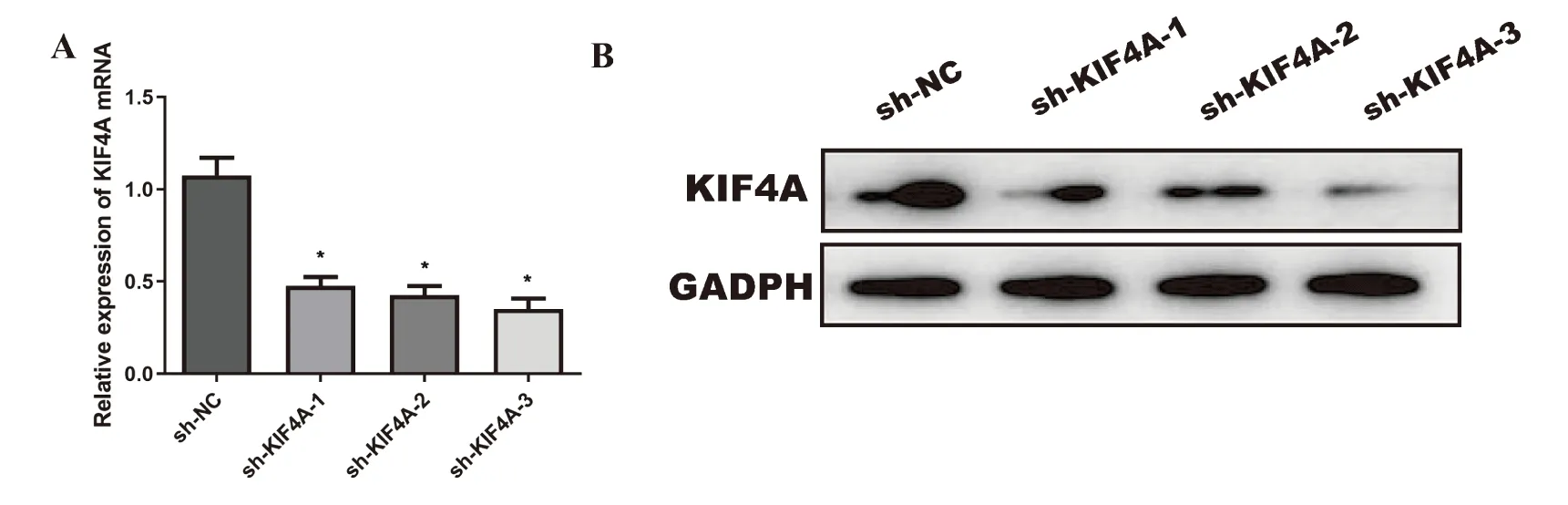
圖4 不同sh-KIF4A的轉(zhuǎn)染效果
2.5 KIF4A對(duì)卵巢癌細(xì)胞遷移的影響
Transwell小室遷移實(shí)驗(yàn)研究KIF4A對(duì)遷移的影響,結(jié)果顯示沉默KIF4A的可以抑制卵巢癌細(xì)胞的遷移,sh-KIF4A(32.3±4.6)組中穿過(guò)小室濾過(guò)膜的細(xì)胞數(shù)明顯少于sh-NC組(56.3±3.8),差別有統(tǒng)計(jì)學(xué)意義(P<0.01) (圖6A)。同時(shí)劃痕實(shí)驗(yàn)同樣證實(shí)了這一結(jié)論(圖6B)。
研究結(jié)果表明,Transwell及劃痕試驗(yàn)均證明了沉默KIF4A可明顯抑制卵巢癌細(xì)胞的遷移能力。
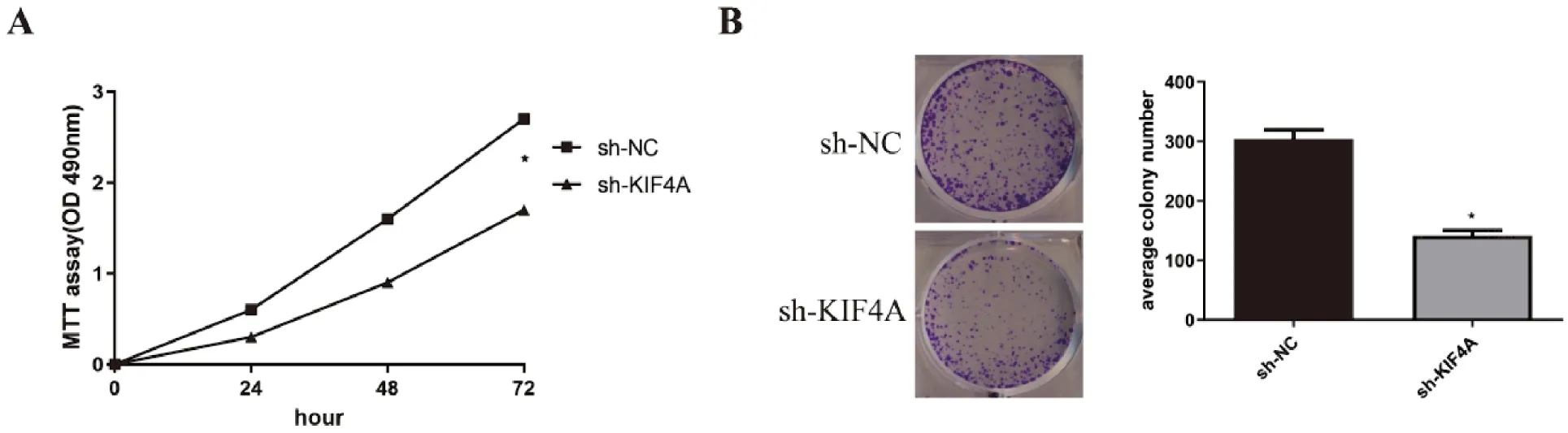
圖5 沉默KIF4A對(duì)卵巢癌細(xì)胞增殖的影響
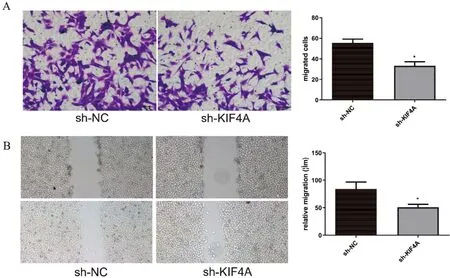
圖6 沉默KIF4A對(duì)卵巢癌細(xì)胞遷移的影響
2.6 KIF4A對(duì)卵巢癌細(xì)胞凋亡的影響
流式細(xì)胞儀檢測(cè)結(jié)果顯示,sh-KIF4A組與sh-NC組的細(xì)胞凋亡率分別為5.832%±0.916%和0.247%±0.017%,sh-KIF4A組凋亡率顯著大于sh-NC組,差異具有統(tǒng)計(jì)學(xué)意義(P<0.01)(圖7)。
研究結(jié)果表明,沉默KIF4A可明顯促進(jìn)卵巢癌細(xì)胞的凋亡。
2.7 KIF4A對(duì)卵巢癌細(xì)胞周期的影響
流式細(xì)胞儀檢測(cè)結(jié)果顯示,sh-NC組與sh-KIF4A組的細(xì)胞周期分布比例 G0/G1期分別為68.124%±0.533%和50.567%±0.753%;S 期分別為30.110%±1.235%和38.443%±1.147%;G2/M 期為別為12.997%±0.012%和12.843%±0.008%。除G2/M 期外,其余周期分布比例差異有統(tǒng)計(jì)學(xué)意義(P<0.01)(圖8)。說(shuō)明沉默KIF4A可影響卵巢癌細(xì)胞各周期分布比例,主要影響 G0/G1 期。
研究結(jié)果表明,沉默KIF4A可將卵巢癌細(xì)胞生長(zhǎng)阻滯于S期并主要影響 G0/G1 期的分布。
3 討 論
卵巢惡性腫瘤在女性生殖器官腫瘤中預(yù)后最差,且相應(yīng)生物學(xué)功能是影響卵巢癌死亡率的重要原因。而靶向治療開(kāi)創(chuàng)了卵巢癌治療的新領(lǐng)域,尋找作用于新靶點(diǎn)的藥物是近年來(lái)研究的熱點(diǎn)。故本研究著重探討KIF4A對(duì)腫瘤細(xì)胞生物學(xué)功能的影響及相關(guān)基因富集分析,這將為卵巢癌的診斷和治療提供重要指導(dǎo)。
KIF4A是驅(qū)動(dòng)蛋白家族的成員之一,該家族可利用ATP水解所釋放的能量沿著微管進(jìn)行包括囊泡、細(xì)胞器、染色體、蛋白質(zhì)復(fù)合物和mRNA等的轉(zhuǎn)運(yùn)。目前該蛋白分子在多種腫瘤中被深入研究,Taniwaki等[9]研究發(fā)現(xiàn)干擾KIF4A在肺癌細(xì)胞中的表達(dá)后,肺癌細(xì)胞的生長(zhǎng)及侵襲受會(huì)受到抑制,提示KIF4A與肺癌的發(fā)生、發(fā)展有關(guān)。Liu等[10]通過(guò)體內(nèi)體外實(shí)驗(yàn)同樣證實(shí)KIF4A可促進(jìn)腎透明細(xì)胞癌的轉(zhuǎn)移及增殖。Gao等[11]發(fā)現(xiàn)KIF4A可調(diào)節(jié)p21啟動(dòng)子促進(jìn)胰腺癌細(xì)胞的增殖、遷移及侵襲,但是對(duì)其細(xì)胞凋亡沒(méi)有影響。雖然上述研究提示KIF4A異常表達(dá)與癌癥發(fā)生、發(fā)展密切相關(guān),相關(guān)生物信息學(xué)研究也表明KIF4A與卵巢癌患者的預(yù)后顯著相關(guān),但目前仍缺乏KIF4A與卵巢癌的生物學(xué)功能試驗(yàn)研究。因此,本研究進(jìn)一步分析KIF4A在卵巢癌中的預(yù)后、生物學(xué)功能及相關(guān)基因富集分析,以期對(duì)卵巢癌的靶向治療提供新思路。
本研究首先通過(guò)生物信息學(xué)方法,在卵巢癌患者公共數(shù)據(jù)庫(kù)中檢索KIF4A基因與卵巢癌患者總生存期及FIGO分期的關(guān)系,結(jié)果顯示高表達(dá)KIF4A生存時(shí)間明顯降低,這與陳柱等[12]和胡國(guó)輝等[13]在乳腺癌及肝癌患者的預(yù)后分析中結(jié)果相一致,這提示KIF4A可能在泛癌中均與預(yù)后有著明顯聯(lián)系。但卵巢癌患者中KIF4A的表達(dá)量卻不隨著腫瘤臨床分期的嚴(yán)重程度所增加,這與之前其他腫瘤中的研究[14]結(jié)果不一致,這需要將來(lái)進(jìn)一步研究。接下來(lái)RT-qPCR檢測(cè)了人卵巢癌正常上皮細(xì)胞株IOSE80和多種卵巢癌細(xì)胞株和中KIF4AmRNA 的相對(duì)表達(dá)水平,發(fā)現(xiàn)卵巢癌細(xì)胞A2780,HO-8910PM,COC1,SKOV3中KIF4AmRNA 的表達(dá)水平顯著高于正常卵巢上皮細(xì)胞。選取其中KIF4A表達(dá)水平最高的細(xì)胞株SKOV3進(jìn)行了后續(xù)功能試驗(yàn)。結(jié)果發(fā)現(xiàn),沉默KIF4A的表達(dá)可抑制卵巢癌細(xì)胞的生長(zhǎng)及遷移并促進(jìn)其凋亡。此外,沉默KIF4A影響卵巢癌的周期分布,主要影響G0/G1期,并使細(xì)胞阻滯在S期,進(jìn)而導(dǎo)致腫瘤的生長(zhǎng)抑制。關(guān)于KIF4A在分子層面的深入機(jī)制已有相關(guān)報(bào)道。研究發(fā)現(xiàn)KIF4A調(diào)控肝癌細(xì)胞的生長(zhǎng)可能是通過(guò)調(diào)節(jié)巨噬細(xì)胞血管生成相關(guān)因子[15],但具體機(jī)制仍需進(jìn)一步闡明。武巖[16]研究發(fā)現(xiàn)NLP蛋白可與KIF4A蛋白一起參與調(diào)控中間小體的生成參與正常及腫瘤細(xì)胞的有絲分裂。在乳腺癌中,KIF4A可被多柔比星誘導(dǎo)低表達(dá)并影響PARP-1的上調(diào)[17],且miR-335可對(duì)其進(jìn)行調(diào)控,并通過(guò)熒光素酶試驗(yàn)進(jìn)行了驗(yàn)證[18]。但是KIF4A在卵巢癌中的深層機(jī)制的研究還未有報(bào)道,這將來(lái)值得進(jìn)一步的深入探討。
KIF4A作為驅(qū)動(dòng)蛋白家族的成員之一,驅(qū)動(dòng)蛋白抑制劑能夠克服抗微管類藥物的耐藥,如有絲分裂驅(qū)動(dòng)蛋白KIF20B[19]及Eg5[20]抑制劑具有抗增殖作用已被證實(shí)可用于肝癌及其他惡性腫瘤的治療。根據(jù)KIF4A在有絲分裂過(guò)程中的作用,選擇性地抑制 KIF4A的活性,進(jìn)而抑制腫瘤細(xì)胞的生長(zhǎng)及分裂,這有可能成為新的卵巢癌患者的治療策略。
綜上所述,我們的研究結(jié)果表明,KIF4A與卵巢癌患者的預(yù)后及細(xì)胞的生物學(xué)具有明顯相關(guān)。但是,KIF4A在卵巢癌中發(fā)生和發(fā)展的具體作用及相關(guān)機(jī)制并未完全闡明,以及相應(yīng)的調(diào)節(jié)機(jī)制也需在動(dòng)物模型進(jìn)行進(jìn)一步的研究,相信在完善相關(guān)基礎(chǔ)及臨床實(shí)驗(yàn)后,KIF4A將有望成為卵巢癌治療的新靶點(diǎn),并改善卵巢癌患者的預(yù)后。
作者聲明:本文全部作者對(duì)于研究和撰寫(xiě)的論文出現(xiàn)的不端行為承擔(dān)相應(yīng)責(zé)任;并承諾論文中涉及的原始圖片、數(shù)據(jù)資料等已按照有關(guān)規(guī)定保存,可接受核查。
學(xué)術(shù)不端:本文在初審、返修及出版前均通過(guò)中國(guó)知網(wǎng)(CNKI)科技期刊學(xué)術(shù)不端文獻(xiàn)檢測(cè)系統(tǒng)的學(xué)術(shù)不端檢測(cè)。
同行評(píng)議:經(jīng)同行專家雙盲外審,達(dá)到刊發(fā)要求。
利益沖突:所有作者均聲明不存在利益沖突。
文章版權(quán):本文出版前已與全體作者簽署了論文授權(quán)書(shū)等協(xié)議。

