人間充質干細胞外泌體通過p38絲裂素活化蛋白激酶信號通路促進小鼠胚胎成骨細胞前體增殖和成骨分化
王新強,吳良邦,章月紅,顧增輝
中國人民解放軍聯勤保障部隊第903醫院骨三科,杭州 310004
骨質疏松癥是60歲以上人群常見的骨代謝疾病,主要特征為骨量減少、骨微結構破壞、骨脆性增加,增高了骨折的風險[1]。骨質疏松癥主要發生機制是成骨細胞介導的骨形成和破骨細胞介導的骨吸收動態失衡,臨床上治療骨質疏松癥的藥物有骨吸收抑制劑、骨形成促進劑和骨礦化促進劑[2],但這些藥物的使用易引發一系列并發癥,如非典型骨折和骨壞死[1]。因此,尋找治療骨質疏松癥的新策略尤為重要。
近年研究[3]發現,間充質干細胞(MSC)可通過分泌外泌體參與骨代謝過程,調控骨相關細胞的增殖、分化和凋亡等功能,并且影響骨組織周圍微環境,為骨質疏松癥等骨代謝疾病的治療提供了新的思路。BMSC分泌的外泌體可促進小鼠胚胎成骨細胞前體細胞(MC3T3-E1細胞)的增殖和分化,促進成骨特異性run相關轉錄因子2(Runx2)和堿性磷酸酶(Alp)的表達,促進骨礦化沉淀[4],但外泌體調控的分子學機制尚不清楚。本研究利用差速離心法獲得人MSC(hMSC)分泌的外泌體,觀察其對MC3T3-E1細胞的增殖和成骨分化的作用,并基于p38絲裂素活化蛋白激酶(p38MAPK)信號通路探討其作用機制。
1 材料與方法
1.1 細胞和主要試劑
hMSC和MC3T3-E1細胞購于中國科學院典型培養物保藏委員會細胞庫(貨號:SCSP-405和GNM15)。PBS、胎牛血清、αMEM培養基和0.05%胰蛋白酶(Gibco,美國);經典成骨誘導液(賽業生物科技有限公司,廣州);p38MAPK抑制劑SB203580(Selleck生物科技有限公司,美國);Alp檢測試劑盒,Alexa Fluor 488標記的CD90、CD105、CD34和CD45抗體(Abcam公司,英國);茜素紅、SDS-PAGE、RIAP、PMSF、磷酸酶抑制劑和PVDF膜(Solarbio Life Sciences公司,中國);TRIzol試劑、PrimeScriptTMRT試劑盒和SYBR-Green qPCR Master Mix(TaKaRa公司,日本);BCA試劑盒(左克生物有限公司,廣州);一抗稀釋液、快速封閉液和二抗稀釋液(碧云天生物技術有限公司,上海)。Runx2抗體(貨號:D1L7F)、Alp抗體(貨號:3E5C7)、Ⅰ型膠原蛋白alpha1(COL1A1)抗體(貨號:E8F4L)、p38MAPK抗體(貨號:D13E1)、磷酸化p38MAPK(p-p38MAPK)抗體(貨號:D3F9)、ALIX抗體(貨號:E6P9B)、CD9抗體(貨號:D3H4P)、TSG101抗體(貨號:D1O5S)、GAPDH抗體(貨號:D16H11)和鼠抗兔二抗(貨號:7074)均購自美國Cell Signaling Technology公司,骨橋蛋白(Opn)抗體(貨號:ab228748,)購自英國Abcam公司;ECL超敏發光液(四正柏生物科技有限公司,北京)。
1.2 hMSC鑒定
將hMSC接種于60 mm培養皿中,待細胞長至80% ~ 90%融合后,用0.05%胰蛋白酶消化。PBS洗滌3次,500×g離心5 min后,再用PBS制成單細胞懸液。取單細胞懸液200 μL放入玻璃管中,分別加入CD90、CD105、CD34和CD45抗體,放置4℃避光孵育1 h后,再過濾去除細胞聚集體,最后流式細胞儀檢測熒光值。
將hMSC種于6孔板內,待長至80% ~ 90%融合后,將培養基更換為成骨誘導液誘導21 d,棄去上清液,PBS洗滌3次,加入4℃多聚甲醛溶液固定15 min,PBS洗滌3次,加入茜素紅染色1 h,放入顯微鏡觀察紅色結節,并拍照記錄。
1.3 hMSC外泌體分離
將hMSC接種于100 mm培養皿中,待細胞長至80%融合后,更換為無血清不含外泌體的αMEM培養基,培養48 h后,收集上清液。用0.22 μm濾膜過濾后,放入超高速離心機通過差速離心法提取外泌體[5]:將過濾的上清液以3 500 r/min、離心半徑9.5 cm、離心40 min,將離心后的上清液移至新PC管內,100 000×g離心90 min,棄去上清液;用500 μL PBS沖洗內壁沉淀物,轉移至新EP管內,混勻后10 000×g離心60 min;將上清液移至超離心管內,100 000×g離心2 h,收集沉淀物。使用透射電子顯微鏡觀察外泌體形態。通過qNano平臺分析外泌體的大小和密度。
1.4 蛋白質印跡法檢測hMSC和外泌體中蛋白質的變化
采用裂解液(RIAP∶PMSF∶磷酸酶抑制劑=100∶1∶1)提取hMSC和外泌體中的總蛋白。通過BCA試劑盒檢測總蛋白濃度。采用SDS-PAGE電泳分離總蛋白,再轉移至PVDF膜上,通過快速封閉液封閉15 min后,TBST洗滌3次,每次10 min。將膜放入1∶1 000稀釋的一抗(ALIX、CD9、TSG101和GAPDH抗體)混懸液中,4℃孵育過夜。用TBST洗滌3次,每次10 min,再放入1∶4 000稀釋的二抗混懸液中,孵育2 h。TBST洗滌3次,每次10 min,采用ECL超敏發光液作為顯色液,放入化學發光成像儀(Invitorgen公司,美國)進行蛋白顯影。通過Image J軟件分析結果,相對蛋白表達以GAPDH標準化。
1.5 外泌體對MC3T3-1細胞增殖和成骨能力的影響
將MC3T3-E1細胞種于96孔板內,分為4組,分別給予外泌體5 mg/L[6]干預(外泌體組)、p38MAPK抑制劑SB203580 10 μmol/L[7]干預(抑制劑組)、SB203580 10 μmol/L干預6 h后再加入外泌體5 mg/L干預(抑制劑+外泌體組),以未干預組作為對照組。細胞培養24 h后,將20 μL MTT溶液加入孔內,在37℃孵育2 h。棄去孔內液體,加入150 μL DMSO溶液,放入振蕩儀振蕩2 min,使用酶標儀490 nm下檢測光密度(OD)值,計算與對照組的相對值作為細胞增殖的速率。每個組設3個復孔,實驗獨立重復3次。
將MC3T3-1接種于6孔板內,待細胞長至40% ~ 50%融合度時,分為對照組、外泌體組、抑制劑組和抑制劑+外泌體組,每3 d換一次含10%胎牛血清的αMEM培養基。21 d后棄去培養基,PBS洗滌3次,加入4℃多聚甲醛固定15 min,加入茜素紅染色1 h,放入倒置顯微鏡觀察各組形成的紅色鈣化結節,拍照記錄。
將MC3T3-1接種于6孔板內,分為對照組、外泌體組、抑制劑組和抑制劑+外泌體組,培養24 h后,以1 000 r/min,離心半徑9.5 cm,離心10 min,收集上清液。每組均取50 μL上清液放入96孔板內,使用Alp檢測試劑盒進行檢測。分別加入檢測緩沖液和顯色底物溶液,避光37℃孵育10 min。每孔加入100 μL反應終止液終止反應,使用酶標儀在405 nm處測定OD值,計算Alp活力。每組6個復孔,獨立重復3次實驗。
1.6 外泌體對MC3T3-1的mRNA和蛋白質表達的影響
4組細胞干預24 h后,采用TRIzol試劑分別提取各組總RNA。以NanoDrop 2000分光光度計檢測各組總RNA純度和濃度后,將各組的RNA濃度調至一致,再使用PrimeScript TM RT試劑盒反轉錄擴增為cDNA(反轉錄條件:37℃ 15 min,85℃ 5 s)。將目的模板cDNA、SYBR-Green qPCR Master Mix和對應的引物(表1)混合后進行實時熒光定量PCR擴增,條件:95℃ 10 min預變性;95℃ 15 s,60℃ 45 s,72℃ 30 s,40個循環。以GAPDH為內參,通過2-△△ct法計算目的基因相對表達量。采用蛋白質印跡法測定Runx2、Alp、COL1A1、Opn、p38/p-p38MAPK蛋白相對表達量,方法同前。

表1 實時熒光定量PCR引物序列Tab. 1 Primer sequences required for real-time fluorescent quantitative PCR
1.7 統計學處理
應用GraphPad Prism 5軟件進行數據處理和作圖。計量資料以±s表示,多組間比較采用單因素方差分析,兩組間比較采用獨立樣本t檢驗;以P<0.05為差異有統計學意義。
2 結 果
2.1 hMSC鑒定
流式細胞術檢測結果顯示,hMSC表面抗原CD90(97.09%)和CD105(99.32%)呈陽性表達,CD34(2.92%)和CD45(1.45%)呈陰性表達,符合BMSC的表面抗原特征(圖1a ~ d)。茜素紅染色結果顯示,hMSC能形成礦化結節,具有誘導成骨能力(圖1e)。

圖1 流式細胞術和茜素紅染色鑒定hMSCFig. 1 Identification of hMSC by flow cytometry and Alizarin Red staining
2.2 外泌體特征
在透射電子顯微鏡下可見hMSC分泌的外泌體呈球形囊泡,形態為圓形或典型的杯形(圖2a),其直徑為40 ~ 160 nm(圖2b)。蛋白質印跡法檢測結果顯示,與hMSC比較,外泌體中的ALIX、CD9和TSG101的表達量增加,差異有統計學意義(P<0.05,圖2c)。
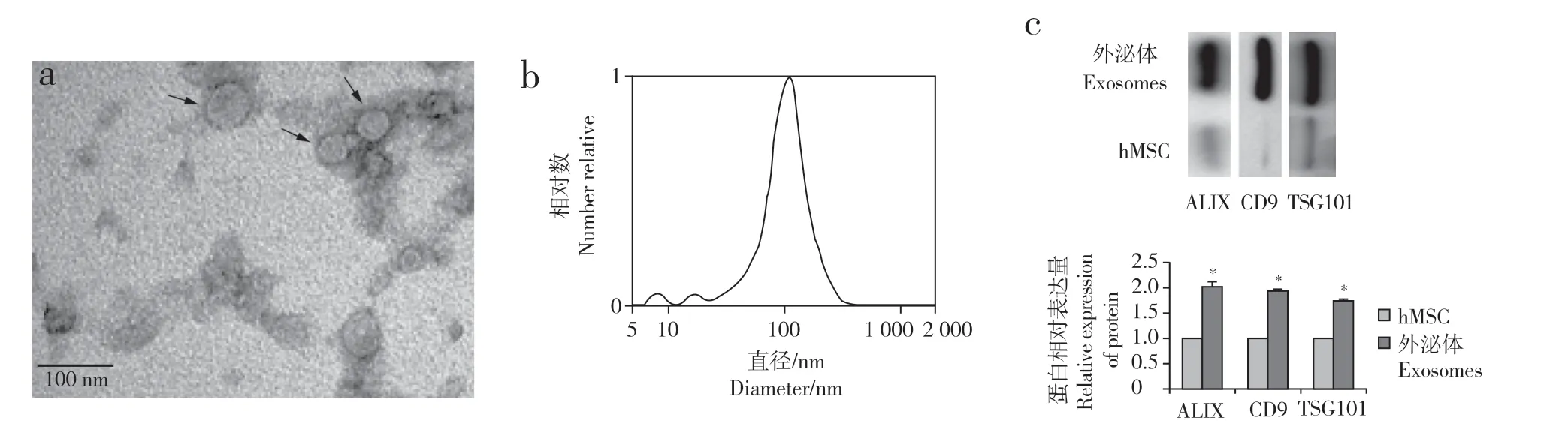
圖2 hMSC分泌的外泌體特征Fig. 2 Characteristics of exosomes secreted by hMSC
2.3 外泌體對MC3T3-E1細胞中p38MAPK信號通路的影響
蛋白質印跡法檢測結果顯示,與對照組相比,抑制劑組和抑制劑+外泌體組中p-p38/p38MAPK的蛋白表達量比值降低,外泌體組中的p-p38/p38MAPK的蛋白表達量比值增加,差異均有統計學意義(P< 0.05,圖3);與抑制劑組相比,抑制劑+外泌體組的p-p38/p38MAPK的蛋白表達量比值無明顯變化(P> 0.05,圖3);與外泌體組比較,抑制劑+外泌體組的p-p38/p38MAPK的蛋白表達量比值降低,差異有統計學意義(P< 0.05,圖3)。
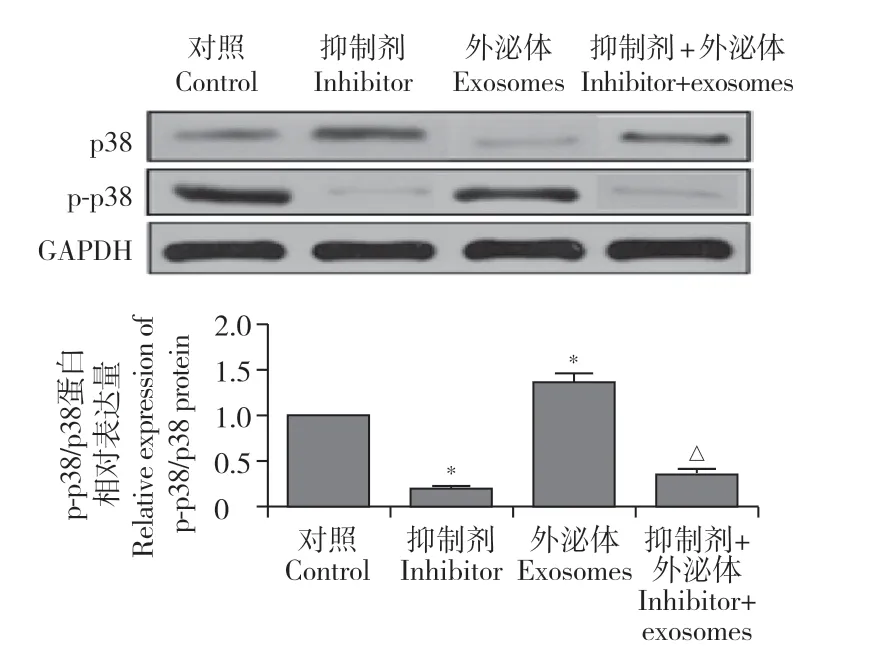
圖3 蛋白質印跡法檢測外泌體對MC3T3-E1細胞中p38MAPK信號通路的影響Fig. 3 Effect of exosomes on p38MAPK signaling pathway in MC3T3-E1 cells detected by Western blotting
2.4 外泌體對MC3T3-E1細胞成骨分化的影響
實時熒光定量PCR和蛋白質印跡法檢測結果顯示,與對照組比較,抑制劑組和抑制劑+外泌體組中成骨相關因子Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量降低,而外泌體組中Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量增加,差異均有統計學意義(P< 0.05,圖4a、b);與抑制劑組比較,抑制劑+外泌體組Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量無明顯變化(P> 0.05,圖4a、b);與外泌體組比較,抑制劑+外泌體組Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量降低,差異有統計學意義(P< 0.05,圖4a、b)。
茜素紅染色和Alp檢測結果顯示,與對照組比較,抑制劑組和抑制劑+外泌體組礦化結節數量減少、Alp活力降低,而外泌體組的礦化結節和Alp活力增加,差異均有統計學意義(P< 0.05,圖4c ~ e);與抑制劑組比較,抑制劑+外泌體組礦化結節數量和Alp活力無明顯變化(P> 0.05,圖4c ~ e);與外泌體組比較,抑制劑+外泌體組礦化結節數量減少、Alp活力降低,差異均有統計學意義(P< 0.05,圖4c ~ e)。

圖4 hMSC外泌體對MC3T3-E1細胞骨形成的影響Fig. 4 Effect of exosomes from hMSC on MC3T3-E1 cells osteogenesis
2.5 外泌體對MC3T3-E1細胞增殖的影響
MTT結果顯示,與對照組比較,抑制劑組和抑制劑+外泌體組的OD值降低,而外泌體組OD值增加,差異均有統計學意義(P< 0.05,圖5);與抑制劑組比較,抑制劑+外泌體組OD值無明顯變化(P> 0.05,圖5);與外泌體組比較,抑制劑+外泌體組OD值降低,差異有統計學意義(P< 0.05,圖5)。
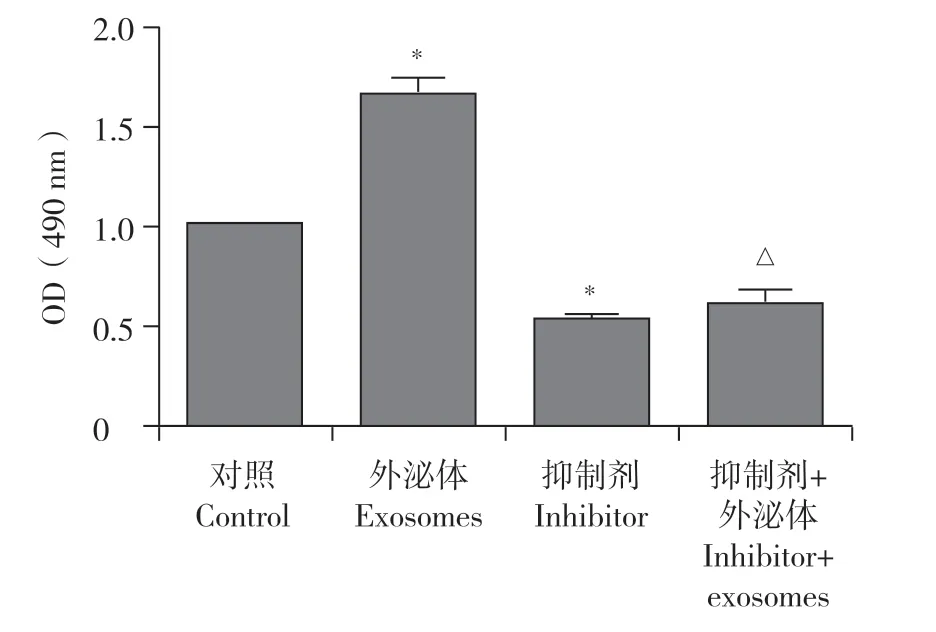
圖5 MTT檢測外泌體對MC3T3-E1細胞增殖的影響Fig. 5 Effect of exosomes on MC3T3-E1 cells proliferation detected by MTT assay
3 討 論
目前,全世界大約有2億人罹患骨質疏松癥,其發病率已躍居世界常見病的第7位[8]。骨質疏松癥及其并發癥(骨折、疼痛和致殘等)對人類健康構成了極大威脅[9]。因此,尋找確切有效的防治方案顯得非常重要。干細胞治療的發展為骨質疏松癥的治療帶來新的希望。hMSC容易獲得,且具有很強的自我更新和多向分化能力,其能定向形成成骨細胞,因此成為“種子細胞”[10]。有研究[11]顯示,hMSC直接注入鼠體內后,能使去勢大鼠的骨密度增加,可成為骨質疏松癥治療的新型策略。本研究茜素紅染色結果顯示,hMSC可誘導形成骨細胞,說明hMSC具有成骨分化能力。
然而,hMSC在治療過程中有免疫排斥防疫及收集過程中細胞受到污染等問題,尋找一種易獲得、性狀穩定、免疫原性和修復效果好的干細胞尤為重要[12]。近年來,有研究[13]表明,hMSC能分泌出直徑30 ~ 160 nm的脂質雙分子層細胞外囊泡,即外泌體,囊內含有豐富的蛋白質、脂質和核酸。本研究采用差速離心法分離出hMSC分泌的外泌體,蛋白質印跡法檢測顯示外泌體中ALIX、CD9和TSG101的表達量較hMSC增加。以外泌體干預MC3T3-E1細胞后,細胞中成骨分化相關因子Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量增加,礦化結節數量增多,ALP活力和細胞增殖能力增高,表明外泌體能促進MC3T3-E1細胞的成骨分化和增殖。
有研究[1]表明,p38MAPK信號通路對MC3T3-E1細胞向成骨細胞特異性分化起著重要的正向調節作用,抑制p38MAPK信號通路會使MC3T3-E1細胞成骨分化受阻。本研究結果顯示,p38MAPK抑制劑干預MC3T3-E1細胞后,成骨分化相關因子Alp、Runx2、COL1A1和Opn蛋白和mRNA表達量受到抑制,礦化結節數量、Alp活力和細胞增殖能力也明顯降低,也證實p38MAPK信號通路正向調控MC3T3-E1細胞成骨分化和增殖。本研究結果顯示,外泌體干預MC3T3-E1細胞后,p-p38/p38MAPK蛋白表達量比值增加,說明外泌體調控p38MAPK信號通路轉導;阻斷MC3T3-E1細胞中p38MAPK信號通路后,再用外泌體干預,細胞中成骨分化相關因子Alp、Runx2、COL1A1和Opn的mRNA和蛋白表達量、礦化結節數量、Alp活力和細胞增殖能力與抑制劑組無差異,說明外泌體通過p38MAPK信號通路調控MC3T3-E1細胞的成骨分化和增殖。
綜上所述,hMSC分泌的外泌體能夠促進MC3T3-E1細胞的成骨分化和增殖,其調控機制可能是通過激活p38MAPK信號通路實現的。

