不同熱轉化氣氛下纖維素焦中有機鉀的遷移特性
趙海波,徐文婷,宋薔
(1國家開發銀行企業局,北京 100031;2清華大學熱科學與動力工程教育部重點實驗室,北京 100084)
生物質由于其可再生、碳中性的優勢而備受重視。然而,生物質中鈣(Ca)、氯(Cl)、硫(S)等礦物元素,特別是鉀(K)的含量通常較高[1]。在其熱利用過程中K的氣相釋放會造成嚴重的換熱面積灰、結渣、腐蝕、顆粒物生成等問題[2-3]。另一方面,K對生物質的熱解、氣化和燃燒具有重要的催化作用[4-7]。因此,研究生物質熱利用過程中K的遷移規律和機理具有重要意義。
研究表明,K在生物質中的賦存形式、熱處理溫度、熱轉化氣氛以及礦物元素對K的釋放都有重要影響[8-13]。例如,當溫度低于700℃時,只有少量K(<10%)釋放到氣相中;當溫度高于700℃時,K的釋放比例隨溫度的增加而明顯增加[9-10]。葉家銘等[12]在相同溫度下進行小麥秸稈的熱解和燃燒實驗,發現氧化性氣氛促進了K的氣態釋放。Knudsen等[10]研究了6種不同的草本生物質燃燒時K的釋放規律,發現Cl會促進K的釋放而硅(Si)對K的釋放具有明顯的抑制作用。
在前人研究基礎上,有學者總結了生物質熱轉化過程中K可能的遷移路徑[3,14-15]。首先,K以無機形式和有機形式存在于原始生物質中。在生物質脫揮發分階段,部分有機K可能以小分子有機K或K原子的形式釋放到氣相中,其余的有機K會轉化為生物質焦中更穩定的有機K(簡稱為char-K)。KCl會與生物質中官能團發生置換反應,釋放出HCl等含氯化合物的同時生成char-K[9,16-17]。在高溫下脫揮發分及生物質焦熱轉化過程中,KCl等無機K會發生氣相釋放,char-K也可能發生直接氣相釋放。在燃燒或氣化氣氛下,隨著生物質焦有機結構的破壞,char-K除可能直接釋放外,也有可能轉化為K2CO3[3]。對于富含Si的草本生物質,K還會與Si反應生成難溶硅酸鹽[14]。
由于原始生物質及生物質焦中K賦存形式多樣,目前尚無法對其中K的賦存形式進行直接的定量測量,導致某些遷移途徑的提出主要基于相關研究推斷,缺乏直接的證據支持。同時,由于前人研究使用的實驗原料和實驗條件差異較大,難以對不同賦存形式K的不同遷移路徑和影響因素進行定量分析。為進一步探究不同賦存形式K的遷移特性和機理,有必要簡化實驗條件,排除其他形式K以及Ca、Si等礦物質元素的干擾。Anicic等[18-19]已使用簡單的無機K化合物進行熱轉化實驗,探究了不同形式無機K(如KCl、K2CO3)的氣相釋放和固相轉化特性。另一方面,char-K是生物質焦中K的重要存在形式,但其在不同熱轉化過程中的氣固相遷移特性仍缺乏直接研究。使用不含礦物質且有機組成簡單的生物質模型化合物有利于對生物質焦中char-K的遷移進行直接觀測。
纖維素是生物質中重要的組成成分,其質量分數可占到生物質有機組成的20%~60%。已有研究證明負載KCl的纖維素在高溫下熱解后的焦中只存在char-K和KCl兩種賦存形式,而其中KCl的含量可以通過測量Cl的含量確定,進而可以確定纖維素焦中char-K的含量[20],因此,本文使用負載KCl的纖維素進行實驗,使用固定床制備了800~1000℃下Ar熱解和O2反應氣氛下不同熱處理時間的固相樣品,通過對固相樣品的定量分析獲得了K的動態釋放比例,并討論了兩種氣氛下char-K的遷移特性和遷移途徑。
1 實驗系統與方法
1.1 實驗原料
使用購買自Sigma-Aldrich的微晶纖維素(CAS號:9004-34-6)作為原料。首先篩分出粒徑在38~74μm范圍內的顆粒,然后用去離子水浸泡3h后沖洗除去可溶性雜質。通過浸漬法負載KCl:稱取20g纖維素和2.5g KCl,置于500mL的燒杯中,加入250mL去離子水,攪拌4h;靜置后除去上清液,將殘留的漿液放入60℃潔凈烘箱中烘干。按照上述方法制備三次樣品,并最終將樣品混合均勻,密封備用。K的負載量通過電感耦合等離子體發射光譜(ICP-AES,Thermo Elemental,USA)測 得,為1.18%,Cl的負載量通過離子色譜(IC,Metrohm761,Swit)測得,為1.06%,K和Cl的含量與典型的草本生物質(如稻稈)中的含量接近[11]。
1.2 實驗裝置
搭建了如圖1所示的固定床實驗系統進行實驗。反應器由內徑為30mm的石英外管與內徑為25mm的石英內管組成,并通過三段電阻爐加熱。石英內管上裝有一可移動的石英托盤,置于電阻爐恒溫區內。內徑為23mm,高度為13mm的鉑金坩堝放在石英托盤上,樣品放置在鉑金坩堝內。石英外管尾部裝有水冷壁,用來快速冷卻樣品。

圖1 固定床實驗系統示意圖
實驗在800~1000℃進行,采用0.5L/min的Ar模擬熱解氣氛進行熱解實驗,采用0.5L/min的O2/Ar混合氣模擬O2反應氣氛進行氧化實驗。氧化實驗中通過調節氧氣濃度來保證不同溫度下纖維素焦的反應速率基本相同,以排除熱處理時間的干擾,方便對不同溫度下K釋放的實驗結果進行對比。通過前期調試,最終800℃、900℃、1000℃時氧氣體積分數分別選擇為3.2%、1.8%、1.3%。選擇低氧氣濃度是為了準確控制樣品溫度,防止溫度因纖維素焦快速氧化放熱而提高,同時可以延長反應時間,方便中間過程取樣。
1.3 實驗方法
(1)Ar熱解氣氛下樣品制備 反應器溫度達到設定溫度后,用2.5L/min的Ar吹掃反應器30min,然后將裝有750mg纖維素顆粒的石英托盤與鉑金坩堝放入恒溫區,將Ar流量調為0.5L/min。當達到設定的熱解時間后,將裝有樣品的石英托盤與珀金坩堝迅速移至水冷壁,并用5L/min的Ar吹掃冷卻至室溫。稱重,收集纖維素焦樣品以待后續分析。
Ar熱解氣氛下纖維素焦轉化率按式(1)計算。

式中,mc,t表示熱解t時間的樣品質量;m0表示初始纖維素質量。
(2)O2反應氣氛下樣品制備 900℃和1000℃下,當纖維素熱解60min后,將氣體切換為O2反應氣氛。由于800℃時纖維素焦熱解超過150min后K仍持續釋放,為了制備800℃氧化后的樣品以分析char-K的遷移規律,采用在900℃熱解60min后的纖維素焦在800℃進行氧化實驗。氧化時間達到設定值后,將樣品冷卻,稱量并收集。
纖維素焦轉化率按式(2)計算。

式中,moxy,t表示氧化t時間的樣品質量;mc,60表示熱解60min得到的纖維素焦樣品質量。
1.4 分析方法
為了獲得兩種氣氛下K的氣相釋放比例,測量了原始纖維素及所得固相樣品中K和Cl的含量。
對于負載KCl的纖維素和熱解得到的樣品,取50mg樣品使用微波消解儀(Berghof SpeedWave4,German)在210℃加壓消解30min,消解液使用9mL HNO3和1mL H2O2的混合溶液,消解后將溶液定容至100mL。對于O2反應氣氛下制備的樣品,每次制樣后將所有固體樣品轉移至微波消解儀內進行消解,消解條件與上面相同,同時將坩堝在20mL HNO3中浸泡3h,最后將兩處溶液合并,定容至200mL。所得溶液過濾后使用ICP-AES測量其中K的濃度。
為了測量固相樣品中Cl的含量,按照ASTM D4208—13標準使用氧彈燃燒法制備溶液,每次測量時使用400mg纖維素或100mg焦樣品,收集的溶液通過離子色譜測量其中Cl的含量。
熱解樣品中K和Cl的釋放比例Rpy通過式(3)進行計算。

式中,wc,t,M表示熱解t時間后樣品中K或者Cl的質量分數;w0,M表示原始纖維素中K或者Cl的質量分數,M=K,Cl。
氧化過程中K的釋放比例Roxy通過式(4)計算。

式中,woxy,t表示氧化t時間后樣品中K的質量分數;wc,60,K表示熱解60min后纖維素焦中K的質量分數。
為分析K在固相中的賦存形式,使用X射線衍射儀(XRD,S2,Japan)分析了800℃下纖維素焦氧化后所得灰分中K的晶體結構。所有樣本的掃描范圍為10°~90°(2θ),分辨率為0.02°。
2 結果與分析
通過對不同熱解和氧化時間后得到的固相樣品進行分析,獲得了熱解和氧化過程中纖維素焦中K的動態釋放規律,并討論不同氣氛下char-K的遷移特性和遷移途徑。
2.1 熱解過程中K和Cl的氣相釋放
圖2給出了負載KCl的纖維素在800~1000℃熱解時K和Cl的釋放比例以及纖維素焦產率隨熱解時間的變化關系。通過對大部分熱解時間的樣品進行重復性實驗發現,實驗誤差在2%以內。在800℃熱解10min、900℃熱解5min以及1000℃熱解3.5min后,纖維素焦產率幾乎不發生變化,因此可以認為脫揮發分過程已經結束,可以將后續熱解過程作為纖維素焦熱解階段。可以看出,在不同溫度下Cl的釋放比例都明顯高于K的釋放比例,但K和Cl的釋放比例隨時間的變化規律有差異。

圖2 負載KCl的纖維素熱解過程中K和Cl的釋放比例以及焦產率隨時間的變化
800℃時,在熱解前10min,Cl的釋放比例達到了50%,而K的釋放比例只有10%左右;從10min到150min,K和Cl的釋放比例隨熱解時間均先快速后緩慢增加。900℃時K和Cl的釋放速率明顯提高,在熱解5min后,Cl的釋放比例達到了80%,熱解20min后,幾乎所有的Cl都釋放到氣相中;K的釋放比例在熱解5min時達到23%左右,然后隨熱解時間增加而明顯增加,到60min時基本穩定在70%左右。1000℃時,K和Cl的釋放速率進一步增加,在熱解3.5min后,幾乎所有的Cl都釋放到氣相中,而K的釋放比例為49%左右;隨后K的釋放比例隨熱解時間增加而增加,在15min時達到71%,之后基本維持不變。
在800℃的前10min、900℃的前5min以及1000℃的前3.5min,Cl的釋放量遠高于K的釋放量,這是因為在脫揮發分階段KCl與纖維素中有機官能團發生反應,大量的Cl以HCl或tar-Cl的形式釋放出來,在此不作詳細介紹。下面主要對纖維素焦熱解階段char-K的釋放進行分析。
之前的研究已經證明在負載KCl的纖維素熱解后生成的纖維素焦中,K主要以KCl和char-K兩種形式存在,K2CO3的含量可以忽略;Cl則主要以KCl的形式存在(高溫下char-Cl的含量可忽略)[20-21]。在纖維素焦熱解階段,Cl會以KCl形式釋放,而K的釋放存在char-K和KCl的釋放兩種途徑。
從圖2可以看出,在三個溫度下纖維素焦熱解的不同時間段內,K和Cl的釋放比例不完全相同。在800℃熱解30min以后的各時間段內,K的釋放比例都略高于Cl的釋放比例。而900℃和1000℃時,這一趨勢更明顯。在900℃熱解5min后,在相同時間段內K的釋放比例明顯比Cl高;當Cl全部釋放后,仍有少量K發生氣相釋放。最終在5~150min內,Cl的釋放比例只有約20%,而K的釋放比例達到46%左右。在1000℃熱解3.5min時,Cl已經幾乎完全釋放,而在3.5~150min內,仍有大約22%的K釋放到氣相中。在纖維素焦熱解階段,K的釋放比例高于Cl的釋放比例,說明有明顯的char-K分解釋放。
在纖維素焦熱解階段,K的釋放比例減去KCl的釋放比例(即Cl的釋放比例)即為char-K的釋放比例。如圖3所示。從圖中看出,隨著熱解溫度升高,char-K的釋放速率明顯增加,且900℃和1000℃時char-K的釋放比例明顯高于800℃。在800℃時,從30min開始,char-K的釋放比例隨時間增加而增加,在150min時達到約12%。在10~30min內,Cl的釋放量略高于K的釋放量,這應該是由于仍有少量Cl以HCl等(由KCl與剛生成的纖維素焦中殘留的官能團反應生成)形式釋放的原因,因此無法通過差減法確定在這一時間段內char-K的釋放比例。在800℃熱解150min后,char-K的釋放比例仍在增加。本實驗將800℃下熱解時間延長至300min后(未在本圖中列示),char-K的釋放比例穩定在22%左右。在900℃時,從5min開始即有明顯的char-K釋放,在60min時釋放比例達到27%左右,且隨時間幾乎不再增加。1000℃與900℃相比,char-K的釋放速率進一步增加,在15min左右即達到穩定,最終釋放比例在21%左右。
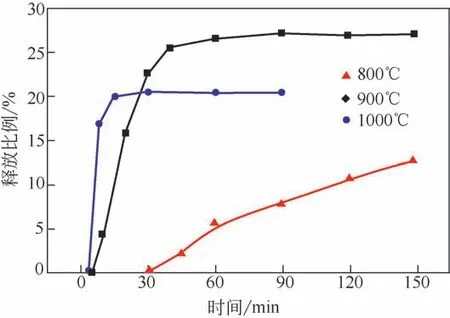
圖3 不同溫度下纖維素焦熱解階段char-K的釋放比例隨熱解時間的變化
1000℃與900℃相比,纖維素焦熱解階段char-K的釋放比例略低,這可能是由于在1000℃時K的釋放速率更快,更多的char-K在前3.5min釋放到氣相中。但由于此階段Cl除了以KCl外,還會以HCl等形式釋放,而K則以char-K和KCl兩種形式釋放,因此無法確定KCl和char-K的釋放比例。從圖2可以看出,900℃時前5min Cl的釋放比例比K高57%,而1000℃時前3.5min Cl的釋放比例只比K高49%。而根據已有研究推測,在不同溫度下脫揮發分階段以HCl等形式釋放的Cl的量基本相同,因此該結果也說明1000℃時更多的有機K在此階段釋放,導致Cl與K釋放比例的差值更低[9]。
以上實驗結果表明高溫下纖維素焦熱解過程中,char-K自身會發生明顯的氣相釋放。而在900℃和1000℃熱解后期,char-K的釋放比例隨熱解時間不再增加,都有接近30%的char-K殘留在固相中。而800℃下熱解300min后,固相中char-K的比例也穩定在30%左右。這說明纖維素焦中有明顯比例的char-K非常穩定,在Ar熱解氣氛下不會發生氣相釋放,而不同溫度下這部分char-K的數量接近,超過初始纖維素焦中char-K總量的一半。不同char-K穩定性的差異應該和與K結合的有機官能團的種類有關,但其具體的結合形式還有待進一步研究。
2.2 纖維素焦氧化過程中K的氣相釋放
為明晰O2反應氣氛對char-K遷移的影響規律和作用途徑,需排除KCl和自身較活躍的char-K釋放的影響,因此選擇熱解氣氛下K的釋放達到穩定后的纖維素焦樣品進行氧化實驗。由圖2可知,在900℃和1000℃熱解60min以上,纖維素焦中的KCl已經完全釋放,并且纖維素焦中的char-K已經達到穩定,因此可以排除KCl和char-K自身釋放的干擾,從而定量研究氧化過程對char-K遷移的影響。由于在800℃時,K的釋放需要很長時間才能穩定,而本研究只要求初始樣品中只含有穩定的char-K,不考慮其他變量,因此也使用900℃熱解60min的纖維素焦在800℃進行氧化實驗。對大部分反應時間的樣品都進行了重復性實驗,除反應時間為60min的實驗點誤差在6%左右,其余實驗點誤差控制在4%以內。
圖4表示了纖維素焦在O2反應氣氛下熱處理120min后(纖維素焦已經被完全氧化),K的釋放比例隨溫度的變化關系。從圖中可以看出,800℃時K的釋放比例低于5%。隨著溫度的增加,K的釋放比例明顯增加,1000℃時,接近95%的K都釋放到氣相中。由于纖維素焦中的char-K已經非常穩定,繼續熱解時不會發生直接的斷鍵釋放。因此,此實驗結果表明O2反應氣氛明顯促進了char-K的氣相釋放,并且隨著溫度的增加,促進作用越明顯。

圖4 不同溫度下纖維素焦氧化120min后K的釋放比例
前人猜測,氧化性氣氛可能通過兩種途徑促進char-K的釋放:一是通過破壞纖維素焦有機結構而直接釋放出K;二是隨著纖維素焦有機結構的消耗,char-K轉化為K2CO3,進一步發生氣相釋放[3,22-23]。為了探究氧化過程中char-K的遷移途徑,測量了900℃和1000℃下K的釋放比例隨時間的變化關系。
圖5表示了900℃和1000℃纖維素焦轉化率和K釋放比例隨時間的變化關系。從圖中可以看出,在900℃和1000℃,通過調整氧氣的濃度,纖維素焦的轉化率隨時間的變化關系幾乎一致。在前80min,纖維素焦轉化率隨熱處理時間幾乎成線形關系,80min時纖維素焦轉化率幾乎達到100%,80~120min為灰分受熱階段。

圖5 纖維素焦轉化率和K的釋放比例隨時間的變化關系
900℃時K的釋放比例隨時間先緩慢增加后快速增加。在0~40min,K的釋放比例大約為5%;在40~80min,K的釋放比例為18%左右;在80~120min灰分受熱階段,K的釋放比例為23%左右;最終K的總釋放比例達到46%。在1000℃時,K的釋放速率比900℃時有明顯提高,釋放比例也隨時間呈現先緩慢增加后快速增加的趨勢,在前40min,K的釋放比例不到10%,在40~80min,K的釋放比例為52%左右,當纖維素焦完全氧化(80~120min)后,仍有約33%的K釋放到氣相中,最終K的釋放比例達到95%。
如果氧化過程通過破壞纖維素焦結構而促進char-K中的K直接氣相釋放,則K的釋放速率應與纖維素焦轉化率成正比。當纖維素焦完全氧化后,應該所有的char-K也會被釋放到氣相中。而在本實驗中,K的釋放速率明顯低于纖維素焦的氧化速率,當纖維素焦完全反應后,仍有明顯的K留在灰分中,且進一步熱處理灰分中仍有明顯的K釋放。因此,O2反應氣氛下K的釋放應該是通過char-K先轉化為K2CO3,然后發生進一步釋放。由于K2CO3的熔點為898℃,O2反應氣氛下K的釋放比例隨溫度的變化關系也與K2CO3的釋放特性一致[24-25]。由于char-K轉化為K2CO3的量應正比于纖維素焦的轉化率,因此當纖維素焦轉化率較低時,生成的K2CO3的量較少,K的釋放速率也較低。隨著纖維素焦氧化過程的進行,生成的K2CO3在固相中逐漸累積,導致K的釋放速率也逐漸增加,這與圖中K的釋放速率隨時間的變化趨勢是一致的。
圖6展示了纖維素焦在800℃完全氧化后所得灰分的XRD譜圖。可以看出,纖維素焦氧化后的灰分中,含有明顯的K2CO3和K2CO3·1.5H2O的晶體峰形,也說明纖維素焦氧化后char-K轉化為了K2CO3。

圖6 纖維素焦在800℃氧化后所得的灰分的XRD譜圖
需要說明的是,本實驗使用的模型化合物與真實生物質組成存在較大差異。在實際生物質熱轉化過程中,其他有機組分(如半纖維素、木質素)生成的char-K性質很可能與本研究存在差異,且生物質中無機組成(如Si、Ca)也會對K的遷移產生影響,這需要后續逐步深入的研究。
3 結論
本文以負載KCl的纖維素為原料,在Ar熱解和O2反應氣氛下進行熱轉化實驗,獲得了熱解和氧化過程中纖維素焦中char-K的遷移特性。在800~1000℃熱解過程中,纖維素焦中都有部分char-K發生氣相釋放,釋放速率隨溫度提高而增加,但最終也有部分char-K留在固相中。在氧化過程中,char-K首先轉化為K2CO3,然后在900℃以上時發生氣相釋放。

