深層溫壓條件下有機酸熱穩定性模擬研究
——以乙酸和乙二酸為例
李靖,李源遽,李朋朋,4,周世新,陳克非,4,張臣,4,孫澤祥,4
1.中國科學院西北生態環境資源研究院,蘭州 730000
2.甘肅省油氣資源研究重點實驗室,蘭州 730000
3.北京大學深圳研究院,廣東深圳 518000
4.中國科學院大學,北京 100049
0 引言
隨著經濟的迅速發展,我國油氣資源的需求量日益增大,而原油產量增長緩慢。近五年我國原油年產量保持在2億噸左右,但原油的消費量逐年增加,2019年我國原油對外依存度已超過70%[1]。從國家能源安全的角度出發,同時考慮淺層油氣可采資源量日漸殆盡且抽采率低的現狀,迫切需要面向深層—超深層尋找油氣資源;而超深井鉆井及超高溫鉆井液技術等工程技術的突破為向深層—超深層進行油氣資源勘探提供了條件[2]。
深層是一個比較籠統的概念,由于不同含油氣盆地地溫梯度、儲層孔滲特征、勘探目的層系不同,對深層的定義也不相同[3?5]。目前國際上相對認可的深層標準是其埋深大于等于4 500 m[2];我國國土資源部發布的《石油天然氣儲量計算規范》將埋深為3 500~4 500 m的地層定義為深層,埋深大于4 500 m的地層定義為超深層[6]。
一般認為,隨著埋深的增加,上覆巖層壓實作用和膠結作用增大,孔隙度和滲透率逐漸減小。然而,鉆井巖芯鏡下觀測、地震資料解釋等顯示,在深層—超深層(埋深大于3 500 m)部分層段仍存在異常高孔隙度發育區,這與次生孔隙的大量發育密切相關[7?8]。深層、超深層的異常高孔隙度發育區為油氣成藏提供了條件,因此研究深層條件下儲集層次生孔隙的形成機制對深層—超深層油氣的勘探有著重要的意義[2,7?8]。前人研究表明,表生淋濾、熱循環對流和有機酸溶蝕作用均可在儲集層中形成一定規模的次生孔隙[9]。其中,有機酸溶蝕作用是儲集層中次生孔隙形成的重要機制,這與國內外許多盆地和地區(例如美國加利福尼亞州圣華金河谷地區、德克薩斯州科珀斯克里斯蒂地區和帕洛杜羅盆地、路易斯安那州西南部地區,我國塔里木盆地、柴達木盆地、渤海灣盆地)油田水中檢測到高濃度的有機酸的事實相吻合[7,10?11]。沉積盆地的水溶液中的有機酸種類非常豐富,包括一元和二元羧酸、氨基酸、苯酚、甲酚等,其中分布廣泛且濃度相對較高的一元和二元羧酸分別是乙酸和乙二酸[12]。關于有機酸的成因[13?15]、有機酸溶蝕礦物種類及效果[16?17],前人進行了大量的實驗研究,取得了諸多研究成果和認識。但對于深層、超深層中,由于埋深增加導致的溫度、壓力升高的情況下有機酸的熱穩定性及其影響因素,以往研究仍相對薄弱且存在一定爭議。
模擬實驗研究顯示,在溫度高達350℃時,有機酸 仍 可 穩 定 存 在[18?21]。McCollomet al.[18]分 析 了 不 同條件下乙酸的分解速率,發現即使在有強氧化劑(赤鐵礦)存在的情況下,乙酸的分解速率依然很低,因此不少學者認為在沒有較強的催化劑存在的地層中乙酸能保存相對較長的時間(大于五十億年)[18,22?23]。但部分沉積盆地的地質資料顯示只有在80℃~140℃地層水中的有機酸才具有較高的濃度,當溫度達到250℃時有機酸的濃度很低[24?27]。造成實際地質資料與室內實驗結果差異的原因可能是實際地質環境中除溫度外流體壓力、pH值、有機酸與礦物的反應等因素也會對有機酸熱穩定性產生影響。早期的研究者認為流體pH值越低,有機酸的分解速率越高[22?23],而McCollomet al.[18]則認為高pH值不一定會抑制乙酸的分解。此外,研究者對深層、超深層中高流體壓力和靜巖壓力對有機酸熱穩定性的影響關注度較低。
鑒于此,本文以油田水中具有代表性的一元和二元有機酸(乙酸和乙二酸)為例,通過模擬實驗,對兩者在深層高溫高壓條件的熱穩定性及其影響因素進行了分析,以期為深層—超深層儲集巖中有機酸賦存形式以及次生孔隙發育特征研究提供借鑒。
1 樣品與方法
1.1 實驗樣品
本次研究選擇的有機酸樣品為濃度為36%的乙酸(醋酸)試劑和乙二酸(草酸)固體顆粒,為配比得到不同pH值且具有相近有機酸根離子濃度的實驗溶液,研究中還使用了乙酸鈉(醋酸鈉)固體顆粒。乙酸試劑、乙二酸和乙酸鈉固體顆粒的純度級別均為分析純。在進行實驗前,利用煮沸處理的去離子水對乙酸、乙酸鈉和乙二酸進行配比,得到不同的實驗初始溶液,實驗初始溶液的pH值和有機酸根離子濃度見表1。實際地層中,有機酸對礦物的溶蝕作用會使pH值等流體特征發生改變,進而可能會對有機酸的熱穩定性產生影響。對于碎屑巖儲層來說,長石類礦物是最易與有機酸發生反應的礦物之一[25]。為探討可溶蝕礦物對有機酸熱穩定性的影響,同時考慮覆壓實驗礦物顆粒的支撐性,本次研究選擇了鉀長石礦物作為對比實驗的研究對象。實驗所使用的鉀長石礦物采集于中國甘肅北山地區的花崗偉晶巖。在去除花崗偉晶巖表面風化層后,初步破碎,篩選出鉀長石顆粒,然后磨碎、篩分出1 mm左右的顆粒作為后續實驗的反應物,其化學組成見表2。
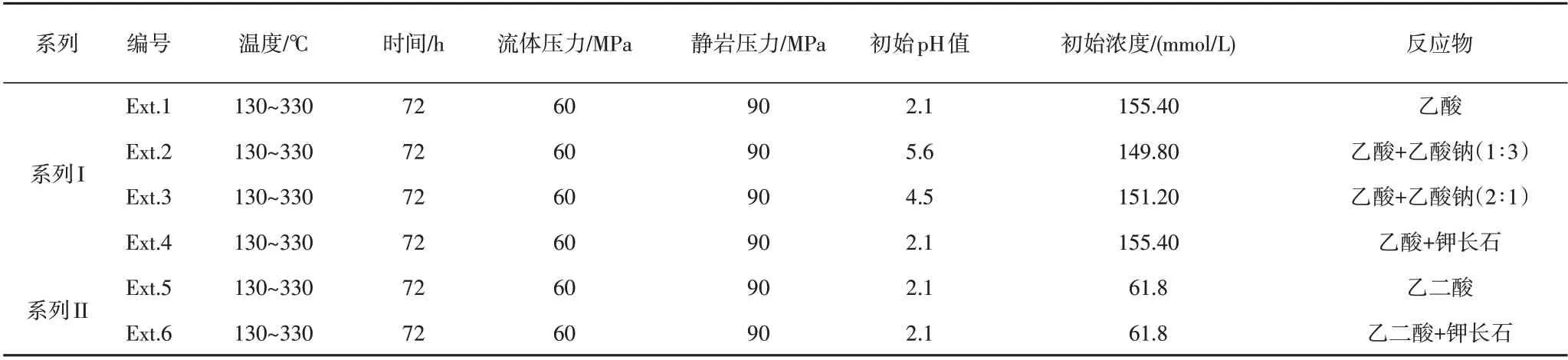
表1 模擬實驗的模擬條件Table 1 Simulated conditions for the experiments

表2 鉀長石化學成分Table 2 Chemical compositions of K?feldspar
1.2 實驗方法
本次研究利用WYMN?3型高溫高壓水—巖模擬儀進行模擬實驗。該裝置模擬環境為半開放系統;實驗中由流體壓力泵模擬流體壓力,由機械壓力系統模擬靜巖壓力。實驗裝置結構圖和實驗原理參見文獻[28]。基于靜水壓力梯度10 MPa/km、上地殼平均密度2.67 g/cm3、平均地溫梯度25℃/km、地表平均氣溫15℃等參數,按照國土資源部的定義,深層(埋深3 500~4 500 m)的流體壓力、靜巖壓力、地層溫度條件約為35~45 MPa、93.45~120 MPa、102.5℃~127.5℃;超深層(埋深大于4 500 m)的流體壓力、靜巖壓力、地層溫度條件約為>45 MPa、>120 MPa、>127.5℃。前人關于有機酸熱穩定性的研究多關注溫度的影響[18,22?23],對流體壓力、靜巖壓力的影響關注度較低。Liet al.[28]分析了流體壓力和靜巖壓力均為45 MPa條件下乙酸的熱穩定性,但其靜巖壓力低于深層條件;王慧媛等[29]分析了覆載壓力為143.4~1153 MPa時乙二酸的熱穩定性,但該研究中并未分析溶液pH值、可溶蝕礦物等對乙二酸熱穩定性的影響。因此,參照深層、超深層的溫壓條件,同時考慮支撐物的抗壓能力,本次研究選取的實驗溫度為130℃~330℃,實驗流體壓力為60 MPa,實驗靜巖壓力為90 MPa(表1)。本次研究共設計了兩個系列六組實驗(系列I包括Ext.1、Ext.2、Ext.3、Ext.4,系列II包括Ext.5、Ext.6),每組實驗包含130℃、180℃、230℃、280℃、330℃五個溫度點,每個溫度點模擬實驗獨立進行,模擬時間為72 h。實驗結束后分別收集氣體產物和實驗流體,并對氣體產物組分和流體中離子濃度進行測定。在Ext.1、Ext.2、Ext.3和Ext.5實驗中,樣品倉中裝入多孔濾片作為支撐物;在Ext.4和Ext.6實驗中,樣品倉中支撐物為鉀長石顆粒。實驗開始前,利用氮氣吹掃裝置對樣品倉中的空氣進行排除并抽真空,后注入實驗溶液開始實驗。實驗的升溫速率、模擬溫度、流體壓力、靜巖壓力、模擬時間等由儀器配套軟件自動控制。
實驗收集的氣體產物采用美國安捷倫公司制造的型號為6890N的氣相色譜儀進行測定,所采用的色譜柱為HP?PLOT?Q。模擬儀剩余流體中的離子濃度采用美國戴安公司制造的ICS3000型離子色譜儀進行測定。離子色譜儀的測試精度為0.1 mg/L,采用的色譜柱為Dionex As19?Ag19離子交換色譜柱。
2 實驗結果
對于系列I,當溫度低于180℃時∑乙酸濃度(乙酸和乙酸根的濃度總和)變化微弱,分解產物CO2和CH4的濃度幾乎為0(圖1)。當溫度從180℃上升到230℃,∑乙酸濃度略微下降,CO2和CH4濃度緩慢上升。對于系列I的Ext.1、Ext.2、Ext.3、Ext.4而言,當溫度小于230℃時∑乙酸濃度、CO2和CH4濃度變化幅度均非常小。當溫度高于230℃,∑乙酸濃度迅速下降,且隨著溫度繼續增加∑乙酸濃度降幅增大,相應乙酸分解的產物CO2和CH4濃度呈現升高的變化趨勢,這表明在該溫度區間乙酸迅速地發生分解反應。對于系列I的Ext.1、Ext.2、Ext.3、Ext.4而言,∑乙酸濃度降低幅度呈Ext.2>Ext.4>Ext.3>Ext.1,CO2和CH4濃度升高幅度也顯示出相同的變化規律。上述實驗現象表明溫度、pH值、鉀長石對乙酸的熱穩定性均有影響。
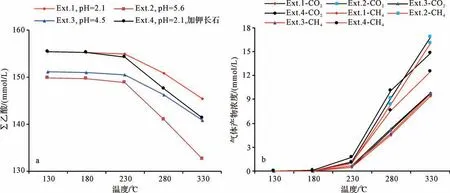
圖1 實驗系列I中乙酸與乙酸鹽總濃度(a)和氣體產物濃度(b)特征(∑乙酸:乙酸和乙酸根的濃度總和)Fig.1 Concentrations of acetate acid in series I experiments(∑acetic acid:total concentration of acetic acid and acetate):(a)acetate;and(b)gas products
系列II不同溫度條件下剩余流體離子濃度如圖2所示。∑乙二酸濃度(乙二酸和乙二酸鹽的濃度總和)隨著溫度變化呈現減小趨勢,但不同時間段降幅不同,其中溫度在180℃~230℃之間降幅最快,在130℃~180℃和230℃~330℃范圍內降幅較慢。當溫度低于180℃,乙二酸的分解速率較低,僅有不到10%的乙二酸發生了分解;180℃~230℃時,乙二酸的濃度明顯降低,50%~60%的乙二酸發生了分解;當溫度高于230℃時乙二酸濃度降幅再次變慢,可能歸因于反應體系中剩余反應物濃度低(小于初始濃度的20%)。當溫度高于180℃,乙二酸發生了大規模的分解反應,這與文獻[30]報道乙二酸發生分解反應的溫度一致。
在測試溫度的范圍內,加入鉀長石實驗Ext.6的∑乙二酸濃度始終低于不加鉀長石的相同條件實驗Ext.5(圖2),這表明Ext.6中乙二酸的分解速率更快,鉀長石的存在加速了乙二酸的分解。
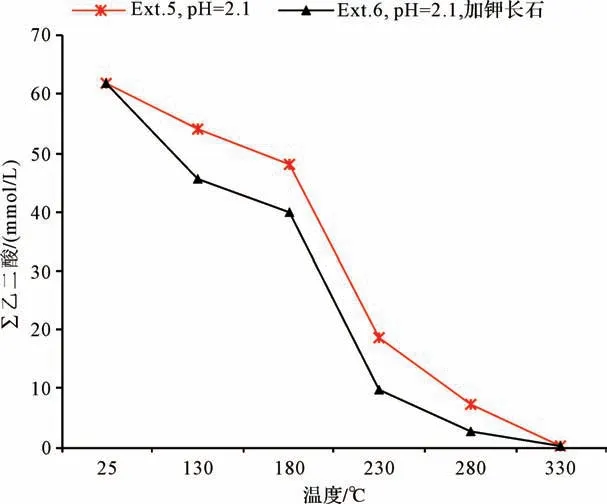
圖2 實驗系列II中乙二酸和乙二酸鹽總濃度特征(∑乙二酸:乙二酸與乙二酸鹽總濃度)Fig.2 Concentrations of oxalic acid and oxalate in series II experiments(∑oxalic acid:total concentration of oxalic acid and oxalate)
3 有機酸熱穩定性評價及影響因素分析
3.1 有機酸分解反應的動力學參數
3.1.1 反應速率
前人研究證實,有機酸的分解過程可以用一階函數表示[18],即:

式中:k為有機酸分解反應的反應速率常數,無量綱;t為反應時間,s;m為有機酸濃度,mmol/L。
對公式(1)進行積分可得公式(2):

式中:m0為有機酸初始濃度,mmol/L;mt為t時刻的有機酸濃度,mmol/L。
因此,利用有機酸濃度變化與時間的關系,可計算有機酸分解反應的反應速率k。
在高溫高壓模擬過程中,乙酸的分解途徑有兩種:脫羧反應(CH3COOH→CO2+CH4)和氧化反應(CH3COOH+2H2O→2CO2+4H4)[28]。由于氧化反應不生成CH4,利用實驗產物中CH4和CO2的濃度,可分別計算脫羧反應的反應速率常數kdecar和氧化反應的反應速率常數koxi。實驗產物CH4和CO2的濃度與乙酸初始濃度、時間和反應速率的關系如公式(3)和(4):

式中:mCH4為t時刻CH4的濃度,mmol/L;mCO2表示t時刻CO2的濃度,mmol/L;m0-CH4為CH4的初始濃度,mmol/L;m0-CO2為CO2的初始濃度,mmol/L。
由于在模擬實驗前,采用煮沸的去離子水稀釋乙酸和乙二酸,可以認為此時體系中沒有CH4和CO2,故假定t=0時,m0-CH4和m0-CO2為0。因此,利用有機酸、CH4和CO2濃度與時間的關系,可計算脫羧反應和氧化反應的反應速率常數。
乙酸分解反應的反應速率常數k、脫羧反應的反應速率常數kdecar、氧化反應的反應速率常數koxi與溫度的關系如圖3所示。對于每組實驗而言,隨著溫度的增加,k和kdecar先緩慢增加(溫度小于230℃)后迅速增加,而koxi呈先增大后減小的趨勢,在280℃達到最大值。這表明隨著溫度增加,乙酸分解反應和脫羧反應更加劇烈,而氧化反應則在280℃時最劇烈。
在乙酸的模擬實驗中,當溫度低于230℃時,分解反應總速率、脫羧反應速率和氧化反應速率均較小,可能是因為未達到脫羧作用和氧化作用的起始溫度,乙酸進行分解反應非常困難或非常緩慢。當溫度高于230℃,在相同的溫度條件下,具有更高初始pH值模擬實驗的反應速率更高(初始pH值Ext.2>Ext.3>Ext.1,反應速率呈相同序列降低)。而在相同初始pH值的條件下,加入鉀長石的模擬實驗Ext.4的分解速率明顯高于純乙酸溶解模擬實驗Ext.1。
乙二酸分解反應的總反應速率可由公式(2)計算獲得,其與溫度的關系如圖4。乙二酸的分解速率同樣隨著溫度的增加而顯著增加,表明溫度越高乙二酸分解反應越劇烈。在所測試溫度范圍內,加入鉀長石模擬實驗Ext.6的反應速率明顯高于無鉀長石模擬實驗Ext.5,表明實驗體系中鉀長石的存在可加快乙二酸的分解。

圖4 實驗系列II中乙二酸分解反應速率(k)與溫度的關系Fig.4 Series II experiments:relationship between temperature and determined rate constant k
乙二酸的分解反應的反應速率常數明顯高于乙酸,尤其在溫度高于180℃時,兩者差距可達2~3個數量級(圖3,4)。上述現象表明乙二酸的熱穩定性相對較差,更容易分解,這和油田水中觀測到的現象(乙酸的濃度明顯高于乙二酸)相吻合。
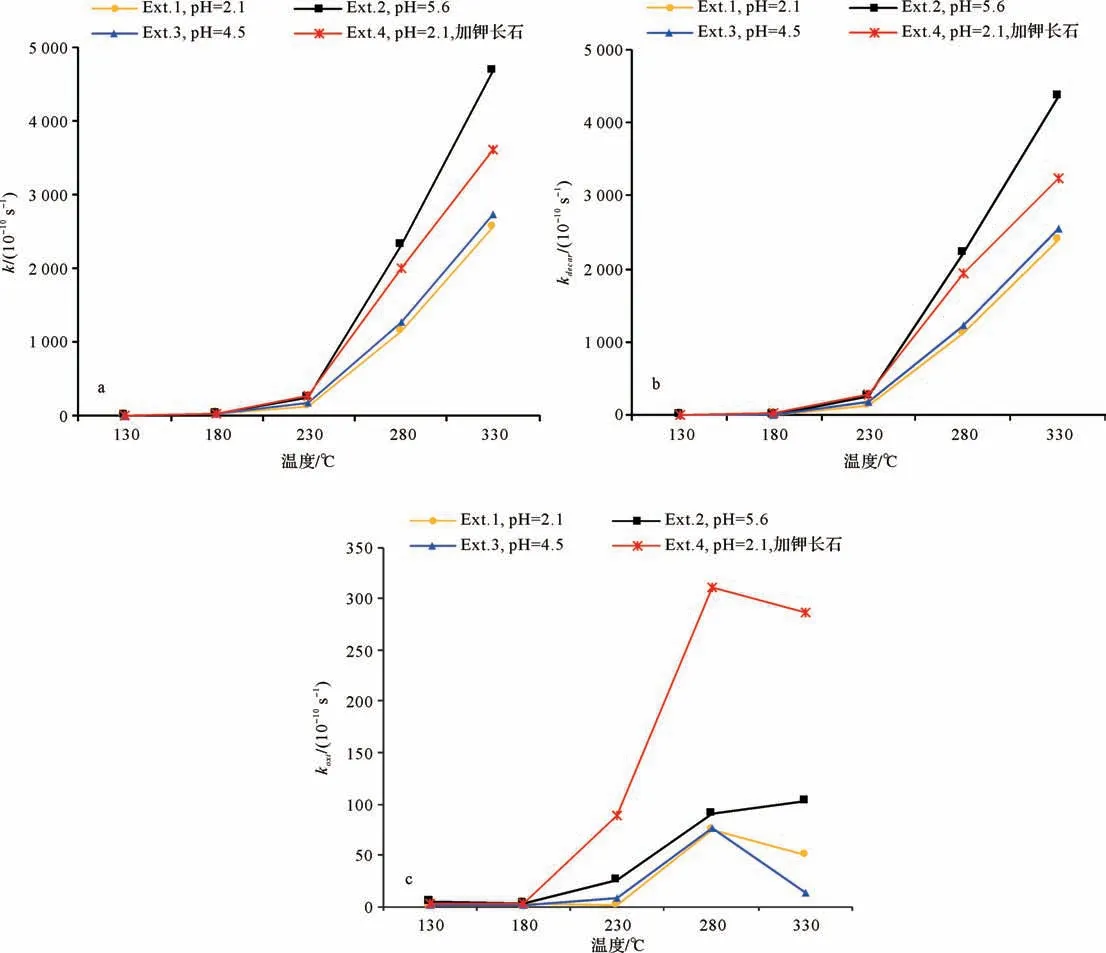
圖3 實驗系列I中分解反應速率k(a)、脫羧反應速率kdecar(b)、氧化反應速率koxi(c)與溫度關系Fig.3 Series I experiments:relationships between temperature and(a)determined rate constant k;(b)decarboxylation rate constants kdecar;and(c)oxidation rate constants koxi
3.1.2 活化能
基于實驗溫度和反應速率常數等參數,利用阿倫尼烏斯公式(5)可計算反應進行的活化能。

式中:A為指前因子,s-1;Ea為活化能,表征反應進行的難易程度,J/mol;T為絕對溫度,K;R為摩爾氣體常數,8.314 J/K·mol。
對公式(5)兩邊同時進行對數運算,可得公式(6):

對lnk和1/T進行線性擬合(圖5)后,擬合直線的截距為lnA,直線的斜率為?Ea。計算得到各組實驗有機酸分解的熱力學參數A和Ea見表3。對于系列I而言,Ext.1、Ext.2、Ext.3、Ext.4的Ea值相差不大,這表明pH值與鉀長石的加入對乙酸分解反應進行的難易程度影響較小,四組實驗乙酸經分解反應后濃度不同與不同實驗條件下反應速率有密切關系。對于系列II而言,有鉀長石存在的模擬實驗(Ext.5)的Ea值高于不加鉀長石乙二酸模擬實驗(Ext.6),表明鉀長石降低了模擬實驗中乙二酸的分解難度。

表3 有機酸分解的動力學參數Table 3 Kinetic parameters for organic acid decomposition
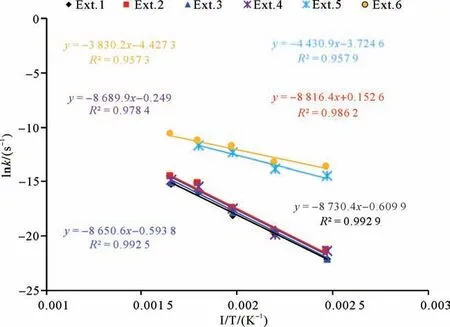
圖5 有機酸熱穩定性實驗中ln k與1/T的關系Fig.5 Relationship between ln k and 1/T in experiments
系列I的Ea值明顯高于系列II,這也和實驗現象相吻合。當溫度低于230℃,乙酸進行分解反應非常困難,乙酸的剩余濃度幾乎無變化,而此條件下,乙二酸發生分解反應的現象顯著,其濃度明顯減小;當溫度高于230℃,乙酸達到分解反應的Ea,乙酸分解反應迅速進行,濃度急劇下降。
3.2 乙酸和乙二酸熱穩定性的影響因素
3.2.1 溫度
活化能Ea反映一個特定的反應能夠發生必須跨越的能峰(最小能量),通常不會隨著溫度的變化而變化。化學反應能否發生取決反應物之間是否存在有效碰撞(活化分子之間的碰撞)。當溫度低于反應起始溫度時,反應體系中活化分子比例低,無法形成有效碰撞,故反應無法進行。當溫度高于反應起始溫度,反應體系中活化分子的比例增加并形成有效碰撞,化學反應發生。當溫度繼續升高,反應物分子活動更為劇烈,有效碰撞頻率迅速增加,進而反應速率常數隨之增加。對于系列I而言,當溫度低于230℃,乙酸分解反應所需的Ea未達到,盡管反應物的碰撞頻率隨著溫度升高而增加,但并未形成有效碰撞,故反應速率常數相對較小。當溫度大于230℃,反應體系中活化分子比例增加,形成有效碰撞,乙酸根離子中兩個碳原子之間的共價鍵發生異裂,乙酸分解反應順利進行。溫度越高,分子活動越劇烈,乙酸根離子中兩個碳原子之間的共價鍵發生異裂的可能性也就越大,故乙酸分解反應速率常數隨著溫度的升高而急劇增加(圖3)。對于系列II而言,乙二酸分解反應速率常數隨溫度升高呈現出相似的變化趨勢。因此,有機酸分解存在特定起始溫度,根據本次研究的實驗結果,乙酸和乙二酸大規模分解的起始溫度分別為230℃和180℃。當達到分解反應的起始溫度后,隨著溫度升高,乙酸和乙二酸的分解速率顯著升高;而相同溫度下,乙二酸的分解速率比乙酸高2~3個數量級。
3.2.2 pH值
實驗Ext.1、Ext.3、Ext.2中,初始反應溶液具有相近的乙酸根離子濃度,而初始pH值依次升高(表1)。三組實驗計算得到的活化能Ea(72.58 kJ/mol、71.92 kJ/mol、73.30 kJ/mol,表3)較為接近,而反應速率則有明顯的增大趨勢(圖3),表明反應體系中溶液的pH值對乙酸的分解難度(活化能)影響較小,而對乙酸分解反應速率影響較大。高pH值的實驗溶液體系中,乙酸的分解速率較高。大部分脫羧反應屬于離子型反應歷程,即羧酸先離解生成羧酸根負離子和氫離子,隨后羧酸根離子與烷基相連的C-C共價鍵斷裂,生成烴基負離子并放出CO2,最后烴基負離子獲得氫離子形成烷烴使反應完成[30]。乙酸屬于弱酸,在溶液中不能完全電離;通常pH值低的溶液中氫離子濃度較高,抑制了乙酸分子的電離,使游離的乙酸根離子濃度降低,進而降低了乙酸脫羧反應的反應速率。
3.2.3 壓力
Liet al.[28]探討了不同流體壓力和靜巖壓力組合對乙酸熱穩定性的影響,結果顯示高流體壓力和靜巖壓力均會降低乙酸的分解速率,而且靜巖壓力的影響更為顯著。王慧媛等[29]采用水熱金剛石壓腔高溫高壓模擬裝置對不同溫度、壓力條件下乙二酸的脫羧反應進行了研究,結果顯示隨著流體壓力升高,乙二酸脫羧反應發生的溫度逐漸升高(反應發生的溫壓條件為224.95℃/381.9 MPa、237.45℃/616.7 MPa、279.85℃/1 153 MPa),表明高壓流體的可以顯著提高乙二酸分解反應發生的溫度。此外,本次乙酸熱穩定性模擬實驗所采用的流體壓力和靜巖壓力分別為60 MPa和90 MPa,計算得到的在280℃和330℃條件下乙酸分解反應速率分別為1.3×10-8s-1和11.6×10-8s-1,明顯低于Liet al.[28]利用相同實驗溶液、在相同溫度、較低流體壓力(45 MPa)和靜巖壓力(45 MPa)模擬得到的乙酸分解反應速率(4.1~6.0×10-8s-1和51~59×10-8s-1)。因此,高的流體壓力和靜巖壓力均會抑制乙酸和乙二酸的分解,在提高有機酸分解反應起始溫度的同時降低分解反應速率。
3.2.4 鉀長石
在乙酸熱穩定性模擬實驗中,Ext.1和Ext.4的初始反應溶液具有相同的pH值和乙酸根離子濃度(表1),Ext.4中加入了鉀長石礦物。兩組實驗中乙酸根離子濃度均于230℃開始明顯下降(圖1a),但加入鉀長石的實驗Ext.4中乙酸根離子分解速率更快(圖3a),表明鉀長石的存在對乙酸分解反應發生的起始溫度影響較小,但會顯著提高乙酸的分解速率。鉀長石作為一種穩定且廣泛分布的鋁硅酸鹽可以與乙酸溶液中的氫離子發生反應,升高反應流體的pH值,從而增加反應體系中乙酸根離子濃度,使乙酸脫羧反應速率升高。本次研究的實驗數據也證實了這一點,從圖3b中可以看出,當溫度高于230℃時加入鉀長石礦物實驗Ext.4的脫羧反應速率明顯高于未加入鉀長石實驗Ext.1。此外,Ext.4實驗的氧化反應速率同樣明顯高于Ext.1,表明鉀長石的存在同樣促進了乙酸(鹽)氧化反應的發生。
在乙二酸模擬實驗中,Ext.5和Ext.6的初始反應溶液具有相同的pH值和乙二酸根離子濃度(表1),加入鉀長石模擬實驗Ext.6的活化能Ea(31.84 kJ/mol)略微低于無鉀長石實驗Ext.5(36.83 kJ/mol,表3),且Ext.6的反應速率更高(圖4)。以上現象表明鉀長石可能作為正催化劑略微地降低了乙二酸分解反應的難度;同時鉀長石同樣提高了乙二酸的分解速率,其機理可能與對乙酸分解反應的影響機理相同。
4 地質意義
儲集層次生孔隙的發育為油氣成藏提供了有利條件。大量鉆井取芯樣品的鏡下觀測、實驗研究和地震資料解釋已證實深層、超深層存在次生孔隙發育區[2,7?8],而有機酸溶蝕作用是其主要成因之一[9]。分析高溫、高壓條件下有機酸的分解機制可以深入理解深層、超深層中的流體特征變化,而探討利于有機酸保存的地層條件可以為深層、超深層油氣勘探提供支持,因此評價深層、超深層條件下有機酸的熱穩定性及其影響因素具有理論和實踐雙重意義。
隨著埋深的增加,儲集層的溫度和壓力均會增加。在上覆巖層壓實作用下儲集層的原生孔隙空間迅速減小。此時儲集層中流體因壓實作用被分隔開,導致其流動性變差,同時有機質生烴作用使流體總量增加,從而造成地層孔隙中流體壓力高于靜水壓力,即超壓現象。世界上許多地質實例已證實某些盆地或層段存在超壓現象,包括歐洲北海盆地、美國猶他盆地、印尼馬哈甘三角洲、美國倫巴德盆地、非洲剛果盆地等[31?34]。前人研究顯示,超壓的發育會抑制有機質的演化。付小東等[35]利用溫—壓雙控模擬儀開展生烴模擬實驗發現,高靜巖壓力和流體壓力可延遲成熟階段原油的生成并延緩過成熟階段原油向烴類的轉化。Haoet al.[36]基于有機質熱演化過程中的體積膨脹效應和產物濃度變化速率揭示了超壓對有機質演化的抑制作用。Carret al.[37]基于熱力學第一定律提出超壓的存在使有機質演化過程中烴類的生成需要額外克服一定的水壓做功,進而提高反應所需的活化能。Ugunaet al.[38?39]也支持該觀點,并提出有機質演化過程中生成的液態產物壓縮系數小且黏度大,其受到超壓的抑制作用相比氣態產物更加明顯。原油和有機酸碳同位素對比以及有機酸模擬實驗結果顯示,有機酸的主要來源可分為兩種:有機質生烴過程中的熱降解作用[14]和烴類的水解作用[13]。有機質生烴的延遲對上述兩類反應都有滯后的作用。因此,在超壓環境下有機酸可在更大的埋深下生成,為次生孔隙的發育和油氣成藏提供條件。
盡管深層、超深層中的高地層溫度會加速有機酸的分解,但其高靜巖壓力和流體壓力能在提高有機酸分解反應起始溫度的同時降低分解反應速率,為有機酸的保存提供條件。雖然鉀長石礦物和實驗體系的高pH值會加速有機酸的分解,但其對有機酸分解反應的起始溫度影響甚微。基于本次研究的實驗結果,在靜巖壓力為90 MPa、流體壓力為60 MPa的條件下,當溫度達到230℃時乙酸仍能大量存在。以我國塔里木盆地為例,其現今平均地溫梯度為20℃/km[40],230℃對應的埋深約為10 750 m;雖然此等埋深條件下,地層的靜巖壓力和流體壓力均顯著高于本次研究的實驗條件,但高的靜巖壓力和流體壓力對有機酸的保存更為有利。因此推測,塔里木盆地深度達10 000 m的地層中有機酸仍能穩定存在,為該盆地深層、超深層優質儲層的形成提供條件。而塔里木盆地塔深1井的鉆探實踐證實:在井深8 408 m處存在溶蝕孔洞并有油氣顯示[2]。深層、超深層的高壓環境可以使有機酸穩定保存,使深層、超深層發育優質儲層、乃至形成工業性油氣藏成為可能。
5 結論
(1)在相同的溫壓條件下,乙二酸分解反應所需的活化能比乙酸低大約40 kJ/mol,且乙二酸分解反應的反應速率常數比乙酸高2~3個數量級。表明乙二酸比乙酸更容易分解,且分解反應的速率更高。當溫度分別高于180℃和230℃,乙二酸和乙酸發生明顯的分解反應。乙酸和乙二酸分解反應的反應速率常數隨著溫度的增加而急劇增加。
(2)脫羧反應是有機酸分解的主要反應過程,屬于離子型反應歷程,即有機酸首先電離成氫離子和羧酸跟離子,隨后羧酸根離子發生分解。反應體系的pH值越高,有機酸根離子濃度越高,其分解反應越容易進行。反應體系中鉀長石的存在明顯提高了乙酸和乙二酸分解反應的反應速率,但對反應活化能和反應起始溫度影響較低。
(3)高流體壓力和靜巖壓力均會抑制乙酸和乙二酸的分解,在提高有機酸分解反應起始溫度的同時降低分解反應速率。因此,相對高壓、低地溫的地層環境更有利于有機酸的保存,低地溫梯度的沉積盆地形成深層—超深層優質儲層的可能性更高。

