兼具水稻紋枯病拮抗功能的生物水稻育苗基質(zhì)效果研究①
戚秀秀,魏 暢,張林利,劉曉丹,楊艷霞,姜 瑛*,馬 超
兼具水稻紋枯病拮抗功能的生物水稻育苗基質(zhì)效果研究①
戚秀秀1,魏 暢1,張林利1,劉曉丹1,楊艷霞2,姜 瑛1*,馬 超3*
(1 河南農(nóng)業(yè)大學(xué)資源與環(huán)境學(xué)院,鄭州 450002;2 西平縣農(nóng)業(yè)技術(shù)推廣中心,河南西平 463900;3安徽農(nóng)業(yè)大學(xué)資源與環(huán)境學(xué)院,農(nóng)田生態(tài)保育與污染防控安徽省重點(diǎn)實(shí)驗(yàn)室,合肥 230036)
水稻紋枯病是水稻上常見的土傳病害之一,為了研發(fā)出可防治水稻紋枯病兼具促生效果的功能型生物水稻育苗基質(zhì),本研究選用前期篩選出具有固氮解磷功能的根際促生菌:LY5枯草芽孢桿菌()、LY11解淀粉芽孢桿菌()、X2摩拉維亞假單胞菌()、X3沙芬西芽孢桿菌()、X8綠針假單胞菌(),首先探索該5株促生菌對(duì)水稻紋枯病病原菌的抑菌率,再將其與水稻紋枯病病原菌混合,在實(shí)驗(yàn)室已篩選出的最適配比基質(zhì)基礎(chǔ)上,研發(fā)功能型生物水稻育苗基質(zhì)。在盆栽條件下,與市售水稻育苗基質(zhì)對(duì)比,驗(yàn)證功能型生物水稻育苗基質(zhì)對(duì)水稻紋枯病發(fā)病率、水稻幼苗生長(zhǎng)和體內(nèi)抗性相關(guān)酶類的影響。結(jié)果表明:①5株根際促生菌對(duì)水稻紋枯病病原菌均具有拮抗作用,抑菌率達(dá)到35.31% ~ 40.20%。②5株拮抗促生菌能夠降低水稻紋枯病的發(fā)病率,其中添加LY11菌株的處理較對(duì)照處理的每盤出苗數(shù)顯著增加了110.41%,而發(fā)病率顯著降低了89.32%。③在含有水稻紋枯病病原菌的育苗基質(zhì)中添加拮抗促生菌后,水稻幼苗的莖粗、百株地下部干物質(zhì)重、百株全株干物質(zhì)重、根系活力、根總表面積、根平均直徑、根總體積、根尖數(shù)等方面均有所提高,其中添加LY11菌株的處理比市售水稻育苗基質(zhì)處理分別顯著提高3.13%、4.21%、4.97%、68.02%、26.77%、16.67%、44.44%、7.82%。④添加拮抗促生菌顯著促進(jìn)了水稻幼苗對(duì)地上和地下部氮磷鉀的吸收。⑤水稻幼苗體內(nèi)超氧化物歧化酶、過氧化物酶、過氧化氫酶的活性以及丙二醛的含量均顯著高于市售水稻育苗基質(zhì)處理,提高幅度為27.08% ~ 122.72%、16.09% ~ 48.15%、53.33% ~ 233.85%、110.24% ~ 511.71%。因此,本研究研發(fā)出5種對(duì)水稻紋枯病具有較好的拮抗效果,同時(shí)可以顯著促進(jìn)水稻幼苗生長(zhǎng)的功能型高效生物水稻育苗基質(zhì),其中添加了菌株LY11的育苗基質(zhì)綜合效果最優(yōu),為功能型高效生物水稻育苗基質(zhì)的研制與應(yīng)用奠定了理論與實(shí)踐基礎(chǔ)。
水稻紋枯病;拮抗促生菌;育苗基質(zhì);根系活力;酶活性
水稻是我國主要的種植作物之一[1]。近年來,隨著農(nóng)業(yè)科技的進(jìn)步和機(jī)械化生產(chǎn)的發(fā)展,我國水稻生產(chǎn)效率不斷提高,水稻生產(chǎn)中面臨的問題也日益突出,除了育苗過程取土困難以及育苗技術(shù)不完善外,水稻病害也日益加劇,其中水稻紋枯病在我國的發(fā)生最為廣泛[2],導(dǎo)致我國水稻產(chǎn)量和品質(zhì)下降。
水稻紋枯病是由立枯絲核菌()侵染引起的一種病害,大多發(fā)生在高溫、多雨的氣候條件下,是主要的土傳病害之一[3]。病原菌以菌核的形式在土壤中或附著在植株上越冬,春播或插秧后附著于水稻植株近水面的葉鞘部位,在適宜的溫度、濕度等條件下再生菌絲可在水稻葉片或葉鞘表面萌發(fā)、生長(zhǎng),然后侵入水稻內(nèi)部,最后菌絲體在水稻組織內(nèi)延伸、蔓延[4];隨著病害的發(fā)展,到達(dá)水稻根莖周圍,會(huì)使根莖的感染部分變黑,最終導(dǎo)致水稻根莖組織壞死,甚至根莖斷裂,造成嚴(yán)重的穗枯萎[5],降低水稻的產(chǎn)量和品質(zhì)。且當(dāng)環(huán)境濕度較高時(shí),白蜘蛛絲狀菌絲體會(huì)出現(xiàn)在感染部位,并逐漸聚集成簇,終形成新的蘿卜種子狀菌核[6]。此外,真菌細(xì)胞在生長(zhǎng)和分化之間的過渡時(shí)期會(huì)產(chǎn)生·OH、O2–·、1O2、H2O2和其他活性氧,用來削減水稻體內(nèi)抗氧化作用。當(dāng)細(xì)胞內(nèi)活性氧過度積累,可形成菌核,抵抗活性氧的毒性,保持真菌的活力[7],同時(shí)當(dāng)水稻體內(nèi)的活性氧含量過高會(huì)對(duì)植物本身產(chǎn)生危害,SOD、CAT、POD等抗氧化酶可以水解H2O2,降低活性氧的含量,維持植物體內(nèi)的活性氧產(chǎn)生與清除之間的平衡[8],降低真菌的活力,提高水稻的抗病性。
現(xiàn)今植物病害主要防治方式仍然是化學(xué)農(nóng)藥,而化肥、農(nóng)藥的大量施用對(duì)病害的防治、作物產(chǎn)量的提高雖然起到了重要的作用,但同時(shí)也帶來了諸多生態(tài)問題[9]。近兩年利用有益微生物進(jìn)行生物防治的相關(guān)研究逐漸成為植物保護(hù)領(lǐng)域的研究熱點(diǎn)之一,例如研發(fā)兼具促生及生防功能的高效生物育苗基質(zhì)[10]。研究發(fā)現(xiàn)植物根際促生菌在促進(jìn)植物生長(zhǎng)發(fā)育、防治病害、改良土壤微生物生態(tài)環(huán)境等方面十分重要,可部分替代化肥、農(nóng)藥[11],降低有害成分對(duì)環(huán)境及人類健康造成的危害,實(shí)現(xiàn)農(nóng)業(yè)的可持續(xù)發(fā)展。
植物根際促生菌(plant growth promoting rhizoba-cteria,PGPR)是指生存于植物根圈范圍內(nèi)的土壤中或植株根系表層能夠促進(jìn)植物生長(zhǎng)、防治病害、增加作物產(chǎn)量的有益細(xì)菌的統(tǒng)稱[12-13]。研究發(fā)現(xiàn)根際促生菌能夠改變土壤中難溶性元素的形態(tài),合成植物生長(zhǎng)素,同時(shí)防止淋失來提高根際周圍養(yǎng)分的生物有效性(如固氮、解磷等),從而促進(jìn)植物對(duì)養(yǎng)分的吸收[14],同時(shí)還能夠在土壤中大量繁殖,與有害微生物產(chǎn)生競(jìng)爭(zhēng),并產(chǎn)生次生代謝產(chǎn)物[15-16]抑制病原菌菌絲、寄生病原菌菌絲生長(zhǎng),誘導(dǎo)水稻產(chǎn)生抗性以及定植在水稻莖稈上減少菌絲對(duì)葉鞘的侵染等[17-18]。目前已有相關(guān)研究將根際促生菌與育苗基質(zhì)相結(jié)合,從而制成兼具促生及生防功能的水稻育苗基質(zhì),如張揚(yáng)等[10]和文春燕等[18]從西瓜和辣椒根際分離得到的根際促生菌可產(chǎn)吲哚乙酸(IAA)和NH3且對(duì)尖孢鐮刀菌和茄科勞爾氏菌均有生防效果,與普通育苗基質(zhì)相結(jié)合而制成生物育苗基質(zhì)在苗期及移栽至大田后均可明顯促進(jìn)黃瓜、番茄、辣椒等秧苗的生長(zhǎng)。但針對(duì)水稻的功能型生物育苗基質(zhì)的研究還未見報(bào)道,故本研究將在前人的研究基礎(chǔ)上對(duì)可防治水稻紋枯病兼具促生效果的功能型生物水稻育苗基質(zhì)進(jìn)行探索,并為其在農(nóng)業(yè)上的應(yīng)用提供理論與實(shí)踐基礎(chǔ)。
1 材料與方法
1.1 試驗(yàn)材料
1.1.1 供試基質(zhì)和稻種 基質(zhì)為本實(shí)驗(yàn)室前期篩選出的優(yōu)勢(shì)配比水稻育苗基質(zhì)[19],即(酒糟+秸稈)堆肥60%+蛭石30%+珍珠巖10%,以1.5% 的硫酸水溶液調(diào)節(jié)至pH 5.0左右。水稻種子是由廣西恒茂農(nóng)業(yè)科技有限公司提供,品種為兩優(yōu)1號(hào)。
1.1.2 供試菌株 菌株為本實(shí)驗(yàn)室前期篩選出的具有固氮解磷能力的菌株,分別為:LY5枯草芽孢桿菌(),LY11解淀粉芽孢桿菌(),X2摩拉維亞假單胞菌(),X3沙芬西芽孢桿菌(),X8綠針假單胞菌(),水稻紋枯病病原菌由河南農(nóng)業(yè)大學(xué)植保學(xué)院提供。
1.1.3 LB 培養(yǎng)基 蛋白胨10 g,酵母粉5 g,NaCl 10 g,去離子水1 000 ml,pH 7.2 ~ 7.4,121 ℃ 高壓滅菌20 min。
1.2 試驗(yàn)設(shè)計(jì)
水稻催芽:室內(nèi)晾曬2 ~ 3 d的水稻種,用20% 鹽水選種,去除秕子及雜物,清水洗去種子表面的鹽分。水浸催芽,定期換水。待種子吸水膨脹出芽2 mm時(shí),攤晾,備用。
拮抗促生菌懸液的制備:將已活化的拮抗促生菌接種于LB液體培養(yǎng)基,30 ℃、170 r/min振蕩培養(yǎng)36 h,4 000 r/min離心10 min,用無菌水重懸–離心洗滌3次后,重懸于無菌水中,調(diào)節(jié)其濃度為108/ml。
病原菌懸液的制備:將已經(jīng)活化的病原菌接種于PDA平板上,28 ℃ 靜置培養(yǎng)5 d,待菌絲布滿平板用無菌涂布棒將菌絲刮下并充分?jǐn)囁椋脽o菌水調(diào)節(jié)其濃度為105/ml。
本試驗(yàn)分別設(shè)置以下7個(gè)處理,T1(最適配比基質(zhì)+病原菌)、T2(最適配比基質(zhì)+菌LY5+病原菌)、T3(最適配比基質(zhì)+菌LY11+病原菌)、T4(最適配比基質(zhì)+菌X2+病原菌)、T5(最適配比基質(zhì)+菌X3+病原菌)、T6(最適配比基質(zhì)+菌X8+病原菌)、T7(普通商品基質(zhì)+病原菌),將菌懸液等量均勻噴灑于相應(yīng)處理中,每盤50 ml,對(duì)照處理噴灑等量無菌水;3 d后噴灑病原菌懸液于相應(yīng)處理中,每盤80 ml,每個(gè)處理重復(fù)3次。按照常規(guī)生產(chǎn)方式裝盤育苗,均勻撒種。用育苗盤為580 mm′280 mm′30 mm帶孔育苗盤,將基質(zhì)均勻平鋪于盤中,每盤播種芽谷130 g,均勻噴水保持基質(zhì)含水量達(dá)到飽和狀態(tài)并維持厚度約3 cm播種后覆土,覆土厚度0.11 cm。濕潤覆土后覆膜保溫保濕。各處理隨機(jī)擺放,保持生長(zhǎng)環(huán)境一致。生長(zhǎng)第22天采樣。
1.3 測(cè)試指標(biāo)與測(cè)定方法
1)采用平板對(duì)峙法確定5株根際促生菌對(duì)水稻紋枯病病原菌的抑菌率。挑取5株促生菌落于LB培養(yǎng)基進(jìn)行純化,后用無菌涂布器均勻涂于PDA培養(yǎng)基培養(yǎng)待用,取已活化的病原菌接于PDA平板中央,28 ℃ 培養(yǎng)24 h,采用對(duì)峙法將該5株根際促生菌的菌株點(diǎn)接在距病原菌菌片20 mm處,每皿接種1個(gè)菌株,對(duì)稱放于兩側(cè)。同時(shí)設(shè)對(duì)照(不接菌),28 ℃ 培養(yǎng)6 d。每個(gè)梯度設(shè)3個(gè)重復(fù)。
抑菌率(%)=(對(duì)照病原菌直徑–與拮抗菌對(duì)峙的病原菌直徑)/對(duì)照病原菌直徑′100%
2)植株農(nóng)藝性狀:株高、莖粗用直尺測(cè)量;地上地下部干重采用烘干法測(cè)定;壯苗指數(shù)= 莖粗/株高′全株干重。
3)根系測(cè)定:根系總長(zhǎng)、根系總面積、根系平均直徑、根系總體積和根尖總數(shù)用根系掃描儀(EPSON EXPERSSION 1680型)測(cè)定;根系活力的測(cè)定采用Leagene植物根系活力定性檢測(cè)液(TTC法)檢測(cè)[20];SPAD值采用SPAD-502葉綠素儀測(cè)定。
4)植株氮磷鉀含量測(cè)定參照《土壤農(nóng)化分析》[21]:用濃硫酸-H2O2消煮,分別用凱氏定氮法、鉬藍(lán)比色法和火焰光度計(jì)法測(cè)定氮磷鉀的含量。
5)植株超氧化物歧化酶(SOD)測(cè)定參考Fridovich[22]方法,過氧化物酶(POD)測(cè)定參考Liang 等[23]方法,過氧化氫酶(CAT)測(cè)定參考Aebi[24]方法,丙二醛(MDA)酶活性采用南京建成生物工程研究所提供的酶試劑盒進(jìn)行測(cè)定。
1.4 數(shù)據(jù)處理及分析
采用Excel 2003和 Origin 8.5軟件進(jìn)行數(shù)據(jù)計(jì)算及作圖;采用IBM SPSS Statistics 20進(jìn)行數(shù)據(jù)統(tǒng)計(jì)分析,LSD和Duncan法進(jìn)行差異顯著性檢驗(yàn)(< 0.05);各指標(biāo)間采用Pearson法進(jìn)行相關(guān)性分析。
2 結(jié)果與分析
2.1 五株根際促生菌對(duì)水稻紋枯病病原菌的抑菌率
采用平板對(duì)峙法確定5株根際促生菌對(duì)水稻紋枯病的抑菌率,如表1可知,5株促生菌對(duì)水稻紋枯病均有抑制作用,其中LY11的抑菌率最高,與其他4株促生菌相比,提高了1.23%、3.08%、3.85%、4.89%,其次是LY5;X8的抑菌率相對(duì)較低,為35.31%。

表1 分離菌株對(duì)水稻紋枯病病原菌生長(zhǎng)的抑制作用
2.2 不同處理對(duì)植株病情防治的效果
從表2可得,不同處理對(duì)水稻基質(zhì)育苗效果影響顯著。T3處理較T1處理的每盤出苗數(shù)顯著增加了110.41%,而發(fā)病率顯著降低了89.32%;T3處理較T7處理在每盤出苗數(shù)、發(fā)病率方面雖無顯著差異,但每盤出苗數(shù)增加了4.16%,而發(fā)病率降低了12.53%。其次是T4處理,在每盤出苗數(shù)、發(fā)病率方面與T3、T7處理差異均不顯著。
2.3 不同處理對(duì)植株農(nóng)藝性狀及干物質(zhì)重的影響
不同處理的水稻幼苗的農(nóng)藝性狀及干物質(zhì)重見表3。由表3可知,與T1處理相比,其他處理的株高、莖粗、SPAD值、干物質(zhì)重以及壯苗指數(shù)均顯著增加(<0.05)。其中,T2 ~ T7處理的水稻株高比T1處理顯著增加6.43% ~ 13.00%,莖粗比T1處理顯著增加3.97% ~ 17.86%,SPAD值增加了57.71% ~ 121.19%,植株壯苗指數(shù)增加了15.73% ~ 19.10%。與T1處理相比,T3、T6處理的植株百株地上部干重、百株地下部干重、百株全株干重分別顯著增加了34.80%、28.81%,7.92%、5.74% 和 25.83%、21.19%。T3處理的莖粗、百株地下部干重、百株全株干重以及T6處理的株高均顯著高于T7市售育苗基質(zhì)處理(<0.05)。
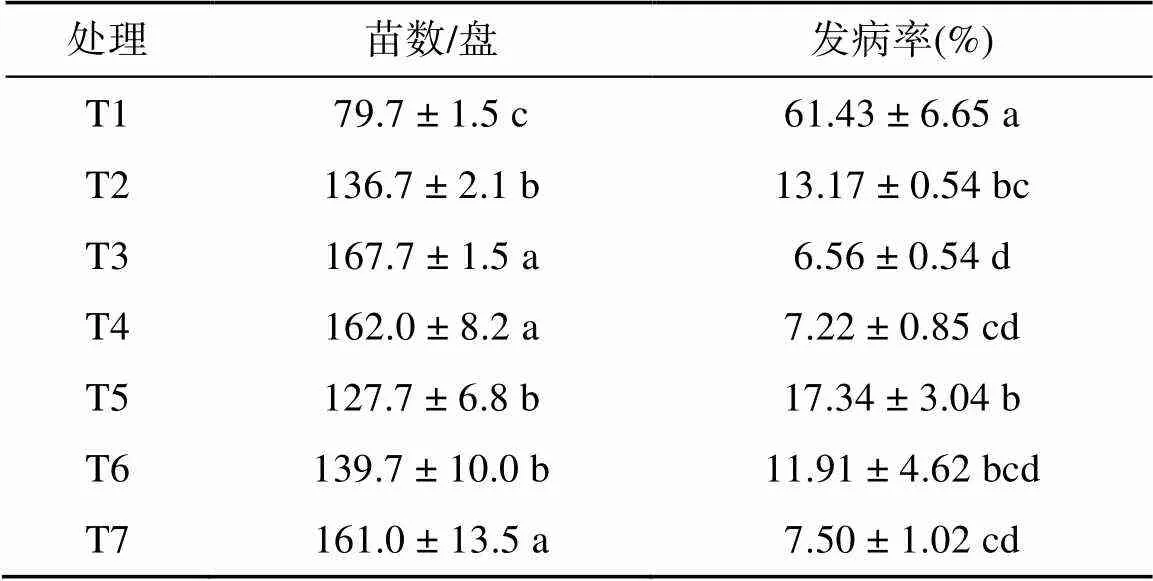
表2 不同處理對(duì)植株病情防治的效果
注:同列小寫字母不同表示處理間差異顯著(<0.05),下同。
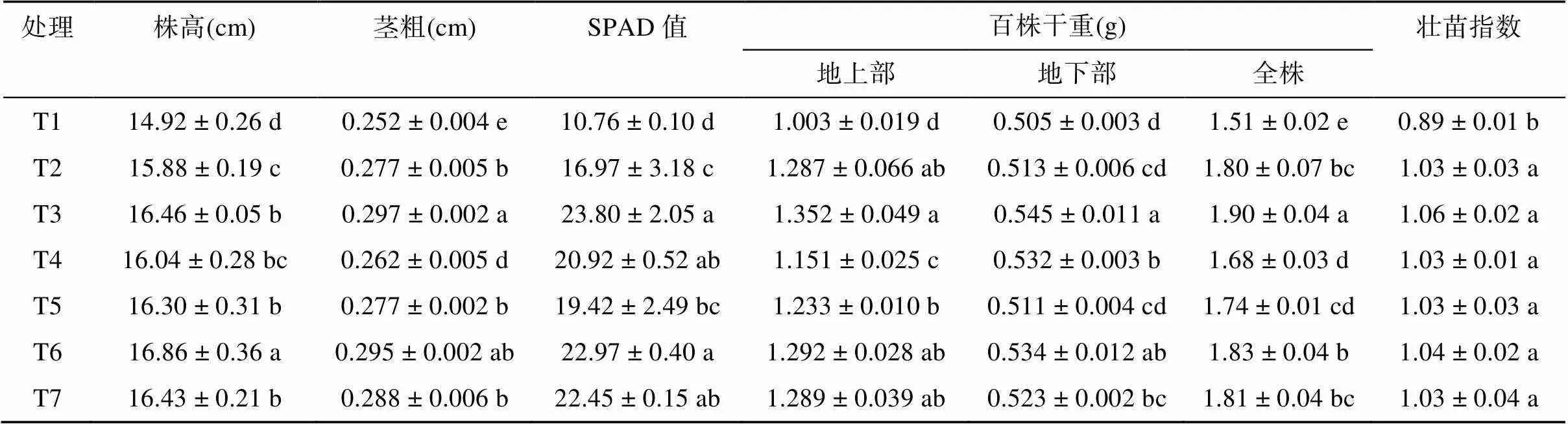
表3 不同處理對(duì)植株農(nóng)藝性狀及干物質(zhì)重的影響
2.4 不同處理對(duì)植株根系的影響
不同處理對(duì)植株根系各指標(biāo)的影響如表4所示。T2 ~ T7處理的植物根系的各指標(biāo)顯著高于T1處理(<0.05),增幅分別為36.62% ~ 147.01%、108.52% ~ 216.71%、94.12% ~ 158.82%、10.77% ~ 37.31%、50.00% ~ 133.33%、97.39% ~ 284.92%,且T3處理效果最好,T6處理次之。與T7處理相比,T3、T6處理的根系活力、根系總表面積、根系平均直徑以及根系總體積均顯著增加,增幅分別為16.67% ~ 68.02%、6.21% ~ 66.61%,且T3處理的根尖數(shù)顯著高于T7處理。與T2、T4、T5、T6處理相比,T3處理的植物根系各項(xiàng)指標(biāo)均有所提高,部分指標(biāo)達(dá)到顯著水平。T6處理的植物根系各項(xiàng)指標(biāo)顯著高于T2處理,根系活力、根系總表面積、根系平均直徑以及根系總體積均顯著高于T4、T5處理。
2.5 不同處理對(duì)植株養(yǎng)分含量的影響
不同處理對(duì)植株養(yǎng)分含量各指標(biāo)的影響如圖1所示。植株地上部氮、鉀含量高于地下部,與T1處理相比,T2 ~ T7處理的植株地上和地下部的氮磷鉀含量均增加,且地上部和地下部的氮含量以及地上部磷含量差異達(dá)到顯著水平(<0.05)。其中T3處理的植株地上和地下部氮鉀含量最優(yōu),T6處理次之,均高于T7處理。與T7處理相比,T3、T6處理植株地上和地下部氮含量分別增加了13.99%、5.66% 和26.21%、12.40%,植株地上和地下部鉀含量分別增加了6.54%、2.69% 和0.13%、0.07%,且T3處理植株地上部氮鉀含量以及T3、T6處理地下部氮含量與T7處理間差異達(dá)顯著水平(<0.05)。在植株地上部和地下部磷含量方面,T2、T3、T6處理均顯著高于T7處理,分別提高32.25%、45.75%,49.44%、58.17% 和87.20%、68.88%。
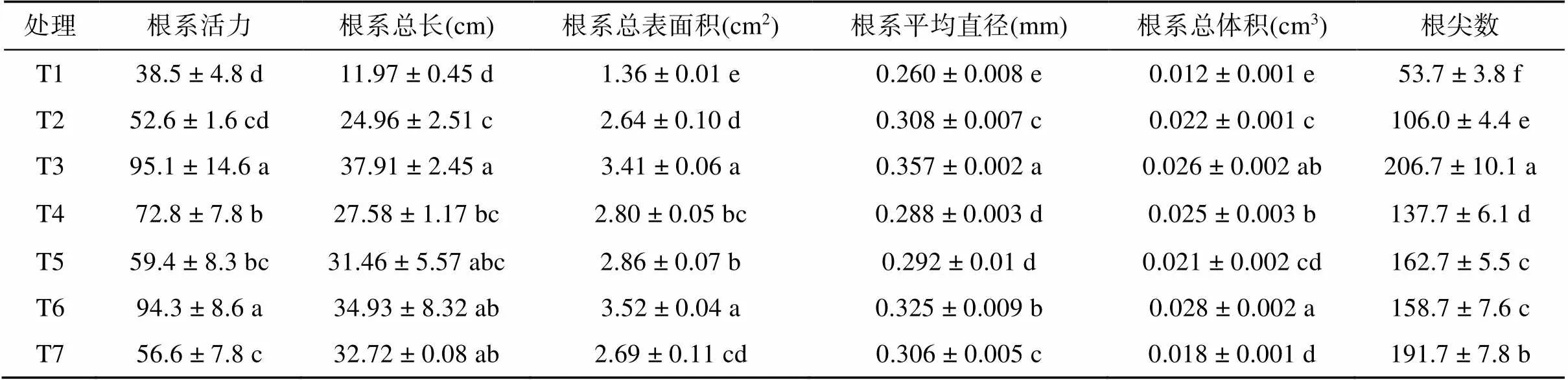
表4 不同處理對(duì)植株根系的影響
2.6 不同處理對(duì)植株體內(nèi)酶的影響
不同處理對(duì)植株體內(nèi)酶活性的影響如表5所示,由表可知T1 ~ T6處理的SOD、POD、CAT酶的活性均顯著高于T7處理,提高幅度為27.08% ~ 122.72%、16.09% ~ 48.15%、53.33% ~ 233.85%,且POD、SOD和CAT活性在T3處理最高,并顯著高于其他6個(gè)處理,其中POD活性在T1和T4處理之間差異不顯著,T5和T6處理之間差異不顯著。對(duì)MDA含量,T1處理為最高,T7處理為最低,與T7處理相比,T1 ~ T6處理的MDA含量增加了1.1 ~ 5.1倍,其中T3處理顯著低于T2、T4、T5,與T6處理差異不顯著。
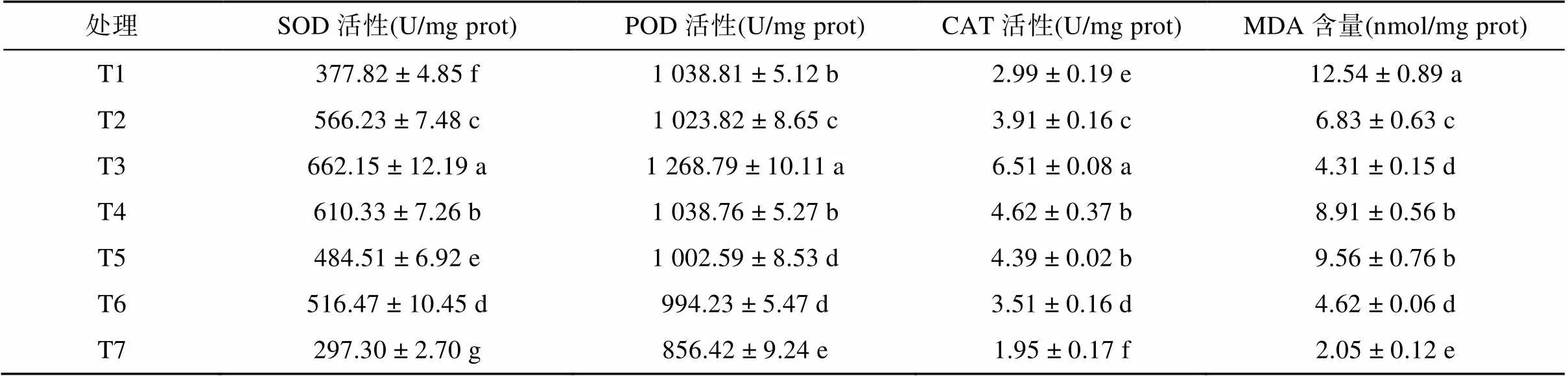
表5 不同處理對(duì)植株體內(nèi)酶活性的影響
3 討論
近年來,隨著生態(tài)農(nóng)業(yè)的不斷發(fā)展,關(guān)于根際促生菌促進(jìn)植物生長(zhǎng)及防治土傳病害的研究開始被報(bào)道[13]。本試驗(yàn)處理中的5株促生菌對(duì)水稻紋枯病均具有較高的抑制率,其中LY11的抑菌率最高,這與盧鈺升[25]等人研究結(jié)果相類似。植物根際促生菌不僅能防治病害、改良土壤微生物生態(tài)環(huán)境,其生長(zhǎng)代謝活動(dòng)也能促進(jìn)或調(diào)節(jié)植物生長(zhǎng),提高植物的出苗率[11]。本研究結(jié)果發(fā)現(xiàn),添加根際促生菌的處理對(duì)水稻紋枯病在實(shí)際育苗中有明顯的抑制作用,且提高了水稻的出苗率,水稻紋枯病發(fā)病率降低可能是因?yàn)楦H促生菌能夠競(jìng)爭(zhēng)生態(tài)位或底物[15],同時(shí)誘導(dǎo)植物產(chǎn)生防御反應(yīng),使其產(chǎn)生抗菌活性物質(zhì),包括酶類、細(xì)菌素、脂肽類、揮發(fā)性物質(zhì)[16]抑制病菌分生孢子萌發(fā)和附著胞形成[17],阻止病原菌侵入。
其中防御酶體系是植株在受到外界傷害如高溫、干旱、鹽堿化、病原菌入侵等時(shí),植物細(xì)胞自發(fā)形成的抵御外界傷害的主要酶保護(hù)系統(tǒng)[26]。近年來的諸多研究結(jié)果均表明,超氧化物歧化酶(SOD)、過氧化物酶(POD)、過氧化氫酶(CAT)等抗氧化酶活性與植株的抗病性密切相關(guān)[27]。本研究中添加病原菌之前先添加本研究所篩選出的拮抗促生菌的相應(yīng)處理的抗氧化酶活性顯著增加,可能是因?yàn)镾OD能夠?qū)⒄婢?xì)胞在生長(zhǎng)和分化之間的過渡時(shí)期產(chǎn)生部分活性氧發(fā)生歧化反應(yīng),形成H2O2和O2,H2O2進(jìn)一步被CAT和POD等分解[8],抑制菌核的形成,降低病原菌的活力,提高水稻的抗性,同時(shí)削減水稻體內(nèi)氧化作用,維持活性氧的平衡,防止過量的活性氧導(dǎo)致水稻體內(nèi)的膜脂過氧化,減少膜系統(tǒng)損傷。丙二醛(MDA)作為膜脂過氧化的主要產(chǎn)物之一,可與膜上蛋白質(zhì)結(jié)合,導(dǎo)致蛋白質(zhì)分子間和分子內(nèi)產(chǎn)生交聯(lián),嚴(yán)重?fù)p失和破壞細(xì)胞膜系統(tǒng),MDA含量高低反映了膜脂的損傷程度[28],其在機(jī)體內(nèi)的積累會(huì)對(duì)細(xì)胞產(chǎn)生毒害作用。本研究中,添加病原菌使植株細(xì)胞膜受到損害,從而促使植株體內(nèi)MDA含量升高,而添加菌株LY11等拮抗促生菌使植株體內(nèi)抗氧化酶活性提高從而降低了其相應(yīng)處理植株體內(nèi)的MDA含量。
同時(shí)相關(guān)研究發(fā)現(xiàn)根際促生菌通過抑制病原菌的生長(zhǎng),減少植物病害的發(fā)生,從而間接促進(jìn)植物生長(zhǎng)。如朱震等人[29]的研究結(jié)果表明,菌株XZ-173,對(duì)番茄青枯病具有較好的拮抗效果,同時(shí)可以顯著促進(jìn)番茄幼苗生長(zhǎng)。本研究結(jié)果發(fā)現(xiàn),添加根際促生菌的處理在株高、莖粗、SPAD值、百株全株干物質(zhì)重、壯苗指數(shù)、根系活力、根系總長(zhǎng)、根平均直徑、根尖數(shù)等方面的作用效果高于對(duì)照組。可能因?yàn)楦H促生菌除了通過在植物幼根表面定殖時(shí)形成一層均勻的保護(hù)層,保護(hù)了病原菌的侵染位點(diǎn),減低了侵染機(jī)會(huì)[18],間接促進(jìn)植物生長(zhǎng)外,還能分泌外源激素物質(zhì),增加植物初生根、次生根和不定根的數(shù)量來改變植物的根系形態(tài)結(jié)構(gòu)[30],為作物地上部的生長(zhǎng)打下基礎(chǔ)。此外,水稻根際促生菌分泌的生長(zhǎng)素、赤霉素、鐵載體等植物生長(zhǎng)促生物質(zhì)[14]能夠提高對(duì)鐵鎂等中微量元素的吸收,有利于作物葉綠素的形成并促進(jìn)光合作用的進(jìn)行,增加有機(jī)物質(zhì)的積累,為水稻固氮和吸收養(yǎng)分提供能量。同時(shí)本實(shí)驗(yàn)室前期研究表明促生菌能夠提高植物碳氮代謝過程中的關(guān)鍵酶,具有固氮解磷作用,從而使株高、莖粗等明顯增加。其中T3處理效果最顯著,這可能是因?yàn)楦H促生菌對(duì)土壤中非寄生性根際有害微生物與有害病原微生物起到生防作用,促進(jìn)植物礦質(zhì)元素的吸收和利用,可產(chǎn)生利于植物生長(zhǎng)的代謝產(chǎn)物,從而促進(jìn)植物生長(zhǎng)發(fā)育。
4 結(jié)論
5株拮抗促生菌與所篩選出的最適配比水稻育苗基質(zhì)相結(jié)合,之后再添加水稻紋枯病病原菌,進(jìn)行水稻育苗,所得水稻幼苗體內(nèi)的抗氧化酶活性提高,發(fā)病率降低,同時(shí)提高了水稻農(nóng)藝性狀及干物質(zhì)重、壯苗指數(shù),明顯改善根系活力和形態(tài)結(jié)構(gòu),提高了水稻的養(yǎng)分含量,且(酒糟+秸稈)堆肥60%+蛭石30%+珍珠巖10%+解淀粉芽孢桿菌()作為高效生物水稻育苗基質(zhì)效果最優(yōu)。
[1] 關(guān)強(qiáng), 蒲瑤瑤, 張欣, 等. 長(zhǎng)期施肥對(duì)水稻根系有機(jī)酸分泌和土壤有機(jī)碳組分的影響[J]. 土壤, 2018, 50(1): 115–121.
[2] 周夢(mèng)琳, 夏園, 劉堯, 等. 水稻紋枯病菌不致病菌株基因組重測(cè)序以及致病力相關(guān)基因分析[J]. 植物病理學(xué)報(bào), 2017, 47(6): 756–766.
[3] 吳志明, 鐘敏, 鹿承建, 等. 新型農(nóng)抗N2粗提物對(duì)水稻紋枯病菌細(xì)胞膜和抗氧化功能的影響[J]. 核農(nóng)學(xué)報(bào), 2018, 32(4): 700–707.
[4] 朱名海. 我國南繁區(qū)水稻紋枯病菌和稻瘟病菌的遺傳多樣性研究[D]. 廣州: 華南農(nóng)業(yè)大學(xué), 2016.
[5] 伏榮桃, 王劍, 盧代華, 等. 水稻紋枯病發(fā)生與防治技術(shù)[J]. 四川農(nóng)業(yè)科技, 2016(11): 32–33.
[6] 喬靜. 水稻紋枯病發(fā)病因素及綜合防治方法研究[J].農(nóng)業(yè)科學(xué), 2019, 2(2): 25–26.
[7] Wang C, Pi L, Jiang S F, et al. ROS and trehalose regulate sclerotial development in Rhizoctonia solani AG-1 IA[J]. Fungal Biology, 2018, 122(5): 322–332.
[8] 韓永強(qiáng), 文禮章, 侯茂林. 水稻施用硅肥對(duì)稻縱卷葉螟幼蟲保護(hù)酶和解毒酶活性的影響[J]. 應(yīng)用昆蟲學(xué)報(bào), 2016, 53(3): 482–490.
[9] 楊帆, 孟遠(yuǎn)奪, 姜義, 等. 2013年我國種植業(yè)化肥施用狀況分析[J]. 植物營養(yǎng)與肥料學(xué)報(bào), 2015, 21(1): 217–225.
[10] 張楊, 王甜甜, 孫玉涵, 等. 西瓜根際促生菌篩選及生物育苗基質(zhì)研制[J]. 土壤學(xué)報(bào), 2017, 54(3): 703–712.
[11] 李劍峰, 楊鑫, 張淑卿, 等. 2種植物內(nèi)生固氮菌對(duì)燕麥種子萌發(fā)及幼苗生長(zhǎng)的效果[J]. 西南農(nóng)業(yè)學(xué)報(bào), 2015, 28(6): 2465–2468.
[12] Abbasi M K, Sharif S, Kazmi M, et al. Isolation of plant growth promoting rhizobacteria from wheat rhizosphere and their effect on improving growth, yield and nutrient uptake of plants[J]. Plant Biosystems - an International Journal Dealing With All Aspects of Plant Biology, 2011, 145(1): 159–168.
[13] Krey T, Caus M, Baum C, et al. Interactive effects of plant growth-promoting rhizobacteria and organic fertilization on P nutrition of Zea mays L. and Brassica napus L[J]. Journal of Plant Nutrition and Soil Science, 2011, 174(4): 602–613.
[14] 劉澤平, 王志剛, 徐偉慧, 等. 水稻根際促生菌的篩選鑒定及促生能力分析[J]. 農(nóng)業(yè)資源與環(huán)境學(xué)報(bào), 2018, 35(2): 119-125.
[15] Prabhukarthikeyan S R, Keerthana U, Raguchander T. Antibiotic-producing Pseudomonas fluorescens mediates rhizome rot disease resistance and promotes plant growth in turmeric plants[J]. Microbiological Research, 2018, 210: 65–73.
[16] 徐婷, 朱天輝, 李姝江, 等. 貝萊斯芽孢桿菌YB15β-葡聚糖酶的抑菌作用與基因克隆[J]. 中國生物防治學(xué)報(bào), 2014, 30(2): 276-281.
[17] 沙月霞, 隋書婷, 曾慶超, 等. 貝萊斯芽孢桿菌E69預(yù)防稻瘟病等多種真菌病害的潛力[J]. 中國農(nóng)業(yè)科學(xué), 2019, 52(11): 1908–1917.
[18] 文春燕, 高琦, 張楊, 等. 含PGPR菌株LZ-8生物育苗基質(zhì)的研制與促生效應(yīng)研究[J]. 土壤, 2016, 48(2): 414–417.
[19] 張林利, 吳大霞, 劉曄, 等. 酒糟等農(nóng)業(yè)廢棄物的堆肥化及水稻育秧基質(zhì)研發(fā)[J]. 土壤, 2019, 51(4): 682–689.
[20] 胡敏, 賀德先. 小麥根系活力的晝夜變化及最佳取樣和測(cè)定時(shí)間[J]. 麥類作物學(xué)報(bào), 2011, 31(6): 1094– 1098.
[21] 鮑士旦. 土壤農(nóng)化分析[M]. 北京: 中國農(nóng)業(yè)出版社, 2000.
[22] Fridovich I. Superoxide radical and superoxide dismutases[J]. Annual Review of Biochemistry, 1995, 64(1): 97–112.
[23] Liang Y C, Sun W C, Si J, et al. Effects of foliar- and root-applied silicon on the enhancement of induced resistance to powdery mildew in Cucumis sativus[J]. Plant Pathology, 2005, 54(5): 678–685.
[24] Aebi H E. Catalase//Bergmeyer H U. ed. Methods of enzymatic analysis[M]. Weinheim: Verlag Chemie, 1974: 273–280.
[25] 盧鈺升, 顧文杰, 蔣瑞萍, 等. 解淀粉芽孢桿菌GB58對(duì)水稻紋枯病的防效及菌劑載體篩選[J]. 中國農(nóng)學(xué)通報(bào), 2017, 33(11): 119–125.
[26] Sumayo M S, Kwon D K, Ghim S Y. Linoleic acid-induced expression of defense genes and enzymes in tobacco[J]. Journal of Plant Physiology, 2014, 171(18): 1757–1762.
[27] 梅小飛, 王智榮, 闞建全. 熒光假單胞菌防治果蔬病害的研究進(jìn)展[J]. 微生物學(xué)報(bào), 2019, 59(11): 2069– 2082.
[28] 郭天榮, 陳麗萍, 馮其芳, 等. Al、Cd脅迫對(duì)空心菜生長(zhǎng)及抗氧化特性的影響[J]. 核農(nóng)學(xué)報(bào), 2015, 29(3): 571-576.
[29] 朱震, 張國漪, 徐陽春, 等. 產(chǎn)脂肽菌株發(fā)酵生物有機(jī)肥的生物防治與促生作用研究[J]. 土壤學(xué)報(bào), 2012, 49(1): 104–110.
[30] Cassán F, Vanderleyden J, Spaepen S. Physiological and agronomical aspects of phytohormone production by model plant-growth-promoting rhizobacteria (PGPR) belonging to the genus azospirillum[J]. Journal of Plant Growth Regulation, 2014, 33(2): 440–459.
Study on Effect of Biological Rice Breeding Substrate with Antagonistic Function of Rice Sheath Blight
QI Xiuxiu1, WEI Chang1, ZHANG Linli1, LIU Xiaodan1, YANG Yanxia2, JIANG Ying1*, MA Chao3*
(1 College of Resources and Environmental Science, Henan Agricultural University, Zhengzhou 450002, China; 2 Xiping Agricultural Technology Extension Center, Xiping, Henan 463900, China; 3 Anhui Key Laboratory of Farmland Ecological Conservation and Pollution Control, College of Resources and Environment, Anhui Agricultural University, Hefei 230036, China)
Rice sheath blight is one of the common soil-borne diseases of rice. To develop a biological rice breeding substrate to prevent and control rice sheath blight and promote rice growth, 5 rhizosphere growth-promoting bacteria with nitrogen fixation and phosphorus removal functions were selected, including LY5 (), LY11 (), X2 (), X3 () and X8 (). Based on the determination of the inhibition rate, the 5 bacteria were mixed with pathogenic bacteria of rice sheath blight, and then the functional biological rice breeding substrates were developed on the basis of the most suitable substrates screened in the laboratory, and a pot experiment was conducted to verify the effects of the developed 5 substrates on the incidence rate of rice sheath blight, growth of rice seedlings and in vivo resistance-related enzymes in rice by comparing with a commercial rice breeding substrate (CK). The results showed that the 5 rhizosphere growth-promoting bacteria all had the antagonistic effect on the pathogen of rice sheath blight with the inhibition rate from 35.31% to 40.20%. Compared with CK, the 5 rhizosphere growth-promoting bacteria all reduced the incidence rate of rice sheath blight, among of which, LY11 treatment significantly reduced the incidence rate by 89.32% and increased the number of emergence per plate by 110.41%. The 5 rhizosphere growth-promoting bacteria increased rice stem diameter, underground dry matter weight of 100 plants, dry matter weight of 100 plants, root activity, total root surface area, average root diameter, total root volume and root tip number, among of them, compared with CK, LY11 treatment significantly increased the above indexes by 3.13%, 4.21%, 4.97%, 68.02%, 26.77%, 16.67%, 44.44% and 7.82%, respectively. Compared with CK, the 5 rhizosphere growth-promoting bacteria significantly promoted the uptake of nitrogen, phosphorus and potassium by rice seedlings, increased significantly the activities of superoxide dismutase, peroxidase and catalase and the content of malondialdehyde in rice seedlings by 27.08%-122.72%, 16.09%-48.15%, 53.33%-233.85% and 110.24%-511.71%, respectively. Therefore, the 5 rhizosphere growth-promoting bacteria have good antagonistic effect against rice sheath blight pathogens andhas the best comprehensive effect, it lays a theoretical and practical basis for developing the high efficient biological rice breeding substrate with growth-promoting and bio-control functions.
Rice sheath blight; Antagonistic growth-promoting rhizobacteria; Nursery substrate; Root activity; Enzyme activity
S435.111
A
10.13758/j.cnki.tr.2021.03.009
戚秀秀, 魏暢, 張林利, 等. 兼具水稻紋枯病拮抗功能的生物水稻育苗基質(zhì)效果研究. 土壤, 2021, 53(3): 505–511.
國家自然科學(xué)基金項(xiàng)目(42077050)和安徽省重大科技專項(xiàng)(18030701188)資助。
(JY27486@163.com;chaoma@ahau.edu.cn)
戚秀秀(1995—),女,河南永城人,碩士研究生,主要從事資源利用與植物保護(hù)研究。E-mail: qixiuxiu0318@163.com

