心肌梗死后前間隔和后間隔穿孔患者的臨床特征及介入封堵治療效果比較
孫子瑞,陳同峰,韓宇,江繼承,蔣亞鵬,張靜,高傳玉,劉煜昊
隨著人民生活水平提高及人口老齡化,心血管疾病患病率持續增長。據估計,到2030年,中國急性心肌梗死(AMI)患者將從2010年的810 萬增至2 260 萬[1]。室間隔穿孔是AMI 最嚴重的機械并發癥之一,臨床表現為血流動力學不穩定、心功能不全和心原性休克等,嚴重時可導致死亡。文獻報道顯示,AMI 患者中室間隔穿孔的總發生率約為0.2%~2.0%,其中前間隔發生的室間隔穿孔較為常見,占66%~78%,后間隔穿孔占17%~22%。與前間隔穿孔相比,后間隔穿孔時血流動力學更不穩定,穿孔特征更為復雜,瓣膜結構受到的影響更大[2-4]。目前,有關前間隔與后間隔穿孔患者的臨床特征及介入封堵術效果的相關報道較少。本研究回顧性分析我院心臟中心67例室間隔穿孔患者,對不同部位室間隔穿孔患者的臨床特征及介入封堵治療效果進行探討。
1 資料與方法
研究對象、分組和研究方法:2015年1 月至2020年5 月我院心臟中心共收治室間隔穿孔患者103例,其中3 周內死亡28例,67例行介入封堵治療的患者被回顧性納入本研究。入選標準:(1)胸骨左緣第3~4 肋間聞及全收縮期雜音;(2)超聲心動圖檢查多切面證實存在室間隔連續性中斷,或左心室造影證實有左向右分流。排除標準:(1)二尖瓣中大量反流;(2)術前循環不穩定或多器官功能衰竭;(3)術前存在嚴重的感染;(4)需行冠狀動脈旁路移植術、心臟瓣膜置換術或因其他原因需要心外科手術等情況;(5)室間隔穿孔直徑>20 mm;(6)其他情況致預期壽命不足1年的患者。所有入選患者按照美國心臟協會(AHA)左心室心肌17分段法[5]將穿孔位置分為前間隔組(n=44)和后間隔組(n=23)。前間隔包括室間隔心尖段、前間隔中段及前間隔基底段;其他間隔位置均為后間隔[5]。分析兩組患者基線、術中、術后資料及術后隨訪結果。
介入封堵方法:所有入組患者先期行冠狀動脈造影檢查,明確罪犯血管并進行血運重建處理。根據既往研究結果,室間隔穿孔介入封堵時機最好延長至心肌梗死后2~3 周進行[6-7],對于血流動力學不太穩定的患者可給予主動脈內球囊反搏、體外膜肺氧合、左心室輔助裝置等輔助治療[8],因此,本組所有患者介入封堵時間均為心肌梗死發作3 周后進行。具體手術方法為:(1)穿刺股動脈和股靜脈;(2)左心室造影:股動脈送入6 F 豬尾導管至左心室,在左前斜35°~60°投照角度下進行,觀察穿孔位置、大小及室壁瘤等情況;(3)建立軌道:6 F JR4 導管指引下泥鰍導絲通過穿孔至右心室并送入肺動脈,股靜脈送入多功能導管,行右心導管檢查,圈套器抓捕泥鰍導絲,建立軌道;(4)送入輸送鞘管至左心室側,按照“穿孔直徑+10 mm”原則選擇室間隔缺損封堵傘(A7B3 高10 mm,上海形狀記憶合金材料有限公司),定位封堵傘后打開左右傘盤,重復左心室造影確認封堵效果,術中通過超聲心動圖檢查評估封堵傘位置、形態及周邊瓣膜反流等情況后釋放封堵傘。
統計學方法:采用SPSS 22.0 軟件進行數據統計分析。定量資料先進行正態性檢驗,符合正態分布的資料用均數±標準差描述,組間比較采用兩獨立樣本t檢驗;非正態分布資料用中位數(四分位數間距)描述。分類資料以例數和百分比描述。不符合正態分布的定量資料及有序分類資料的組間比較采用Mann-Whitney U 檢驗;二分類資料采用卡方檢驗。所有檢驗均采用雙側檢驗,生存曲線用Kaplan-Meier 法,并用log-rank 檢驗進行比較。P<0.05 為差異有統計學意義。
2 結果
兩組患者的術前基線資料比較(表1):與前間隔組相比,后間隔組二尖瓣、三尖瓣反流面積更大,收縮壓、舒張壓較低,N 末端B 型利鈉肽原對數值較高,差異均有統計學意義(P均<0.05)。前間隔組罪犯血管100%為左前降支,后間隔組罪犯血管以右冠狀動脈為主(60.87%)。兩組其余基線資料的差異均無統計學意義(P均>0.05)。
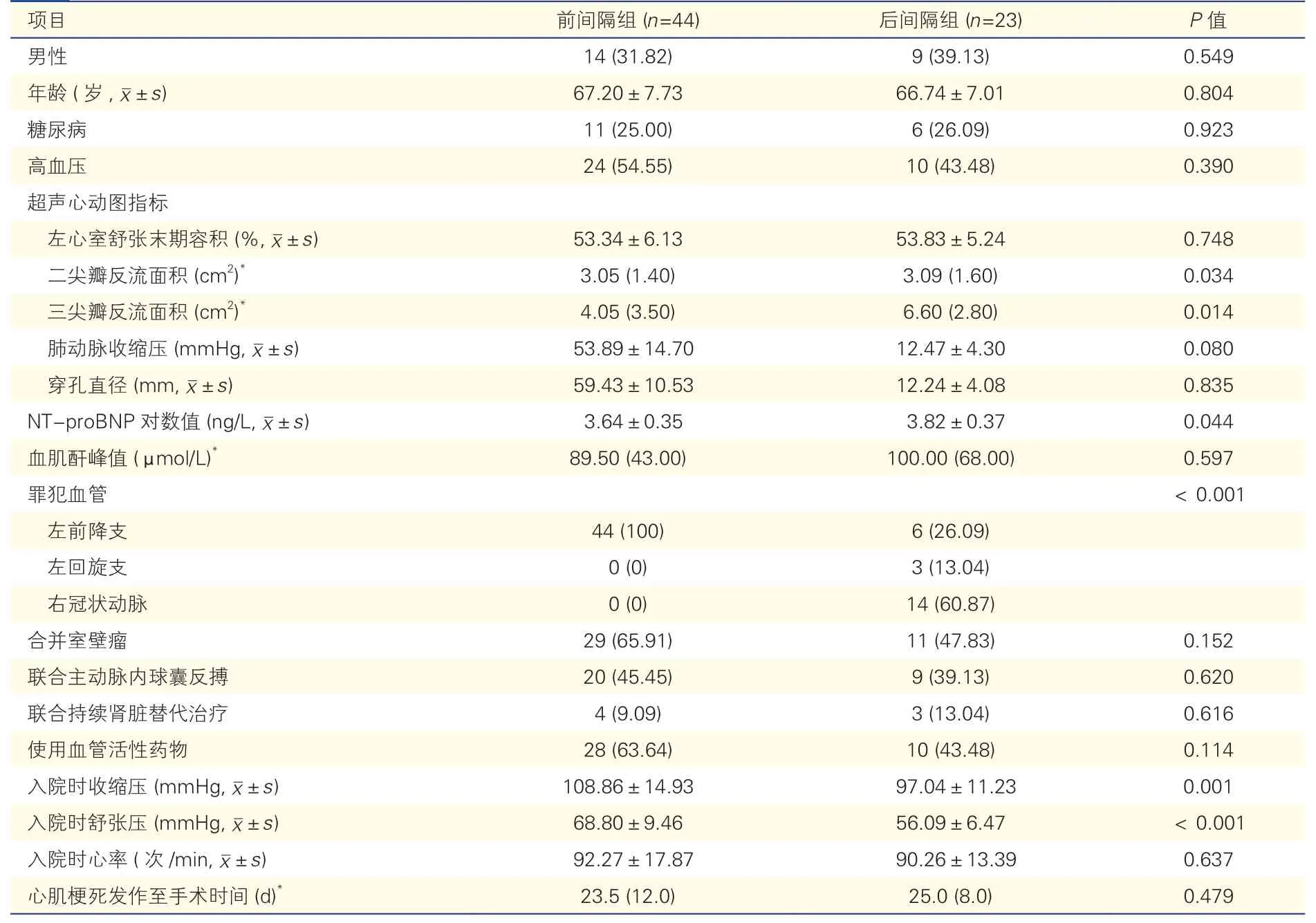
表1 兩組患者的術前基線資料比較[例(%)]
兩組患者的手術情況、術中和術后資料比較:67例患者中,手術失敗4例,其中前間隔組2例,原因均為心臟破裂;后間隔組2例,1例因術中反復心室顫動而放棄封堵,1例封堵器脫落轉外科治療。兩組介入封堵術成功的患者(前間隔組42例,后間隔組21例)在手術時間、X 線輻射量、封堵器直徑等方面的差異均無統計學意義(P均>0.05)。封堵術后,后間隔組的二尖瓣反流面積仍明顯大于前間隔組,差異有統計學意義(P=0.002);兩組術后殘余分流、重癥監護室滯留時間、術后三尖瓣反流面積等資料的差異均無統計學意義(P均>0.05),具體情況見表2。63例手術成功患者中,院內死亡7例(11.11%)。前間隔組6例(14.29%)死亡,其中4例因二尖瓣、三尖瓣大量反流引起心功能衰竭,最終死亡;2例嚴重溶血,導致多器官功能衰竭死亡。后間隔組1例(4.76%)患者于術后第二天因突發心臟驟停而死亡。兩組患者的院內死亡率差異無統計學意義(P>0.05)。
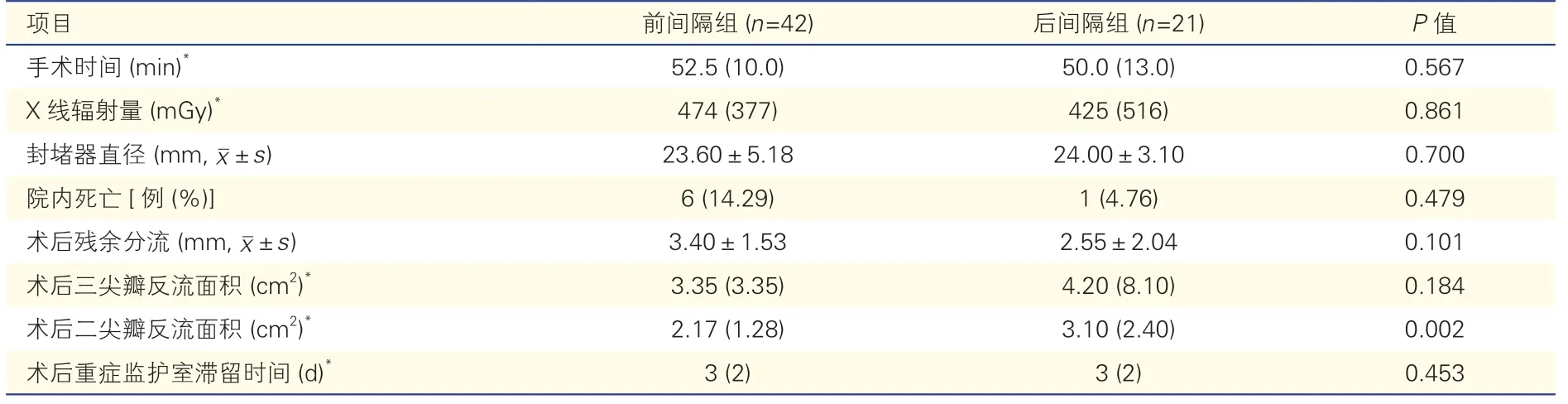
表2 兩組介入封堵術成功的患者術中及術后資料比較
患者出院后的隨訪結果:56例出院患者均完成隨訪,其中前間隔組36例,后間隔組20例,中位隨訪時間為447.5(860.0)d。兩組在再次住院率及新發腦梗死、腦出血、二次冠狀動脈事件發生率等方面的差異均無統計學意義(P均>0.05),具體情況見表3。Kaplan-Meier 生存曲線分析顯示,兩組的遠期生存率差異無統計學意義(P>0.05),見圖1。
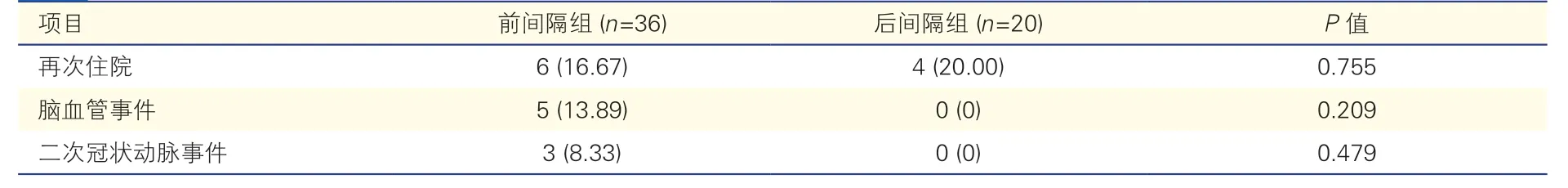
表3 患者出院后的隨訪結果[例(%)]
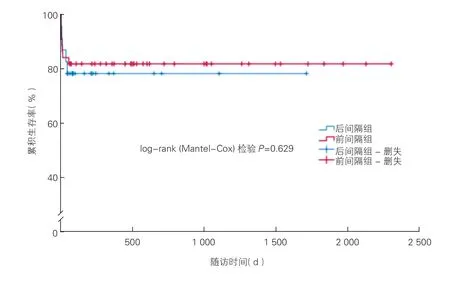
圖1 前間隔組和后間隔組患者的Kaplan-Meier 生存曲線
3 討論
室間隔穿孔是AMI 最為嚴重的機械并發癥之一,多見于單支冠狀動脈病變且側支循環沒有建立的患者,多為AMI 發作后的2~4 d 發生[9-10]。研究顯示,室間隔穿孔發生部位與冠狀動脈分布關系密切,前壁心肌梗死多引起心尖部的室間隔穿孔,部位多為前間隔;下壁和側壁心肌梗死多引起室間隔后部及與心室后壁交界處的基底部穿孔,部位多為后間隔[11-13]。本研究顯示,前間隔組患者的罪犯血管均為左前降支,后間隔組罪犯血管中右冠狀動脈占比為60.87%,左回旋支占13.04%,左前降支占26.09%,與既往報道結果相符。
室間隔穿孔一旦發生,由于巨大的左、右心室壓力差,大量血液由左心室向右心室分流,導致右心負荷加重,肺循環血量增加,進而加重了左心室的容量負荷;另外,室間隔穿孔后由于代償作用導致機體小血管呈收縮狀態,體循環阻力增加,進而左心室的后負荷增加,又進一步增加了左向右的分流量,引起血流動力學進一步惡化[14-15]。除了上述因素外,后間隔穿孔常合并不同程度的右心室心肌缺血壞死,同時由于解剖關系易導致乳頭肌及腱索功能不良以及二尖瓣、三尖瓣反流,這些因素又會加劇右心功能不全的嚴重程度[16-17]。本研究顯示,后間隔組患者的術前血流動力學指標如血壓、肺動脈收縮壓、血肌酐及N 末端B 型利鈉肽原水平等與前間隔組相比更差,二尖瓣、三尖瓣反流程度也更重。
由于前間隔穿孔和后間隔穿孔解剖特征的不同,其介入操作技巧及術中注意事項也明顯不同。前間隔穿孔患者特點為出口和入口多在同一水平,穿孔通道較為規則、平直,建立軌道較為容易,但由于穿孔位置多為近心尖部位,輸送鞘易產生彎曲打折現象,這為封堵器的輸送帶來了很大困難,必要時需要通過頸內靜脈途徑進行封堵,以降低輸送鞘打折現象的發生;同時,前間隔穿孔患者建立軌道過程中易引起心包填塞,故動作需輕柔。而后間隔室間隔穿孔出入口多處于不同水平,穿孔部位通常靠后、靠近基底部,形態較為復雜,多為不規則或多個破口,部分病例導絲通過穿孔較為困難,這為軌道建立帶來很大的困難,通過孔道時導管需向后旋轉,必要時需更換不同導管進行嘗試,但是一旦軌道建立后,輸送鞘形態較為順暢,封堵器輸送較為容易。本研究顯示,兩組患者在手術操作時間及X 線輻射量方面未見明顯差別。
由于后間隔穿孔更易導致乳頭肌及腱索功能不良,同時與前間隔穿孔相比,后間隔穿孔距離二尖瓣及三尖瓣瓣下結構近,因此封堵器傘盤易影響二尖瓣、三尖瓣瓣下結構而導致瓣膜反流,這也會影響手術的效果 。本研究顯示,后間隔組患者術后二尖瓣反流較前間隔組更嚴重。因此,建議后間隔穿孔患者術前進行心臟CT 檢查,了解穿孔位置及與周邊結構之間的關系,必要時可行心臟3D 模型打印,以充分評估穿孔與瓣膜結構的關系;對于穿孔與瓣膜結構關系密切的患者,建議行外科手術治療。
本研究顯示,兩組患者術后遠期隨訪結果及生存率無明顯差異,考慮可能原因如下:(1)根據以往研究及本心臟中心經驗,室間隔穿孔介入封堵時機一般為AMI 發作3 周以后,部分病情較重的患者在等待介入治療的過程中就已經死亡,而剩下的存活患者病情都比較穩定,因此介入封堵術后兩組的遠期效果差異不明顯;(2)研究顯示,后間隔穿孔患者單支冠狀動脈病變發生率較高,遠期再次發生冠狀動脈事件的風險降低[18-19];(3)本研究術前進行了仔細評估,除了常規超聲心動圖外,部分患者進行了心臟CT 掃描或心臟3D 模型打印,從而保證了較好的遠期手術效果。
綜上所述,由于解剖學特征不同,后間隔穿孔患者介入封堵術前心臟瓣膜反流更為明顯,同時由于封堵傘的特點,封堵術后后間隔穿孔患者二尖瓣反流較為明顯,因此術前需仔細評估;前間隔、后間隔穿孔患者封堵術后遠期療效相當,因此后室間隔穿孔患者經仔細評估后接受介入封堵術是可行的。但本研究為單中心回顧性研究,且樣本量較小,需要收集更多的病例及數據,進一步進行研究來證實。
利益沖突:所有作者均聲明不存在利益沖突

