R134a-DMF吸收式制冷系統(tǒng)熱力學(xué)模型選擇
陳 鑫, 李 慧、2、3, 單明珠
(1.山東建筑大學(xué) 熱能工程學(xué)院, 山東 濟南 250101; 2.山東建筑大學(xué)可再生能源建筑利用技術(shù)教育部重點實驗室, 山東 濟南 250101; 3.山東省可再生能源建筑應(yīng)用技術(shù)重點實驗室, 山東 濟南 250101)
1 概述
吸收式制冷系統(tǒng)利用太陽能、地?zé)崮堋⒌推肺粺嵩吹葹轵?qū)動力,僅使用較少的電能來實現(xiàn)為用戶提供冷源的目標(biāo),對于全球所面臨的資源短缺及環(huán)境污染問題可以起到很好的緩解作用。本文旨在為R134a-DMF吸收式制冷系統(tǒng)提供基礎(chǔ)性研究之一,即熱力學(xué)模型的選擇。
孟學(xué)林等人[1]基于PENG-ROB狀態(tài)方程對R134a-DMF二元溶液物性進行了描述,并在此基礎(chǔ)上使用Aspen Plus軟件模擬了復(fù)合式制冷循環(huán)系統(tǒng),得到了很好的驗證。管文潔[2]在對R1234yf-NMP二元溶液相平衡研究過程中,用NRTL熱力學(xué)模型與相平衡數(shù)據(jù)進行關(guān)聯(lián),其計算的相對壓力平均誤差與相對最大誤差分別為1.37%與3.51%。回曉洋[3]基于PENG-ROB熱力學(xué)模型模擬了以R134a-DMF為工質(zhì)對的吸收式制冷循環(huán)系統(tǒng),模擬系統(tǒng)的性能結(jié)果分別與H2O-LiBr、NH3-H2O吸收式制冷系統(tǒng)進行了對比。鄧如雷[4]基于測定的R134a-DMF相平衡數(shù)據(jù),分別對PENG-ROB與NRTL熱力學(xué)模型進行回歸處理,兩種熱力學(xué)模型均能得到很好的回歸結(jié)果。Han等人[5]進行R134a-DMF二元溶液溶解度測定時,其測得的實驗數(shù)據(jù)與活度系數(shù)模型NRTL進行關(guān)聯(lián),其平均相對誤差及最大誤差均在誤差允許范圍內(nèi)。Zehioua等人[6]對R134a-DMF二元溶液相平衡實驗數(shù)據(jù)關(guān)聯(lián)發(fā)現(xiàn),PENG-ROB與合適的混合規(guī)則及NRTL聯(lián)立時能夠更好地描述相平衡實驗數(shù)據(jù)。以上學(xué)者進行實驗數(shù)據(jù)與熱力學(xué)模型關(guān)聯(lián)時對熱力學(xué)模型的選擇均沒有詳細(xì)介紹,且應(yīng)用于R134a-DMF二元溶液的各種熱力學(xué)模型的相對誤差對比研究相對較少。
本文以R134a-DMF二元溶液為研究對象,首先使用熱力學(xué)模型決策樹初步選擇適合該二元溶液的熱力學(xué)模性,然后基于Zehioua等人[6]測定的部分氣液平衡(Vapor Liquid Equilibrium,VLE)實驗數(shù)據(jù),利用Aspen Plus軟件對熱力學(xué)模型參數(shù)進行回歸,由于Aspen Plus軟件內(nèi)包含各種熱力學(xué)模型且?guī)в谢貧w功能,可直接輸入實驗數(shù)據(jù)計算方程的回歸結(jié)果,最后根據(jù)回歸結(jié)果確定最優(yōu)熱力學(xué)模型。
2 決策樹法熱力學(xué)模型的選擇
2.1 熱力學(xué)模型決策樹
熱力學(xué)模型決策樹是由Carlson于1996年提出的,該方法在熱力學(xué)模型選取過程中得到了眾多學(xué)者的認(rèn)可,決策樹法熱力學(xué)模型的選擇流程見圖1。從圖中可以看出,熱力學(xué)模型選擇可分為以下幾步。

圖1 熱力學(xué)模型決策樹
① 確定分子的極性。分子極性越大,分子間的交互作用越強。混合物內(nèi)有極性組分的存在,就應(yīng)該選擇極性分支。
② 此時所需確定的參數(shù)取決于第一步參數(shù)的確定。如果混合物是極性的,必須考慮混合物內(nèi)是否存在電解質(zhì)組分,若存在電解質(zhì)組分,則選擇ELECNRTL,否則進行步驟③;如果混合物全部為非極性的,必須考慮混合物內(nèi)是否全部為真實組分,若全部為真實組分,則選擇PENG-ROB、RK-SOAVE、PR-BM、LK-PLOCK、RKS-BM、SRK,否則進行步驟④。
③ 對于極性非電解質(zhì)混合物,需考慮混合物壓力范圍。該類混合物壓力范圍以100 kPa為臨界點。當(dāng)壓力小于等于100 kPa時,進行步驟⑤;當(dāng)壓力大于100 kPa時,考慮混合物是否存在二元交互作用參數(shù),存在二元交互作用參數(shù)選擇SR-POLAR、PRWS、RKSWS、PRMHV2、RKSMHV2,不存在二元交互作用參數(shù)選擇PSRK、RKSMHV2。
④ 對于非極性虛擬和真實組分混合物,需考慮混合物壓力范圍,該類混合物壓力范圍以大氣壓為臨界點。壓力大于101.325 kPa時,選擇CHAOSEA、BK-10、GARYSON;壓力小于101.325 kPa時,選擇BK-10、IDEAL。
⑤ 對于壓力小于等于100 kPa的極性非電解質(zhì)混合物,當(dāng)該類混合物不存在二元交互作用參數(shù)且不為液液平衡時選擇UNIFAC、UNIF-LBY、UNIF-DMD;該類混合物不存在二元交互作用參數(shù)但為液液平衡時選擇UNIF-LL;該類混合物存在二元交互參數(shù)且為液液平衡時選擇NRTL、UNIQUAC;該類混合物存在二元交互作用參數(shù)但不為液液平衡時選擇WILSON、NRTL、UNIQUAC。
2.2 確定熱力學(xué)模型決策樹判定參數(shù)
熱力學(xué)模型決策樹判定參數(shù)即決策樹內(nèi)的判定條件,分別由是否為極性、是否為真實或虛擬組分、是否為電解質(zhì)、是否滿足壓力范圍、是否存在交互作用參數(shù)及液液平衡組成。本文熱力學(xué)模型決策樹參數(shù)通過Aspen Plus軟件以R134a-DMF為研究對象,來完成熱力學(xué)模型選擇過程中所需決策樹判定參數(shù)的確定。
基于Aspen Plus軟件內(nèi)的分子結(jié)構(gòu)功能,確定R134a與DMF的分子結(jié)構(gòu)進而確定分子極性。R134a的分子結(jié)構(gòu)見圖2,DMF的分子結(jié)構(gòu)見圖3。根據(jù)二者的分子結(jié)構(gòu)可知,R134a-DMF二元溶液為極性體系且存在分子間交互作用,溶液內(nèi)不存在游離態(tài)離子,故不為電解質(zhì)溶液。
圖2 R134a的分子結(jié)構(gòu)
圖3 DMF的分子結(jié)構(gòu)
基于Aspen Plus軟件確定R134a-DMF二元溶液VLE實驗壓力范圍,VLE實驗壓力一般不超過R134a在各溫度下的飽和蒸氣壓,通過Aspen Plus軟件獲得R134a的飽和蒸氣壓曲線來確定壓力范圍。在Aspen Plus軟件中,選擇PENG-ROB物性方法,使用軟件內(nèi)純物質(zhì)分析功能,選擇變量為飽和壓力與溫度,即可得到R134a的飽和蒸氣壓曲線,見圖4。
本文研究對象為應(yīng)用于吸收式制冷系統(tǒng)的R134a-DMF二元溶液。若吸收式制冷系統(tǒng)熱源來自太陽能集熱系統(tǒng),該系統(tǒng)在發(fā)生器內(nèi)換熱后,發(fā)生溫度約80 ℃。假定吸收式制冷系統(tǒng)高壓側(cè)(發(fā)生器側(cè))溫度為80℃,高壓側(cè)為吸收式制冷系統(tǒng)壓力最高側(cè),同時對應(yīng)溫度最高側(cè),根據(jù)系統(tǒng)最高溫度確定系統(tǒng)的壓力范圍。由圖4可確定溫度在80 ℃時,對應(yīng)最大壓力為2.7 MPa,故二元體系壓力范圍為0~2.7 MPa,VLE實驗過程中存在氣液兩相。
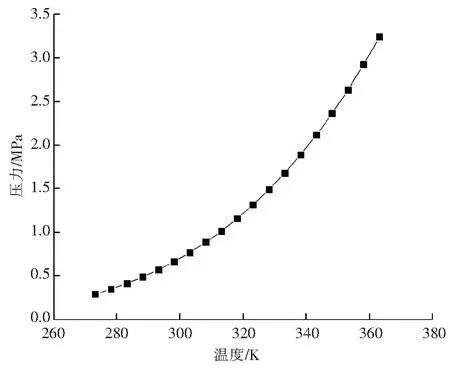
圖4 R134a的飽和蒸氣壓曲線
綜上所述,R134a-DMF二元溶液的熱力學(xué)模型決策樹參數(shù)為極性體系、非電解質(zhì)且壓力范圍為0~2.7 MPa,分子間有交互作用且存在氣相與液相兩種狀態(tài)。
2.3 確定熱力學(xué)模型
根據(jù)上文確定的R134a-DMF二元溶液熱力學(xué)模型決策樹參數(shù),最終選擇熱力學(xué)模型為:壓力小于等于100 kPa時,熱力學(xué)模型為WILSON、NRTL、UNIQUAC;當(dāng)壓力大于100 kPa時,熱力學(xué)模型為PRWS、RKSWS、PRMHV2、RKSMHV2。經(jīng)查閱文獻[7],R134a-DMF二元溶液常使用的物性方法為PENG-ROB與NRTL,Zehioua等人[6]使用PRMHV2對R134a-DMF二元溶液相平衡數(shù)據(jù)進行了擬合,故本文在上述熱力學(xué)模型中選擇PENG-ROB、NRTL、PRMHV2基于R134a-DMF二元溶液VLE實驗數(shù)據(jù)進行擬合,并對擬合結(jié)果進行比較。
3 熱力學(xué)模型回歸
PENG-ROB狀態(tài)方程的表達式見文獻[8],NRTL熱力學(xué)模型的表達式見文獻[9],PRMHV2模型的表達式見文獻[10]。在實際應(yīng)用中,為了能夠更好地描述溶液的相平衡行為,通常不會直接使用熱力學(xué)模型的原參數(shù),而是基于VLE實驗數(shù)據(jù),對方程進行參數(shù)的擬合,擬合出更加接近于實際工程的新參數(shù)。基于Zehioua等人[6]測定的R134a-DMF二元溶液VLE實驗數(shù)據(jù),使用Aspen Plus軟件分別對PENG-ROB、NRTL與PRMHV2這3種熱力學(xué)模型進行擬合,并對比擬合結(jié)果,實驗數(shù)據(jù)溫度與壓力范圍分別為303.3 K、353.24 K及0~2.7 MPa。
基于上述實驗數(shù)據(jù),利用Aspen Plus軟件內(nèi)的回歸功能,對模型進行參數(shù)回歸。在Aspen Plus中選擇PENG-ROB物性方法,輸入實驗數(shù)據(jù),設(shè)置回歸過程PENG-ROB物性方法所需回歸參數(shù)后,運行軟件內(nèi)回歸功能,得到回歸曲線見圖5,圖中x表示系統(tǒng)內(nèi)液相R134a摩爾分?jǐn)?shù)、y表示系統(tǒng)內(nèi)氣相R134a摩爾分?jǐn)?shù)。同樣對熱力學(xué)模型NRTL及PRMHV2進行參數(shù)回歸,結(jié)果見圖6和圖7。回歸過程中,回歸參數(shù)的選取依據(jù)所選取熱力學(xué)模型而定,不同熱力學(xué)模型選取的參數(shù)不同。

圖6 303.3 K下基于NRTL熱力學(xué)模型回歸數(shù)據(jù)與實驗數(shù)據(jù)對比

圖7 303.3 K下基于PRMHV2熱力學(xué)模型回歸數(shù)據(jù)與實驗數(shù)據(jù)對比
從圖5~7可知,基于實驗數(shù)據(jù)回歸后的熱力學(xué)模型與實驗數(shù)據(jù)之間的誤差均很小。利用Aspen Plus軟件內(nèi)Regression功能對溫度為353.24 K時的實驗數(shù)據(jù)進行回歸,并結(jié)合溫度為303.3 K下的回歸結(jié)果,計算出上述3種熱力學(xué)模型分別在溫度為303.3 K與353.24 K時的回歸相對誤差,計算方法見式(1)。相對誤差見圖8。
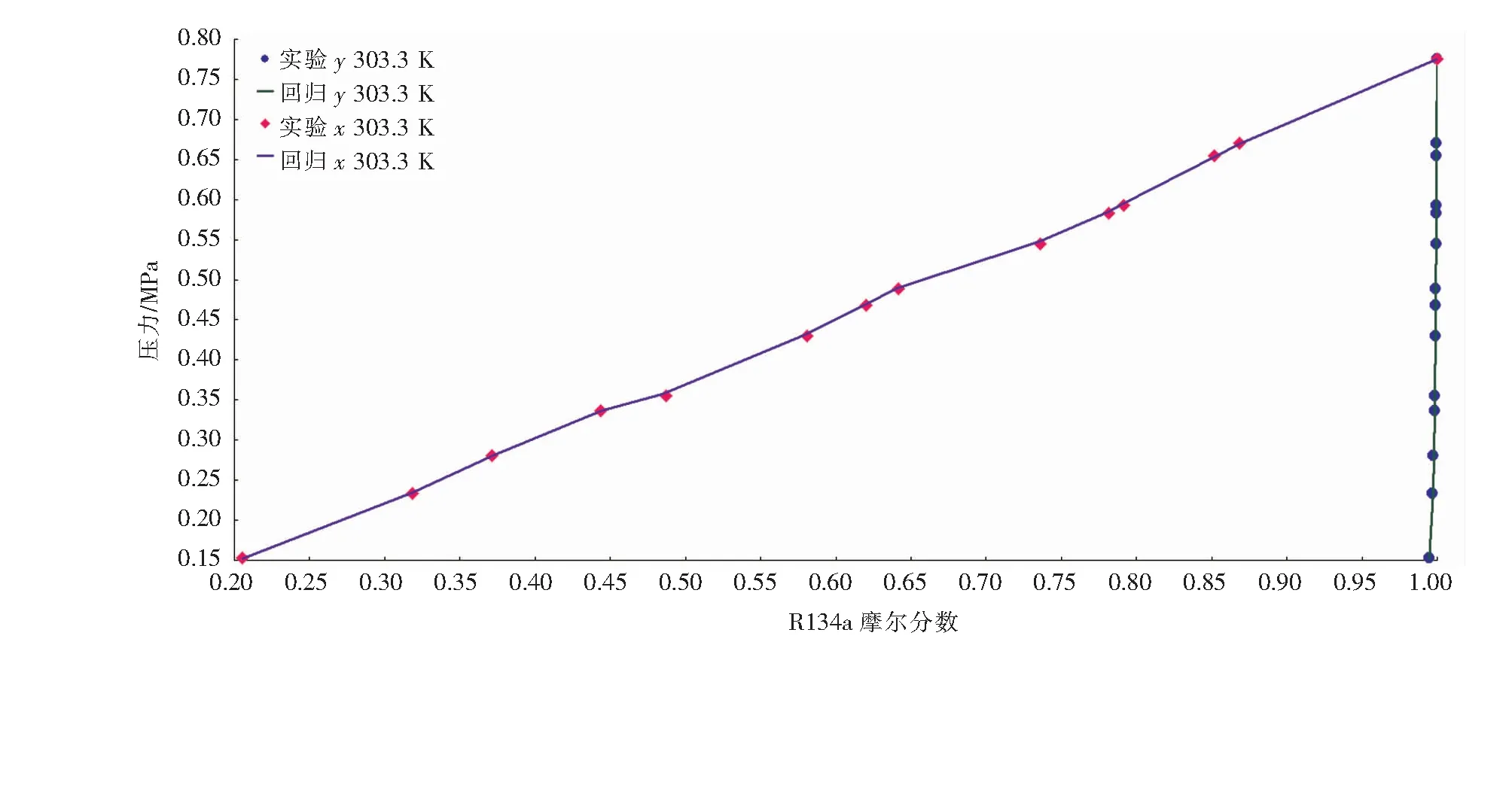
圖5 303.3 K下基于PENG-ROB熱力學(xué)模型回歸數(shù)據(jù)與實驗數(shù)據(jù)對比
(1)
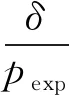
δ——誤差,MPa
pext——估算壓力,MPa
pexp——實驗壓力,MPa
由圖8可知,3種熱力學(xué)模型通過參數(shù)回歸后,與實驗值產(chǎn)生的相對誤差均在2%以內(nèi),同時可以看出在溫度為303.3 K與353.24 K時,回歸后的PENG-ROB熱力學(xué)模型的相對誤差最小。回歸后的NRTL熱力學(xué)模型除去溫度為353.24 K時兩個相對誤差最高點外,其相對誤差值偏高于回歸后的PENG-ROB熱力學(xué)模型。回歸后的PRMHV2熱力學(xué)模型,在溫度為303.3 K與353.24 K時,除個別點相對誤差低于回歸后的NRTL熱力學(xué)模型外,其相對誤差值為3種回歸后的熱力學(xué)方法中的最大值。根據(jù)式(2)計算平均相對誤差,回歸后的3種熱力學(xué)模型的平均相對誤差見表1。
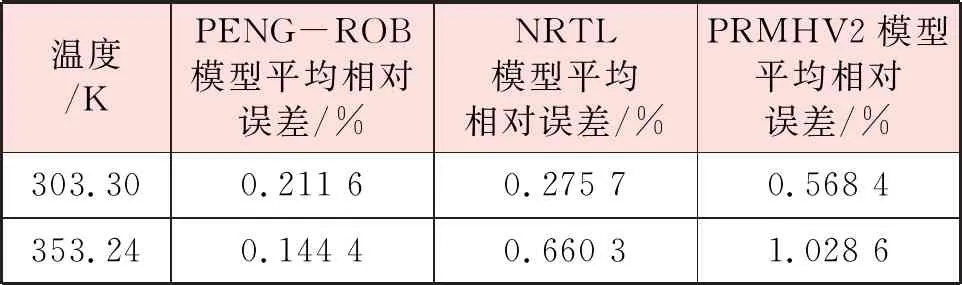
表1 3種熱力學(xué)模型回歸壓力平均相對誤差
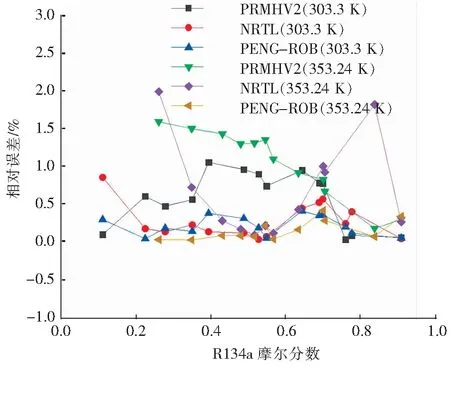
圖8 303.3 K與353.24 K下三種熱力學(xué)模型的回歸相對誤差
(2)

N——總相對誤差數(shù)
i——計數(shù)變量
δi——第i組誤差,MPa
pexp,i——第i組實驗壓力,MPa
由表1可知,3種熱力學(xué)模型回歸壓力的平均相對誤差,PENG-ROB最小,NRTL次之,PRMHV2最大,故選取R134a-DMF二元溶液熱力學(xué)模型為PENG-ROB,其回歸參數(shù)為-0.000 138 782,該值可直接應(yīng)用于接下來的吸收式制冷循環(huán)系統(tǒng)的模擬過程中。
4 結(jié)論
以R134a-DMF二元溶液為研究對象,基于Aspen Plus軟件,對該二元溶液在溫度303.3 K、353.24 K下,應(yīng)用于吸收式制冷模擬的熱力學(xué)模型的選擇進行了研究。
① 基于Aspen Plus軟件分析了二元溶液的分子結(jié)構(gòu)及制冷劑R134a的飽和蒸氣壓曲線,確定了R134a-DMF二元溶液為極性體系及在制冷系統(tǒng)內(nèi)的運行壓力范圍,按照熱力學(xué)模型決策樹的方法,根據(jù)該二元混合物的極性、壓力范圍等判定條件初步確定了PENG-ROB、NRTL與PRMHV2共3種熱力學(xué)模型。
② 結(jié)合R134a-DMF二元溶液的氣液平衡實驗數(shù)據(jù),基于Aspen Plus軟件,對3種熱力學(xué)模型進行了回歸。回歸后的PENG-ROB熱力學(xué)模型的壓力平均相對誤差最小,故選擇PENG-ROB熱力學(xué)模型作為研究以R134a-DMF為工質(zhì)對的吸收式制冷循環(huán)系統(tǒng)的物性方法,回歸后的二元交互作用參數(shù)為-0.000 138 782。

