芎芪醒腦方對輕、中度阿爾茨海默病患者臨床療效及血清炎癥因子的影響?
楊淑荃, 范德輝, 盧桂梅, 袁智先, 蘇美意, 張振寧, 林 穎, 唐 明
(1.廣州中醫藥大學研究生院,廣州 510405; 2.廣東省第二中醫院,廣州 510095)
阿爾茨海默病(alzheimer’s disease, AD)約占老年癡呆的50%~75%,主要表現為認知功能減退、精神行為異常及生活自理能力受限[1]。1項國際研究預測,截至2050年受AD影響的人數將達1.14億[2]。目前AD的治療藥物應用最廣泛的是膽堿酯酶抑制劑,如多奈哌齊能減少乙酰膽堿分解,增強神經沖動傳遞,但不良反應較多,且5 mg/d的劑量只對AD早中期有效,不能阻止AD病情進展。同時AD新藥研發時間長、成本高,且血腦屏障的保護作用一般藥物分子難以進入顱內[3]。中藥復方因安全有效、多環節、多途徑的治療特點,對于防治AD具有獨特優勢[4]。盧桂梅教授是第四批全國名老中醫藥學術經驗傳承工作指導老師,其辨證精準、用藥靈活,自擬芎芪醒腦方用于治療AD取得良好療效。有研究表明,炎癥反應在AD早期階段至關重要[5]。筆者結合自身臨床實踐及AD病理機制,觀察芎芪醒腦方對輕、中度AD患者的臨床療效及血清炎癥因子的影響,現報道如下。本研究經廣東省第二中醫院醫學倫理委員會批準并監督,粵二中醫(2017)倫審第023號。
1 資料與方法
1.1 一般資料
選取廣東省第二中醫院2018年9月至2019年12月康復科門診及住院部收治的70例輕、中度AD患者為研究對象。患者首次就診時按隨機數字表法將患者分為觀察組36例和對照組34例。經過培訓的專業人員不參與研究過程的隨機分組和臨床治療,只負責病例資料的記錄評估、數據分析等。觀察組男21例,女15例;年齡58~79歲,平均年齡(68.37±15.20)歲;病程6個月~4年,平均病程(2.71±0.84)年;AD輕度19例,中度17例;文盲5例,小學13例,中學及以上18例;臨床癡呆評定量表(clinical dementia rating, CDR)評分(1.87±0.95)分。對照組男20例,女14例;年齡56~80歲,平均年齡(67.02±16.13)歲;病程8個月~5年,平均病程(2.84±0.79)年;AD輕度18例,中度16例;文盲3例,小學12例,中學及以上19例;CDR評分(1.92±0.86)分。2組基線特征比較差異無統計學意義(P>0.05),具有可比性。
1.2 診斷標準
西醫診斷標準參照2011年美國衰老研究所和阿爾茨海默病學會(NIA-AA)[6]、2018年中國醫師協會神經內科醫師分會認知障礙疾病專業委員會制定的《中國癡呆與認知障礙診治指南》(簡稱2018指南)[7]中AD的相關標準制定。中醫診斷標準(腎虛髓減、氣虛血瘀型)參照2002年《中藥新藥臨床研究指導原則》[8]制定。主癥:智能減退,腰膝酸軟,倦怠思臥。次癥:表情呆板、思維遲鈍,善驚易恐,腦轉,耳鳴或有幻聽,面頰潮紅,小便失禁,大便自遺,舌紅、少苔,脈細數。主癥具備2項(智能減退必備),次癥至少具備2項以上。
1.3 納入標準
符合上述中西醫診斷標準;病程≥6個月,年齡55~80歲;簡易精神狀態檢查量表評分(mini-mental state examination, MMSE)10~26分,<17分(文盲)、20分(小學)、24分(中學及以上)[10];CDR=1.0, 2.0;日常生活能力量表(activity of daily living scale, ADL)>22分[11];Hachinski缺血指數量表≤4分;Hamilton抑郁量表≤17分;患者有能夠進行測試的視力和聽力;患者及家屬知情同意。
1.4 排除標準
重度AD或其他理化因素誘發AD;有明確的腦血管疾病;老年精神分裂癥;有嚴重內科疾病,如惡性腫瘤、出血性疾病;合并嚴重胃、十二指腸疾病影響藥物吸收者;過敏體質且對本試驗藥物過敏或難以耐受者;依從性差,不遵守本研究相關規定;近期使用過對本研究有干擾作用的藥物;無可靠陪護。
1.5 治療方法
基礎治療:2組調控血壓、血糖、血脂、同型半胱氨酸水平等對癥處理。結合必要的康復措施,如記憶力、語言訓練等,每次60 min,每日1次,連續6 d為1個療程,間隔休息1 d,治療8周。
對照組:基礎治療+多奈哌齊片口服(衛材(中國)藥業有限公司,批準文號5 mg國藥準字H20050978,10 mg國藥準字H20070181),前4周每日5 mg,后4周每日10 mg,20∶00服用。
觀察組:基礎治療+芎芪醒腦方顆粒沖服。藥物組成:黃芪、丹參、黨參各30 g,熟地、女貞子各20 g,川芎10 g,赤芍、地龍各15 g,僵蠶12 g,田三七、全蝎各6 g,蜈蚣2條并隨癥加減用藥[11],中藥統一采用廣東一方制藥有限公司出產的配方顆粒。囑患者將配好的中藥顆粒熱水沖服400 ml,于9∶00和20∶00分2次服用,每日1劑,連服8周。
1.6 觀察指標
①智能變化:1)MMSE,包括定向力、即刻記憶、注意力及計算力、回憶能力、語言功能等,正常、輕度、中度、重度分別為27~30、21~26、10~20、<10分[9];2)AD認知評定量表(alzheimer's disease assessment scale-cognitive subscale, ADAS-Cog),包括詞語回憶、執行指令、定向力、語言表達、注意力等項目共75分,大于15.5分為異常[12]。
②日常生活能力:ADL,14項56分,完全正常、不同程度的功能下降、明顯的功能障礙,依次為<16分、16~22分、>22分[10]。
③精神行為變化:神經精神癥狀問卷(neuropsychiatric inventory questionnaire, NPI),12個亞項,每項附3個問題,由輕到重依次為0~3分、0~2分、0~5分共120分[13]。
④血清炎癥因子:采用酶聯免疫吸附法檢測血清腫瘤壞死因子α(TNF-α)、白細胞介素-4、6、10(IL-4、IL-6、IL-10)含量。試劑盒購于廣州欣博盛生物科技有限公司,嚴格按照說明書操作。
⑤不良反應:治療前后患者行血常規、尿常規、肝腎功能及心電圖檢查,臨床醫生判定患者服藥后反應。
1.7 療效標準
臨床療效評定以MMSE改善率進行療效分級。MMSE改善率=(治療后評分-治療前評分)/治療后評分×100%[14],顯效、有效、無效,改善率依次為>20%、10%~20%、<10%,總有效率=顯效率+有效率。
1.8 統計學方法
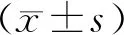
2 結果
2.1 2組臨床療效比較
表1示,2組總有效率比較差異有統計學意義(P<0.05),觀察組優于對照組。

表1 2組臨床療效比較[例(%)]
2.2 2組各量表評分比較
表2示,與治療前比較,觀察組治療4周后和治療8周后、對照組治療8周后的MMSE升高(P<0.05),ADAS-Cog、ADL、NPI降低(P<0.05)。與對照組比較,觀察組治療4周后和治療8周后的MMSE升高(P<0.05)。
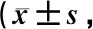
表2 2組各量表評分比較分)
2.3 2組血清炎癥因子比較
表3示,與治療前比較,2組治療4周后和治療8周后TNF-α、IL-6降低(P<0.05),IL-4、IL-10升高(P<0.05)。與對照組比較,觀察組治療4周后和治療8周后 TNF-α、IL-6降低(P<0.05),IL-4、IL-10升高(P<0.05)。

表3 2組炎癥因子數比較
2.4 不良反應比較
觀察組出現頭暈1例,惡心1例,食欲下降1例,總不良反應率8.33%(3/36)。對照組出現頭暈2例,惡心2例,乏力1例,失眠1例,食欲下降2例,總不良反應率23.53%(8/34),2組比較差異有統計學意義(P<0.05),觀察組明顯低于對照組。
3 討論
2018指南[7]A級推薦AD患者選用膽堿酯酶抑制劑治療。目前多奈哌齊片最常用,并取得較理想的療效[15]。本研究中,5 mg/d的多奈哌齊治療4周后,MMSE、ADAS-Cog、ADL、NPI無明顯變化,而繼續以10 mg/d的多奈哌齊治療4周后,MMSE升高,ADAS-Cog、ADL、NPI降低,可能與其加量有關。其藥品說明書2018年7月24日修訂指出,根據多奈哌齊抑制乙酰膽堿水解的作用機制推測,隨著病程進展,功能完整的膽堿神經元逐漸減少,多奈哌齊的作用可能減弱;持續24周的臨床試驗也顯示,10 mg/d的治療劑量(以往大多為5 mg/d)可有效改善中重度AD患者的認知功能。西醫治療AD局限于單一的病理過程,并不能阻止AD病情進展且不良反應較多。中藥具有多靶點、多系統的治療優勢,開發出高效低毒的AD中藥復方有較大的發展空間[16]。
AD屬于中醫學“癡呆”“善忘”“癲證”等范疇,大多本虛標實。腎虛為本,精髓不足,腦海空虛,清竅失養;腎氣不足,血行緩慢,氣虛血瘀,干擾清竅。芎芪醒腦方補氣益腎、活血祛瘀。方中黃芪、黨參補氣以生血、益氣以行血,熟地、女貞子滋腎陰、填腎精,丹參、赤芍、川芎、田三七活血祛瘀,地龍、僵蠶、全蝎、蜈蚣走竄通絡。本方攻補兼施,補而不滯,補中有通。近年來AD的炎癥機制備受重視[17],也有研究表明中藥復方可以調節AD炎癥因子數[18]。TNF-α、IL-6是常見的促炎細胞因子,IL-4、IL-10是常見的抗炎細胞因子[19]。動物實驗發現,黃芪甲苷對腦缺血再灌注大鼠具有抗炎抗衰老的生物活性,可減少TNF-α、IL-6數量[20];富硒女貞子粗多糖可提高小鼠IL-4生成水平,從而增強免疫功能[21];赤芍能下調糖尿病腎病大鼠腎臟TNF-α的表達[22];川芎揮發油顯著抑制脂多糖致血管認知障礙小鼠TNF-α的表達[23];丹參莖葉酚酸組分能降低潰瘍性結腸炎模型小鼠IL-6數量[24]。本研究中,觀察組ADAS-Cog、ADL、NPI治療后較治療前明顯降低,且治療4周和8周后的MMSE較對照組明顯升高,表明芎芪醒腦方對輕、中度AD患者有較好的臨床療效,能改善AD患者的認知功能、日常生活自理能力及精神行為狀態。與對照組比較,觀察組治療4周后和8周后的IL-4、IL-10升高,TNF-α、IL-6降低,表明芎芪醒腦方的作用機制可能與調節血清炎癥因子有關。
臨床上,西醫往往待AD完全診斷明確后給予藥物治療,但2018指南[8]指出,AD起病隱匿、病程緩慢、進行性加重,若早期干預能體現中醫治未病思想[25],能否減少AD發病率、阻止病情惡化,需要中醫藥研究者進一步發掘中醫藥預防優勢。本研究只納入輕、中度AD患者,其遠期療效如何有待完善。

