氫碘酸還原山梨醇合成2-己烯及碘己烷的機理研究
司亞威,王智超,葉躍元*,張朝霞,王 奪,李水榮,劉運權,鄭志鋒
(1.廈門大學能源學院,福建省生物質清潔高值化技術工程研究中心,福建 廈門 361102;2.廈門大學化學化工學院,醇醚酯化工清潔生產國家工程實驗室,福建 廈門 361005)
自19世紀以來,石油和天然氣等不可再生的化石資源一直是生產燃料和化工用品的重要資源[1].但隨著化石資源日漸枯竭,環境問題日漸嚴重,人們急需找到化石資源的替代品[2-4].生物質是世界上存在的唯一的可再生有機碳資源,且生物質在轉化利用過程中是碳中性的[5],它的高效利用對于解決世界范圍內的能源危機與環境污染具有重要意義.生物質主要由纖維素、半纖維素和木質素組成[6-7],通過轉化可以得到糖、有機酸(如己二酸等)[8]、多元醇、醛類化合物等多種平臺化合物.生物質基多元醇如山梨醇和木糖醇就是典型的平臺分子,均可由纖維素和半纖維素轉化生成[9-12];甘油又是生產生物柴油的主要副產物,因此生物質基多元醇來源廣泛,使得生物質基多元醇的轉化利用研究受到人們越來越多的關注.
氫鹵酸(如鹽酸)[13]在生物質去官能化制備高附加值化學品中具有廣泛應用,氫碘酸是所有氫鹵酸中還原性最強的,它經常應用于生物質的還原過程.1938年,Mitchell等[14]提出了一種利用氫碘酸定量羥基的方法,利用過量的氫碘酸與醇反應生成烴類和碘單質,通過定量碘單質來對醇分子上的羥基進行定量.Konieczny等[15]使用氫碘酸還原多環醌類、對二苯酚和苯酚類化合物,使其轉化為相應的烴類.Liu等[16]提出使用氫碘酸將含有4~8個碳的內脂和相關的單羥基正烷酸轉化為單碘代正烷酸和正烷酸的反應機理為:氫碘酸提供的碘離子首先取代羥基生成碘代烷,然后一分子的氫碘酸再與碘代烷反應生成碘單質和烴.Robinson等[17]使用氫碘酸還原多元醇制備碘代烷烴及C12、C18的高碳烷烴作為生物燃油,并用亞磷酸或次磷酸為還原劑將反應過程中產生的碘單質原位還原成氫碘酸;Lv等[18-19]對上述過程進行了系統研究.Yang等[20-23]采用氫碘酸還原葡萄糖、果糖和纖維素制備5-甲基糠醛和2,5-二甲基四氫呋喃,并在金屬催化劑和氫氣共同作用下將碘單質原位還原成氫碘酸.
本研究以山梨醇為底物,在氫碘酸、金屬催化劑和氫氣共同作用下,還原生成碘己烷和少量的己烯.碘己烷是有機合成的重要原料,也是生產醫藥化學品的重要中間體;而己烯是制備聚合物的重要原料,也可用作溶劑或醫藥中間體.以生物質基多元醇為原料制備碘己烷和己烯為生物質的高效應用提供了更多的途徑,這對于可再生資源的應用具有重要意義.此外本研究以多種模型化合物作為底物,考察其與氫碘酸反應后的產物分布,以推斷氫碘酸還原山梨醇合成碘己烷和己烯的可行反應路徑,為調控產物組成和提高產率提供一定的理論依據.
1 實驗部分
1.1 原料與試劑
山梨醇(98%)、PdCl2(99%)、甘油(99%)、氫碘酸(57%)、2-己醇(98%)、3-己醇(98%)、1,2-己二醇(98%)、1-己烯(99%)、2-己烯(85%)、3-己烯-1-醇(97%)、2-己烯-1-醇(97%)、環己烷(99.9%)、1-碘丙烷(99%)、烯丙基碘(97%)和1,3-二碘丙烷(98%)均購自阿拉丁試劑公司,1,2-丙二醇(99%)、2-碘丙烷(99%)、異丙醇(99%)、1,3-丙二醇(98%)和正丙醇(99.5%)均購自麥克林試劑公司,3-己烯(99%)購自九鼎化學試劑公司,括號中均為質量分數.所有試劑均直接使用,未經過純化處理.
1.2 實驗方法
將一定量的底物、氫碘酸、PdCl2、環己烷加入到包裹聚四氟乙烯內襯的高壓反應釜中,關閉反應釜,用1 MPa的氫氣換氣3次,然后通入一定壓力的氫氣,開啟攪拌并加熱反應釜,當溫度達到設定溫度后開始計時;反應持續一定時間后,取出反應釜放在冷水中降溫,待溫度降至室溫后,打開反應釜,排出氣體;反應液分為有機相和水相,有機相經分液并用環己烷多次萃取后定容到25 mL,取1 mL用于氣相色譜-質譜(GC-MS)和氣相色譜-火焰離子檢測(GC-FID),其他有機相經旋轉蒸發去除有機溶劑后用于核磁共振(NMR)檢測,所得譜圖與標準譜圖進行對比.
1.3 分析方法
產物的定性分析通過NMR(Bruker AV600)和GC-MS(QP2010SE)進行測定.NMR分析前,通過旋轉蒸發去除環己烷,取20 mg樣品溶于0.6 mL氘代三氯甲烷(CDCl3)中,放入5 mm核磁管中檢測. GC分析條件:使用Rtx-5MS毛細管柱(30 m×0.25 mm×0.25 μm),載氣為純度99.9999%的氦氣,載氣流量1 mL/min,進樣量1 μL,分流比50∶1;烘箱初始溫度30 ℃,并保持4 min,然后以10 ℃/min的速度升溫至270 ℃,并保持5 min,總耗時為33 min.MS分析條件:使用電子轟擊離子源(EI),電子能量70 eV,離子源溫度200 ℃,接口溫度270 ℃.通過GC-FID(Agilent 7890A)對產物進行定量分析,分析條件:使用聚乙二醇(PEG)毛細管柱(30 m×0.25 mm×0.25 μm),柱箱初始溫度40 ℃,并保持2 min,然后以10 ℃/min的速度升溫至240 ℃,并保持5 min,總耗時27 min;進樣器溫度為250 ℃,每次進樣1 μL.利用外標法對產物進行定量,產物的產率可由下式計算:
2 結果與討論
2.1 反應體系的建立
氫碘酸作為還原劑用于還原反應時,在反應過程中會生成碘單質,這不僅會阻礙還原反應的繼續進行,而且會造成反應產物的污染導致產物難于分離,因此必需將生成的碘單質原位還原為氫碘酸.Yang等[21]提出了將金屬催化劑和氫氣共同作用于碘單質原位再生的方法.本研究選用PdCl2作為加氫催化劑,加入環己烷用于萃取有機產物.表1為不同反應體系中氫碘酸還原山梨醇的產物分布.在由氫碘酸、PdCl2、氫氣和環己烷共同組成的反應體系下,山梨醇可轉化得到4.74%的2-己烯、15.91%的2-碘己烷和23.87%的3-碘己烷,總產率可達44.52%;當反應體系中沒有氫氣或PdCl2催化劑時,反應結束后有機相和水相都呈深紅褐色,無法進行分液操作,通過淀粉試紙檢測,反應體系中有大量碘單質生成;當反應體系中不加氫碘酸水溶液,而以10.89 mL的去離子水代替時,反應結束后有機相中無任何產物生成,如表1中序號5實驗所示.該結果表明:PdCl2和氫氣對山梨醇的轉化反應沒有影響,只對碘單質的原位再生起作用,而這正符合本研究的預期.當反應前不加環己烷時,2-己烯產率變化不大,而2-碘己烷和3-碘己烷的產率大幅降低,說明提前加入有機萃取溶劑對提高2-碘己烷和3-碘己烷的產率有利,這可能是因為有機溶劑將反應產物聚集到有機相中,促進了烯烴與氫碘酸的反應從而提高總產率.因此,選用由氫碘酸、PdCl2催化劑、環己烷和氫氣共同組成的反應體系用于氫碘酸還原山梨醇的反應.
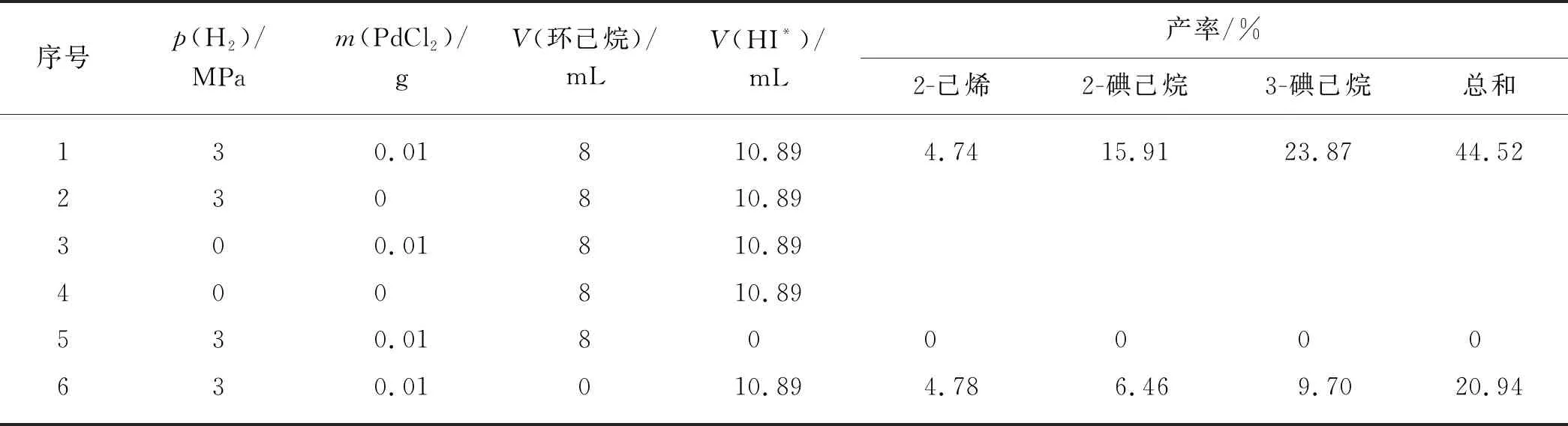
表1 不同反應體系下氫碘酸還原山梨醇的產物分布
2.2 反應參數對產物分布的影響
首先利用單因素試驗研究山梨醇在不同條件下被氫碘酸還原合成2-己烯和碘己烷的產物分布,實驗結果如表2所示.山梨醇在氫碘酸的作用下可脫去羥基,還原產物為2-碘己烷、3-碘己烷及少量的2-己烯,其中3-碘己烷的產率最高.使用47%(質量分數,下同)的氫碘酸,在溫度較低(80 ℃)時,山梨醇在氫碘酸作用下,只有少量的2-己烯生成,無碘己烷生成;而溫度過高(170 ℃)時,產物產率降低,說明氫碘酸還原山梨醇需要在一定的溫度下才能發生,然而過高的溫度并不利于目標反應的進行.當反應溫度110 ℃、氫氣壓力3 MPa、47%氫碘酸(0.06 mmol)反應時間僅為1 h時,2-己烯、2-碘己烷和3-碘己烷的產率分別為8.40%,11.22%和16.84%;當反應時間延長到3 h時,3種產物的產率分別為4.74%,15.91%和23.87%,2-己烯產率降低,而兩種碘己烷產率都有一定程度升高;繼續延長反應時間到6 h,2-己烯產率繼續降低至4.12%,同時2-碘己烷和3-碘己烷產率也稍有降低,說明為保證反應進行完全,一定的反應時間是必要的,但過長的反應時間則不利于產率的升高,3 h的反應時間是較合適的.為將還原過程中產生的碘單質還原成氫碘酸,在反應體系中通入一定壓力的氫氣,對產物的產率也有一定的影響.與反應時間相似,隨著氫氣壓力的增大兩種碘己烷的產率都呈現先升高后降低的趨勢,而2-己烯產率則隨之不斷降低,這是因為隨氫氣壓力的增大,烯烴的分壓減小,在液相中更容易轉化為碘代烷烴.氫碘酸濃度對產物分布有很大的影響,當氫碘酸的濃度較低(質量分數≤31.33%)時,無任何產物生成,說明較低濃度的氫碘酸不能還原山梨醇;當使用57%的氫碘酸時,兩種碘己烷的產率都大幅升高,而2-己烯產率很低,僅為1.03%,說明氫碘酸濃度對氫碘酸還原山梨醇合成碘己烷的影響很大,高濃度的氫碘酸對合成碘己烷有利.增加氫碘酸的用量時,兩種碘己烷的產率都有所增加,而2-己烯產率略有降低,總產率增加,因此增加氫碘酸的用量對合成碘己烷也有利.在表2的序號12實驗中,反應結束后氫氣幾乎耗盡,為繼續提高產率,適當增大氫氣壓力,結果顯示:當氫氣壓力增大到4 MPa 時,兩種碘己烷的產率都有所升高,且無2-己烯生成.在此基礎上繼續增加氫碘酸的用量,兩種碘己烷的產率繼續升高,兩者總產率可達93.92%.
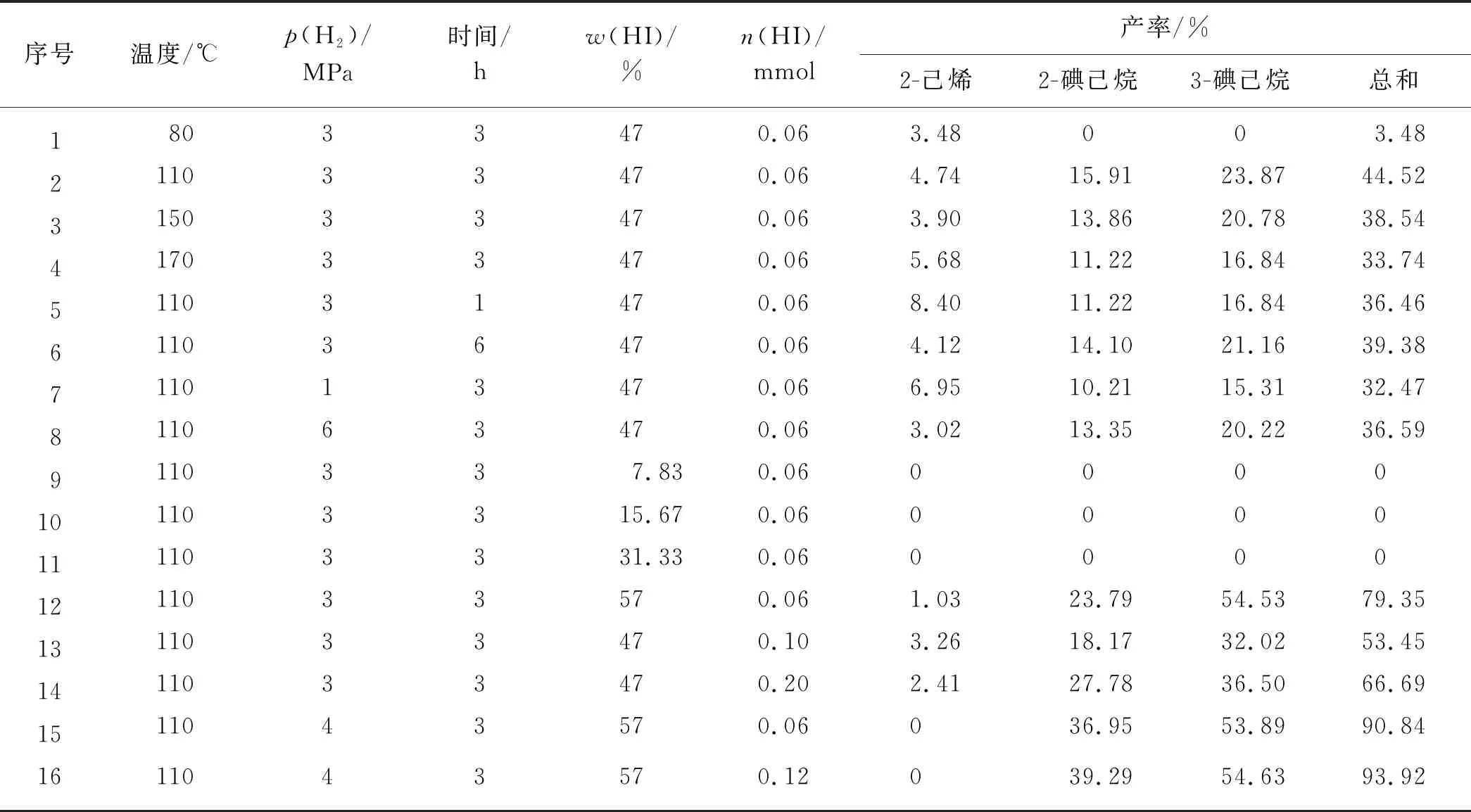
表2 氫碘酸還原山梨醇合成2-己烯與碘己烷的結果
為研究氫碘酸還原山梨醇的反應路徑,縮短反應時間以期獲得可能涉及的中間產物,結果顯示:除反應時間外,其他條件與表2的序號2實驗相同,當反應時間縮短到10和30 min時,有機相中的產物類型與反應3 h時一致,這可能是因為反應中涉及的中間產物并不穩定,在氫碘酸的環境中很快轉化為最終產物.當反應時間為10 min時,2-己烯、2-碘己烷和3-碘己烷的產率分別為3.79%,5.85%和8.23%;反應時間為30 min時,三者的產率分別為7.74%,8.35%和12.78%.隨著反應時間延長,2-己烯產率先增加后減少,而兩種碘己烷產率均增加,因此,2-己烯可能是山梨醇轉化為碘己烷過程中的中間產物.當以2-己烯為反應底物與氫碘酸反應后,得到22.60%的2-碘己烷、50.12%的3-碘己烷和極少量的己烷,并有6.16%的2-己烯殘留.可見兩種碘己烷是由氫碘酸與2-己烯發生2位和3位加成反應得到的,極少量己烷的生成可能是由2-己烯在金屬催化劑作用下與氫氣發生加成反應得到的.
2.3 碳平衡計算
在最佳反應條件下,有機相中2-己烯、2-碘己烷和3-碘己烷的總產率可達93.92%;此外有機相中還存在極少量的C12化合物,含量很低且結構復雜,沒有市售的標準品,無法對它們進行定量.收集的氣相中,除氫氣外未檢測到其他有機產物.取2 mL反應后分離出的水相,用1 mol/L的NaOH水溶液中和后再用去離子水定容到50 mL,用于有機碳檢測.結果顯示,在水相中存在4.7%的有機碳,這些有機碳可能是未反應的山梨醇,也有可能是水溶性中間產物.可檢測到的有機碳可達98.62%,其余未檢測到的有機碳可能在分離過程中損失,也有一部分是難以被GC-FID檢測到的其他產物.
2.4 C3模型化合物的轉化

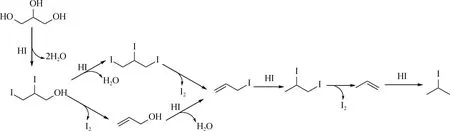
圖1 甘油與氫碘酸反應生成2-碘丙烷的反應機理[24]
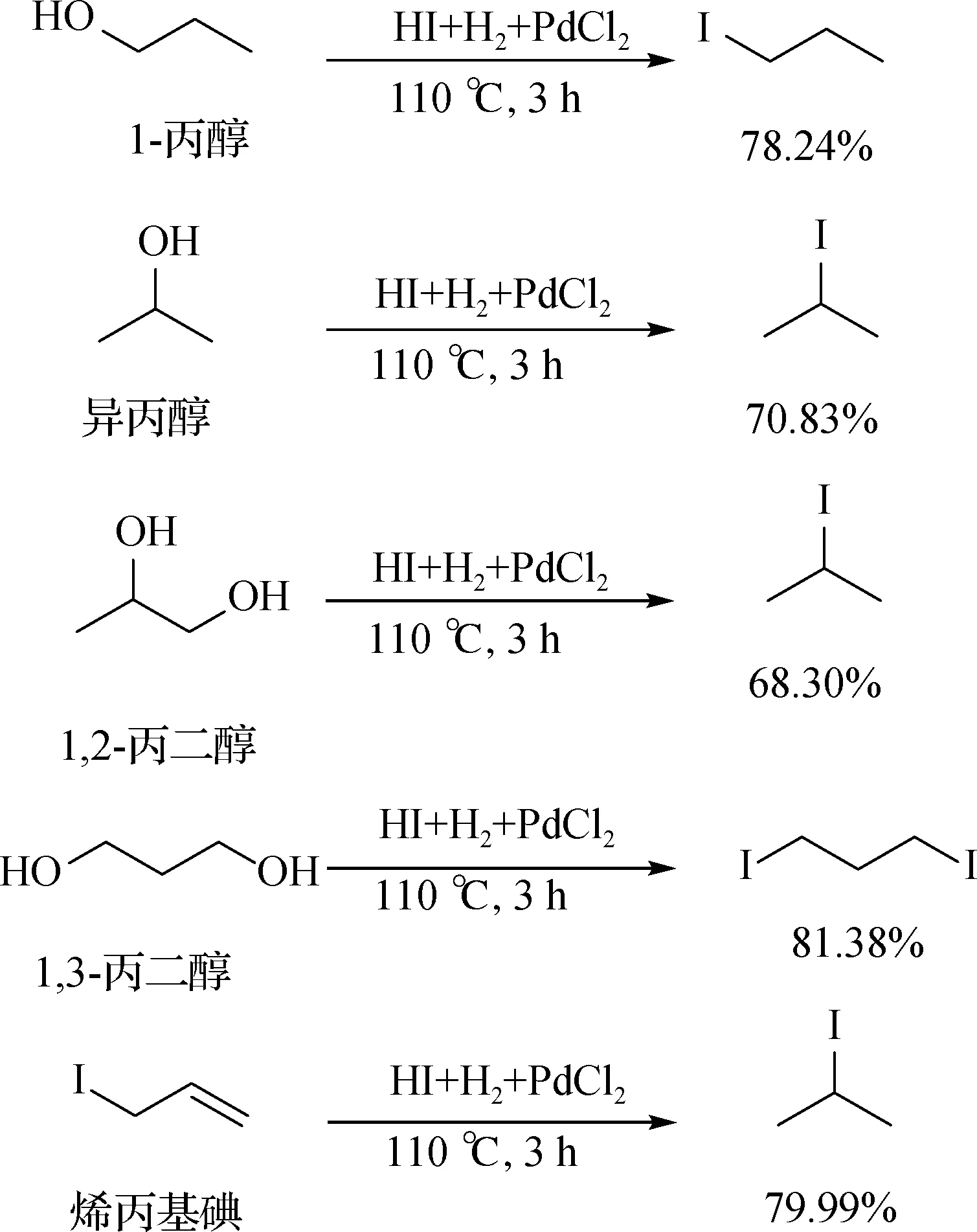
圖2 甘油類模型化合物與氫碘酸的反應
2.5 C6模型化合物的轉化
與甘油相似,氫碘酸還原山梨醇很有可能也涉及取代、消去和加成反應,為驗證此假設,以多種C6模型化合物為反應底物進行實驗.首先是一元醇模型化合物實驗,結果如圖3所示:1-己醇與氫碘酸反應只發生取代反應生成1-碘己烷,2-己醇與氫碘酸反應后得到2-碘己烷和3-碘己烷.這可能是因為2-己醇與氫碘酸反應過程中,不僅發生了取代反應,還發生了消去反應,2-己醇在酸性條件下脫水生成2-己烯,然后2-己烯與氫碘酸發生加成反應生成2-碘己烷和3-碘己烷.反應產物中的2-碘己烷是2-己醇取代和2-己烯加成兩種反應的共同產物.3-己醇與氫碘酸反應后也得到了2-碘己烷和3-碘己烷兩種產物.與2-己醇一樣,反應過程中發生了己醇的消去和己烯的加成反應.醇的消去和取代反應均為單分子一級反應,醇首先被質子化,然后脫去H2O后形成碳正離子.由于碘離子半徑較大,與1位碳正離子相比,碘離子與2位和3位碳正離子結合時具有更大的空間位阻,并且2-己醇和3-己醇均為二級醇,所以與1-己醇相比,2-己醇和3-己醇更易發生消去反應生成己烯,己烯加成后生成2-碘己烷和3-碘己烷.
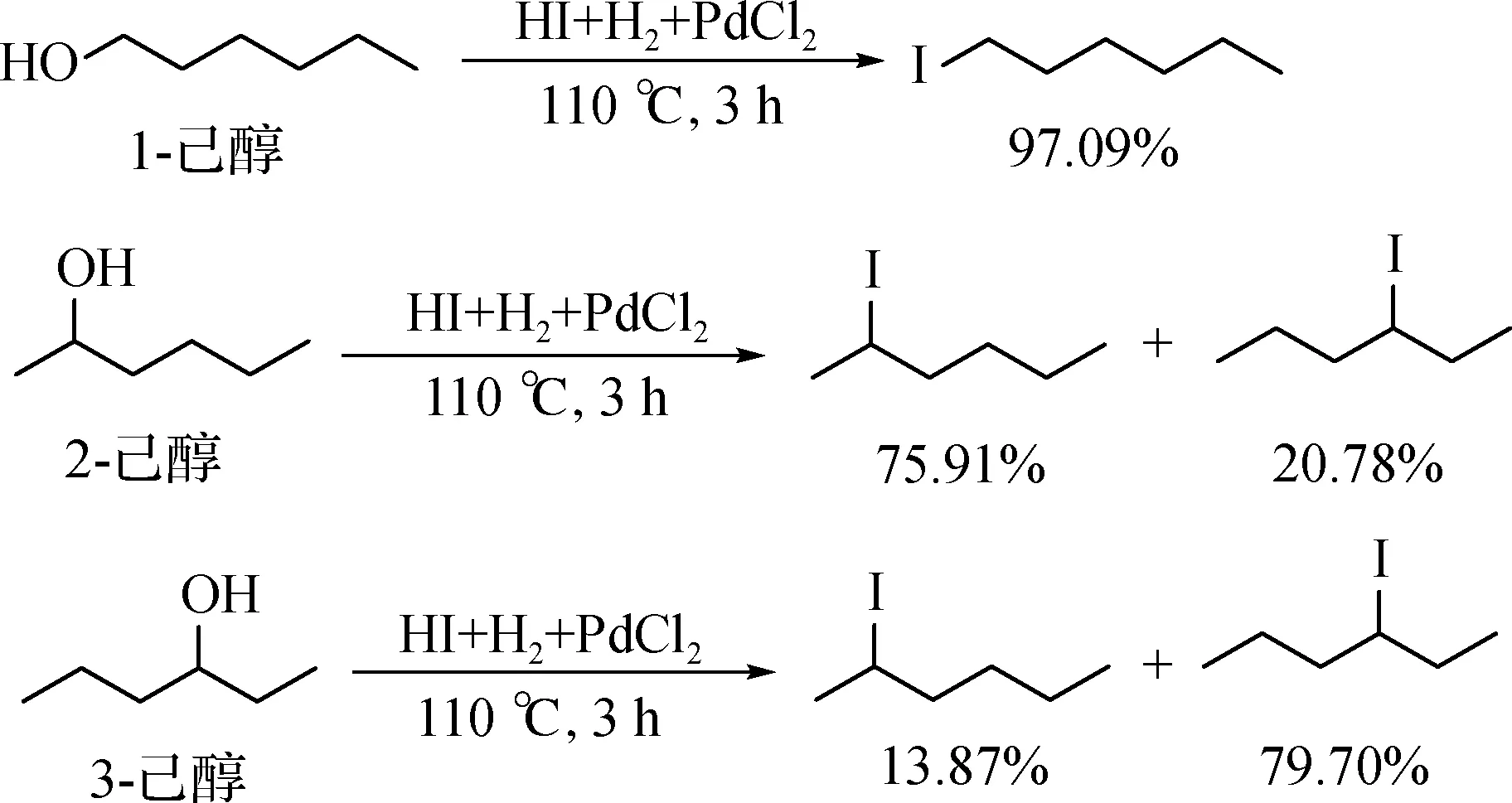
圖3 一元醇模型化合物與氫碘酸的反應

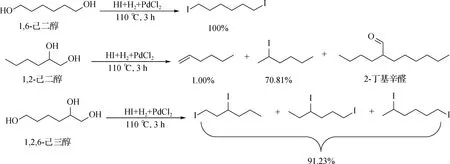
圖4 二元醇和三元醇模型化合物與氫碘酸的反應


圖5 己烯醇類模型化合物與氫碘酸的反應
此外,當以1-碘己烷為反應底物與氫碘酸反應后,有機相中僅檢測到1-碘己烷,無2-己烯、2-碘己烷和3-碘己烷生成,因此,在氫碘酸還原山梨醇的過程中2-碘己烷和3-碘己烷的生成并不是通過1-碘己烷異構化完成的.同樣地,當以1,6-二碘己烷為反應底物時,反應結束后有機相中仍然只有1,6-二碘己烷,無其他產物生成,這再次說明當兩個碘離子處于不相鄰碳原子上時無法發生消去反應.根據空間位阻效應,當碘離子攻擊羥基時,處于端位的羥基更容易被攻擊從而被碘離子取代,實驗結果表明:氫碘酸還原山梨醇反應生成己烯和碘己烷是從山梨醇分子的兩端開始進行的.
2.6 可能反應路徑

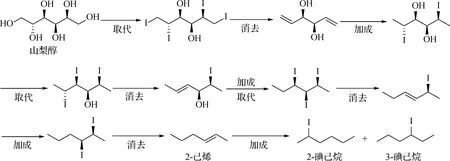
圖6 氫碘酸還原山梨醇生成己烯和碘己烷可能的反應機理
當然,由于有些推斷的中間化合物目前尚無市售的產品,所以山梨醇的部分反應歷程是結合模型化合物反應產物的特點推斷的,有待進一步的研究.
3 結 論
山梨醇在氫碘酸作用下可被還原為2-己烯、2-碘己烷和3-碘己烷,且反應溫度、時間和氫氣壓力對產率均有一定的影響,提高氫碘酸濃度對合成碘己烷有利,在最佳條件下3種產物的總產率可達93.92%.通過多種模型化合物實驗可得氫碘酸還原山梨醇過程的可能反應路徑:反應從兩端向中間依次進行,通過多次的取代、消去和加成反應,山梨醇被還原為2-己烯,然后2-己烯與氫碘酸進一步發生加成反應生成2-碘己烷和3-碘己烷.

